|
|
| (3人の利用者による、間の45版が非表示) |
| 1行目: |
1行目: |
| <div align="right">
| | '''「概要」''' |
| <font size="+1">[http://researchmap.jp/hirofumitokuoka 徳岡 宏文]、[http://researchmap.jp/hiroshiichinose 一瀬 宏]</font><br>
| |
| ''東京工業大学大学''<br> | |
| DOI:<selfdoi /> 原稿受付日:2012年6月15日 原稿完成日:2012年10月1日<br>
| |
| 担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br>
| |
| </div>
| |
|
| |
|
| {{chembox
| | ノルアドレナリン(noradrenaline, NA)はノルエピネフリン(norepinephrine, NE)とも呼ばれる。モノアミンの一種、またカテコールアミンの一種である。生体内において、神経伝達物質またはホルモンとして働く。生体内ではチロシンから合成される。ノルアドレナリンの受容体はアドレナリン受容体ファミリーであり、三量体Gタンパク質共役型である。末梢神経系では交感神経における神経伝達物質として重要である。中枢神経系では、橋にある青斑核にノルアドレナリン作動性神経細胞が多く存在し、そこからほぼ脳全域に投射している。中枢神経系ノルアドレナリンは覚醒-睡眠や[[ストレス]]に関する働きをし、注意、記憶や学習などにも影響すると考えられている。 |
| | Verifiedfields = changed
| |
| | UNII_Ref = {{fdacite|correct|FDA}}
| |
| | UNII = X4W3ENH1CV
| |
| | verifiedrevid = 477170789
| |
| | ImageFile = 1NA_fig1.jpg
| |
| | ImageSize = 180px
| |
| | ImageFile1 = Norepinephrine-3d-CPK.png
| |
| | ImageSize1 = 180px
| |
| | Name = Norepinephrine
| |
| | Reference =<ref>''Merck Index'', 11th Edition, '''6612'''.</ref>
| |
| | IUPACName = 4-[(1''R'')-2-amino-1-hydroxyethyl]benzene-1,2-diol
| |
| | OtherNames = Noradrenaline<br />(''R'')-(–)-Norepinephrine<br />l-1-(3,4-Dihydroxyphenyl)-2-aminoethanol<ref name="51-41-2">{{cite web|title=51-41-2|url=https://scifinder-cas-org.proxy.library.nd.edu:9443/scifinder/view/scifinder/scifinderExplore.jsf|work=SciFinder|publisher=SciFinder|accessdate=14 November 2011}}</ref>
| |
| | Section1 = {{Chembox Identifiers
| |
| | InChI = 1/C8H11NO3/c9-4-8(12)5-1-2-6(10)7(11)3-5/h1-3,8,10-12H,4,9H2/t8-/m0/s1
| |
| | InChIKey = SFLSHLFXELFNJZ-QMMMGPOBBL
| |
| | DrugBank_Ref = {{drugbankcite|correct|drugbank}}
| |
| | DrugBank = DB00368
| |
| | ChEBI_Ref = {{ebicite|correct|EBI}}
| |
| | ChEBI = 18357
| |
| | SMILES = Oc1ccc(cc1O)[C@@H](O)CN
| |
| | StdInChI_Ref = {{stdinchicite|correct|chemspider}}
| |
| | StdInChI = 1S/C8H11NO3/c9-4-8(12)5-1-2-6(10)7(11)3-5/h1-3,8,10-12H,4,9H2/t8-/m0/s1
| |
| | StdInChIKey_Ref = {{stdinchicite|correct|chemspider}}
| |
| | StdInChIKey = SFLSHLFXELFNJZ-QMMMGPOBSA-N
| |
| | CASNo_Ref = {{cascite|changed|??}}
| |
| | CASNo = 51-41-2 (l)
| |
| | CASOther = [http://www.commonchemistry.org/ChemicalDetail.aspx?ref=138-65-8 138-65-8](dl)
| |
| | PubChem = 439260
| |
| | ChEMBL_Ref = {{ebicite|correct|EBI}}
| |
| | ChEMBL = 1437
| |
| | ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}}
| |
| | ChemSpiderID = 388394
| |
| | KEGG_Ref = {{keggcite|correct|kegg}}
| |
| | KEGG = D00076
| |
| | ATCCode_prefix = C01
| |
| | ATCCode_suffix = CA03
| |
| }}
| |
| | Section2 = {{Chembox Properties
| |
| | Formula = |C=8|H=11|N=1|O=3
| |
| | MolarMass = 169.18 g/mol
| |
| | MeltingPt = L: 216.5–218 °C (''decomp.'')<br />D/L: 191 °C (''decomp.'')
| |
| | Density = 1.397±0.06 g/cm^3 (20 °C and 760 Torr)<ref name="51-41-2"></ref>
| |
| | VaporPressure = 1.30e-8 Torr<ref name="51-41-2"></ref>
| |
| | pKa = 9.57±0.10<ref name="51-41-2"></ref>
| |
| | BoilingPt = 442.6±40.0 °C (760 Torr)<ref name="51-41-2"></ref>
| |
| }}
| |
| }}
| |
|
| |
|
| 英:noradrenaline, norepinephrine 独:Noradrenalin, Norepinephrin 仏:noradrénaline, norépinéphrine 略称:NA, NE
| | <br> '''「発見」''' |
|
| |
|
| 同義語:ノルエピネフリン
| | 1946年、Ulf Svante von Euler(スウェーデン)およびPeter Holtz(ドイツ)により、ノルアドレナリンがほ乳類の交感神経において神経伝達物質として働くことが示された<ref name="ref1">'''U S von Euler'''<br> A Specific Sympathomimetic Ergone in Adrenergic Nerve Fibres (Sympathin) and its Relations to Adrenaline and Nor-Adrenaline <br> ''Acta Physiol., Scand. '':1946, 12; 73–97</ref> <ref name="ref2">'''P Holtz'''<br> Uber die sympathicomimetische Wirksamkeit von Gehiraex- trakten.<br>''Acta Physiol., Scand. '': 1950, 20; 354–362</ref>。 |
|
| |
|
| {{box|text=
| | <br> '''「構造」''' |
| ノルアドレナリンは[[モノアミン]]の一種、また[[カテコールアミン]]の一種である。生体内において、[[神経伝達物質]]または[[wikipedia:ja:ホルモン|ホルモン]]として働く。生体内では[[wikipedia:ja:チロシン|チロシン]]から合成される。ノルアドレナリンの[[受容体]]は[[アドレナリン受容体]]ファミリーであり、三量体[[Gタンパク質共役型]]である。[[末梢神経]]系では[[交感神経]]における神経伝達物質として重要である。[[中枢神経]]系では、[[橋]]にある[[青斑核]]にノルアドレナリン作動性神経細胞が多く存在し、そこからほぼ脳全域に投射している。中枢神経系ノルアドレナリンは[[覚醒]]-[[睡眠]]や[[ストレス]]に関する働きをし、[[注意]]、[[記憶]]や[[学習]]などにも影響すると考えられている。
| |
| }}
| |
|
| |
|
| == 発見 ==
| | カテコール基と一級アミノ基をもつ、カテコールアミン神経伝達物質の一種。また、ドーパミン、セロトニン、ヒスタミンなどとともにモノアミン系神経伝達物質のグループを形成する。 |
|
| |
|
| 1946年、[[wikipedia:ja:ウルフ・スファンテ・フォン・オイラー|Ulf Svante von Euler]](スウェーデン)および[[wikipedia:de:Peter Holtz|Peter Holtz]](ドイツ)により、ノルアドレナリンが[[wikipedia:ja:ほ乳類|ほ乳類]]の交感神経において神経伝達物質として働くことが示された<ref name="ref1">'''U S von Euler'''<br> A Specific Sympathomimetic Ergone in Adrenergic Nerve Fibres (Sympathin) and its Relations to Adrenaline and Nor-Adrenaline <br> ''Acta Physiol., Scand. '':1946, 12; 73–97</ref> <ref name="ref2">'''P Holtz'''<br>Über die sympathicomimetische Wirksamkeit von Gehirnextrakten.<br>''Acta Physiol., Scand. '': 1950, 20; 354–362</ref>。
| | <br> |
|
| |
|
| == 構造 ==
| | [[Image:1NA fig1.jpg|200px]] |
|
| |
|
| [[wikipedia:ja:カテコール|カテコール]]基と[[wikipedia:ja:アミン|一級アミノ基]]をもつ、カテコールアミン神経伝達物質の一種。また、[[ドーパミン]]、[[セロトニン]]、[[ヒスタミン]]などとともに[[モノアミン系]]神経伝達物質のグループを形成する。
| | <br> '''「合成」''' 。他に、副腎髄質中にあるクロム親和性細胞においても合成されている。酵素に関わる酵素は以下の通り。 |
|
| |
|
| == 合成 == | | *'''チロシン水酸化酵素 tyrosine hydroxylase (TH):'''EC 1.14.16.2。チロシンよりL-DOPA (L-3,4-dihydroxyphenylalanine)を合成する<ref name="ref3"><pubmed> 15569247 </pubmed></ref> <ref name="ref4"><pubmed> 21176768 </pubmed></ref> <ref name="ref5"><pubmed> 2575455</pubmed></ref>。反応には、Tetrahydrobiopterin, O<sub>2</sub>, Fe<sup>2+</sup>が必要。カテコールアミン合成において、律速段階の酵素であると考えられている。その活性制御は、主にタンパク質の量と、リン酸化による。全てのカテコールアミン産生細胞に存在する。補因子であるTetrahydrobiopterinはGTPより合成される。律速酵素はGTP cyclohydrolase Iである<ref name="ref6"><pubmed> 10727395 </pubmed></ref>。<br> |
| | *'''芳香族アミノ酸脱炭酸酵素 aromatic L-amino acid decarboxylase (AADC)''':芳香族アミノ酸脱炭酸酵素 aromatic L-amino acid decarboxylase (AADC):EC 4.1.1.28。L-DOPAよりドーパミンを合成する。他に、この酵素は5-hydroxytryptophanからセロトニン(5-hydroxytryptamine, 5-HT)を合成する反応も触媒する。Pyridoxal phosphateが必要。全てのカテコールアミン産生細胞に存在する<ref name="ref7"><pubmed> 8897471</pubmed></ref>。<br> |
| | *'''ドーパミンβ水酸化酵素 Dopamine β-hydroxylase (DBH)''':EC 1.14.2.1。ドーパミンよりノルアドレナリンを合成する。アスコルビン酸、O<sub>2</sub>、Cu<sup>2+</sup>が必要。ノルアドレナリン、アドレナリン産生細胞のシナプス小胞の中に存在し、シナプス小胞に取り込まれたドーパミンをノルアドレナリンに変換する<ref name="ref8"><pubmed> 6998654 </pubmed></ref>。 |
|
| |
|
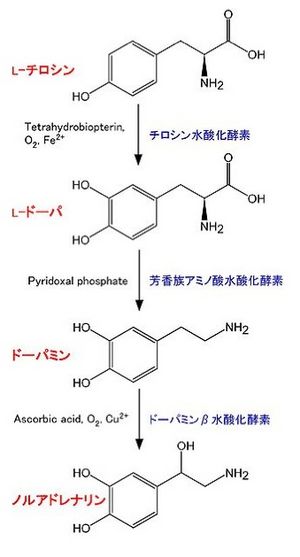
| [[Image:1NA fig2.jpg|thumb|250px|'''図1 ノルアドレナリン生合成経路''']] 中枢神経系のノルアドレナリン神経系の他、[[副腎髄質]]中にある[[クロム親和性細胞]]においても合成されている。合成に関わる酵素は以下の通り(図1)。
| | <br> |
|
| |
|
| === チロシン水酸化酵素 ===
| | [[Image:1NA fig2.jpg|300px]] |
| Tyrosine hydroxylase (TH):EC 1.14.16.2
| |
|
| |
|
| チロシンより[[L-DOPA]] (L-3,4-dihydroxyphenylalanine)を合成する<ref name="ref3"><pubmed> 15569247 </pubmed></ref> <ref name="ref4"><pubmed> 21176768 </pubmed></ref> <ref name="ref5"><pubmed> 2575455</pubmed></ref>。反応には、[[テトラヒドロビオプテリン]] (tetrahydrobiopterin), O<sub>2</sub>, Fe<sup>2+</sup>が必要。カテコールアミン合成において、[[wikipedia:ja:律速段階|律速段階]]の酵素であると考えられている。その活性制御は、主にタンパク質の量と、[[リン酸化]]による。全てのカテコールアミン産生細胞に存在する。[[wikipedia:ja:補因子|補因子]]であるテトラヒドロビオプテリンはGTPより合成される。律速酵素は[[GTPシクロヒドラーゼI]] (GTP cyclohydrolase I)である<ref name="ref6"><pubmed> 10727395 </pubmed></ref>。
| | <br> '''「放出、再取り込み」''' |
|
| |
|
| === 芳香族アミノ酸脱炭酸酵素 === | | ノルアドレナリンの前駆体であるドーパミンは小胞型モノアミントランスポーター(vesicular monoamine transporter, vMAT)によりシナプス小胞内に輸送される。vMAT1は主に副腎のクロム親和性細胞、vMAT2は神経細胞で発現している。vMATはH<sup>+</sup>との交換輸送によりモノアミンを小胞内に蓄積させる<ref name="ref9"><pubmed> 11099462 </pubmed></ref>。<br> ノルアドレナリンの放出は他の神経伝達物質と同様に、神経活動依存的、カルシウム依存的なシナプス小胞のエキソサイトーシスによる。<br> 放出された後、ノルエピネフリントランスポーター(NET、またはノルアドレナリントランスポーター(NAT))により再取り込みされる。他のカテコールアミン同様、細胞外に放出されたノルアドレナリンの量の調節は、この再取込みの寄与が高い<ref name="ref10"><pubmed> 10769386 </pubmed></ref>。NETはNa<sup>+</sup>/K<sup>+</sup>-ATPase依存的で、Na<sup>+</sup>/Cl<sup>-</sup>の共輸送によりノルアドレナリンを細胞内に輸送する。またNETはリン酸化により制御される<ref name="ref11"><pubmed> 16539676 </pubmed></ref>。<br> |
| Aromatic L-amino acid decarboxylase (AADC):EC 4.1.1.28
| |
|
| |
|
| L-DOPAよりドーパミンを合成する。他に、この酵素は[[5-ヒドロキシトリプトファン]] (5-hydroxytryptophan)からセロトニン(5-hydroxytryptamine, 5-HT)を合成する反応も触媒する。[[wikipedia:ja:ピリドキサールリン酸|ピリドキサールリン酸]] (pyridoxal phosphate)が必要。全てのカテコールアミン産生細胞に存在する<ref name="ref7"><pubmed> 8897471</pubmed></ref>。
| | <br> |
|
| |
|
| === ドーパミンβ水酸化酵素 ===
| | '''「代謝分解」''' |
| Dopamine β-hydroxylase (DBH):EC 1.14.2.1
| |
|
| |
|
| ドーパミンよりノルアドレナリンを合成する。[[wikipedia:ja:アスコルビン酸|アスコルビン酸]]、O<sub>2</sub>、Cu<sup>2+</sup>が必要。ノルアドレナリン、アドレナリン産生細胞の[[シナプス小胞]]の中に存在し、シナプス小胞に取り込まれたドーパミンをノルアドレナリンに変換する<ref name="ref8"><pubmed> 6998654 </pubmed></ref>。
| | ノルアドレナリンの代謝分解には次の二つの酵素が重要である。 |
|
| |
|
| == 放出、再取り込み == | | *'''モノアミン酸化酵素(monoamine oxidase, MAO)''':MAOはモノアミンのアミノ基をアルデヒド基に酸化する。MAOはミトコンドリア外膜に局在しに存在し、細胞内のノルアドレナリン(再取込みされたものを含む)の分解に関与する。ただしMAOに比べてvMAT2の方がノルアドレナリンに対する親和性がずっと高いため、シナプス小胞への取り込みの方がMAOによる分解よりも優先されると考えられる<ref name="ref12"><pubmed> 16552415</pubmed></ref>。MAOにはMAO-AとMAO-Bがあり、二つの別の遺伝子によりコードされている。MAO-AとMAO-Bはモノアミン作動性神経細胞およびグリア細胞に発現しているが、発現量は細胞の種類により異なり、また動物種によっても違いが見られる<ref name="ref12" />。マウス脳のノルアドレナリン作動性神経細胞には主にMAO-Aが発現している<ref name="ref13"><pubmed> 11793338 </pubmed></ref>。。 |
| | *'''カテコール-''O''-メチル基転移酵素(catechol-''O''-methyltransferase, COMT)''':これはカテコール基のm-水酸基にメチル基を転移させる。腎臓や肝臓に豊富だが、カテコールアミン作動性神経細胞の投射先においても発現している。細胞外で働くと考えられている<ref name="ref14"><pubmed> 21846718 </pubmed></ref>。 |
|
| |
|
| ノルアドレナリンの前駆体であるドーパミンは[[小胞型モノアミントランスポーター]](vesicular monoamine transporter, vMAT)によりシナプス小胞内に輸送される。vMAT1は主に副腎のクロム親和性細胞、vMAT2は神経細胞で発現している。vMATはH<sup>+</sup>との交換輸送によりモノアミンを小胞内に蓄積させる<ref name="ref9"><pubmed> 11099462 </pubmed></ref>。<br> ノルアドレナリンの放出は他の神経伝達物質と同様に、神経活動依存的、[[カルシウム]]依存的なシナプス小胞のエキソサイトーシスによる。
| | 脳においてノルアドレナリンの多くは、MAO、アルデヒド還元酵素、およびCOMTにより3-methoxy-4-hydroxyphenylglycol(MHPG)へ代謝され、さらに3-methoxy-4-hydroxymandelic acid (VMA)となって尿中に排出される<ref name="ref15">'''D E Golan, A H Tashjian Jr, E J Armstrong, A W Armstrong'''<br> Principles of Pharmacology, Second Edition<br>''Wolters Kluwer Health (Philadelphia)'':2002</ref>。MHPGの硫酸化物も尿中に排出される<ref name="ref15" />。 |
|
| |
|
| 放出された後、[[ノルエピネフリントランスポーター]](norepinephrine transporter, NET、または[[ノルアドレナリントランスポーター]] (noradrenaline transporter, NAT))により再取り込みされる。他のカテコールアミン同様、細胞外に放出されたノルアドレナリンの量の調節は、この再取込みの寄与が高い<ref name="ref10"><pubmed> 10769386 </pubmed></ref>。NETは[[Na+/K+-ATPase|Na<sup>+</sup>/K<sup>+</sup>-ATPase]]依存的で、Na<sup>+</sup>/Cl<sup>-</sup>の共輸送によりノルアドレナリンを細胞内に輸送する。またNETはリン酸化により制御される<ref name="ref11"><pubmed> 16539676 </pubmed></ref>。<br>
| | <br> '''「主たる投射系と機能」''' |
|
| |
|
| == 代謝分解 ==
| | (1) 中枢神経系 |
|
| |
|
| ノルアドレナリンの代謝分解には[[モノアミン酸化酵素]](monoamine oxidase, MAO)、[[カテコール-O-メチル基転移酵素|カテコール-''O''-メチル基転移酵素]](catechol-''O''-methyltransferase, COMT)が重要である。
| | 脳におけるノルアドレナリン作動性の神経細胞群は、主に髄質、橋に存在し、A1-A7に分けられている。<br>A1、A2:A1は髄質の腹外側に位置し、A2は背側に位置する。共に視床下部に上行性投射をし、循環器系や内分泌系の調節を行う。<br>A5、A7:橋の腹外側に位置し、脊髄へ投射し、自律神経反射や、痛覚の調節を行う。<br>A6:青斑核(Locus Ceruleus)と呼ばれる。橋の背側に位置し、最も主要なノルアドレナリン作動性神経細胞の核である。青斑核からは、大脳皮質、視床、視床下部、小脳、中脳、脊髄、など脳のほぼ全域にわたって投射している。青斑核のノルアドレナリン作動性神経細胞は覚醒状態や不意な環境変化への応答性に関係している<ref name="ref16"><pubmed> 19190638 </pubmed></ref>。例えば、ラット青斑核神経細胞の発火頻度は、覚醒-睡眠のサイクルに応じて変化し、また継続中の行動を中断するような場合に上昇する<ref name="ref17"><pubmed> 7346592 </pubmed></ref>。さらに近年、ノルアドレナリンの注意、記憶、学習への関与、またシナプス可塑性への関与が報告されている<ref name="ref16" /> <ref name="ref18"><pubmed> 20465834</pubmed></ref>。これらのことから、ノルアドレナリンの働きは、動物が環境の変化に適応する際に、注意や認知のシフト、そして行動の適応化を早めることであると提唱されている<ref name="ref16" />。<br> |
|
| |
|
| 脳においてノルアドレナリンの多くは、MAO、[[アルデヒド還元酵素]]、およびCOMTにより[[wikipedia:3-Methoxy-4-hydroxyphenylglycol|3-メトキシ-4-ヒドロキシフェニルグリコール]] (3-methoxy-4-hydroxyphenylglycol, MHPG)へ代謝され、さらに[[wikipedia:Vanillylmandelic acid|3-メトキシ-4-ヒドロキシマンデル酸]] (3-methoxy-4-hydroxymandelic acid) (または[[wikipedia:Vanillylmandelic acid|バニリルマンデル酸]] (vanillylmandelic acid, VMA)となって尿中に排出される<ref name="ref15">'''D E Golan, A H Tashjian Jr, E J Armstrong, A W Armstrong'''<br> Principles of Pharmacology, Second Edition<br>''Wolters Kluwer Health (Philadelphia)'':2002</ref>。MHPGの硫酸化物も尿中に排出される<ref name="ref15" />。
| | <br> |
|
| |
|
| === モノアミン酸化酵素 ===
| | (2)自律神経系 |
| MAOはモノアミンのアミノ基を[[wj:アルデヒド|アルデヒド]]基に酸化する。MAOは[[ミトコンドリア]]外膜に局在し、細胞内のノルアドレナリン(再取込みされたものを含む)の分解に関与する。ただしMAOに比べてvMAT2の方がノルアドレナリンに対する親和性がずっと高いため、シナプス小胞への取り込みの方がMAOによる分解よりも優先されると考えられる<ref name="ref12"><pubmed> 16552415</pubmed></ref>。MAOには[[MAO-A]]と[[MAO-B]]があり、二つの別の遺伝子によりコードされている。MAO-AとMAO-Bはモノアミン作動性神経細胞および[[グリア細胞]]に発現しているが、発現量は細胞の種類により異なり、また動物種によっても違いが見られる<ref name="ref12" />。[[マウス]]脳のノルアドレナリン作動性神経細胞には主にMAO-Aが発現している<ref name="ref13"><pubmed> 11793338 </pubmed></ref>。
| |
| === カテコール-''O''-メチル基転移酵素 ===
| |
| これはカテコール基の[[wj:メタ|メタ]]位[[wj:水酸基|水酸基]]に[[wj:メチル基|メチル基]]を転移させる。[[wj:腎臓|腎臓]]や[[wj:肝臓|肝臓]]に豊富だが、カテコールアミン作動性神経細胞の投射先においても発現している。細胞外で働くと考えられている<ref name="ref14"><pubmed> 21846718 </pubmed></ref>。
| |
|
| |
|
|
| | 自律神経系のうちの交感神経系では、節後神経細胞がノルアドレナリン作動性であり、脊髄中の節前神経細胞よりアセチルコリン性の入力を受け、ノルアドレナリン性の出力を内臓器官に与える。その結果、血管の収縮、血圧の上昇、心拍数の増加、などを引き起こす。 |
|
| |
|
| == 受容体 ==
| | <br> '''「受容体」''' |
| ===分類===
| |
| ノルアドレナリンはアドレナリンと共にアドレナリン受容体(adrenergic receptorまたはadrenoceptor)に結合し活性化する。αおよびβのサブファミリーからなる(表)。より細かくは、α<sub>1A</sub>-α<sub>1D</sub>、α<sub>2A</sub>-α<sub>2C</sub>、β<sub>1</sub>-β<sub>3</sub>、から構成されている。いずれも三量体[[Gタンパク質共役型受容体]]である。α<sub>1</sub>はG<sub>q</sub>、α<sub>2</sub>はG<sub>i</sub>、β<sub>1</sub>-β<sub>3</sub>はG<sub>s</sub>と共役し、異なる[[シグナル伝達]]を行う。Gqは[[ホスホリパーゼC]]を活性化し、 [[イノシトール−1,4,5-三リン酸]] (IP<sub>3</sub>) の産生から[[IP3受容体]]を介して細胞内[[カルシウム]]の上昇を引き起こす。また[[ジアシルグリセロール]] (diacylglicerol, DAG) の産生を介して[[Ca2+/リン脂質依存性タンパク質リン酸化酵素|Ca<sup>2+</sup>/リン脂質依存性タンパク質リン酸化酵素]] (Cキナーゼ)の活性化を引き起こす。G<sub>i</sub>、G<sub>s</sub>はそれぞれ[[アデニル酸シクラーゼ]]を阻害、または活性化し、[[CAMP|cAMP]]の産生の増減、そして[[CAMP依存性タンパク質リン酸化酵素|cAMP依存性タンパク質リン酸化酵素]] (A-kinase, PKA)活性の増減を引き起こす。
| |
| ===中枢神経系===
| |
| 中枢神経系において、ノルアドレナリンは主にα<sub>1</sub>、α<sub>2</sub>、そしてβ<sub>1</sub>受容体を介して作用する。海馬神経細胞において、β1受容体の活性化は[[カリウムチャネル#.E3.82.AB.E3.83.AB.E3.82.B7.E3.82.A6.E3.83.A0.E4.BE.9D.E5.AD.98.E6.80.A7.E3.82.AB.E3.83.AA.E3.82.A6.E3.83.A0.E3.83.81.E3.83.A3.E3.83.B3.E3.83.8D.E3.83.AB|カルシウム依存性カリウムチャンネル]]を阻害し、afterhyperpolarizationを減少させ、結果的に[[シナプス]]入力依存的な発火を亢進させる<ref name="ref18"><pubmed> 2873241</pubmed></ref><ref name="ref19"><pubmed> 6300681</pubmed></ref>。この作用はcAMPを介している<ref name="ref20"><pubmed> 8274274</pubmed></ref>。さらに、β受容体は海馬における[[シナプス長期増強]](LTP)をポジティブに調節する<ref name="ref21"><pubmed> 6311345</pubmed></ref><ref name="ref22"><pubmed> 20043991</pubmed></ref>。そのメカニズムとして、[[樹状突起]]上の[[カリウムチャネル#A.E9.9B.BB.E6.B5.81|A型カリウムチャンネル]]の不活性化によるbackpropagationの促進が考えられている<ref name="ref23"><pubmed> 9914302</pubmed></ref><ref name="ref24"><pubmed> 12077183</pubmed></ref>。また、[[カリウムチャネル#.E3.82.AB.E3.83.AB.E3.82.B7.E3.82.A6.E3.83.A0.E6.B4.BB.E6.80.A7.E5.8C.96.E3.82.AB.E3.83.AA.E3.82.A6.E3.83.A0.E3.83.81.E3.83.A3.E3.83.8D.E3.83.AB|SK型カリウムチャンネル]]の活性化や[[グルタミン酸受容体]]の[[リン酸化]]の可能性も指摘されている<ref name="ref25"><pubmed> 20043991</pubmed></ref>。[[前頭前野]]では、α1、α2、そしてβ1受容体が異なる働きを示すことが示唆されている<ref name="ref26"><pubmed> 17303246</pubmed></ref>。<br>
| |
| ===末梢組織===
| |
| [[末梢神経系]]において、ノルアドレナリンはα<sub>1</sub>およびβ<sub>1</sub>アドレナリン受容体のアゴニストとして作用する。(アドレナリンは、低濃度ではβ<sub>1</sub>およびβ<sub>2</sub>アドレナリン受容体に作用し、高濃度ではα<sub>1</sub>を介した作用が主となる。)
| |
|
| |
|
| [[心筋]]において、β1受容体はGsを介してアデニル酸シクラーゼの活性化、cAMPの産生、PKAの活性化が引き起こす。さらに、環状ヌクレオチドが[[イオンチャネル#HCN.E3.83.81.E3.83.A3.E3.83.8D.E3.83.AB.E3.81.A8CNG.E3.83.81.E3.83.A3.E3.83.8D.E3.83.AB|hyperpolarization-activated cyclic nucleotide gated (HCN) channel]]に直接結合し、チャネル活性を亢進し、心筋の興奮性を高める<ref name="ref27"><pubmed> 20156590</pubmed></ref><ref name="ref28"><pubmed> 18953682</pubmed></ref>。また、PKAにより[[カルシウムチャネル#Cav1_.28L.E5.9E.8B.29|L型電位依存性カルシウムチャンネル]]や、筋[[小胞体]][[リアノジン受容体]]がリン酸化されて活性化し、細胞内のカルシウム濃度が上昇、結果的に心筋の興奮性を亢進する。この時[[A-kinase anchoring protein]] ([[AKAP]])が受容体とPKAの相互作用を手助けする<ref name="ref29"><pubmed> 20156590</pubmed></ref><ref name="ref30"><pubmed> 9687361</pubmed></ref>。また、[[カリウムチャネル#.E5.86.85.E5.90.91.E3.81.8D.E6.95.B4.E6.B5.81.E6.80.A7.E3.82.AB.E3.83.AA.E3.82.A6.E3.83.A0.E3.83.81.E3.83.A3.E3.83.8D.E3.83.AB|内向き整流性カリウムチャネル]]の一種であるslowly activated K channels (IKs) もPKAのリン酸化を受け、活性化する<ref name="ref29" />)。これにより、心拍数が増加した時でも、心臓の拡張期の時間が適切に調節されると考えられる。アドレナリンによるα2受容体の活性化は、Giを介して上記β1受容体と逆の効果がある。
| | ノルアドレナリンはアドレナリンと共にアドレナリン受容体(adrenergic receptorまたはadrenoceptor)に結合し活性化する。αおよびβのサブファミリーからなる。より細かくは、α<sub>1A</sub>-α<sub>1D</sub>、α<sub>2A</sub>-α<sub>2C</sub>、β<sub>1</sub>、β<sub>2</sub>、β<sub>3</sub>、から構成されている。いずれも三量体Gタンパク質共役型の受容体である。α<sub>1</sub>はG<sub>q</sub>、α<sub>2</sub>はG<sub>i</sub>、β<sub>1</sub>-β<sub>3</sub>はG<sub>s</sub>と共役している。<br>中枢神経系において、ノルアドレナリンは主にα<sub>1</sub>、α<sub>2</sub>、そしてβ<sub>1</sub>受容体を介して作用し、それぞれに異なる影響を与える。さらにノルアドレナリンの働きは、標的細胞における他の入力にも依存するので、複雑である。<br> 末梢神経系において、ノルアドレナリンはα<sub>1</sub>およびβ<sub>1</sub>アドレナリン受容体のアゴニストとして作用する。(アドレナリンは、低濃度ではβ<sub>1</sub>およびβ<sub>2</sub>アドレナリン受容体に作用し、高濃度ではα<sub>1</sub>を介した作用が主となる。)<br>α<sub>2</sub>アドレナリン受容体はノルアドレナリン軸索終末に存在し(オートレセプター)、ノルアドレナリンの放出を抑制する<ref name="ref19"><pubmed> 11520889 </pubmed></ref>。<br> |
|
| |
|
| [[wikipedia:ja:平滑筋|平滑筋]]において、ノルアドレナリンα1受容体の活性化は、Gqを介してホスホリパーゼCの活性化、IP<sub>3</sub>とジアシルグリセロールの産生、IP<sub>3</sub>受容体の活性化による[[細胞内カルシウムストア]]からのカルシウム放出、[[ミオシン軽鎖キナーゼ]] (myosin-light chain kinase, MLCK)の活性化、そして結果的に筋収縮を引き起こす<ref name="ref15" /> <ref name="ref31"><pubmed> 11096123</pubmed></ref>。<br>逆に、アドレナリンによるβ2受容体の活性化は、Gsを介してPKAの活性化、MLCKのリン酸化による抑制の結果、筋弛緩をもたらすと考えられる<ref name="ref15" /><ref name="ref32"><pubmed> 6259152</pubmed></ref>。<br>
| | <br> '''「抗うつ薬とノルアドレナリン」''' |
|
| |
|
| α<sub>2</sub>アドレナリン受容体はノルアドレナリン[[軸索終末]]に存在し([[自己受容体]]またはオートレセプター)、ノルアドレナリンの放出を抑制する<ref name="ref33"><pubmed> 11520889 </pubmed></ref>。
| | 気分障害の治療に使われる薬のうち、歴史的に古いMAO阻害剤、三環系抗うつ薬はセロトニン系だけでなくノルアドレナリン系を刺激する。近年使用頻度が増えている薬に選択的セロトニン再取り込み阻害剤(SSRI)あるが、これはノルアドレナリン系には作用しない。さらに、セロトニン・ノルエピネフリン再取り込み阻害剤(SNRI)も開発され、これはその名の通り、セロトニン系とノルエピネフリン系の両方を選択的に刺激する。<br> こうした薬の作用から、うつ状態の原因がセロトニンやノルアドレナリンなどのモノアミンの減少によるのではないかというモノアミン仮説が生まれた。しかし、これらの薬の治療効果が現れるのは、モノアミン神経伝達が亢進されるよりもずっと遅いことから、この仮説よりももっと複雑なことが起きていると考えられている<ref name="ref20">'''E R Kandel, J H Schwartz, T M Jessell'''<br> Principles of Neural Science, Fourth Edition<br>''Mc Graw Hill (New York)'':2000</ref> <ref name="ref21">'''N R Carlson'''<br> Physiology of Behavior, Tenth Edition<br>''Pearson Education (Boston)'':2009</ref>。<br> |
|
| |
|
| {| class="wikitable"
| | <br> |
| |-
| |
| ! style="white-space:nowrap" | 受容体
| |
| ! [[アゴニスト]]選択性
| |
| ! 主な作用
| |
| ! 細胞内シグナル
| |
| ! style="white-space:nowrap" | [[wikipedia:Adrenergic agonist|アゴニスト]]
| |
| ! style="white-space:nowrap" | [[wikipedia:Adrenergic antagonist|アンタゴニスト]]
| |
| |-
| |
| | style="white-space:nowrap" | [[wikipedia:Α1 adrenergic receptor|α]]<sub>1</sub>:<br>[[wikipedia:Alpha-1A adrenergic receptor|A]], [[wikipedia:Alpha-1B adrenergic receptor|B]], [[wikipedia:Alpha-1D adrenergic receptor|D]]<sup>†</sup>
| |
| | style="white-space:nowrap" | [[ノルアドレナリン]] > [[アドレナリン]] >> [[イソプレナリン]]
| |
| | [[wikipedia:ja:平滑筋|平滑筋]]収縮
| |
| | [[Gq alpha subunit|G<sub>q</sub>]]: [[ホスホリパーゼC]] (PLC) 活性化により[[イノシトール3リン酸]]と[[ジアシルグリセロール]]、細胞内[[カルシウム]]の上昇
| |
| | style="white-space:nowrap" |
| |
| ''([[wikipedia:Alpha-adrenergic agonist|α1アゴニスト]])''
| |
|
| |
|
| *[[ノルアドレナリン]]
| |
| *[[フェニレフリン]]
| |
| *[[メトキサミン]]
| |
| *[[シラゾリン]]
| |
| *[[キシロメタゾリン]]
| |
| *[[ミドドリン]]
| |
| *[[メタラミノール]]
| |
|
| |
| | style="white-space:nowrap" |
| |
| ''([[wikipedia:Alpha-1 blocker|α1アンタゴニスト]])''
| |
|
| |
| *[[アルフゾシン]]
| |
| *[[ドキサゾシン]]
| |
| *[[フェノキシベンザミン]]
| |
| *[[フェントラミン]]
| |
| *[[プラゾシン]]
| |
| *[[タムスロシン]]
| |
| *[[テラゾシン]]
| |
|
| |
| |-
| |
| | [[Α2 adrenergic receptor|α<sub>2</sub>]]:<br>[[Alpha-2A adrenergic receptor|A]], [[Alpha-2B adrenergic receptor|B]], [[Alpha-2C adrenergic receptor|C]]
| |
| | [[アドレナリン]] ≥ [[ノルアドレナリン]] >> [[イソプレナリン]]
| |
| | [[自己受容体]]活性化による[[神経伝達物質]]放出減少<br>[[wikipedia:ja:心筋|心筋]]弛緩、[[wikipedia:ja:血小板|血小板]]活性化
| |
| | [[Gi alpha subunit|G<sub>i</sub>]]: [[アデニル酸シクラーゼ]]抑制, [[サイクリックAMP|cAMP]]減少
| |
| |
| |
| ''([[wikipedia:Alpha-adrenergic agonist|α2アゴニスト]])''
| |
|
| |
| *[[デクスメデトミジン]]
| |
| *[[メデトミジン]]
| |
| *[[ロミフィジン]]
| |
| *[[クロニジン]]
| |
| *[[ブリモニジン]]
| |
| *[[デトミジン]]
| |
| *[[ロフェキシジン]]
| |
| *[[キシラジン]]
| |
| *[[チザニジン]]
| |
| *[[グアンファシン]]
| |
| *[[アミトラズ]]
| |
|
| |
| | style="white-space:nowrap" |
| |
| ''([[wikipedia:Α2 blocker|α2アンタゴニスト]])''
| |
|
| |
| *[[フェントラミン]]
| |
| *[[ヨヒンビン]]
| |
| *[[イダゾキサン]]
| |
| *[[アチパメゾール]]
| |
|
| |
| |-
| |
| | [[Beta-1 adrenergic receptor|β<sub>1</sub>]]
| |
| | [[イソプレナリン]] > [[アドレナリン]] = [[ノルアドレナリン]]
| |
| | 心筋収縮
| |
| | [[Gs alpha subunit|G<sub>s</sub>]]: [[アデニル酸シクラーゼ]]活性化、[[サイクリックAMP|cAMP]]上昇
| |
| |
| |
| ''([[wikipedia:Beta1-adrenergic agonist|β1アゴニスト]])''
| |
|
| |
| *[[ドブタミン]]
| |
| *[[イソプレナリン]]
| |
| *[[ノルアドレナリン]]
| |
|
| |
| |
| |
| ''([[wikipedia:ja:交感神経β受容体遮断薬|β1アンタゴニスト]])''
| |
|
| |
| *[[メトプロロール]]
| |
| *[[アテノロール]]
| |
|
| |
| |-
| |
| | [[Beta-2 adrenergic receptor|β<sub>2</sub>]]
| |
| | [[イソプレナリン]] > [[アドレナリン]] >> [[ノルアドレナリン]]
| |
| | 平滑筋弛緩
| |
| | [[Gs alpha subunit|G<sub>s</sub>]]: [[アデニル酸シクラーゼ]]活性化、[[サイクリックAMP|cAMP]]上昇 ([[Gi alpha subunit|Gi]]と共役することもある)
| |
| | style="white-space:nowrap" |
| |
| ''([[wikipedia:ja:交感神経β2受容体作動薬|β2アゴニスト]])''
| |
|
| |
| *[[サルブタモール]]
| |
| *[[ビトルテロール]]
| |
| *[[ホルモテロール]]
| |
| *[[イソプレナリン]]
| |
| *[[アイロミール]]
| |
| *[[メタプロテレノール]]
| |
| *[[サルメテロール]]
| |
| *[[テルブタリン]]
| |
| *[[リトドリン]]
| |
|
| |
| |
| |
| ''([[wikipedia:ja:交感神経β受容体遮断薬|β2アンタゴニスト]])''
| |
|
| |
| *[[ブトキサミン]]
| |
| *[[プロプラノロール]]
| |
|
| |
| |-
| |
| | [[Beta-3 adrenergic receptor|β<sub>3</sub>]]
| |
| | [[イソプレナリン]] = [[ノルアドレナリン]] > [[アドレナリン]]
| |
| | [[wikipedia:ja:脂肪|脂肪]]代謝亢進、[[wikipedia:ja:脂肪|膀胱排尿筋]]弛緩
| |
| | [[Gs alpha subunit|G<sub>s</sub>]]: [[アデニル酸シクラーゼ]]活性化、[[サイクリックAMP|cAMP]]上昇
| |
| |
| |
| *[[L-796568]]
| |
| *[[アミベグロン]]
| |
| *[[ソラベグロン]]
| |
|
| |
| |
| |
| *[[SR 59230A]]
| |
|
| |
| |}
| |
|
| |
| '''表 アドレナリン性受容体''' Wikipedia項目[[wikipedia:Adrenergic Receptor|Adrenergic Receptor]]から翻訳、修正の上転載。 <sup>†</sup>α<sub>1C</sub>受容体と呼ばれる物は、存在しない。
| |
|
| |
| == 主たる投射系 ==
| |
|
| |
| 中枢神経系<br> 脳におけるノルアドレナリン作動性の神経細胞群は、主に延髄(medulla)、橋(pons)に存在し、A1-A7に分けられている。
| |
|
| |
| *'''A1'''、'''A2''':A1は髄質の腹外側に位置し、A2は背側に位置する。共に[[視床下部]]に上行性投射をし、ホルモン循環器系やホルモン内分泌系の調節を行う。
| |
| *'''A5'''、'''A7''':橋の腹外側に位置し、脊髄へ投射し、自律神経反射や、痛覚の調節を行う。
| |
| *'''A6''':青斑核(locus ceruleus)と呼ばれる。橋の背側に位置し、最も主要なノルアドレナリン作動性神経細胞の核である。青斑核からは、[[大脳皮質]]、[[視床]]、視床下部、[[小脳]]、[[中脳]]、[[脊髄]]、など脳のほぼ全域にわたって投射している(図2:文献<ref name="ref34"><pubmed> 756202</pubmed></ref>より許可を得て改変)。
| |
|
| |
| [[自律神経系]]のうちの[[交感神経]]系では、[[節後神経]]細胞がノルアドレナリン作動性であり、脊髄中の[[節前神経]]細胞より[[アセチルコリン]]性の入力を受け、ノルアドレナリン性の出力を内臓器官に与える。その結果、[[wikipedia:ja:血管|血管]]の収縮、[[wikipedia:ja:血圧|血圧]]の上昇、[[wikipedia:ja:心拍数|心拍数]]の増加、などを引き起こす。
| |
|
| |
| [[Image:NEprojection.jpg|thumb|400px|'''図2 青斑核からのノルアドレナリン投射経路''']]
| |
|
| |
| == 中枢神経系におけるノルアドレナリンの機能 ==
| |
|
| |
| === 覚醒状態との関係 ===
| |
|
| |
| 青斑核は古くから[[覚醒]]状態に関係していると考えられてきた。1949年、Guiseppe MoruzziとHorace Magounは青斑核を含む脳幹部(紋様体)を刺激すると大脳皮質の脳波が様々に変化することを見いだし<ref name="ref35"><pubmed> 18421835</pubmed></ref>、この部位が脳の覚醒に関係することが示唆された。ラット青斑核神経細胞の発火頻度は、覚醒-睡眠のサイクルに応じて変化し、また継続中の行動を中断するような場合に上昇する<ref name="ref36"><pubmed> 7346592</pubmed></ref><ref name="ref37"><pubmed> 6771765</pubmed></ref>。その後の研究により、ノルアドレナリンは他の重要な機能を持つことが明らかとなってきた(下記)。
| |
|
| |
| === 感覚入力の調節 ===
| |
|
| |
| ノルアドレナリンは、他の神経伝達物質による感覚入力の情報処理を修飾する。[[wikipedia:ja:サル|サル]]の[[聴覚野]]にノルアドレナリンを投与すると、聴覚刺激に対する応答のS/N比が亢進する、すなわち自発的活動(ノイズ)が減少するが、感覚入力依存的活動は維持される<ref name="ref38"><pubmed> 234774</pubmed></ref>。[[wikipedia:ja:ラット|ラット]]の[[体性感覚野]]<ref name="ref39"><pubmed> 7349980</pubmed></ref>や[[海馬]]<ref name="ref40"><pubmed> 178411</pubmed></ref>にても同様の報告がなされている。さらに、発火の応答速度や同期性が向上することがラット体性感覚野<ref name="ref41"><pubmed> 15128405</pubmed></ref>や[[嗅皮質]]<ref name="ref42"><pubmed> 12492432</pubmed></ref>で報告されている。
| |
|
| |
| === 注意 ===
| |
|
| |
| α<sub>2</sub>アドレナリン受容体のアゴニストであるクロニジンを低濃度で局所的に投与すると、軸索終末の自己受容体を介してノルアドレナリンの放出が減少する。この方法を用いて、ラットにて上行性のノルアドレナリン投射を低下させると、[[注意]]を必要とする前頭前野依存的な行動試験の成績が低下する<ref name="ref43"><pubmed> 15830223</pubmed></ref>。サルでは低濃度のclonidineにより[[認知機能]]が低下するが、高濃度では逆に認知機能が亢進し、特に老齢のサルで効果が認められた<ref name="ref44"><pubmed> 2999977</pubmed></ref><ref name="ref45"><pubmed> 17303246</pubmed></ref>。この効果は前頭前野におけるHyperpolarization-activated cyclic nucleotide-gated (HCN) channelsの活性化によると報告されている<ref name="ref46"><pubmed> 17448997</pubmed></ref>。[[wikipedia:ja:ヒト|ヒト]]においてもクロニジンは覚醒状態に依存した効果を示し、視覚的注意に依存する作業を向上させる<ref name="ref47"><pubmed> 10600416</pubmed></ref>。
| |
|
| |
| === 記憶 ===
| |
|
| |
| [[記憶]]の[[固定]]におけるノルアドレナリンの働きは、主に行動薬理学的実験により明らかになってきた。ノルアドレナリンは[[扁桃体]]や海馬において他の神経伝達物質やホルモンなどと相互作用し、[[長期記憶]]の形成を促進する<ref name="ref48"><pubmed> 18704369</pubmed></ref>。また、ノルアドレナリンはβ受容体を介して、記憶固定における遅いステージに関与していると報告されている<ref name="ref49"><pubmed> 10327234</pubmed></ref><ref name="ref50"><pubmed> 15254217</pubmed></ref>。記憶の想起においてもノルアドレナリンが関与している。ラットにおいて、ノルアドレナリン放出の促進や青斑核の電気刺激により記憶の想起が促進される<ref name="ref51"><pubmed> 3345434</pubmed></ref><ref name="ref52"><pubmed> 2543356</pubmed></ref>。ドーパミンβ水酸化酵素の[[コンディショナル・ノックアウトマウス]]を用いた研究でも記憶の想起におけるノルアドレナリンの関与が示されている<ref name="ref53"><pubmed> 15066288</pubmed></ref>。
| |
|
| |
| [[心的外傷後ストレス障害]](PTSD)においてもノルアドレナリンが関わると考えられる<ref name="ref54"><pubmed> 17354267</pubmed></ref>。PTSDに使用される薬剤クロニジンはα2受容体のアゴニスト、プラゾシンはα<sub>1</sub>受容体のアンタゴニストである。PTSDの患者が、当該の出来事を想起し表出する際には、ノルアドレナリンが大量に放出される<ref name="ref54" />。β受容体が記憶の[[再固定]](reconsolidation)に関与するとの知見から、PTSDの治療にβ受容体の阻害が試みられている<ref name="ref55"><pubmed> 16891611</pubmed></ref><ref name="ref56"><pubmed> 18410917</pubmed></ref><ref name="ref57"><pubmed> 17588604</pubmed></ref>。
| |
|
| |
| == 抗うつ薬とノルアドレナリン ==
| |
|
| |
| 気分障害の治療に使われる薬のうち、歴史的に古い[[MAO阻害剤]]、[[三環系抗うつ薬]]はセロトニン系だけでなくノルアドレナリン系を刺激する。近年使用頻度が増えている薬に[[選択的セロトニン再取り込み阻害剤]](SSRI)あるが、これはノルアドレナリン系には作用しない。さらに、[[セロトニン・ノルエピネフリン再取り込み阻害剤]](SNRI)も開発され、これはその名の通り、セロトニン系とノルエピネフリン系の両方を選択的に刺激する。
| |
|
| |
| こうした薬の作用から、うつ状態の原因がセロトニンやノルアドレナリンなどのモノアミンの減少によるのではないかという[[モノアミン仮説]]が生まれた。しかし、これらの薬の治療効果が現れるのは、モノアミン神経伝達が亢進されるよりもずっと遅いことから、この仮説よりももっと複雑なことが起きていると考えられている<ref name="ref58">'''E R Kandel, J H Schwartz, T M Jessell'''<br> Principles of Neural Science, Fourth Edition<br>''Mc Graw Hill (New York)'':2000</ref> <ref name="ref59">'''N R Carlson'''<br> Physiology of Behavior, Tenth Edition<br>''Pearson Education (Boston)'':2009</ref>。
| |
|
| |
| == 関連項目 ==
| |
|
| |
| *[[モノアミン]]
| |
| *[[モノアミン系]]
| |
| *[[モノアミン仮説]]
| |
| *[[カテコールアミン]]
| |
| *[[アドレナリン]]
| |
| *[[青斑核]]
| |
|
| |
| == 参考文献 ==
| |
| <references /> | | <references /> |
「概要」
ノルアドレナリン(noradrenaline, NA)はノルエピネフリン(norepinephrine, NE)とも呼ばれる。モノアミンの一種、またカテコールアミンの一種である。生体内において、神経伝達物質またはホルモンとして働く。生体内ではチロシンから合成される。ノルアドレナリンの受容体はアドレナリン受容体ファミリーであり、三量体Gタンパク質共役型である。末梢神経系では交感神経における神経伝達物質として重要である。中枢神経系では、橋にある青斑核にノルアドレナリン作動性神経細胞が多く存在し、そこからほぼ脳全域に投射している。中枢神経系ノルアドレナリンは覚醒-睡眠やストレスに関する働きをし、注意、記憶や学習などにも影響すると考えられている。
「発見」
1946年、Ulf Svante von Euler(スウェーデン)およびPeter Holtz(ドイツ)により、ノルアドレナリンがほ乳類の交感神経において神経伝達物質として働くことが示された[1] [2]。
「構造」
カテコール基と一級アミノ基をもつ、カテコールアミン神経伝達物質の一種。また、ドーパミン、セロトニン、ヒスタミンなどとともにモノアミン系神経伝達物質のグループを形成する。
「合成」 。他に、副腎髄質中にあるクロム親和性細胞においても合成されている。酵素に関わる酵素は以下の通り。
- チロシン水酸化酵素 tyrosine hydroxylase (TH):EC 1.14.16.2。チロシンよりL-DOPA (L-3,4-dihydroxyphenylalanine)を合成する[3] [4] [5]。反応には、Tetrahydrobiopterin, O2, Fe2+が必要。カテコールアミン合成において、律速段階の酵素であると考えられている。その活性制御は、主にタンパク質の量と、リン酸化による。全てのカテコールアミン産生細胞に存在する。補因子であるTetrahydrobiopterinはGTPより合成される。律速酵素はGTP cyclohydrolase Iである[6]。
- 芳香族アミノ酸脱炭酸酵素 aromatic L-amino acid decarboxylase (AADC):芳香族アミノ酸脱炭酸酵素 aromatic L-amino acid decarboxylase (AADC):EC 4.1.1.28。L-DOPAよりドーパミンを合成する。他に、この酵素は5-hydroxytryptophanからセロトニン(5-hydroxytryptamine, 5-HT)を合成する反応も触媒する。Pyridoxal phosphateが必要。全てのカテコールアミン産生細胞に存在する[7]。
- ドーパミンβ水酸化酵素 Dopamine β-hydroxylase (DBH):EC 1.14.2.1。ドーパミンよりノルアドレナリンを合成する。アスコルビン酸、O2、Cu2+が必要。ノルアドレナリン、アドレナリン産生細胞のシナプス小胞の中に存在し、シナプス小胞に取り込まれたドーパミンをノルアドレナリンに変換する[8]。
「放出、再取り込み」
ノルアドレナリンの前駆体であるドーパミンは小胞型モノアミントランスポーター(vesicular monoamine transporter, vMAT)によりシナプス小胞内に輸送される。vMAT1は主に副腎のクロム親和性細胞、vMAT2は神経細胞で発現している。vMATはH+との交換輸送によりモノアミンを小胞内に蓄積させる[9]。
ノルアドレナリンの放出は他の神経伝達物質と同様に、神経活動依存的、カルシウム依存的なシナプス小胞のエキソサイトーシスによる。
放出された後、ノルエピネフリントランスポーター(NET、またはノルアドレナリントランスポーター(NAT))により再取り込みされる。他のカテコールアミン同様、細胞外に放出されたノルアドレナリンの量の調節は、この再取込みの寄与が高い[10]。NETはNa+/K+-ATPase依存的で、Na+/Cl-の共輸送によりノルアドレナリンを細胞内に輸送する。またNETはリン酸化により制御される[11]。
「代謝分解」
ノルアドレナリンの代謝分解には次の二つの酵素が重要である。
- モノアミン酸化酵素(monoamine oxidase, MAO):MAOはモノアミンのアミノ基をアルデヒド基に酸化する。MAOはミトコンドリア外膜に局在しに存在し、細胞内のノルアドレナリン(再取込みされたものを含む)の分解に関与する。ただしMAOに比べてvMAT2の方がノルアドレナリンに対する親和性がずっと高いため、シナプス小胞への取り込みの方がMAOによる分解よりも優先されると考えられる[12]。MAOにはMAO-AとMAO-Bがあり、二つの別の遺伝子によりコードされている。MAO-AとMAO-Bはモノアミン作動性神経細胞およびグリア細胞に発現しているが、発現量は細胞の種類により異なり、また動物種によっても違いが見られる[12]。マウス脳のノルアドレナリン作動性神経細胞には主にMAO-Aが発現している[13]。。
- カテコール-O-メチル基転移酵素(catechol-O-methyltransferase, COMT):これはカテコール基のm-水酸基にメチル基を転移させる。腎臓や肝臓に豊富だが、カテコールアミン作動性神経細胞の投射先においても発現している。細胞外で働くと考えられている[14]。
脳においてノルアドレナリンの多くは、MAO、アルデヒド還元酵素、およびCOMTにより3-methoxy-4-hydroxyphenylglycol(MHPG)へ代謝され、さらに3-methoxy-4-hydroxymandelic acid (VMA)となって尿中に排出される[15]。MHPGの硫酸化物も尿中に排出される[15]。
「主たる投射系と機能」
(1) 中枢神経系
脳におけるノルアドレナリン作動性の神経細胞群は、主に髄質、橋に存在し、A1-A7に分けられている。
A1、A2:A1は髄質の腹外側に位置し、A2は背側に位置する。共に視床下部に上行性投射をし、循環器系や内分泌系の調節を行う。
A5、A7:橋の腹外側に位置し、脊髄へ投射し、自律神経反射や、痛覚の調節を行う。
A6:青斑核(Locus Ceruleus)と呼ばれる。橋の背側に位置し、最も主要なノルアドレナリン作動性神経細胞の核である。青斑核からは、大脳皮質、視床、視床下部、小脳、中脳、脊髄、など脳のほぼ全域にわたって投射している。青斑核のノルアドレナリン作動性神経細胞は覚醒状態や不意な環境変化への応答性に関係している[16]。例えば、ラット青斑核神経細胞の発火頻度は、覚醒-睡眠のサイクルに応じて変化し、また継続中の行動を中断するような場合に上昇する[17]。さらに近年、ノルアドレナリンの注意、記憶、学習への関与、またシナプス可塑性への関与が報告されている[16] [18]。これらのことから、ノルアドレナリンの働きは、動物が環境の変化に適応する際に、注意や認知のシフト、そして行動の適応化を早めることであると提唱されている[16]。
(2)自律神経系
自律神経系のうちの交感神経系では、節後神経細胞がノルアドレナリン作動性であり、脊髄中の節前神経細胞よりアセチルコリン性の入力を受け、ノルアドレナリン性の出力を内臓器官に与える。その結果、血管の収縮、血圧の上昇、心拍数の増加、などを引き起こす。
「受容体」
ノルアドレナリンはアドレナリンと共にアドレナリン受容体(adrenergic receptorまたはadrenoceptor)に結合し活性化する。αおよびβのサブファミリーからなる。より細かくは、α1A-α1D、α2A-α2C、β1、β2、β3、から構成されている。いずれも三量体Gタンパク質共役型の受容体である。α1はGq、α2はGi、β1-β3はGsと共役している。
中枢神経系において、ノルアドレナリンは主にα1、α2、そしてβ1受容体を介して作用し、それぞれに異なる影響を与える。さらにノルアドレナリンの働きは、標的細胞における他の入力にも依存するので、複雑である。
末梢神経系において、ノルアドレナリンはα1およびβ1アドレナリン受容体のアゴニストとして作用する。(アドレナリンは、低濃度ではβ1およびβ2アドレナリン受容体に作用し、高濃度ではα1を介した作用が主となる。)
α2アドレナリン受容体はノルアドレナリン軸索終末に存在し(オートレセプター)、ノルアドレナリンの放出を抑制する[19]。
「抗うつ薬とノルアドレナリン」
気分障害の治療に使われる薬のうち、歴史的に古いMAO阻害剤、三環系抗うつ薬はセロトニン系だけでなくノルアドレナリン系を刺激する。近年使用頻度が増えている薬に選択的セロトニン再取り込み阻害剤(SSRI)あるが、これはノルアドレナリン系には作用しない。さらに、セロトニン・ノルエピネフリン再取り込み阻害剤(SNRI)も開発され、これはその名の通り、セロトニン系とノルエピネフリン系の両方を選択的に刺激する。
こうした薬の作用から、うつ状態の原因がセロトニンやノルアドレナリンなどのモノアミンの減少によるのではないかというモノアミン仮説が生まれた。しかし、これらの薬の治療効果が現れるのは、モノアミン神経伝達が亢進されるよりもずっと遅いことから、この仮説よりももっと複雑なことが起きていると考えられている[20] [21]。
- ↑ U S von Euler
A Specific Sympathomimetic Ergone in Adrenergic Nerve Fibres (Sympathin) and its Relations to Adrenaline and Nor-Adrenaline
Acta Physiol., Scand. :1946, 12; 73–97
- ↑ P Holtz
Uber die sympathicomimetische Wirksamkeit von Gehiraex- trakten.
Acta Physiol., Scand. : 1950, 20; 354–362
- ↑
Dunkley, P.R., Bobrovskaya, L., Graham, M.E., von Nagy-Felsobuki, E.I., & Dickson, P.W. (2004).
Tyrosine hydroxylase phosphorylation: regulation and consequences. Journal of neurochemistry, 91(5), 1025-43.
[PubMed:15569247]
[WorldCat]
[DOI]
- ↑
Daubner, S.C., Le, T., & Wang, S. (2011).
Tyrosine hydroxylase and regulation of dopamine synthesis. Archives of biochemistry and biophysics, 508(1), 1-12.
[PubMed:21176768]
[PMC]
[WorldCat]
[DOI]
- ↑
Nagatsu, T. (1989).
The human tyrosine hydroxylase gene. Cellular and molecular neurobiology, 9(3), 313-21.
[PubMed:2575455]
[WorldCat]
[DOI]
- ↑
Thöny, B., Auerbach, G., & Blau, N. (2000).
Tetrahydrobiopterin biosynthesis, regeneration and functions. The Biochemical journal, 347 Pt 1, 1-16.
[PubMed:10727395]
[PMC]
[WorldCat]
- ↑
Berry, M.D., Juorio, A.V., Li, X.M., & Boulton, A.A. (1996).
Aromatic L-amino acid decarboxylase: a neglected and misunderstood enzyme. Neurochemical research, 21(9), 1075-87.
[PubMed:8897471]
[WorldCat]
[DOI]
- ↑
Rush, R.A., & Geffen, L.B. (1980).
Dopamine beta-hydroxylase in health and disease. Critical reviews in clinical laboratory sciences, 12(3), 241-77.
[PubMed:6998654]
[WorldCat]
[DOI]
- ↑
Erickson, J.D., & Varoqui, H. (2000).
Molecular analysis of vesicular amine transporter function and targeting to secretory organelles. FASEB journal : official publication of the Federation of American Societies for Experimental Biology, 14(15), 2450-8.
[PubMed:11099462]
[WorldCat]
[DOI]
- ↑
Xu, F., Gainetdinov, R.R., Wetsel, W.C., Jones, S.R., Bohn, L.M., Miller, G.W., ..., & Caron, M.G. (2000).
Mice lacking the norepinephrine transporter are supersensitive to psychostimulants. Nature neuroscience, 3(5), 465-71.
[PubMed:10769386]
[WorldCat]
[DOI]
- ↑
Mandela, P., & Ordway, G.A. (2006).
The norepinephrine transporter and its regulation. Journal of neurochemistry, 97(2), 310-33.
[PubMed:16539676]
[WorldCat]
[DOI]
- ↑ 12.0 12.1
Youdim, M.B., Edmondson, D., & Tipton, K.F. (2006).
The therapeutic potential of monoamine oxidase inhibitors. Nature reviews. Neuroscience, 7(4), 295-309.
[PubMed:16552415]
[WorldCat]
[DOI]
- ↑
Vitalis, T., Fouquet, C., Alvarez, C., Seif, I., Price, D., Gaspar, P., & Cases, O. (2002).
Developmental expression of monoamine oxidases A and B in the central and peripheral nervous systems of the mouse. The Journal of comparative neurology, 442(4), 331-47.
[PubMed:11793338]
[WorldCat]
[DOI]
- ↑
Chen, J., Song, J., Yuan, P., Tian, Q., Ji, Y., Ren-Patterson, R., ..., & Weinberger, D.R. (2011).
Orientation and cellular distribution of membrane-bound catechol-O-methyltransferase in cortical neurons: implications for drug development. The Journal of biological chemistry, 286(40), 34752-60.
[PubMed:21846718]
[PMC]
[WorldCat]
[DOI]
- ↑ 15.0 15.1 D E Golan, A H Tashjian Jr, E J Armstrong, A W Armstrong
Principles of Pharmacology, Second Edition
Wolters Kluwer Health (Philadelphia):2002
- ↑ 16.0 16.1 16.2
Sara, S.J. (2009).
The locus coeruleus and noradrenergic modulation of cognition. Nature reviews. Neuroscience, 10(3), 211-23.
[PubMed:19190638]
[WorldCat]
[DOI]
- ↑
Aston-Jones, G., & Bloom, F.E. (1981).
Activity of norepinephrine-containing locus coeruleus neurons in behaving rats anticipates fluctuations in the sleep-waking cycle. The Journal of neuroscience : the official journal of the Society for Neuroscience, 1(8), 876-86.
[PubMed:7346592]
[WorldCat]
- ↑
Tully, K., & Bolshakov, V.Y. (2010).
Emotional enhancement of memory: how norepinephrine enables synaptic plasticity. Molecular brain, 3, 15.
[PubMed:20465834]
[PMC]
[WorldCat]
[DOI]
- ↑
Starke, K. (2001).
Presynaptic autoreceptors in the third decade: focus on alpha2-adrenoceptors. Journal of neurochemistry, 78(4), 685-93.
[PubMed:11520889]
[WorldCat]
[DOI]
- ↑ E R Kandel, J H Schwartz, T M Jessell
Principles of Neural Science, Fourth Edition
Mc Graw Hill (New York):2000
- ↑ N R Carlson
Physiology of Behavior, Tenth Edition
Pearson Education (Boston):2009

