「ボツリヌス毒素」の版間の差分
Tomokokohda (トーク | 投稿記録) 細 →分類 |
|||
| (3人の利用者による、間の8版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0077838 幸田 知子]、[http://researchmap.jp/read0077839 小崎 俊司]</font><br> | <font size="+1">[http://researchmap.jp/read0077838 幸田 知子]、[http://researchmap.jp/read0077839 小崎 俊司]</font><br> | ||
''大阪府立大学 大学院生命環境科学研究科 獣医学専攻''<br> | ''大阪府立大学 大学院生命環境科学研究科 獣医学専攻''<br> | ||
DOI XXXX/XXXX 原稿受付日:2014年4月15日 原稿完成日:2014年月日<br> | |||
担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | 担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | ||
</div> | </div> | ||
| 34行目: | 34行目: | ||
==分類== | ==分類== | ||
ボツリヌス菌は産生する神経毒素活性を持つ毒素の抗原性により分類されA〜G型の7型がある。ヒトのボツリヌス症は、主としてA、BおよびE型により起こり、稀にF型による事例が報告されている。わが国では1951年「[[wj:飯寿司|いずし]]」を原因食品とするE型菌による[[wj:食中毒|食中毒]]が初めて報告され、その後北海道、東北地方を中心に中毒の発生が多い。アメリカ、カリフォルニア州で1歳未満、特に生後2週から3ヶ月の乳児に麻痺症状を呈する患者が多数発生したことを契機として、1976年には、乳児の消化管内で菌の増殖にともなう毒素産生によって起こる乳児ボツリヌス症が確認された<ref name=ref1><pubmed>62164</pubmed></ref>。本症は北アメリカ以外に、南アメリカ、ヨーロッパ、日本、オーストラリアの各地で発生が報告されている。 | ボツリヌス菌は産生する神経毒素活性を持つ毒素の抗原性により分類されA〜G型の7型がある。ヒトのボツリヌス症は、主としてA、BおよびE型により起こり、稀にF型による事例が報告されている。わが国では1951年「[[wj:飯寿司|いずし]]」を原因食品とするE型菌による[[wj:食中毒|食中毒]]が初めて報告され、その後北海道、東北地方を中心に中毒の発生が多い。アメリカ、カリフォルニア州で1歳未満、特に生後2週から3ヶ月の乳児に麻痺症状を呈する患者が多数発生したことを契機として、1976年には、乳児の消化管内で菌の増殖にともなう毒素産生によって起こる乳児ボツリヌス症が確認された<ref name=ref1><pubmed>62164</pubmed></ref>。本症は北アメリカ以外に、南アメリカ、ヨーロッパ、日本、オーストラリアの各地で発生が報告されている。 | ||
2013年には、G型毒素が発見されて以来、約40年ぶりとなる新型ボツリヌス毒素(H型毒素)産生菌が、米国の乳児ボツリヌス症患者から分離された<ref name=ref02><pubmed>24106296</pubmed></ref>。この菌は、B型とH型毒素の2種類を産生する株(Bh型)であり、産生毒素は、A型~G型の抗毒素血清に中和されなかった。また、[[wj:二重免疫拡散試験|二重免疫拡散試験]]、毒素アミノ酸配列比較からも、既存のA型~G型毒素とは異なる型であると考えられた。アミノ酸配列から軽鎖領域はF型毒素と類似し、重鎖C末端領域はA型毒素と類似している<ref name=ref03><pubmed>24106295</pubmed></ref>。しかしながら、いずれの領域も毒素の中和とは関係ないことから新規の毒素型と判断された。H型毒素を単独で産生する株が発見されていないことから、複数の毒素を産生する株も含めて、今後慎重な型別をする必要がある。 | 2013年には、G型毒素が発見されて以来、約40年ぶりとなる新型ボツリヌス毒素(H型毒素)産生菌が、米国の乳児ボツリヌス症患者から分離された<ref name=ref02><pubmed>24106296</pubmed></ref>。この菌は、B型とH型毒素の2種類を産生する株(Bh型)であり、産生毒素は、A型~G型の抗毒素血清に中和されなかった。また、[[wj:二重免疫拡散試験|二重免疫拡散試験]]、毒素アミノ酸配列比較からも、既存のA型~G型毒素とは異なる型であると考えられた。アミノ酸配列から軽鎖領域はF型毒素と類似し、重鎖C末端領域はA型毒素と類似している<ref name=ref03><pubmed>24106295</pubmed></ref>。しかしながら、いずれの領域も毒素の中和とは関係ないことから新規の毒素型と判断された。H型毒素を単独で産生する株が発見されていないことから、複数の毒素を産生する株も含めて、今後慎重な型別をする必要がある。 | ||
C2毒素は、ボツリヌス菌が産生する2成分毒素であるが、ボツリヌス神経毒素とは構造および生物活性が全く異なる。細胞内[[アクチン]]を[[ADPリボシル]]化し、アクチンの重合化を妨げ、[[細胞骨格]]を破壊すると考えられている<ref name=ref04><pubmed>3335520</pubmed></ref>。 | C2毒素は、ボツリヌス菌が産生する2成分毒素であるが、ボツリヌス神経毒素とは構造および生物活性が全く異なる。細胞内[[アクチン]]を[[ADPリボシル]]化し、アクチンの重合化を妨げ、[[細胞骨格]]を破壊すると考えられている<ref name=ref04><pubmed>3335520</pubmed></ref>。 | ||
C3酵素は、C型菌が産生する第3番目の酵素、C3毒素として報告されたが、C3毒素はC1(神経毒素)やC2毒素のような致死活性はないため、C3酵素と呼ばれる。C3酵素の分子レベルの活性は、ADPリボシル化による[[Rhoファミリー低分子量Gタンパク質]]の不活化である<ref name=ref05><pubmed>3805032</pubmed></ref>。 | C3酵素は、C型菌が産生する第3番目の酵素、C3毒素として報告されたが、C3毒素はC1(神経毒素)やC2毒素のような致死活性はないため、C3酵素と呼ばれる。C3酵素の分子レベルの活性は、ADPリボシル化による[[Rhoファミリー低分子量Gタンパク質]]の不活化である<ref name=ref05><pubmed>3805032</pubmed></ref>。 | ||
| 59行目: | 57行目: | ||
|- | |- | ||
| rowspan="2" | | | rowspan="2" | | ||
| colspan="7" style="text-align:center" | ''' | | colspan="7" style="text-align:center" | '''種''' | ||
|- | |- | ||
| 67行目: | 65行目: | ||
| style="text-align:center" | '''''C. tetani''''' | | style="text-align:center" | '''''C. tetani''''' | ||
|- | |- | ||
| ''' | | '''グループ''' | ||
| style="text-align:center" | I | | style="text-align:center" | I | ||
| style="text-align:center" | II | | style="text-align:center" | II | ||
| 85行目: | 83行目: | ||
| style="text-align:center" | TeNT | | style="text-align:center" | TeNT | ||
|- | |- | ||
| '''タンパク質分解性<br> | | '''タンパク質分解性<br>ゼラチン融解''' | ||
| style="text-align:center" | + | | style="text-align:center" | + | ||
| style="text-align:center" | - | | style="text-align:center" | - | ||
| 103行目: | 101行目: | ||
| style="text-align:center" | - | | style="text-align:center" | - | ||
|- | |- | ||
| ''' | | '''リパーゼ活性''' | ||
| style="text-align:center" | + | | style="text-align:center" | + | ||
| style="text-align:center" | + | | style="text-align:center" | + | ||
| 121行目: | 119行目: | ||
| style="text-align:center" | 37℃ | | style="text-align:center" | 37℃ | ||
|- | |- | ||
| ''' | | '''芽胞耐熱限界温度''' | ||
| style="text-align:center" | 112℃ | | style="text-align:center" | 112℃ | ||
| style="text-align:center" | 80℃ | | style="text-align:center" | 80℃ | ||
| 153行目: | 151行目: | ||
===成人腸管定着性ボツリヌス症=== | ===成人腸管定着性ボツリヌス症=== | ||
1歳以上の子供や成人でも乳児ボツリヌス症と同様に、腸管内で芽胞が発芽、増殖して発病することが報告されている。起因は外科手術や[[wj:抗菌剤|抗菌剤]]の投与によって | 1歳以上の子供や成人でも乳児ボツリヌス症と同様に、腸管内で芽胞が発芽、増殖して発病することが報告されている。起因は外科手術や[[wj:抗菌剤|抗菌剤]]の投与によって[wj:腸管細菌叢|腸管細菌叢]]が変化することによると考えられている。 | ||
[[Image:ボツリヌス毒素4.jpg|thumb|300px|'''図1. ボツリヌス毒素の構造'''<br>M毒素は、1分子の神経毒素と1分子の血球凝集活性のない無毒成分(non-toxic non-HA:NTHA)から構成されている。A, B, C, D型のNTHAは、酵素によりN末端側が切断されるが、E, F型菌では、その部位近傍の33残基が欠損している。L毒素はM毒素にHAが結合している。HAは4つのサブコンポーネント(HA-52, HA-35, HA-20, HA-15)で構成され、型により、多少分子量が異なる。LL毒素は、2分子のL毒素がHA-35を介して結合している。図はA型毒素の構成成分を記載している。神経毒素は血球凝集活性の有無にかかわらず、生体内の弱アルカリ条件下で解離し、神経毒素が作用部位に到達すると考えられている。<ref><pubmed>8521962</pubmed></ref>]] | [[Image:ボツリヌス毒素4.jpg|thumb|300px|'''図1. ボツリヌス毒素の構造'''<br>M毒素は、1分子の神経毒素と1分子の血球凝集活性のない無毒成分(non-toxic non-HA:NTHA)から構成されている。A, B, C, D型のNTHAは、酵素によりN末端側が切断されるが、E, F型菌では、その部位近傍の33残基が欠損している。L毒素はM毒素にHAが結合している。HAは4つのサブコンポーネント(HA-52, HA-35, HA-20, HA-15)で構成され、型により、多少分子量が異なる。LL毒素は、2分子のL毒素がHA-35を介して結合している。図はA型毒素の構成成分を記載している。神経毒素は血球凝集活性の有無にかかわらず、生体内の弱アルカリ条件下で解離し、神経毒素が作用部位に到達すると考えられている。<ref><pubmed>8521962</pubmed></ref>]] | ||
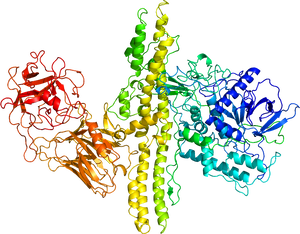
[[ファイル:Botulinus toxin 1.png|right|thumb|250px|'''図2. ボツリヌス神経毒素の構造''']] | [[ファイル:Botulinus toxin 1.png|right|thumb|250px|'''図2. ボツリヌス神経毒素の構造''']] | ||
==構造== | ==構造== | ||
===複合体毒素=== | ===複合体毒素=== | ||
| 167行目: | 164行目: | ||
===神経毒素=== | ===神経毒素=== | ||
神経毒素は菌体内で1本鎖ポリペプチドの形(intact form)で産生され、培養液中あるいは[[wj:消化管|消化管]]内で[[wj:トリプシン|トリプシン]]などの[[タンパク質分解酵素]]により、分子内に解裂(nicking)が生じ分子量5万の軽鎖(light chain)と分子量10万の重鎖(heavy chain)がジスルフィド(SS)結合で結ばれた2本鎖フラグメント構造(nicked | 神経毒素は菌体内で1本鎖ポリペプチドの形(intact form)で産生され、培養液中あるいは[[wj:消化管|消化管]]内で[[wj:トリプシン|トリプシン]]などの[[タンパク質分解酵素]]により、分子内に解裂(nicking)が生じ分子量5万の軽鎖(light chain)と分子量10万の重鎖(heavy chain)がジスルフィド(SS)結合で結ばれた2本鎖フラグメント構造(nicked form)へ変化する。第Ⅰ群菌(これはA-Gの分類とどのような関係にあるのでしょうか)では自己の産生するトリプシン様酵素が神経毒素のnicked formへの変化に関与している。神経毒素はこの分子内解裂による変化により数倍から数百倍に毒力が上昇するが、この活性化現象はタンパク質非分解性B、E型菌に著明に認められる。軽鎖と重鎖はnicked formの神経毒素から還元処理により分離することができる。重鎖はさらに分子量のほぼ等しいN末端領域(H<small>N</small>)とC末端流域(H<small>C</small>)の機能の異なる2つのドメインに分けられる<ref name=ref3><pubmed>2824382</pubmed></ref>。 | ||
===無毒成分=== | ===無毒成分=== | ||
| 182行目: | 179行目: | ||
シナプス小胞内の神経伝達物質を放出するには[[シナプス前]]膜との融合が必要であり、その一連の過程で[[SNARE|SNAP(soluble NSF attachment protein)受容体]](SNARE)と呼ばれタンパク質群([[VAMP]]/[[シナプトブレビン]]、[[SNAP-25]]、[[シンタキシン]])が関与している。軽鎖は亜鉛依存性プロテアーゼ活性を持ち、これらSNAREタンパク質のいずれかを分解する<ref name=ref9><pubmed>22289120</pubmed></ref>(図3)。B, D, F, G型毒素はVAMP/シナプトブレビンを(図4)、A, E型毒素はSNAP-25を、C型毒素はSNAP-25とシンタキシンを、それぞれ切断する<ref name=ref10936621><pubmed>10936621</pubmed></ref>。その結果、シナプス小胞と前膜の融合が起こらず神経伝達物質の放出が阻止される。軽鎖の持つプロテアーゼ活性は基質特異性が高く、これがボツリヌス毒素の持つ神経に対する高い毒性を反映している。 | シナプス小胞内の神経伝達物質を放出するには[[シナプス前]]膜との融合が必要であり、その一連の過程で[[SNARE|SNAP(soluble NSF attachment protein)受容体]](SNARE)と呼ばれタンパク質群([[VAMP]]/[[シナプトブレビン]]、[[SNAP-25]]、[[シンタキシン]])が関与している。軽鎖は亜鉛依存性プロテアーゼ活性を持ち、これらSNAREタンパク質のいずれかを分解する<ref name=ref9><pubmed>22289120</pubmed></ref>(図3)。B, D, F, G型毒素はVAMP/シナプトブレビンを(図4)、A, E型毒素はSNAP-25を、C型毒素はSNAP-25とシンタキシンを、それぞれ切断する<ref name=ref10936621><pubmed>10936621</pubmed></ref>。その結果、シナプス小胞と前膜の融合が起こらず神経伝達物質の放出が阻止される。軽鎖の持つプロテアーゼ活性は基質特異性が高く、これがボツリヌス毒素の持つ神経に対する高い毒性を反映している。 | ||
一方、脳[[シナプトソーム]]や[[初代神経培養細胞]]に対する毒作用解析から、神経毒素は[[シナプス前膜]]に存在する特異的な受容体に結合後、神経細胞内に侵入し、アセチルコリン以外の種々の神経伝達物質の放出も阻害することが明らかになっている<ref name=ref4><pubmed>19264088</pubmed></ref> | 一方、脳[[シナプトソーム]]や[[初代神経培養細胞]]に対する毒作用解析から、神経毒素は[[シナプス前膜]]に存在する特異的な受容体に結合後、神経細胞内に侵入し、アセチルコリン以外の種々の神経伝達物質の放出も阻害することが明らかになっている<ref name=ref4><pubmed>19264088</pubmed></ref>。臨床的に中枢神経作用があまり問題にならないのは、テタヌス毒素とは異なり、ボツリヌス毒素は脳血液関門を通らないためと考えられている。 | ||
==治療== | ==治療== | ||
2014年5月9日 (金) 09:49時点における版
幸田 知子、小崎 俊司
大阪府立大学 大学院生命環境科学研究科 獣医学専攻
DOI XXXX/XXXX 原稿受付日:2014年4月15日 原稿完成日:2014年月日
担当編集委員:林 康紀(独立行政法人理化学研究所 脳科学総合研究センター)
英語名:botulinum toxin 独:Botulinumtoxin 仏:toxine botulique
ボツリヌス神経毒素は偏性嫌気性有芽胞菌であるボツリヌス菌Clostridium botulinumによって産生される致死性の高いタンパク質毒素である。亜鉛依存性プロテアーゼ活性を持ち、神経筋結合部や自律神経終末においてSNAREタンパク質を分解することで神経伝達物質であるアセチルコリンの放出を阻害し、弛緩性の麻痺を引き起こす。菌は産生する毒素の抗原性の違いにより、A〜Gの毒素型に分類され、異なった基質特異性を持つ。近年、欧米を中心に毒素の高い麻痺活性を利用し、ジストニアや痙縮などの筋緊張の亢進症に対し、治療薬として臨床応用されている。
| Peptidase_M27 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
A型毒素の結晶構造 | |||||||||
| Identifiers | |||||||||
| Symbol | ? | ||||||||
| Pfam | PF01742 | ||||||||
| Pfam clan | CL0126 | ||||||||
| PROSITE | PDOC00129 | ||||||||
| MEROPS | M27 | ||||||||
| SCOP | 3bta | ||||||||
| SUPERFAMILY | 3bta | ||||||||
| |||||||||
背景
ボツリヌス菌は、芽胞の形で自然界に広く分布し、産生する毒素によりヒトを含む種々の哺乳動物や鳥類が特異な神経症状を呈するボツリヌス症を起こす。古くから本菌は食品内で増殖し、その際産生する毒素をヒトが摂取することにより典型的な毒素型食中毒を起こすことが知られていた。ボツリヌス症(botulism)の語源は、原因食品である「ソーセージ」のラテン語である「botulus」に由来する。
分類
ボツリヌス菌は産生する神経毒素活性を持つ毒素の抗原性により分類されA〜G型の7型がある。ヒトのボツリヌス症は、主としてA、BおよびE型により起こり、稀にF型による事例が報告されている。わが国では1951年「いずし」を原因食品とするE型菌による食中毒が初めて報告され、その後北海道、東北地方を中心に中毒の発生が多い。アメリカ、カリフォルニア州で1歳未満、特に生後2週から3ヶ月の乳児に麻痺症状を呈する患者が多数発生したことを契機として、1976年には、乳児の消化管内で菌の増殖にともなう毒素産生によって起こる乳児ボツリヌス症が確認された[1]。本症は北アメリカ以外に、南アメリカ、ヨーロッパ、日本、オーストラリアの各地で発生が報告されている。
2013年には、G型毒素が発見されて以来、約40年ぶりとなる新型ボツリヌス毒素(H型毒素)産生菌が、米国の乳児ボツリヌス症患者から分離された[2]。この菌は、B型とH型毒素の2種類を産生する株(Bh型)であり、産生毒素は、A型~G型の抗毒素血清に中和されなかった。また、二重免疫拡散試験、毒素アミノ酸配列比較からも、既存のA型~G型毒素とは異なる型であると考えられた。アミノ酸配列から軽鎖領域はF型毒素と類似し、重鎖C末端領域はA型毒素と類似している[3]。しかしながら、いずれの領域も毒素の中和とは関係ないことから新規の毒素型と判断された。H型毒素を単独で産生する株が発見されていないことから、複数の毒素を産生する株も含めて、今後慎重な型別をする必要がある。
C2毒素は、ボツリヌス菌が産生する2成分毒素であるが、ボツリヌス神経毒素とは構造および生物活性が全く異なる。細胞内アクチンをADPリボシル化し、アクチンの重合化を妨げ、細胞骨格を破壊すると考えられている[4]。
C3酵素は、C型菌が産生する第3番目の酵素、C3毒素として報告されたが、C3毒素はC1(神経毒素)やC2毒素のような致死活性はないため、C3酵素と呼ばれる。C3酵素の分子レベルの活性は、ADPリボシル化によるRhoファミリー低分子量Gタンパク質の不活化である[5]。
ボツリヌス菌の生化学的性状
ボツリヌス菌の生化学的な性状は、産生する毒素型とは無関係で4群に分類することができる。
第I群菌には全てのA型菌とタンパク質分解性のB、F型菌が属し、最も耐熱性の高い芽胞を形成する。第I群菌とClostridium sporogenesとは毒素産生性以外の性状で区別することは困難である。
第II群菌には全てのE型菌とタンパク質非分解性のB、 F型菌が属し、比較的易熱性の芽胞を形成する。発育至適温度も最も低い。菌はタンパク質分解酵素を欠くため、毒素は毒性が低いか全く毒性のない前駆体の形で産生される。
第III群としてC、D型菌が属している。本菌は、増殖に対して酸素許容量が低く、高い嫌気条件を必要とする。C. novyiが極めて類似した性状を示す。
第IV群菌に属するG型菌は他の群と異なり、糖非分解性でリパーゼを産生しない。芽胞形成能が低く、また形成された芽胞の大部分は易熱性である。G型菌と遺伝学的に相同性のある菌群に対してC. argentinenseの名称が提唱されている。欧米で発生した乳児ボツリヌス症から分類された菌の中で、C. butyricum、C. baratiiがそれぞれE、F型と非常に類似した毒素を産生することが分かっている。
| 種 | |||||||
| C. botulinum | C. butylicum | C. baratii | C. tetani | ||||
| グループ | I | II | III | IV | |||
| 毒素型 | A, B, F | B, E, F | C, D | G | E | F | TeNT |
| タンパク質分解性 ゼラチン融解 |
+ | - | ± | + | - | - | - |
| 糖分解性 | + | + | + | - | - | + | - |
| リパーゼ活性 | + | + | + | - | - | - | - |
| 発育至適温度 | 30-37℃ | 25-30℃ | 30-37℃ | 30-37℃ | 30-37℃ | 30-45℃ | 37℃ |
| 芽胞耐熱限界温度 | 112℃ | 80℃ | 104℃ | 104℃ | |||
| 関連するクロストリジウム属 | C. sporogenes | C. novyi | C. subterminale | ||||
臨床症状
現在、ボツリヌス中毒は発病機序により食餌性ボツリヌス症(foodborne botulism)、乳児ボツリヌス症(infant botulism)、創傷ボツリヌス症(wound botulism)、および成人腸管定着性ボツリヌス症(adult colonization botulism)の4型に分類されている。
食餌性ボツリヌス症
症状は通常喫食後12~72時間後に出現するが、14日後に発症した例もある。一般的には潜伏期が短いほど重篤な症状を示すことが多い。食餌性ボツリヌス症の場合(特にE型中毒)、特徴的な神経症状が出現する前に嘔気、嘔吐を呈することがある。これらは乳児ボツリヌス症や創傷ボツリヌス症では見られないことから非特異的な症状と思われる。その後、脱力感、倦怠感、めまいなどの症状が現れ、さらに視力障害(弱視、複視、眼瞼下垂)、発声困難、嚥下困難、口渇、嗄声が現れる。消化器症状としては、一時的な下痢に続く重度の便秘、腹部膨満、腹痛が見られる。他の症状としては、尿閉、血圧低下が見られる。筋麻痺も著明で握力低下、歩行困難になる。体温は正常である。死亡の原因は呼吸失調による。症状は最終的には完全に回復するが、軽度の脱力感、視力障書、便秘などは数か月間続く。致死率は他の食中毒と比べてかなり高い。
乳児ボツリヌス症
乳児の腸管内で芽胞の発芽・増殖に伴って産生された毒素により発症する疾病である。症状は便秘に始まり、吸乳力の低下、全身筋肉緊張の低下が見られる。頚部筋肉の弛緩により頭部が支えられなくなる。泣き声が弱いことも顕著な症状である。顔面が無表情になり、瞳孔散大、眼瞼下垂、対光反射の緩慢などボツリヌス食中毒と同様の症状が現れる。これらの症状は長期間持続し、6週間あるいはそれ以上続くこともある。呼吸障害が生じ重症化すると死に至ることもあるが、一般には食餌性ボツリヌス症と比べて致死率は2 %程度と低い。
創傷ボツリヌス症
患者の創傷部位で芽胞が発芽、増殖し産生された毒素により発症する。米国では麻薬中毒患者の注射痕から菌の感染が起こる事例が多数報告されている。
成人腸管定着性ボツリヌス症
1歳以上の子供や成人でも乳児ボツリヌス症と同様に、腸管内で芽胞が発芽、増殖して発病することが報告されている。起因は外科手術や抗菌剤の投与によって[wj:腸管細菌叢|腸管細菌叢]]が変化することによると考えられている。
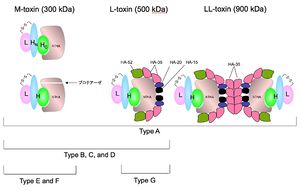
M毒素は、1分子の神経毒素と1分子の血球凝集活性のない無毒成分(non-toxic non-HA:NTHA)から構成されている。A, B, C, D型のNTHAは、酵素によりN末端側が切断されるが、E, F型菌では、その部位近傍の33残基が欠損している。L毒素はM毒素にHAが結合している。HAは4つのサブコンポーネント(HA-52, HA-35, HA-20, HA-15)で構成され、型により、多少分子量が異なる。LL毒素は、2分子のL毒素がHA-35を介して結合している。図はA型毒素の構成成分を記載している。神経毒素は血球凝集活性の有無にかかわらず、生体内の弱アルカリ条件下で解離し、神経毒素が作用部位に到達すると考えられている。[6]
構造
複合体毒素
すべての型の毒素は菌体内で分子量約15万の神経毒素と無毒成分の複合体毒素として、菌融解時に放出される。
複合体毒素は分子量の違いにより、LL毒素(分子量90万)、L毒素(分子量50万)、M毒素(分子量30万)に分けられる(図1)。LL毒素、L毒素の無毒成分は血球凝集活性を持っている。A型菌は3種類(LL、L、M)の毒素、B、C、D型菌は2種類(L、M)の毒素、EおよびF型菌はM毒素、G型菌はL毒素のそれぞれ1種類のみを産生する[7]。
弱アルカリ(pH 7.2以上)条件下で神経毒素(図2)と無毒成分に速やかに解離する。このため食品内で産生された毒素は複合体の形で経口的に摂取され、小腸上部で吸収された後、リンパ管内あるいは血中で神経毒素と無毒成分に解離する。
神経毒素
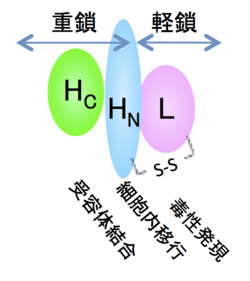
神経毒素は菌体内で1本鎖ポリペプチドの形(intact form)で産生され、培養液中あるいは消化管内でトリプシンなどのタンパク質分解酵素により、分子内に解裂(nicking)が生じ分子量5万の軽鎖(light chain)と分子量10万の重鎖(heavy chain)がジスルフィド(SS)結合で結ばれた2本鎖フラグメント構造(nicked form)へ変化する。第Ⅰ群菌(これはA-Gの分類とどのような関係にあるのでしょうか)では自己の産生するトリプシン様酵素が神経毒素のnicked formへの変化に関与している。神経毒素はこの分子内解裂による変化により数倍から数百倍に毒力が上昇するが、この活性化現象はタンパク質非分解性B、E型菌に著明に認められる。軽鎖と重鎖はnicked formの神経毒素から還元処理により分離することができる。重鎖はさらに分子量のほぼ等しいN末端領域(HN)とC末端流域(HC)の機能の異なる2つのドメインに分けられる[8]。
無毒成分
神経毒素を胃酸、あるいはペプシンなどの消化酵素による分解から保護し、腸管上皮細胞への吸収を促進する働きがあることから、ボツリヌス毒素が食餌性ボツリヌス症を起こす経口毒の活性を持つために重要な役割を果たしていると考えられている。
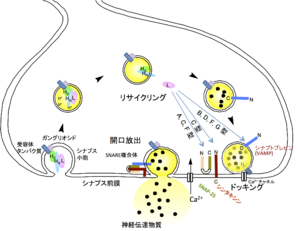
神経毒素は重鎖C末端領域を介して受容体に結合し、receptor -mediated endocytosisにより、神経細胞内に侵入する。エンドソーム内の酸性化に伴い、HCの構造変化とHNによるエンドソーム膜のチャネル形成により、軽鎖が細胞質内に移行する。軽鎖は毒素型特異的なSNAREタンパク質群を切断することにより、シナプス小胞のシナプス前膜への融合が阻止され、神経伝達物質放出の阻害が起こると考えられている。
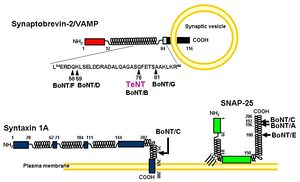
クロストリジウム属毒素であるテタヌス毒素とボツリヌス毒素について示す
相川義勝、高森茂雄らによるテタヌス毒素の項目より引用
作用機能
シナプス終末への侵入
神経毒素は生体内ではコリン作動性末梢神経に作用し、アセチルコリンの遊離を阻害することにより麻痺を引き起こすと考えられている。神経毒素は温度非依存的に重鎖、特にHCを介して神経細胞膜表面にある受容体に結合する。A型およびB型神経毒素の受容体はそれぞれシナプス小胞膜に存在するタンパク質 SV2(synaptic vesicle protein 2)[9]とシナプトタグミン[10]であることがわかった。これらの受容体タンパク質は、神経細胞膜に豊富に存在する糖脂質であるガングリオシド存在下で、より高い毒素結合活性を持つ[11]。シナプス小胞は神経伝達物質を放出後、再び細胞内に取り込まれるが受容体に結合した毒素は、この小胞のリサイクリングを巧みに利用することで細胞内に侵入する[12]。重鎖HNには毒素の型に共通した構造が存在し、この部分が膜にチャネルを形成することで軽鎖の細胞質内への移行が起こると考えられている。
SNARE分解活性
シナプス小胞内の神経伝達物質を放出するにはシナプス前膜との融合が必要であり、その一連の過程でSNAP(soluble NSF attachment protein)受容体(SNARE)と呼ばれタンパク質群(VAMP/シナプトブレビン、SNAP-25、シンタキシン)が関与している。軽鎖は亜鉛依存性プロテアーゼ活性を持ち、これらSNAREタンパク質のいずれかを分解する[13](図3)。B, D, F, G型毒素はVAMP/シナプトブレビンを(図4)、A, E型毒素はSNAP-25を、C型毒素はSNAP-25とシンタキシンを、それぞれ切断する[14]。その結果、シナプス小胞と前膜の融合が起こらず神経伝達物質の放出が阻止される。軽鎖の持つプロテアーゼ活性は基質特異性が高く、これがボツリヌス毒素の持つ神経に対する高い毒性を反映している。
一方、脳シナプトソームや初代神経培養細胞に対する毒作用解析から、神経毒素はシナプス前膜に存在する特異的な受容体に結合後、神経細胞内に侵入し、アセチルコリン以外の種々の神経伝達物質の放出も阻害することが明らかになっている[15]。臨床的に中枢神経作用があまり問題にならないのは、テタヌス毒素とは異なり、ボツリヌス毒素は脳血液関門を通らないためと考えられている。
治療
治療で最も重要なことは迅速な呼吸管理(気道確保と人工呼吸)である。また、消化管に滞留している内容物中の菌や毒素を体外に排除するために、胃洗浄や浣腸は有効とされている。しかし、大半の患者は便秘のために浣腸によっても排便は困難であることが知られ、特に、乳児ボツリヌス症では糞便中に高濃度の毒素が存在しているため腸粘膜の損傷に注意を払う必要がある。ボツリヌス抗毒素血清による治療は、特に早期治療に有効とされるが、食餌性ボツリヌス症と乳児ボツリヌス症では適応が大きく異なる。食餌性ボツリヌス症では治療用ウマ抗毒素製剤が用いられる。抗毒素治療は、死亡率を低下させるばかりでなく、麻痺などの症状の軽減に有効とされている。一方、乳児ボツリヌス症は死亡率が低く、患者血清中に毒素を証明することが少なく、異種蛋白であるウマ抗毒素の使用を避けるために、一般的には用いられていない。
発症機序から、乳児ボツリヌス症と創傷性ボツリヌス症は抗生物質投与の対象と考えられる。創傷性ボツリヌス症が多発している米国では抗生物質の投与が推奨されている。乳児ボツリヌス症では抗生物質の投与効果が不明なため、通常は投与されず、二次感染(誤嚥性肺炎など)を併発した場合にのみ投与される。菌の増殖抑制にはペニシリンの投与が有効である。アミノグルコシド系およびマグネシウムを含む浣腸薬は神経—筋障害を増強させる恐れがあるため禁忌である。
神経毒素の臨床応用
筋弛緩作用を有するボツリヌス毒素の医薬品としての応用は、まず斜視の治療に用いられて以来、眼瞼痙攣、痙性斜頚、ジストニア、痛みならびに泌尿器疾患など多岐にわたる治療に利用されている[16] [17] [18]。微量の使用で治療効果が高いボツリヌス毒素製剤は、現在では神経疾患の治療薬として不可欠なものとなりつつある。
関連項目
参考文献
- ↑
Midura, T.F., & Arnon, S.S. (1976).
Infant botulism. Identification of Clostridium botulinum and its toxins in faeces. Lancet (London, England), 2(7992), 934-6. [PubMed:62164] [WorldCat] [DOI] - ↑
Barash, J.R., & Arnon, S.S. (2014).
A novel strain of Clostridium botulinum that produces type B and type H botulinum toxins. The Journal of infectious diseases, 209(2), 183-91. [PubMed:24106296] [WorldCat] [DOI] - ↑
Dover, N., Barash, J.R., Hill, K.K., Xie, G., & Arnon, S.S. (2014).
Molecular characterization of a novel botulinum neurotoxin type H gene. The Journal of infectious diseases, 209(2), 192-202. [PubMed:24106295] [WorldCat] [DOI] - ↑
Vandekerckhove, J., Schering, B., Bärmann, M., & Aktories, K. (1988).
Botulinum C2 toxin ADP-ribosylates cytoplasmic beta/gamma-actin in arginine 177. The Journal of biological chemistry, 263(2), 696-700. [PubMed:3335520] [WorldCat] - ↑
Ohashi, Y., & Narumiya, S. (1987).
ADP-ribosylation of a Mr 21,000 membrane protein by type D botulinum toxin. The Journal of biological chemistry, 262(4), 1430-3. [PubMed:3805032] [WorldCat] - ↑
Fujita, R., Fujinaga, Y., Inoue, K., Nakajima, H., Kumon, H., & Oguma, K. (1995).
Molecular characterization of two forms of nontoxic-nonhemagglutinin components of Clostridium botulinum type A progenitor toxins. FEBS letters, 376(1-2), 41-4. [PubMed:8521962] [WorldCat] [DOI] - ↑
Sakaguchi, G. (1982).
Clostridium botulinum toxins. Pharmacology & therapeutics, 19(2), 165-94. [PubMed:6763707] [WorldCat] [DOI] - ↑
Kozaki, S., Ogasawara, J., Shimote, Y., Kamata, Y., & Sakaguchi, G. (1987).
Antigenic structure of Clostridium botulinum type B neurotoxin and its interaction with gangliosides, cerebroside, and free fatty acids. Infection and immunity, 55(12), 3051-6. [PubMed:2824382] [PMC] [WorldCat] - ↑
Dong, M., Yeh, F., Tepp, W.H., Dean, C., Johnson, E.A., Janz, R., & Chapman, E.R. (2006).
SV2 is the protein receptor for botulinum neurotoxin A. Science (New York, N.Y.), 312(5773), 592-6. [PubMed:16543415] [WorldCat] [DOI] - ↑
Nishiki, T., Kamata, Y., Nemoto, Y., Omori, A., Ito, T., Takahashi, M., & Kozaki, S. (1994).
Identification of protein receptor for Clostridium botulinum type B neurotoxin in rat brain synaptosomes. The Journal of biological chemistry, 269(14), 10498-503. [PubMed:8144634] [WorldCat] - ↑ 居原 秀、小崎俊司
細菌性神経毒素とガングリオシド
生体の科学 60:228-233, 2009. - ↑ 小崎俊司、居原 秀
クロストリジウム神経毒素の受容体認識
実験医学 27:1598-1605,2009. - ↑
Yamamoto, H., Ida, T., Tsutsuki, H., Mori, M., Matsumoto, T., Kohda, T., ..., & Ihara, H. (2012).
Specificity of botulinum protease for human VAMP family proteins. Microbiology and immunology, 56(4), 245-53. [PubMed:22289120] [WorldCat] [DOI] - ↑
Rossetto, O., Seveso, M., Caccin, P., Schiavo, G., & Montecucco, C. (2001).
Tetanus and botulinum neurotoxins: turning bad guys into good by research. Toxicon : official journal of the International Society on Toxinology, 39(1), 27-41. [PubMed:10936621] [WorldCat] [DOI] - ↑
Caleo, M., & Schiavo, G. (2009).
Central effects of tetanus and botulinum neurotoxins. Toxicon : official journal of the International Society on Toxinology, 54(5), 593-9. [PubMed:19264088] [WorldCat] [DOI] - ↑
Casale, R., & Tugnoli, V. (2008).
Botulinum toxin for pain. Drugs in R&D, 9(1), 11-27. [PubMed:18095750] [WorldCat] [DOI] - ↑
Lucioni, A., Reynolds, W.S., Rapp, D.E., Katz, M., & Bales, G.T. (2008).
The use of botulinum toxin for treatment of lower urinary tract symptoms. Minerva urologica e nefrologica = The Italian journal of urology and nephrology, 60(2), 93-103. [PubMed:18500224] [WorldCat] - ↑
Truong, D.D., & Jost, W.H. (2006).
Botulinum toxin: clinical use. Parkinsonism & related disorders, 12(6), 331-55. [PubMed:16870487] [WorldCat] [DOI]