「ミエリン関連糖タンパク質」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| (3人の利用者による、間の16版が非表示) | |||
| 1行目: | 1行目: | ||
{{PBB|geneid=4099}} | {{PBB|geneid=4099}} | ||
英語名:Myelin associated | 英語名:Myelin associated glycoprotein | ||
== | == 分子について == | ||
MAGは、分子量約100kDaの[[中枢]]、[[末梢]]の両方の[[ミエリン]]画分に存在する膜糖タンパク質である。ミエリン蛋白の中では比較的マイナーな蛋白であるが、ミエリンに存在する糖画分の約30%がMAG上の糖鎖に由来する。L2/HNK−1抗体で認識される[[wikipedia:JA:抗原|抗原]]構造を有する糖鎖を持つ。細胞外領域は5つの[[免疫]][[グロブリンドメイン]]からなり、膜貫通領域そして細胞内領域を持つ。[[wikipedia:JA:選択的|選択的]][[wikipedia:JA:スプライシング|スプライシング]]による細胞内領域の異なるアイソフォームが存在し、主にL(Large)フォームとS(Small)フォームからなるが、糖付加の違いによる更なるアイソフォームも存在する。発生段階では中枢ではLフォームが主であるが、末梢ではSフォームが主である。アダルトにおいてはSフォームが中枢、末梢の両者で主である<ref><pubmed>1716323</pubmed></ref>。 MAGは別名Siglec-4とも呼ばれSIGLECファミリーに属する[[wikipedia:JA:シアル酸|シアル酸]]に結合する活性を有する蛋白質である事も明らかにされた<ref><pubmed>12464312</pubmed></ref>。In vitroの活性からMAGは細胞接着因子であることが明らかにされ、また、MAGがシュワン細胞がミエリン形成を開始する際の神経の軸索に接する部分の突起の所に局在することから、ミエリン形成における[[アクソン]]ー[[グリア]]相互作用に関与する重要な分子であることが予想されていた<ref><pubmed>10625334</pubmed></ref><ref><pubmed>17241126</pubmed></ref>。 梅森らは、[[チロシンキナーゼ]]のc−fynがL-MAGに結合していて、ミエリン形成の初期にチロシンの[[リン酸化]]がみられること及び、L-MAGをクロスリンクすることによってc-fynが活性化されることを報告し、MAGとfynがミエリン形成に重要であることを示唆していた<ref><pubmed>7509042</pubmed></ref>。 | |||
== 遺伝子クローニングからノックアウトマウスの作製へ == | |||
[[Image:脳科学辞典01.jpg|thumb|right||250px|'''図1 ミエリン形成された神経軸索の模式図''']] | |||
1987年に3つのグループがMAGの[[wikipedia:JA:cDNA|cDNA]]クローニングを行った。少し遅れて日本でも宮武らのグループがヒトのcDNAのクローニングを報告した。 1994年に[[wikipedia:JA:ノックアウトマウス|ノックアウトマウス]]が2つのグループによって報告され、in vitroの結果から予測されたようなドラスティックな異常はみられず、ミエリン形成がほとんど正常におこっていたことから、研究者を非常にがっかりさせた。しかしながら、そのマウスでは[[脱髄]]のあとの回復が遅れていたことから、MAGはおそらく[[神経再生]]においてのミエリン形成には重要なのではないかと考えられた<ref><pubmed>7519026</pubmed></ref><ref><pubmed>7516497</pubmed></ref>。また、MAGノックアウトマウスにおいては別の分子がその機能を代償しているのではないかと考えられた。事実、MAGと[[wikipedia:JA:ガラクト脂質合成酵素|ガラクト脂質合成酵素]](MAGに結合するシアル酸の合成酵素)のダブルノックアウトマウスでは[[ノード]]とパラノードの形成はおこるものの、その構造の維持がおこらないことから、MAGはこのようなミエリン化された神経の構造の維持に重要であると考えられている(図1)<ref><pubmed>11827985</pubmed></ref>。 | |||
== ミエリンインヒビターとしての論争 == | |||
ノックアウトマウスの報告とほぼ同じ頃に驚くべき報告が行われた。Martin Schwabらは彼らの長年の研究からミエリンに神経の成長を抑制する分子が存在すると考え、ミエリンアソシエイティドインヒビターとしてその単離を試みていた。1994年に2つのグループから実はMAGがそのミエリンインヒビターではないかという報告がされたのである<ref><pubmed>7524558</pubmed></ref><ref><pubmed>7522484</pubmed></ref>。一つはモントリオールのAlbert Aguayoの流れを汲むSam Davidのグループとミエリン研究グループの共同研究であり、もう一つはニューヨークのMarie Filbinのグループである。どちらも、データとしては確固たるものであったが、in vitroのデータをもとにしたものであった。それに対して、SchwabのグループはMAGノックアウトマウスを作ったグループと共同で、ノックアウトマウスのミエリンでもまだインヒビターの活性があることから、ミエリンインヒビターはMAGではないという反論の論文をすぐさまだした<ref><pubmed>8845160</pubmed></ref>。 それに対して、Sam Davidのグループは地道にそれに対する反論の論文をだしていき、また、Marie FilbinのグループもMAGの神経成長抑制の活性についての解析の論文をだしていった。そうこうしているうちに、Schwabと一緒に論文を書いていたMAGノックアウトマウスを作製したグループもSchwabを抜きに、MAGノックアウトマウスでは神経再生の促進がみられるという論文をだし、実はMAGもミエリンインヒビターの一つではないかということを示唆していた<ref><pubmed>8663987</pubmed></ref>。 | |||
== | == 実はNogo受容体のリガンドだった == | ||
[[Image:脳科学辞典02.jpg|thumb|right|250px|'''図2 MAGとその受容体によるシグナル系路''']] | |||
Schwabのグループはその後も地道に生化学的に彼らのミエリンインヒビターの精製と同定を進めていた。その彼らの発表した部分アミノ酸配列をもとに2000年に3つのグループがこの分子の同定を発表し、Nogoと呼ばれたこの分子はMAGとは構造的に異なるものであった。その後、2001年に[[Nogo]]のクローニングを行った3つのグループの1つであるSteven StrittmatterのグループによってNogo受容体が同定された。その後、2002年に再び驚くべき報告がなされた。StrittmatterのグループとFilbinのグループが実はMAGもNogo受容体のリガンドであることを明らかにしたのである<ref><pubmed>12160746</pubmed></ref><ref><pubmed>12089450</pubmed></ref>。 また、山下らはMAGの神経成長阻害の活性はp75を介しておこることを示していたが、その数ヶ月後に実はNogo受容体はp75と結合しMAGを含むNogoリガンドは[[p75]]を通じて神経成長阻害を示すことが別の2つのグループによって明らかにされた<ref><pubmed>12426574</pubmed></ref><ref><pubmed>12422217</pubmed></ref>。つまり、ミエリンアソシエイティドインヒビターには幾つかのものがあり、MAGもその一つで、Nogo受容体とp75を介して神経成長を抑制するということである(図2)。このMAGの活性と[[シグナル]]系路が正常のミエリン形成等においてどのような機能を果たしているかについてははっきりしていない。Nogoを含むミエリンインヒビターについてはその項を参照されたい。 | |||
== 疾患との関係 == | == 疾患との関係 == | ||
MAGに対する抗体(特にIgM)は末梢性の[[ニューロパチー]]に関与していることが知られている<ref><pubmed>20842571</pubmed></ref>。これはMAGに抗原性の高い糖鎖が付着していることによるのかもしれない。抗体の存在は病態のマーカーともなりうるし、また、治療の対象ともなると考えられる。 | |||
| 61行目: | 38行目: | ||
* [[Nogo]] | * [[Nogo]] | ||
* [[ミエリンインヒビター]] | * [[ミエリンインヒビター]] | ||
* [[ | * [[ミエリン塩基性蛋白質]] | ||
* [[PLP]] | * [[PLP]] | ||
* [[P0]] | * [[P0]] | ||
| 67行目: | 44行目: | ||
== 参考文献 == | == 参考文献 == | ||
<references /> | <references /> | ||
(執筆者:櫻井武 担当編集委員:岡野栄之) | |||
2012年2月29日 (水) 20:10時点における版
| Myelin associated glycoprotein | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Identifiers | |||||||||||||
| Symbols | MAG; GMA; S-MAG; SIGLEC-4A; SIGLEC4A | ||||||||||||
| External IDs | OMIM: 159460 HomoloGene: 1771 GeneCards: MAG Gene | ||||||||||||
| |||||||||||||
| Orthologs | |||||||||||||
| Species | Human | Mouse | |||||||||||
| Entrez | 4099 | 17136 | |||||||||||
| Ensembl | ENSG00000105695 | ENSMUSG00000036634 | |||||||||||
| UniProt | P20916 | P20917 | |||||||||||
| RefSeq (mRNA) | n/a | NM_010758.2 | |||||||||||
| RefSeq (protein) | n/a | NP_034888.1 | |||||||||||
| Location (UCSC) |
Chr 19: 35.78 – 35.8 Mb |
Chr 7: 31.68 – 31.7 Mb | |||||||||||
| PubMed search | [1] | [2] | |||||||||||
英語名:Myelin associated glycoprotein
分子について
MAGは、分子量約100kDaの中枢、末梢の両方のミエリン画分に存在する膜糖タンパク質である。ミエリン蛋白の中では比較的マイナーな蛋白であるが、ミエリンに存在する糖画分の約30%がMAG上の糖鎖に由来する。L2/HNK−1抗体で認識される抗原構造を有する糖鎖を持つ。細胞外領域は5つの免疫グロブリンドメインからなり、膜貫通領域そして細胞内領域を持つ。選択的スプライシングによる細胞内領域の異なるアイソフォームが存在し、主にL(Large)フォームとS(Small)フォームからなるが、糖付加の違いによる更なるアイソフォームも存在する。発生段階では中枢ではLフォームが主であるが、末梢ではSフォームが主である。アダルトにおいてはSフォームが中枢、末梢の両者で主である[1]。 MAGは別名Siglec-4とも呼ばれSIGLECファミリーに属するシアル酸に結合する活性を有する蛋白質である事も明らかにされた[2]。In vitroの活性からMAGは細胞接着因子であることが明らかにされ、また、MAGがシュワン細胞がミエリン形成を開始する際の神経の軸索に接する部分の突起の所に局在することから、ミエリン形成におけるアクソンーグリア相互作用に関与する重要な分子であることが予想されていた[3][4]。 梅森らは、チロシンキナーゼのc−fynがL-MAGに結合していて、ミエリン形成の初期にチロシンのリン酸化がみられること及び、L-MAGをクロスリンクすることによってc-fynが活性化されることを報告し、MAGとfynがミエリン形成に重要であることを示唆していた[5]。
遺伝子クローニングからノックアウトマウスの作製へ
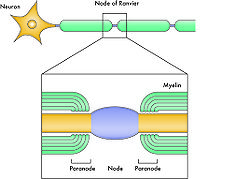
1987年に3つのグループがMAGのcDNAクローニングを行った。少し遅れて日本でも宮武らのグループがヒトのcDNAのクローニングを報告した。 1994年にノックアウトマウスが2つのグループによって報告され、in vitroの結果から予測されたようなドラスティックな異常はみられず、ミエリン形成がほとんど正常におこっていたことから、研究者を非常にがっかりさせた。しかしながら、そのマウスでは脱髄のあとの回復が遅れていたことから、MAGはおそらく神経再生においてのミエリン形成には重要なのではないかと考えられた[6][7]。また、MAGノックアウトマウスにおいては別の分子がその機能を代償しているのではないかと考えられた。事実、MAGとガラクト脂質合成酵素(MAGに結合するシアル酸の合成酵素)のダブルノックアウトマウスではノードとパラノードの形成はおこるものの、その構造の維持がおこらないことから、MAGはこのようなミエリン化された神経の構造の維持に重要であると考えられている(図1)[8]。
ミエリンインヒビターとしての論争
ノックアウトマウスの報告とほぼ同じ頃に驚くべき報告が行われた。Martin Schwabらは彼らの長年の研究からミエリンに神経の成長を抑制する分子が存在すると考え、ミエリンアソシエイティドインヒビターとしてその単離を試みていた。1994年に2つのグループから実はMAGがそのミエリンインヒビターではないかという報告がされたのである[9][10]。一つはモントリオールのAlbert Aguayoの流れを汲むSam Davidのグループとミエリン研究グループの共同研究であり、もう一つはニューヨークのMarie Filbinのグループである。どちらも、データとしては確固たるものであったが、in vitroのデータをもとにしたものであった。それに対して、SchwabのグループはMAGノックアウトマウスを作ったグループと共同で、ノックアウトマウスのミエリンでもまだインヒビターの活性があることから、ミエリンインヒビターはMAGではないという反論の論文をすぐさまだした[11]。 それに対して、Sam Davidのグループは地道にそれに対する反論の論文をだしていき、また、Marie FilbinのグループもMAGの神経成長抑制の活性についての解析の論文をだしていった。そうこうしているうちに、Schwabと一緒に論文を書いていたMAGノックアウトマウスを作製したグループもSchwabを抜きに、MAGノックアウトマウスでは神経再生の促進がみられるという論文をだし、実はMAGもミエリンインヒビターの一つではないかということを示唆していた[12]。
実はNogo受容体のリガンドだった
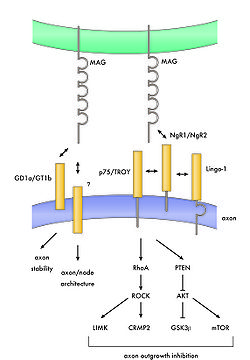
Schwabのグループはその後も地道に生化学的に彼らのミエリンインヒビターの精製と同定を進めていた。その彼らの発表した部分アミノ酸配列をもとに2000年に3つのグループがこの分子の同定を発表し、Nogoと呼ばれたこの分子はMAGとは構造的に異なるものであった。その後、2001年にNogoのクローニングを行った3つのグループの1つであるSteven StrittmatterのグループによってNogo受容体が同定された。その後、2002年に再び驚くべき報告がなされた。StrittmatterのグループとFilbinのグループが実はMAGもNogo受容体のリガンドであることを明らかにしたのである[13][14]。 また、山下らはMAGの神経成長阻害の活性はp75を介しておこることを示していたが、その数ヶ月後に実はNogo受容体はp75と結合しMAGを含むNogoリガンドはp75を通じて神経成長阻害を示すことが別の2つのグループによって明らかにされた[15][16]。つまり、ミエリンアソシエイティドインヒビターには幾つかのものがあり、MAGもその一つで、Nogo受容体とp75を介して神経成長を抑制するということである(図2)。このMAGの活性とシグナル系路が正常のミエリン形成等においてどのような機能を果たしているかについてははっきりしていない。Nogoを含むミエリンインヒビターについてはその項を参照されたい。
疾患との関係
MAGに対する抗体(特にIgM)は末梢性のニューロパチーに関与していることが知られている[17]。これはMAGに抗原性の高い糖鎖が付着していることによるのかもしれない。抗体の存在は病態のマーカーともなりうるし、また、治療の対象ともなると考えられる。
関連項目
参考文献
- ↑
Pedraza, L., Frey, A.B., Hempstead, B.L., Colman, D.R., & Salzer, J.L. (1991).
Differential expression of MAG isoforms during development. Journal of neuroscience research, 29(2), 141-8. [PubMed:1716323] [WorldCat] [DOI] - ↑
Crocker, P.R. (2002).
Siglecs: sialic-acid-binding immunoglobulin-like lectins in cell-cell interactions and signalling. Current opinion in structural biology, 12(5), 609-15. [PubMed:12464312] [WorldCat] - ↑
Schachner, M., & Bartsch, U. (2000).
Multiple functions of the myelin-associated glycoprotein MAG (siglec-4a) in formation and maintenance of myelin. Glia, 29(2), 154-65. [PubMed:10625334] [WorldCat] - ↑
Quarles, R.H. (2007).
Myelin-associated glycoprotein (MAG): past, present and beyond. Journal of neurochemistry, 100(6), 1431-48. [PubMed:17241126] [WorldCat] [DOI] - ↑
Umemori, H., Sato, S., Yagi, T., Aizawa, S., & Yamamoto, T. (1994).
Initial events of myelination involve Fyn tyrosine kinase signalling. Nature, 367(6463), 572-6. [PubMed:7509042] [WorldCat] [DOI] - ↑
Montag, D., Giese, K.P., Bartsch, U., Martini, R., Lang, Y., Blüthmann, H., ..., & Nave, K.A. (1994).
Mice deficient for the myelin-associated glycoprotein show subtle abnormalities in myelin. Neuron, 13(1), 229-46. [PubMed:7519026] [WorldCat] [DOI] - ↑
Li, C., Tropak, M.B., Gerlai, R., Clapoff, S., Abramow-Newerly, W., Trapp, B., ..., & Roder, J. (1994).
Myelination in the absence of myelin-associated glycoprotein. Nature, 369(6483), 747-50. [PubMed:7516497] [WorldCat] [DOI] - ↑
Marcus, J., Dupree, J.L., & Popko, B. (2002).
Myelin-associated glycoprotein and myelin galactolipids stabilize developing axo-glial interactions. The Journal of cell biology, 156(3), 567-77. [PubMed:11827985] [PMC] [WorldCat] [DOI] - ↑
McKerracher, L., David, S., Jackson, D.L., Kottis, V., Dunn, R.J., & Braun, P.E. (1994).
Identification of myelin-associated glycoprotein as a major myelin-derived inhibitor of neurite growth. Neuron, 13(4), 805-11. [PubMed:7524558] [WorldCat] [DOI] - ↑
Mukhopadhyay, G., Doherty, P., Walsh, F.S., Crocker, P.R., & Filbin, M.T. (1994).
A novel role for myelin-associated glycoprotein as an inhibitor of axonal regeneration. Neuron, 13(3), 757-67. [PubMed:7522484] [WorldCat] [DOI] - ↑
Bartsch, U., Bandtlow, C.E., Schnell, L., Bartsch, S., Spillmann, A.A., Rubin, B.P., ..., & Schachner, M. (1995).
Lack of evidence that myelin-associated glycoprotein is a major inhibitor of axonal regeneration in the CNS. Neuron, 15(6), 1375-81. [PubMed:8845160] [WorldCat] [DOI] - ↑
Schäfer, M., Fruttiger, M., Montag, D., Schachner, M., & Martini, R. (1996).
Disruption of the gene for the myelin-associated glycoprotein improves axonal regrowth along myelin in C57BL/Wlds mice. Neuron, 16(6), 1107-13. [PubMed:8663987] [WorldCat] [DOI] - ↑
Domeniconi, M., Cao, Z., Spencer, T., Sivasankaran, R., Wang, K., Nikulina, E., ..., & Filbin, M. (2002).
Myelin-associated glycoprotein interacts with the Nogo66 receptor to inhibit neurite outgrowth. Neuron, 35(2), 283-90. [PubMed:12160746] [WorldCat] [DOI] - ↑
Liu, B.P., Fournier, A., GrandPré, T., & Strittmatter, S.M. (2002).
Myelin-associated glycoprotein as a functional ligand for the Nogo-66 receptor. Science (New York, N.Y.), 297(5584), 1190-3. [PubMed:12089450] [WorldCat] [DOI] - ↑
Wong, S.T., Henley, J.R., Kanning, K.C., Huang, K.H., Bothwell, M., & Poo, M.M. (2002).
A p75(NTR) and Nogo receptor complex mediates repulsive signaling by myelin-associated glycoprotein. Nature neuroscience, 5(12), 1302-8. [PubMed:12426574] [WorldCat] [DOI] - ↑
Wang, K.C., Kim, J.A., Sivasankaran, R., Segal, R., & He, Z. (2002).
P75 interacts with the Nogo receptor as a co-receptor for Nogo, MAG and OMgp. Nature, 420(6911), 74-8. [PubMed:12422217] [WorldCat] [DOI] - ↑
Dalakas, M.C. (2010).
Pathogenesis and Treatment of Anti-MAG Neuropathy. Current treatment options in neurology, 12(2), 71-83. [PubMed:20842571] [WorldCat] [DOI]
(執筆者:櫻井武 担当編集委員:岡野栄之)