「拮抗薬」の版間の差分
細編集の要約なし |
Shujikaneko (トーク | 投稿記録) 細編集の要約なし |
||
| (同じ利用者による、間の2版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0013268 金子 周司]</font><br> | <font size="+1">[http://researchmap.jp/read0013268 金子 周司]</font><br> | ||
''京都大学大学院薬学研究科 薬学研究科 医療薬科学専攻''<br> | ''京都大学大学院薬学研究科 薬学研究科 医療薬科学専攻''<br> | ||
DOI: <selfdoi /> | DOI: <selfdoi /> 原稿受付日:2016年1月1日 原稿完成日:2016年X月X日<br> | ||
担当編集委員:[http://researchmap.jp/haruokasai 河西 春郎](東京大学 大学院医学系研究科)<br> | 担当編集委員:[http://researchmap.jp/haruokasai 河西 春郎](東京大学 大学院医学系研究科)<br> | ||
</div> | </div> | ||
| 11行目: | 11行目: | ||
対義語:作動薬(agonist) | 対義語:作動薬(agonist) | ||
== 拮抗薬とは == | == 拮抗薬とは == | ||
| 20行目: | 18行目: | ||
これらの物質は、酵素基質、[[神経伝達物質]]、[[ホルモン]]などの内在性リガンドが結合する部位において競合的に拮抗する場合と、それ以外の部位(これをアロステリック部位という)に結合してタンパク質構造を変化させることによって作用する場合に分けられる。 | これらの物質は、酵素基質、[[神経伝達物質]]、[[ホルモン]]などの内在性リガンドが結合する部位において競合的に拮抗する場合と、それ以外の部位(これをアロステリック部位という)に結合してタンパク質構造を変化させることによって作用する場合に分けられる。 | ||
代表的な遮断薬(アンタゴニストまたは拮抗薬antagonist)は,受容体の刺激薬結合部位に結合して刺激薬の作用に競合する物質である。このような拮抗様式は競合的competitiveであると言われ,その物質は[[競合的遮断薬]] competitive antagonismと呼ばれる。競合的遮断薬は,刺激薬の[[用量反応曲線]]を右にシフトさせ,ED50値を増大させる。しかし,競合する刺激薬の濃度を増やした場合には遮断薬は競合的に排除されるため,刺激薬の最大効果は不変である。なお,競合的遮断薬の作用強度を表す指標として,しばしば[[pA2]]が用いられる。これは刺激薬単独時のED50を2倍にするために必要な遮断薬の量(または濃度)と定義される。このpA2を求める場合、様々な濃度の拮抗薬存在下における用量依存曲線のED50濃度比rを求め、拮抗薬の対数モル濃度に対してlog (r-1) | 代表的な遮断薬(アンタゴニストまたは拮抗薬antagonist)は,受容体の刺激薬結合部位に結合して刺激薬の作用に競合する物質である。このような拮抗様式は競合的competitiveであると言われ,その物質は[[競合的遮断薬]] competitive antagonismと呼ばれる。競合的遮断薬は,刺激薬の[[用量反応曲線]]を右にシフトさせ,ED50値を増大させる。しかし,競合する刺激薬の濃度を増やした場合には遮断薬は競合的に排除されるため,刺激薬の最大効果は不変である。なお,競合的遮断薬の作用強度を表す指標として,しばしば[[pA2]]が用いられる。これは刺激薬単独時のED50を2倍にするために必要な遮断薬の量(または濃度)と定義される。このpA2を求める場合、様々な濃度の拮抗薬存在下における用量依存曲線のED50濃度比rを求め、拮抗薬の対数モル濃度に対してlog (r-1)を縦軸にプロットするSchild plotが用いられ、横軸切片がpA2値となる。 | ||
[[ファイル:Antagonist.jpg|サムネイル|400px| '''図. 拮抗薬の阻害様式''']] | [[ファイル:Antagonist.jpg|サムネイル|400px| '''図. 拮抗薬の阻害様式''']] | ||
| 29行目: | 27行目: | ||
== 逆作動薬 == | == 逆作動薬 == | ||
なお、受容体によってはリガンドが存在しない状態でも[[細胞内情報伝達系]]が恒常的に活性化されている場合がある。このような恒常活性化型の受容体に結合して細胞内情報伝達系を抑制する物質は[[逆作動薬]](inverse agonist)と呼ばれる。名称に「作動薬」が含まれているが、実際には拮抗薬の作用を発揮する。多くの[[Gタンパク質共役型受容体]]に対する拮抗薬が実際には逆作動薬であることが知られている。 | |||
==関連項目== | ==関連項目== | ||
| 36行目: | 34行目: | ||
==参考文献== | ==参考文献== | ||
1. D E Golan, A H Tashjian Jr, E J Armstrong, A W Armstrong | |||
Principles of Pharmacology Third Edition, Pharmacodynamics pp.17-26 (2012) | |||
2016年1月2日 (土) 17:44時点における版
金子 周司
京都大学大学院薬学研究科 薬学研究科 医療薬科学専攻
DOI: 10.14931/bsd.3361 原稿受付日:2016年1月1日 原稿完成日:2016年X月X日
担当編集委員:河西 春郎(東京大学 大学院医学系研究科)
英:antagonist 独:Antagonist 仏:antagoniste
同義語:アンタゴニスト、遮断薬、拮抗型阻害薬、阻害薬、インヒビター
対義語:作動薬(agonist)
拮抗薬とは
生体内タンパク質に作用して内在性物質に対する拮抗作用や機能阻害作用を発揮する薬物を指す。その標的タンパク質が酵素の場合は阻害薬(inhibitor)、受容体の場合は拮抗薬(antagonist)、イオンチャネルの場合は遮断薬(blocker)等と用語が使い分けられるが、その区別は厳密なものではない。
競合的遮断薬と非競合的遮断薬
これらの物質は、酵素基質、神経伝達物質、ホルモンなどの内在性リガンドが結合する部位において競合的に拮抗する場合と、それ以外の部位(これをアロステリック部位という)に結合してタンパク質構造を変化させることによって作用する場合に分けられる。
代表的な遮断薬(アンタゴニストまたは拮抗薬antagonist)は,受容体の刺激薬結合部位に結合して刺激薬の作用に競合する物質である。このような拮抗様式は競合的competitiveであると言われ,その物質は競合的遮断薬 competitive antagonismと呼ばれる。競合的遮断薬は,刺激薬の用量反応曲線を右にシフトさせ,ED50値を増大させる。しかし,競合する刺激薬の濃度を増やした場合には遮断薬は競合的に排除されるため,刺激薬の最大効果は不変である。なお,競合的遮断薬の作用強度を表す指標として,しばしばpA2が用いられる。これは刺激薬単独時のED50を2倍にするために必要な遮断薬の量(または濃度)と定義される。このpA2を求める場合、様々な濃度の拮抗薬存在下における用量依存曲線のED50濃度比rを求め、拮抗薬の対数モル濃度に対してlog (r-1)を縦軸にプロットするSchild plotが用いられ、横軸切片がpA2値となる。
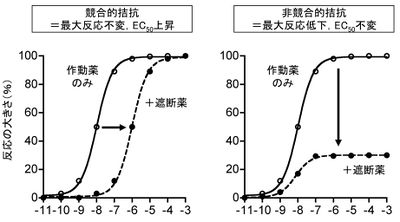
一方,遮断薬が受容体の刺激薬結合部位とは異なるアロステリック部位allosteric siteに結合して刺激薬の受容体親和性を減弱させる場合や,受容体以降の応答に至るまでの経路のどこかに作用して刺激薬の作用を見かけ上弱める拮抗作用は,非競合的noncompetitiveであると言われ,そのような物質は非競合的遮断薬 noncompetitive antagonistと呼ばれる。非競合的遮断薬は,刺激薬の用量反応曲線において最大効果を減少させるが,ED50値には影響しない。
なお,遮断薬の受容体への結合の多くは非共有結合であり,作用は可逆的reversibleである。しかし,一部の遮断薬は受容体に共有結合を形成するので,不可逆的irreversibleな作用を発揮する。また,細胞内において生理学的な拮抗をもたらす非競合的遮断薬の一部では,作用はほとんど不可逆的である。受容体に対する親和性が刺激薬に比べて極めて高い遮断薬の場合にも,拮抗作用が洗い流されないことから作用が見かけ上,不可逆的となりinsurmountableであると表現される。
逆作動薬
なお、受容体によってはリガンドが存在しない状態でも細胞内情報伝達系が恒常的に活性化されている場合がある。このような恒常活性化型の受容体に結合して細胞内情報伝達系を抑制する物質は逆作動薬(inverse agonist)と呼ばれる。名称に「作動薬」が含まれているが、実際には拮抗薬の作用を発揮する。多くのGタンパク質共役型受容体に対する拮抗薬が実際には逆作動薬であることが知られている。
関連項目
参考文献
1. D E Golan, A H Tashjian Jr, E J Armstrong, A W Armstrong Principles of Pharmacology Third Edition, Pharmacodynamics pp.17-26 (2012)