「CAST」の版間の差分
細 →サブファミリー |
細編集の要約なし |
||
| (同じ利用者による、間の2版が非表示) | |||
| 1行目: | 1行目: | ||
<div align="right"> | <div align="right"> | ||
<font size="+1">[https://researchmap.jp/ | <font size="+1">[https://researchmap.jp/read0124089/ 大塚 稔久]</font><br> | ||
''山梨大学医学部 生化学講座第1教室''<br> | ''山梨大学医学部 生化学講座第1教室''<br> | ||
DOI:<selfdoi /> 原稿受付日:2020年10月1日 原稿完成日:2020年10月13日<br> | DOI:<selfdoi /> 原稿受付日:2020年10月1日 原稿完成日:2020年10月13日<br> | ||
| 6行目: | 6行目: | ||
</div> | </div> | ||
{{box|text= CASTは神経終末のアクティブゾーン(活性帯)に存在する細胞骨格タンパク質の一種である。他のアクティブゾーンタンパク質であるBassoon, Piccolo, RIM, Munc13と直接結合して巨大な分子複合体を形成する。放出確率やシナプス短期可塑性などを制御し、電位依存性カルシウムチャネルの局在化に関わる。}} | {{box|text= CASTは神経終末のアクティブゾーン(活性帯)に存在する細胞骨格タンパク質の一種である。他のアクティブゾーンタンパク質であるBassoon, Piccolo, RIM,Munc13と直接結合して巨大な分子複合体を形成する。放出確率やシナプス短期可塑性などを制御し、電位依存性カルシウムチャネルの局在化に関わる。}} | ||
[[file:Ohtsuka CAST Fig1.png|サムネイル|'''図1. 免疫電顕法によるCASTの局在'''<br>中央が樹状突起。電子密度の高いPSDの反対側、プレシナプス形質膜直下にCASTのシグナルが見られる。<ref name=Ohtsuka2002 /> | [[file:Ohtsuka CAST Fig1.png|サムネイル|'''図1. 免疫電顕法によるCASTの局在'''<br>中央が樹状突起。電子密度の高いPSDの反対側、プレシナプス形質膜直下にCASTのシグナルが見られる。<ref name=Ohtsuka2002 />のFigure 5より転載]] | ||
[[file:Ohtsuka CAST Fig2.png|サムネイル|'''図2. アクティブゾーンタンパク質の構造]] | [[file:Ohtsuka CAST Fig2.png|サムネイル|'''図2. アクティブゾーンタンパク質の構造]] | ||
[[ファイル:Ohtsuka CAST Fig3.png|サムネイル|'''図3. プレシナプス末端におけるアクティブゾーンタンパク質の結合模式図'''<br>CAST/ELKSはコイルドコイルドメインにおいて、Munc13-1、Bassoon, Piccolo及びVDCC βサブユニットと結合し、C末端はRIM1と結合する。]] | [[ファイル:Ohtsuka CAST Fig3.png|サムネイル|'''図3. プレシナプス末端におけるアクティブゾーンタンパク質の結合模式図'''<br>CAST/ELKSはコイルドコイルドメインにおいて、Munc13-1、Bassoon, Piccolo及びVDCC βサブユニットと結合し、C末端はRIM1と結合する。]] | ||
| 15行目: | 15行目: | ||
== CASTとは == | == CASTとは == | ||
CASTはラット大脳から、シナプス分画に濃縮しているタンパク質として精製同定された120kDaのタンパク質である<ref name=Ohtsuka2002><pubmed>12163476</pubmed></ref> [1]。免疫電顕でも、CASTがアクティブゾーンに特異的に局在していることが示された('''図1''')。名前の由来は、Cytomatrix at the Active zone-associated STructural proteinから来ている。2002年、アクティブゾーンタンパク質RIM1の結合タンパク質としてYeast Two Hybridによっても同定された<ref name=Wang2002><pubmed>12391317</pubmed></ref> [2]。アクティブゾーンは比較的電子密度が高い構造体として知られており、CASTを介したアクティブゾーンタンパク質の複合体が、その分子構造基盤ではないかと考えられている('''図2''','''図3''')。 | |||
2006年にはショウジョウバエにおいて、CASTのホモログが同定されBruchpilot(Brp)と命名された<ref name=Wagh2006><pubmed>16543132</pubmed></ref> [3]('''図4''')。 | |||
高等動物の中枢神経では、遺伝子改変マウスを用いた解析から、シナプス小胞内のグルタミン酸の量<ref name=Kobayashi2016><pubmed>27422015</pubmed></ref> [4]、放出確率<ref name=Hald2016><pubmed>27253063</pubmed></ref><ref name=Dong2018><pubmed>29996090</pubmed></ref> [5][6]、即時放出可能プール (readily releasable pool: RRP) のサイズ<ref name=Dong2018><pubmed>29996090</pubmed></ref> [6]などを制御していることが明らかとなっている。また、最近の研究からは、電位依存性のカルシウムチャネルと相互作用して、アクティブゾーンにおけるチャネルの局在とクラスター化を制御していることが示唆されている<ref name=Dong2018><pubmed>29996090</pubmed></ref><ref name=Kiyonaka2012><pubmed>22577167</pubmed></ref><ref name=Ohara-Imaizumi2019><pubmed>30699350</pubmed></ref> [6][7][8]。 | |||
== 構造 == | == 構造 == | ||
分子量は約120kDaで、全体がコイルドコイルで構成されている。酵素活性を持つような特徴的なドメインは有していないが、C末端にIWAという3つのアミノ酸が存在する。このIWA配列はRIM1との相互作用に必須である[1]。RIM1以外の結合タンパク質はコイルドコイルドメインに結合する<ref name=Hida2010><pubmed>20581014</pubmed></ref><ref name=Hamada2018><pubmed>29275163</pubmed></ref> [9][10]。 | |||
== サブファミリー == | == サブファミリー == | ||
マウスではELKSが知られる('''表''')。ELKSは、もともとある種の甲状腺がんにおいて異なる染色体に転座した遺伝子産物として同定されていた<ref name=Nakata1999><pubmed>10337992</pubmed></ref> [11]。その後、生化学的および形態学的な解析から、ELKSがアクティブゾーンに局在していることが報告された<ref name=Deguchi-Tawarada2004><pubmed>14723704</pubmed></ref> [12]。CASTとELKSは比較的高い相同性を有し(約70%のアミノ酸の一致)、おそらくNおよびC末端のコイルドコイル領域を介してヘテロまたはホモオリゴマーを形成すると考えられている<ref name=Inoue2006><pubmed>16716196</pubmed></ref> [13]。 | |||
ショウジョウバエではCASTのホモログはBrpとして知られている<ref name=Wagh2006><pubmed>16543132</pubmed></ref>[3]。BrpはN末領域が比較的CASTと相同性が高い。C末は相同性が低く、CAST/ELKSに特徴的なIWAモチーフを欠損している[3]。 | |||
{| class="wikitable" | {| class="wikitable" | ||
|+表. 哺乳動物CASTサブファミリーの呼称一覧 | |+表. 哺乳動物CASTサブファミリーの呼称一覧 | ||
|- | |- | ||
| CAST = | | CAST = CAST1 = Erc2 = ELKS2 | ||
|- | |- | ||
| ELKS = | | ELKS = CAST2 = RAB6 interacting protein 2 = Erc1=ELKS1 | ||
|} | |} | ||
== 発現 == | == 発現 == | ||
CASTは主に脳神経系で発現し、ELKSは脳神経系および脳以外のさまざまな組織・細胞で発現している<ref name=Deguchi-Tawarada2004><pubmed>14723704</pubmed></ref> | CASTは主に脳神経系で発現し、ELKSは脳神経系および脳以外のさまざまな組織・細胞で発現している<ref name=Deguchi-Tawarada2004><pubmed>14723704</pubmed></ref> [12]。CASTは嗅球や海馬において高い発現を示すが、脳全体で発現している[1]。ELKSは中枢神経では主に小脳において強い発現が見られる<ref name=Deguchi-Tawarada2004><pubmed>14723704</pubmed></ref> [12]。末梢神経では、マウスの神経筋接合部では、ELKSは発現しているがCASTは発現していないようである<ref name=Nishimune2012><pubmed>22701595</pubmed></ref> [14]。 | ||
シナプスではいずれもアクティブゾーンに局在することが電子顕微鏡で明らかにされている<ref name=Deguchi-Tawarada2004><pubmed>14723704</pubmed></ref> | シナプスではいずれもアクティブゾーンに局在することが電子顕微鏡で明らかにされている<ref name=Deguchi-Tawarada2004><pubmed>14723704</pubmed></ref> [12]。特に、網膜のリボンシナプスでは、CASTはネックの部分に、ELKSはリボン全体に分布している<ref name=Deguchi-Tawarada2006><pubmed>16485285</pubmed></ref> [15]。 | ||
末梢の組織では、ELKSがインスリンの開口放出を制御していることが知られており、膵臓細胞内で血管側に近い膜近傍での局在が電子顕微鏡によって明らかにされている<ref name=Ohara-Imaizumi2005><pubmed>15888548</pubmed></ref> [16]。また、下垂体では、CASTは後葉に、ELKSは前葉、中葉および後葉に発現している<ref name=Hagiwara2020><pubmed>32251313</pubmed></ref> [17]。CASTノックアウトマウスの下垂体後葉では、ELKSの発現が約2倍増加することから、二つのタンパク質は相補的に機能していると考えられる。同様の相補的な現象は、海馬や網膜おいても観察される<ref name=Kobayashi2016><pubmed>27422015</pubmed></ref><ref name=tomDieck2012><pubmed>22933801</pubmed></ref> [4][18]。 | |||
== 機能 == | == 機能 == | ||
=== 構造およびシナプス機能 === | === 構造およびシナプス機能 === | ||
CASTは複数の結合タンパク質を有しており、アクティブゾーンにおいて足場タンパク質としての役割を果たしている。例えば、C末のIWA配列を欠損させてもCASTはアクティブゾーンに局在するが、CASTに結合するRIM1のPDZドメインを欠失させるとRIM1はdiffuseな局在を示すようになる<ref name=Ohtsuka2002><pubmed>12163476</pubmed></ref> [1]。また、シナプス分画において、CASTノックアウトマウスではRIM1が可溶性画分で増加することから、CASTがRIM1のanchoringタンパク質として機能していると考えられる<ref name=Kaeser2009><pubmed>19874790</pubmed></ref> [29]。さらに、CASTのコイルドコイルドメインにおいてCAST/ELKSの二量体形成だけでなくMunc13-1<ref name=Brose1995><pubmed>7559667</pubmed></ref> [19]、RIM1<ref name=Wang1997><pubmed>9252191</pubmed></ref> [20]、Bassoon<ref name=tomDieck1998><pubmed>9679147</pubmed></ref> [21]、Piccolo<ref name= Cases-Langhoff1996><pubmed>8900486</pubmed></ref><ref name=Wang1999><pubmed>10508862</pubmed></ref><ref name=Fenster2000><pubmed>10707984</pubmed></ref> [22][23][24]など他のアクティブゾーンタンパク質と結合することが生化学的解析により明らかになっている<ref name=Takao-Rikitsu2004><pubmed>14734538</pubmed></ref> [25]。同様に、中枢神経系のCalyx of HeldシナプスでCAST/ELKSを欠損させると、電位依存性カルシウムチャネルのクラスター化が阻害される<ref name=Dong2018><pubmed>29996090</pubmed></ref> [6]。CASTノックアウトマウスの網膜では稈体細胞のアクティブゾーンであるリボンシナプスの長さが半分以下に縮小し、野生型であれば外網状層 (Outer plexiform layer: OPL) に水平細胞や双極細胞と形成されるシナプスが、外顆粒層 (Outer nuclear layer: ONL) に異所性に形成されることや<ref name=tomDieck2012><pubmed>22933801</pubmed></ref> [18]、CAST/ELKSダブルノックアウトでは、これらの表現型が亢進するとともに稈体細胞のアポトーシスが誘導されるなど網膜の神経回路形成において重要な役割を果たしている<ref name=Hagiwara2018><pubmed>30190286</pubmed></ref> [26]。また、ショウジョウバエではBrpを欠損させると特徴的なアクティブゾーンであるT-barが完全に消失することが示された<ref name=Kittel2006><pubmed>16614170</pubmed></ref> [27]。しかし、線虫ではそのような表現型は見いだされていない<ref name=Deken2005><pubmed>15976086</pubmed></ref> [28] 。 | |||
シナプス伝達に関しては、CASTノックアウトマウスの急性海馬スライスにおいて、海馬CA1の抑制性神経細胞では二発抑圧 (paired-pulse depression: PPD) が更新し、スクロース投与により惹起される電流量が増大したことから、放出確率やRRPサイズを制限していることが示唆されている<ref name=Kaeser2009><pubmed>19874790</pubmed></ref> [29]。さらにCAST/ELKSダブルノックアウトでは抑制性神経細胞のシナプス末端でのCa2+流入量が低下することが分かっている<ref name=Liu2014><pubmed>25209271</pubmed></ref> [30]。また興奮性神経細胞においてはノックアウトマウスで入力―出力比、二発促通 (paired-pulse facilitation: PPF) が増大、反復持続刺激後の回復の遅れ、シナプス間隙のグルタミン酸濃度の増加を反映する低親和性AMPA受容体阻害剤の感受性の低下が観察されており、シナプス小胞のリサイクリングの制御に関与する可能性が示唆されている<ref name=Kobayashi2016><pubmed>27422015</pubmed></ref> [4]。 | |||
また、CASTおよびELKSは神経活動依存的にプレシナプス性キナーゼSAD-BによりN末端領域がリン酸化され、少なくとも上頸神経節 (superior cervical ganglion: SCG) においてCASTのリン酸化はシナプス小胞の再補充を遅らせ、RRPサイズを下げる。こうした事実から、神経細胞の活性化時にRRPサイズを調節することで一時的にシナプスレベルでの抑制をかけている可能性が示唆されている<ref name=Mochida2016><pubmed>27626661</pubmed></ref> [31]。 | |||
=== 個体機能 === | === 個体機能 === | ||
遺伝子改変マウスを用いた解析から、CASTノックアウトマウスの母親では、巣作りやリトリービングといった子育て行動に異常が見いだされている<ref name=Hagiwara2020><pubmed>32251313</pubmed></ref> [17]。また、全脳CASTノックアウトマウスにα-CaMKII陽性神経細胞特異的ELKSノックアウトマウスを掛け合わせると生後1日で死亡するが、そのメカニズムに関しては不明である<ref name=Hagiwara2020b><pubmed>31996256</pubmed></ref> [32]。 | |||
== 疾患との関わり == | == 疾患との関わり == | ||
CASTと具体的な疾患との関連性は現在知られていないが、ファミリーメンバーELKSは、言語障害を特徴とする自閉症スペクトラムとの関連が示唆されている<ref name=Thevenon2012><pubmed>22713806</pubmed></ref><ref name=Silva2014><pubmed>24613754</pubmed></ref> [33][34]。 | |||
== 関連語 == | == 関連語 == | ||
* [[足場タンパク質]] | * [[足場タンパク質]] | ||
* [[シナプス小胞]] | * [[シナプス小胞]] | ||
2020年10月13日 (火) 20:32時点における版
大塚 稔久
山梨大学医学部 生化学講座第1教室
DOI:10.14931/bsd.9436 原稿受付日:2020年10月1日 原稿完成日:2020年10月13日
担当編集委員:古屋敷 智之(神戸大学大学院医学研究科・医学部 薬理学分野)
CASTは神経終末のアクティブゾーン(活性帯)に存在する細胞骨格タンパク質の一種である。他のアクティブゾーンタンパク質であるBassoon, Piccolo, RIM,Munc13と直接結合して巨大な分子複合体を形成する。放出確率やシナプス短期可塑性などを制御し、電位依存性カルシウムチャネルの局在化に関わる。
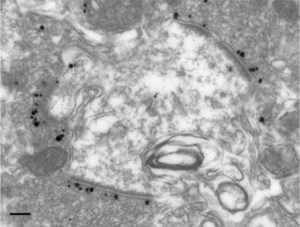
中央が樹状突起。電子密度の高いPSDの反対側、プレシナプス形質膜直下にCASTのシグナルが見られる。[1]のFigure 5より転載
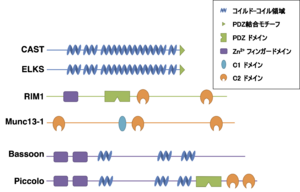
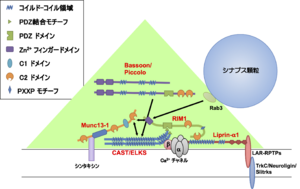
CAST/ELKSはコイルドコイルドメインにおいて、Munc13-1、Bassoon, Piccolo及びVDCC βサブユニットと結合し、C末端はRIM1と結合する。
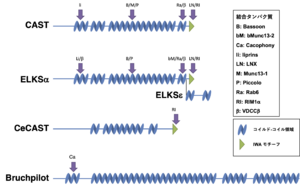
哺乳類CAST/ELKS、線虫CAST (CeCAST)、ショウジョウバエのホモログBruchpilotの構造の比較。矢印は結合タンパク質の結合部位を示す。
CASTとは
CASTはラット大脳から、シナプス分画に濃縮しているタンパク質として精製同定された120kDaのタンパク質である[1] [1]。免疫電顕でも、CASTがアクティブゾーンに特異的に局在していることが示された(図1)。名前の由来は、Cytomatrix at the Active zone-associated STructural proteinから来ている。2002年、アクティブゾーンタンパク質RIM1の結合タンパク質としてYeast Two Hybridによっても同定された[2] [2]。アクティブゾーンは比較的電子密度が高い構造体として知られており、CASTを介したアクティブゾーンタンパク質の複合体が、その分子構造基盤ではないかと考えられている(図2,図3)。
2006年にはショウジョウバエにおいて、CASTのホモログが同定されBruchpilot(Brp)と命名された[3] [3](図4)。
高等動物の中枢神経では、遺伝子改変マウスを用いた解析から、シナプス小胞内のグルタミン酸の量[4] [4]、放出確率[5][6] [5][6]、即時放出可能プール (readily releasable pool: RRP) のサイズ[6] [6]などを制御していることが明らかとなっている。また、最近の研究からは、電位依存性のカルシウムチャネルと相互作用して、アクティブゾーンにおけるチャネルの局在とクラスター化を制御していることが示唆されている[6][7][8] [6][7][8]。
構造
分子量は約120kDaで、全体がコイルドコイルで構成されている。酵素活性を持つような特徴的なドメインは有していないが、C末端にIWAという3つのアミノ酸が存在する。このIWA配列はRIM1との相互作用に必須である[1]。RIM1以外の結合タンパク質はコイルドコイルドメインに結合する[9][10] [9][10]。
サブファミリー
マウスではELKSが知られる(表)。ELKSは、もともとある種の甲状腺がんにおいて異なる染色体に転座した遺伝子産物として同定されていた[11] [11]。その後、生化学的および形態学的な解析から、ELKSがアクティブゾーンに局在していることが報告された[12] [12]。CASTとELKSは比較的高い相同性を有し(約70%のアミノ酸の一致)、おそらくNおよびC末端のコイルドコイル領域を介してヘテロまたはホモオリゴマーを形成すると考えられている[13] [13]。 ショウジョウバエではCASTのホモログはBrpとして知られている[3][3]。BrpはN末領域が比較的CASTと相同性が高い。C末は相同性が低く、CAST/ELKSに特徴的なIWAモチーフを欠損している[3]。
| CAST = CAST1 = Erc2 = ELKS2 |
| ELKS = CAST2 = RAB6 interacting protein 2 = Erc1=ELKS1 |
発現
CASTは主に脳神経系で発現し、ELKSは脳神経系および脳以外のさまざまな組織・細胞で発現している[12] [12]。CASTは嗅球や海馬において高い発現を示すが、脳全体で発現している[1]。ELKSは中枢神経では主に小脳において強い発現が見られる[12] [12]。末梢神経では、マウスの神経筋接合部では、ELKSは発現しているがCASTは発現していないようである[14] [14]。
シナプスではいずれもアクティブゾーンに局在することが電子顕微鏡で明らかにされている[12] [12]。特に、網膜のリボンシナプスでは、CASTはネックの部分に、ELKSはリボン全体に分布している[15] [15]。
末梢の組織では、ELKSがインスリンの開口放出を制御していることが知られており、膵臓細胞内で血管側に近い膜近傍での局在が電子顕微鏡によって明らかにされている[16] [16]。また、下垂体では、CASTは後葉に、ELKSは前葉、中葉および後葉に発現している[17] [17]。CASTノックアウトマウスの下垂体後葉では、ELKSの発現が約2倍増加することから、二つのタンパク質は相補的に機能していると考えられる。同様の相補的な現象は、海馬や網膜おいても観察される[4][18] [4][18]。
機能
構造およびシナプス機能
CASTは複数の結合タンパク質を有しており、アクティブゾーンにおいて足場タンパク質としての役割を果たしている。例えば、C末のIWA配列を欠損させてもCASTはアクティブゾーンに局在するが、CASTに結合するRIM1のPDZドメインを欠失させるとRIM1はdiffuseな局在を示すようになる[1] [1]。また、シナプス分画において、CASTノックアウトマウスではRIM1が可溶性画分で増加することから、CASTがRIM1のanchoringタンパク質として機能していると考えられる[19] [29]。さらに、CASTのコイルドコイルドメインにおいてCAST/ELKSの二量体形成だけでなくMunc13-1[20] [19]、RIM1[21] [20]、Bassoon[22] [21]、Piccolo[23][24][25] [22][23][24]など他のアクティブゾーンタンパク質と結合することが生化学的解析により明らかになっている[26] [25]。同様に、中枢神経系のCalyx of HeldシナプスでCAST/ELKSを欠損させると、電位依存性カルシウムチャネルのクラスター化が阻害される[6] [6]。CASTノックアウトマウスの網膜では稈体細胞のアクティブゾーンであるリボンシナプスの長さが半分以下に縮小し、野生型であれば外網状層 (Outer plexiform layer: OPL) に水平細胞や双極細胞と形成されるシナプスが、外顆粒層 (Outer nuclear layer: ONL) に異所性に形成されることや[18] [18]、CAST/ELKSダブルノックアウトでは、これらの表現型が亢進するとともに稈体細胞のアポトーシスが誘導されるなど網膜の神経回路形成において重要な役割を果たしている[27] [26]。また、ショウジョウバエではBrpを欠損させると特徴的なアクティブゾーンであるT-barが完全に消失することが示された[28] [27]。しかし、線虫ではそのような表現型は見いだされていない[29] [28] 。
シナプス伝達に関しては、CASTノックアウトマウスの急性海馬スライスにおいて、海馬CA1の抑制性神経細胞では二発抑圧 (paired-pulse depression: PPD) が更新し、スクロース投与により惹起される電流量が増大したことから、放出確率やRRPサイズを制限していることが示唆されている[19] [29]。さらにCAST/ELKSダブルノックアウトでは抑制性神経細胞のシナプス末端でのCa2+流入量が低下することが分かっている[30] [30]。また興奮性神経細胞においてはノックアウトマウスで入力―出力比、二発促通 (paired-pulse facilitation: PPF) が増大、反復持続刺激後の回復の遅れ、シナプス間隙のグルタミン酸濃度の増加を反映する低親和性AMPA受容体阻害剤の感受性の低下が観察されており、シナプス小胞のリサイクリングの制御に関与する可能性が示唆されている[4] [4]。
また、CASTおよびELKSは神経活動依存的にプレシナプス性キナーゼSAD-BによりN末端領域がリン酸化され、少なくとも上頸神経節 (superior cervical ganglion: SCG) においてCASTのリン酸化はシナプス小胞の再補充を遅らせ、RRPサイズを下げる。こうした事実から、神経細胞の活性化時にRRPサイズを調節することで一時的にシナプスレベルでの抑制をかけている可能性が示唆されている[31] [31]。
個体機能
遺伝子改変マウスを用いた解析から、CASTノックアウトマウスの母親では、巣作りやリトリービングといった子育て行動に異常が見いだされている[17] [17]。また、全脳CASTノックアウトマウスにα-CaMKII陽性神経細胞特異的ELKSノックアウトマウスを掛け合わせると生後1日で死亡するが、そのメカニズムに関しては不明である[32] [32]。
疾患との関わり
CASTと具体的な疾患との関連性は現在知られていないが、ファミリーメンバーELKSは、言語障害を特徴とする自閉症スペクトラムとの関連が示唆されている[33][34] [33][34]。
関連語
参考文献
- ↑ 1.0 1.1 1.2
Ohtsuka, T., Takao-Rikitsu, E., Inoue, E., Inoue, M., Takeuchi, M., Matsubara, K., ..., & Takai, Y. (2002).
Cast: a novel protein of the cytomatrix at the active zone of synapses that forms a ternary complex with RIM1 and munc13-1. The Journal of cell biology, 158(3), 577-90. [PubMed:12163476] [PMC] [WorldCat] [DOI] - ↑
Wang, Y., Liu, X., Biederer, T., & Südhof, T.C. (2002).
A family of RIM-binding proteins regulated by alternative splicing: Implications for the genesis of synaptic active zones. Proceedings of the National Academy of Sciences of the United States of America, 99(22), 14464-9. [PubMed:12391317] [PMC] [WorldCat] [DOI] - ↑ 3.0 3.1
Wagh, D.A., Rasse, T.M., Asan, E., Hofbauer, A., Schwenkert, I., Dürrbeck, H., ..., & Buchner, E. (2006).
Bruchpilot, a protein with homology to ELKS/CAST, is required for structural integrity and function of synaptic active zones in Drosophila. Neuron, 49(6), 833-44. [PubMed:16543132] [WorldCat] [DOI] - ↑ 4.0 4.1 4.2
Kobayashi, S., Hida, Y., Ishizaki, H., Inoue, E., Tanaka-Okamoto, M., Yamasaki, M., ..., & Manabe, T. (2016).
The active zone protein CAST regulates synaptic vesicle recycling and quantal size in the mouse hippocampus. The European journal of neuroscience, 44(5), 2272-84. [PubMed:27422015] [WorldCat] [DOI] - ↑
Held, R.G., Liu, C., & Kaeser, P.S. (2016).
ELKS controls the pool of readily releasable vesicles at excitatory synapses through its N-terminal coiled-coil domains. eLife, 5. [PubMed:27253063] [PMC] [WorldCat] [DOI] - ↑ 6.0 6.1 6.2 6.3
Dong, W., Radulovic, T., Goral, R.O., Thomas, C., Suarez Montesinos, M., Guerrero-Given, D., ..., & Young, S.M. (2018).
CAST/ELKS Proteins Control Voltage-Gated Ca2+ Channel Density and Synaptic Release Probability at a Mammalian Central Synapse. Cell reports, 24(2), 284-293.e6. [PubMed:29996090] [PMC] [WorldCat] [DOI] - ↑
Kiyonaka, S., Nakajima, H., Takada, Y., Hida, Y., Yoshioka, T., Hagiwara, A., ..., & Ohtsuka, T. (2012).
Physical and functional interaction of the active zone protein CAST/ERC2 and the β-subunit of the voltage-dependent Ca(2+) channel. Journal of biochemistry, 152(2), 149-59. [PubMed:22577167] [WorldCat] [DOI] - ↑
Ohara-Imaizumi, M., Aoyagi, K., Yamauchi, H., Yoshida, M., Mori, M.X., Hida, Y., ..., & Ohtsuka, T. (2019).
ELKS/Voltage-Dependent Ca2+ Channel-β Subunit Module Regulates Polarized Ca2+ Influx in Pancreatic β Cells. Cell reports, 26(5), 1213-1226.e7. [PubMed:30699350] [WorldCat] [DOI] - ↑
Hida, Y., & Ohtsuka, T. (2010).
CAST and ELKS proteins: structural and functional determinants of the presynaptic active zone. Journal of biochemistry, 148(2), 131-7. [PubMed:20581014] [WorldCat] [DOI] - ↑
Hamada, S., & Ohtsuka, T. (2018).
CAST: Its molecular structure and phosphorylation-dependent regulation of presynaptic plasticity. Neuroscience research, 127, 25-32. [PubMed:29275163] [WorldCat] [DOI] - ↑
Nakata, T., Kitamura, Y., Shimizu, K., Tanaka, S., Fujimori, M., Yokoyama, S., ..., & Emi, M. (1999).
Fusion of a novel gene, ELKS, to RET due to translocation t(10;12)(q11;p13) in a papillary thyroid carcinoma. Genes, chromosomes & cancer, 25(2), 97-103. [PubMed:10337992] [WorldCat] [DOI] - ↑ 12.0 12.1 12.2 12.3
Deguchi-Tawarada, M., Inoue, E., Takao-Rikitsu, E., Inoue, M., Ohtsuka, T., & Takai, Y. (2004).
CAST2: identification and characterization of a protein structurally related to the presynaptic cytomatrix protein CAST. Genes to cells : devoted to molecular & cellular mechanisms, 9(1), 15-23. [PubMed:14723704] [WorldCat] [DOI] - ↑
Inoue, E., Deguchi-Tawarada, M., Takao-Rikitsu, E., Inoue, M., Kitajima, I., Ohtsuka, T., & Takai, Y. (2006).
ELKS, a protein structurally related to the active zone protein CAST, is involved in Ca2+-dependent exocytosis from PC12 cells. Genes to cells : devoted to molecular & cellular mechanisms, 11(6), 659-72. [PubMed:16716196] [WorldCat] [DOI] - ↑
Nishimune, H., Numata, T., Chen, J., Aoki, Y., Wang, Y., Starr, M.P., ..., & Stanford, J.A. (2012).
Active zone protein Bassoon co-localizes with presynaptic calcium channel, modifies channel function, and recovers from aging related loss by exercise. PloS one, 7(6), e38029. [PubMed:22701595] [PMC] [WorldCat] [DOI] - ↑
Deguchi-Tawarada, M., Inoue, E., Takao-Rikitsu, E., Inoue, M., Kitajima, I., Ohtsuka, T., & Takai, Y. (2006).
Active zone protein CAST is a component of conventional and ribbon synapses in mouse retina. The Journal of comparative neurology, 495(4), 480-96. [PubMed:16485285] [WorldCat] [DOI] - ↑
Ohara-Imaizumi, M., Ohtsuka, T., Matsushima, S., Akimoto, Y., Nishiwaki, C., Nakamichi, Y., ..., & Nagamatsu, S. (2005).
ELKS, a protein structurally related to the active zone-associated protein CAST, is expressed in pancreatic beta cells and functions in insulin exocytosis: interaction of ELKS with exocytotic machinery analyzed by total internal reflection fluorescence microscopy. Molecular biology of the cell, 16(7), 3289-300. [PubMed:15888548] [PMC] [WorldCat] [DOI] - ↑ 17.0 17.1
Hagiwara, A., Sugiyama, N., & Ohtsuka, T. (2020).
Impaired experience-dependent maternal care in presynaptic active zone protein CAST-deficient dams. Scientific reports, 10(1), 5238. [PubMed:32251313] [PMC] [WorldCat] [DOI] - ↑ 18.0 18.1
tom Dieck, S., Specht, D., Strenzke, N., Hida, Y., Krishnamoorthy, V., Schmidt, K.F., ..., & Moser, T. (2012).
Deletion of the presynaptic scaffold CAST reduces active zone size in rod photoreceptors and impairs visual processing. The Journal of neuroscience : the official journal of the Society for Neuroscience, 32(35), 12192-203. [PubMed:22933801] [PMC] [WorldCat] [DOI] - ↑ 19.0 19.1
Kaeser, P.S., Deng, L., Chávez, A.E., Liu, X., Castillo, P.E., & Südhof, T.C. (2009).
ELKS2alpha/CAST deletion selectively increases neurotransmitter release at inhibitory synapses. Neuron, 64(2), 227-39. [PubMed:19874790] [PMC] [WorldCat] [DOI] - ↑
Brose, N., Hofmann, K., Hata, Y., & Südhof, T.C. (1995).
Mammalian homologues of Caenorhabditis elegans unc-13 gene define novel family of C2-domain proteins. The Journal of biological chemistry, 270(42), 25273-80. [PubMed:7559667] [WorldCat] [DOI] - ↑
Wang, Y., Okamoto, M., Schmitz, F., Hofmann, K., & Südhof, T.C. (1997).
Rim is a putative Rab3 effector in regulating synaptic-vesicle fusion. Nature, 388(6642), 593-8. [PubMed:9252191] [WorldCat] [DOI] - ↑
tom Dieck, S., Sanmartí-Vila, L., Langnaese, K., Richter, K., Kindler, S., Soyke, A., ..., & Gundelfinger, E.D. (1998).
Bassoon, a novel zinc-finger CAG/glutamine-repeat protein selectively localized at the active zone of presynaptic nerve terminals. The Journal of cell biology, 142(2), 499-509. [PubMed:9679147] [PMC] [WorldCat] [DOI] - ↑
Cases-Langhoff, C., Voss, B., Garner, A.M., Appeltauer, U., Takei, K., Kindler, S., ..., & Garner, C.C. (1996).
Piccolo, a novel 420 kDa protein associated with the presynaptic cytomatrix. European journal of cell biology, 69(3), 214-23. [PubMed:8900486] [WorldCat] - ↑
Wang, X., Kibschull, M., Laue, M.M., Lichte, B., Petrasch-Parwez, E., & Kilimann, M.W. (1999).
Aczonin, a 550-kD putative scaffolding protein of presynaptic active zones, shares homology regions with Rim and Bassoon and binds profilin. The Journal of cell biology, 147(1), 151-62. [PubMed:10508862] [PMC] [WorldCat] [DOI] - ↑
Fenster, S.D., Chung, W.J., Zhai, R., Cases-Langhoff, C., Voss, B., Garner, A.M., ..., & Garner, C.C. (2000).
Piccolo, a presynaptic zinc finger protein structurally related to bassoon. Neuron, 25(1), 203-14. [PubMed:10707984] [WorldCat] [DOI] - ↑
Takao-Rikitsu, E., Mochida, S., Inoue, E., Deguchi-Tawarada, M., Inoue, M., Ohtsuka, T., & Takai, Y. (2004).
Physical and functional interaction of the active zone proteins, CAST, RIM1, and Bassoon, in neurotransmitter release. The Journal of cell biology, 164(2), 301-11. [PubMed:14734538] [PMC] [WorldCat] [DOI] - ↑
Hagiwara, A., Kitahara, Y., Grabner, C.P., Vogl, C., Abe, M., Kitta, R., ..., & Ohtsuka, T. (2018).
Cytomatrix proteins CAST and ELKS regulate retinal photoreceptor development and maintenance. The Journal of cell biology, 217(11), 3993-4006. [PubMed:30190286] [PMC] [WorldCat] [DOI] - ↑
Kittel, R.J., Wichmann, C., Rasse, T.M., Fouquet, W., Schmidt, M., Schmid, A., ..., & Sigrist, S.J. (2006).
Bruchpilot promotes active zone assembly, Ca2+ channel clustering, and vesicle release. Science (New York, N.Y.), 312(5776), 1051-4. [PubMed:16614170] [WorldCat] [DOI] - ↑
Deken, S.L., Vincent, R., Hadwiger, G., Liu, Q., Wang, Z.W., & Nonet, M.L. (2005).
Redundant localization mechanisms of RIM and ELKS in Caenorhabditis elegans. The Journal of neuroscience : the official journal of the Society for Neuroscience, 25(25), 5975-83. [PubMed:15976086] [PMC] [WorldCat] [DOI] - ↑
Liu, C., Bickford, L.S., Held, R.G., Nyitrai, H., Südhof, T.C., & Kaeser, P.S. (2014).
The active zone protein family ELKS supports Ca2+ influx at nerve terminals of inhibitory hippocampal neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 34(37), 12289-303. [PubMed:25209271] [PMC] [WorldCat] [DOI] - ↑
Mochida, S., Hida, Y., Tanifuji, S., Hagiwara, A., Hamada, S., Abe, M., ..., & Ohtsuka, T. (2016).
SAD-B Phosphorylation of CAST Controls Active Zone Vesicle Recycling for Synaptic Depression. Cell reports, 16(11), 2901-2913. [PubMed:27626661] [WorldCat] [DOI] - ↑
Hagiwara, A., Hamada, S., Hida, Y., & Ohtsuka, T. (2020).
Double deletion of the active zone proteins CAST/ELKS in the mouse forebrain causes high mortality of newborn pups. Molecular brain, 13(1), 13. [PubMed:31996256] [PMC] [WorldCat] [DOI] - ↑
Thevenon, J., Callier, P., Andrieux, J., Delobel, B., David, A., Sukno, S., ..., & Faivre, L. (2013).
12p13.33 microdeletion including ELKS/ERC1, a new locus associated with childhood apraxia of speech. European journal of human genetics : EJHG, 21(1), 82-8. [PubMed:22713806] [PMC] [WorldCat] [DOI] - ↑
Silva, I.M., Rosenfeld, J., Antoniuk, S.A., Raskin, S., & Sotomaior, V.S. (2014).
A 1.5Mb terminal deletion of 12p associated with autism spectrum disorder. Gene, 542(1), 83-6. [PubMed:24613754] [WorldCat] [DOI]