「分裂促進因子活性化タンパク質キナーゼ8相互作用タンパク質」の版間の差分
細編集の要約なし |
|||
| (同じ利用者による、間の4版が非表示) | |||
| 1行目: | 1行目: | ||
和歌山県立医科大学 | <div align="right"> | ||
<font size="+1">平井 秀一</font><br> | |||
''和歌山県立医科大学''<br> | |||
DOI:<selfdoi /> 原稿受付日:2025年12月16日 原稿完成日:2026年1月3日<br> | |||
担当編集委員:[http://researchmap.jp/wadancnp 和田 圭司](国立研究開発法人国立精神・神経医療研究センター) | |||
</div> | |||
英語名:MAPK8IP (Mitogen-activated protein kinase 8-interacting protein) | 英語名:MAPK8IP (Mitogen-activated protein kinase 8-interacting protein)<br> | ||
同義語:JIP (JNK-interacting protein), IB (Islet brain) | 同義語:JIP (JNK-interacting protein), IB (Islet brain) | ||
| 29行目: | 33行目: | ||
MAPK8IP1および2とは構造が全く異なるJNK結合足場タンパク質としてJun N-terminal protein kinase /stress-activated protein kinase-associated protein 1 (JSAP1) <ref name=Ito1999><pubmed>10523642</pubmed></ref> [6]が同定された。これはJIP3<ref name=Kelkar2000><pubmed>10629060</pubmed></ref>[7]とも呼ばれたが、現在はMAPK8IP3とよばれている。 | MAPK8IP1および2とは構造が全く異なるJNK結合足場タンパク質としてJun N-terminal protein kinase /stress-activated protein kinase-associated protein 1 (JSAP1) <ref name=Ito1999><pubmed>10523642</pubmed></ref> [6]が同定された。これはJIP3<ref name=Kelkar2000><pubmed>10629060</pubmed></ref>[7]とも呼ばれたが、現在はMAPK8IP3とよばれている。 | ||
そのパラログとして[[JNK-associated leucine zipper protein]] (JLP)[8]/[[sperm-associated antigen 9]] (SPAG9)[9]/JIP4[10]が同定されたが、現在はMAPK8IP4とよばれている<ref name=Lee2002><pubmed>12391307</pubmed></ref><ref name=Jagadish2005><pubmed>16077255</pubmed></ref><ref name=Kelkar2005><pubmed>15767678</pubmed></ref>。 | |||
== 構造 == | == 構造 == | ||
| 46行目: | 50行目: | ||
== 神経細胞での機能 == | == 神経細胞での機能 == | ||
MAPK8IP1-4は、種々の膜タンパク質との結合を介して小胞、リソソーム、オートファゴソームなどの[[細胞小器官]]と結合するとともに、キネシン、ダイナクチン-ダイニンといったモータータンパク質と結合することにより[[軸索輸送]]を支えるアダブター分子となっている<ref name=Fu2013><pubmed>23897889</pubmed></ref><ref name=Celestino2022><pubmed>35829703</pubmed></ref><ref name=Gowrishankar2021><pubmed>33788575</pubmed></ref><ref name=Cason2023><pubmed>37909920</pubmed></ref> [16] [17] [18] [19]。MAPK8IP3のショウジョウバエホモログであるSunday driver (SYD)は、これの変異により軸索内の小胞輸送が滞り、小胞の“渋滞”を招くことからこの名称がある<ref name=Bowman2000><pubmed>11106729</pubmed></ref> [12]。哺乳類神経細胞においては、MAPK8IP3ノックダウンにより軸索内でのプロテアーゼ欠損型リソソームの滞留とこれによる[[アミロイドβ]]42タンパク質の蓄積が認められる<ref name=Gowrishankar2021><pubmed>33788575</pubmed></ref> [18]。MAPK8IP3とそのパラログMAPK8IP4についてはさらに、小胞輸送に関わるARF6などの低分子量Gタンパク質による制御を受けつつモータータンパク質を活性化することにより、軸索輸送の効率や方向を決める分子である可能性が指摘されている<ref name=Gowrishankar2021><pubmed>33788575</pubmed></ref><ref name=Cason2023><pubmed>37909920</pubmed></ref> [17] [18] [19]。一方、結合しているJNKがどのような形でこういった機能の制御に関わっているかなど、未だ不明な点も多い。 | MAPK8IP1-4は、種々の膜タンパク質との結合を介して小胞、リソソーム、オートファゴソームなどの[[細胞小器官]]と結合するとともに、キネシン、ダイナクチン-ダイニンといったモータータンパク質と結合することにより[[軸索輸送]]を支えるアダブター分子となっている<ref name=Fu2013><pubmed>23897889</pubmed></ref><ref name=Celestino2022><pubmed>35829703</pubmed></ref><ref name=Gowrishankar2021><pubmed>33788575</pubmed></ref><ref name=Cason2023><pubmed>37909920</pubmed></ref> [16] [17] [18] [19]。MAPK8IP3のショウジョウバエホモログであるSunday driver (SYD)は、これの変異により軸索内の小胞輸送が滞り、小胞の“渋滞”を招くことからこの名称がある<ref name=Bowman2000><pubmed>11106729</pubmed></ref> [12]。哺乳類神経細胞においては、MAPK8IP3ノックダウンにより軸索内でのプロテアーゼ欠損型リソソームの滞留とこれによる[[アミロイドβ]]42タンパク質の蓄積が認められる<ref name=Gowrishankar2021><pubmed>33788575</pubmed></ref> [18]。MAPK8IP3とそのパラログMAPK8IP4についてはさらに、小胞輸送に関わるARF6などの低分子量Gタンパク質による制御を受けつつモータータンパク質を活性化することにより、軸索輸送の効率や方向を決める分子である可能性が指摘されている<ref name=Celestino2022><pubmed>35829703</pubmed></ref><ref name=Gowrishankar2021><pubmed>33788575</pubmed></ref><ref name=Cason2023><pubmed>37909920</pubmed></ref> [17] [18] [19]。一方、結合しているJNKがどのような形でこういった機能の制御に関わっているかなど、未だ不明な点も多い。 | ||
== ノックアウトマウス == | == ノックアウトマウス == | ||
=== MAPK8IP1ノックアウトマウス === | === MAPK8IP1ノックアウトマウス === | ||
寿命や生殖能力に異常はないが、[[海馬]]神経細胞において[[興奮毒性]]に関わるJNK活性化と[[細胞死]]が抑制される<ref name=Whitmarsh2001><pubmed>11562351</pubmed></ref> [20]他、高脂肪食により脂肪細胞で誘発されるJNK活性化とこれによるインスリン抵抗性が抑制される<ref name=Jaeschke2004><pubmed>15314024</pubmed></ref> [21]。MAPK8IP1とMAPK8IP2の双方をノックアウトした場合は [[低血糖]]による顕著な成長遅延を呈し、生後2週間程度で死亡する<ref name=Standen2009><pubmed>19564410</pubmed></ref> [22]。 | 寿命や生殖能力に異常はないが、[[海馬]]神経細胞において[[興奮毒性]]に関わるJNK活性化と[[細胞死]]が抑制される<ref name=Whitmarsh2001><pubmed>11562351</pubmed></ref> [20]他、高脂肪食により脂肪細胞で誘発されるJNK活性化とこれによるインスリン抵抗性が抑制される<ref name=Jaeschke2004><pubmed>15314024</pubmed></ref> [21]。MAPK8IP1とMAPK8IP2の双方をノックアウトした場合は [[低血糖]]による顕著な成長遅延を呈し、生後2週間程度で死亡する<ref name=Standen2009><pubmed>19564410</pubmed></ref> [22]。 | ||
=== | === MAPK8IP3ノックアウトマウス === | ||
[[終脳]]形成に異常を呈し、呼吸不全により生後間もなく死亡する<ref name=Kelkar2003><pubmed>12897243</pubmed></ref> [23]。 | [[終脳]]形成に異常を呈し、呼吸不全により生後間もなく死亡する<ref name=Kelkar2003><pubmed>12897243</pubmed></ref> [23]。 | ||
=== | === MAPK8IP4ノックアウトマウス === | ||
[[精子]]の運動性低下が原因と見られる[[雄性不妊]]の傾向が認められる<ref name=Iwanaga2008><pubmed>18574703</pubmed></ref> [24]。ただし成長や精巣の形態に異常はなく、上記の分子機能との関連性は不明。またノックアウトマウスから採取した[[B細胞]]においては[[リポ多糖]] ([[LPS]])刺激後の[[CD40]]の内在化([[エンドサイトーシス]])が抑制される<ref name=Wang2015><pubmed>25586186</pubmed></ref> [25]。 | [[精子]]の運動性低下が原因と見られる[[雄性不妊]]の傾向が認められる<ref name=Iwanaga2008><pubmed>18574703</pubmed></ref> [24]。ただし成長や精巣の形態に異常はなく、上記の分子機能との関連性は不明。またノックアウトマウスから採取した[[B細胞]]においては[[リポ多糖]] ([[LPS]])刺激後の[[CD40]]の内在化([[エンドサイトーシス]])が抑制される<ref name=Wang2015><pubmed>25586186</pubmed></ref> [25]。 | ||
2026年1月17日 (土) 11:26時点における最新版
平井 秀一
和歌山県立医科大学
DOI:10.14931/bsd.11462 原稿受付日:2025年12月16日 原稿完成日:2026年1月3日
担当編集委員:和田 圭司(国立研究開発法人国立精神・神経医療研究センター)
英語名:MAPK8IP (Mitogen-activated protein kinase 8-interacting protein)
同義語:JIP (JNK-interacting protein), IB (Islet brain)
分裂促進因子活性化タンパク質キナーゼ8相互作用タンパク質 (MAPK8IP)は、MAPK8及びこれの活性化に関わるタンパク質リン酸化酵素群と結合する足場タンパク質であるとともに、キネシンやダイナクチン-ダイニンと結合することにより細胞内輸送にも係る多機能タンパク質である。パラログとしてMAPK8IP1および2が存在する他、分子構造は全く異なるものの同じく細胞内輸送に係るMAPK8結合タンパク質としてMAPK8IP3およびMAPK8IP4が存在する。
分裂促進因子活性化タンパク質キナーゼ8相互作用タンパク質とは
分裂促進因子活性化タンパク質キナーゼ (mitogen-activated kinase, MAPK)に属するタンパク質リン酸化酵素は上流のMAP2Kに属するタンパク質リン酸化酵素によりリン酸化されることで活性化し、MAP2Kはさらに上流のMAP3Kに属するタンパク質リン酸化酵素によりリン酸化されることで活性化する。このシグナル伝達機構は酵母から哺乳類まで保存されておりMAPキナーゼカスケードと呼ばれている。
酵母でこういったリン酸化を介したシグナル伝達の効率を高める足場タンパク質として、STE5が同定された[1] [1]。哺乳類においても、MAPKの一つであるc-Jun N-terminal kinase (JNK)と結合してこれを阻害するタンパク質として同定されたJNK-interacting protein 1 (JIP1、現在はMAPK8IP1と呼ばれる) [2] [2]が、STE5様の足場タンパク質として機能する(ホモログではない)と考えられるようになった[3] [3]。さらにMAPK8IP1はJNKのみならず、JNKの上流であるMAP2KやMAP3Kとも結合することが示された。
線虫やショウジョウバエのMAPK8IP3ホモログであるUNC16 [4] [11]やSunday driver (SYD) [5] [12]が神経細胞における軸索輸送に係ることが示されたことに加え、MAPK8IP1,2のC末端部にキネシン軽鎖結合配列が見つかった[6] [13]ことにより、これらMAPK8IPファミリータンパク質の細胞内輸送における機能についても注目を集めている。
サブファミリー
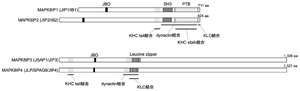
MAPK8IP1(JIP1/IB1)、MAPK8IP2(JIP2/IB2)、MAPK8IP3(JIP3/JSAP1)、MAPK8IP4(JIP4/JLP/SPAG9)の一次構造を模式的に示す。各タンパク質は JNK結合ドメイン(JNK-binding domain; JBD)を有し、MAPK8IP1/2のC末端には Src homology 3(SH3)ドメインおよび phosphotyrosine-binding(PTB)ドメインが、MAPK8IP3/4には ロイシンジッパー(leucine zipper)モチーフが存在する。上の図にはこれらに加え、キネシン重鎖(kinesin heavy chain; KHC)、キネシン軽鎖(kinesin light chain; KLC)、およびダイナクチンとの結合部位が示されている。
現在、ヒトのMAPK関連遺伝子に統一的な名称が使用されるようになり、JNK1自体がMAPK8と呼称されるようになったのに合わせ、もとJIP1-4と呼ばれていたタンパク質もmitogen-activated protein kinase 8 interacting protein (MAPK8IP1-4)呼ばれる様になった。ただし、その結合がMAPK8特異的ということではなく、MAPK9 (JNK2)、MAPK10 (JNK3)とも結合する[7][8] [5] [6]。
MAPK8IP1および2
MAPK8IP1 (JIP1)、MAPK8IP2 (JIP2)が属する。
MAPK8IP1はインスリン受容体からのシグナル伝達を制御する因子としても独立に発見されており、その発現パターンからislet brain-1 (IB1)とも呼ばれている[9] [4]。そのパラログとしてはMAPK8IP2はIB2としても知られている[7] [5]。
MAPK8IP3および4
MAPK8IP3 (JSAP1/JIP3)、MAPK8IP4 (JLP/SPAG9/JIP4)が属する。
MAPK8IP1および2とは構造が全く異なるJNK結合足場タンパク質としてJun N-terminal protein kinase /stress-activated protein kinase-associated protein 1 (JSAP1) [8] [6]が同定された。これはJIP3[10][7]とも呼ばれたが、現在はMAPK8IP3とよばれている。
そのパラログとしてJNK-associated leucine zipper protein (JLP)[8]/sperm-associated antigen 9 (SPAG9)[9]/JIP4[10]が同定されたが、現在はMAPK8IP4とよばれている[11][12][13]。
構造
MAPK8IP1及びMAPK8IP2はMAPK8結合ドメイン(JBD)に加え、src homology 3 (SH3)ドメイン及びphosphotyrosine binding (PTB)ドメインを有する(図)。MAPK8IP3及びMAPK8IP4はMAPK8結合ドメイン(JBD)に加え、ロイシンジッパーを有する。MAPK8IP1はホモ二量体を形成するとともにMAPK8IP2やMAPK8IP3とも結合する[7][13] [5] [10]。またキネシン重鎖、軽鎖およびダイナクチンも結合することが知られている。また、いずれについてもスプライスバリアントの存在が知られているが、ここではヒトのタンパク質で最も分子量の大きいものの構造を示している。
発現
MAPK8IP1~4はいずれも脳において高い発現が認められる[9][7][8][13] [4] [5] [6] [10]。MAPK8IP1は膵島においても[9] [4]、MAPK8IP4については腎臓、肝臓、精巣においても[11][12][13] [8] [9] [10]高い発現が認められる。いずれも細胞質に分布する他、膵島細胞においてMAPK8IP1は核質にも分布する[9] [4]。MAPK8IP3,4は膜貫通ドメイン様のアミノ酸配列を有するが、膜構造への結合は限定的とされる[13] [10]。
分子機能
MAPK8IP1, 2
JNKと呼ばれるグループのMAPK (MAPK8~10)の活性化に関わるキナーゼカスケードの足場タンパク質としてMAP2K7、MAP3K9~13と結合する[3][7] [3] [5]。インスリン受容体からのシグナル伝達においては、insulin receptor substrate 1 (IRS1)と結合してこれのJNKによるリン酸化を促すことによりインスリンシグナルを抑制する[9] [4]。他にもアミロイド前駆タンパク質 (APP)やアポリポタンパク質E受容体2 (ApoER2)など多様なタンパク質と結合する[14][15] [14] [15]ことに加え、キネシンやダイナクチン-ダイニンといったモータータンパク質と結合することで、細胞内輸送におけるアタプターとして様々な分子や小胞の輸送に関わる[6][16] [13] [16]。
MAPK8IP3, 4
JNKグループに属するMAPKの活性化に関わるキナーゼカスケードの足場としても機能する[8] [10] [6] [7]他、MAPK8IP4についてはp38と呼ばれるグループに属するMAPK (MAPK14)の活性化にも関わる[11][13] [8] [10]。線虫のUNC16及びショウジョウバエのsynapse defective protein (SYD)のホモログであり、キネシンやダイナクチン-ダイニンと結合することによりリソソームやオートファゴソームを含む様々な種類の小胞の輸送を支えるアダプターとして機能する[17][18] [17] [18]。さらに、MAPK8IP3, 4はダイニンモーターを活性化することに加え、輸送の制御に関わる低分子量Gタンパク質の一つARF6のエフェクターとして位置付けられている[19] [19]。
神経細胞での機能
MAPK8IP1-4は、種々の膜タンパク質との結合を介して小胞、リソソーム、オートファゴソームなどの細胞小器官と結合するとともに、キネシン、ダイナクチン-ダイニンといったモータータンパク質と結合することにより軸索輸送を支えるアダブター分子となっている[16][17][18][19] [16] [17] [18] [19]。MAPK8IP3のショウジョウバエホモログであるSunday driver (SYD)は、これの変異により軸索内の小胞輸送が滞り、小胞の“渋滞”を招くことからこの名称がある[5] [12]。哺乳類神経細胞においては、MAPK8IP3ノックダウンにより軸索内でのプロテアーゼ欠損型リソソームの滞留とこれによるアミロイドβ42タンパク質の蓄積が認められる[18] [18]。MAPK8IP3とそのパラログMAPK8IP4についてはさらに、小胞輸送に関わるARF6などの低分子量Gタンパク質による制御を受けつつモータータンパク質を活性化することにより、軸索輸送の効率や方向を決める分子である可能性が指摘されている[17][18][19] [17] [18] [19]。一方、結合しているJNKがどのような形でこういった機能の制御に関わっているかなど、未だ不明な点も多い。
ノックアウトマウス
MAPK8IP1ノックアウトマウス
寿命や生殖能力に異常はないが、海馬神経細胞において興奮毒性に関わるJNK活性化と細胞死が抑制される[20] [20]他、高脂肪食により脂肪細胞で誘発されるJNK活性化とこれによるインスリン抵抗性が抑制される[21] [21]。MAPK8IP1とMAPK8IP2の双方をノックアウトした場合は 低血糖による顕著な成長遅延を呈し、生後2週間程度で死亡する[22] [22]。
MAPK8IP3ノックアウトマウス
終脳形成に異常を呈し、呼吸不全により生後間もなく死亡する[23] [23]。
MAPK8IP4ノックアウトマウス
精子の運動性低下が原因と見られる雄性不妊の傾向が認められる[24] [24]。ただし成長や精巣の形態に異常はなく、上記の分子機能との関連性は不明。またノックアウトマウスから採取したB細胞においてはリポ多糖 (LPS)刺激後のCD40の内在化(エンドサイトーシス)が抑制される[25] [25]。
疾患との関わり
MAPK8IP1のプロモーター領域における点変異と低密度リポタンパク質受容体関連タンパク質(LRP1)遺伝子のミスセンス変異が重なることでアルツハイマー病などの認知症発症リスクが高まるとされている[26] [26]。また、ある2型糖尿病家系において疾患との関連性が認められるMAPK8IP1遺伝子のミスセンス変異が見つかっている[27] [27]。
多様な脳奇形を伴う/伴わない神経発達障害を発症している血縁のない十数名においてMAPK8IP3遺伝子のナンセンス・ミスセンス変異およびフレームシフトが見つかっている[28] [28]。健常者においてはほぼ見つからないことから、MAPK8IP3の機能不全がこの疾患の原因となり得るものと考えられている。
関連語
参考文献
- ↑
Choi, K.Y., Satterberg, B., Lyons, D.M., & Elion, E.A. (1994).
Ste5 tethers multiple protein kinases in the MAP kinase cascade required for mating in S. cerevisiae. Cell, 78(3), 499-512. [PubMed:8062390] [WorldCat] [DOI] - ↑
Dickens, M., Rogers, J.S., Cavanagh, J., Raitano, A., Xia, Z., Halpern, J.R., ..., & Davis, R.J. (1997).
A cytoplasmic inhibitor of the JNK signal transduction pathway. Science (New York, N.Y.), 277(5326), 693-6. [PubMed:9235893] [WorldCat] [DOI] - ↑ 3.0 3.1
Whitmarsh, A.J., Cavanagh, J., Tournier, C., Yasuda, J., & Davis, R.J. (1998).
A mammalian scaffold complex that selectively mediates MAP kinase activation. Science (New York, N.Y.), 281(5383), 1671-4. [PubMed:9733513] [WorldCat] [DOI] - ↑
Byrd, D.T., Kawasaki, M., Walcoff, M., Hisamoto, N., Matsumoto, K., & Jin, Y. (2001).
UNC-16, a JNK-signaling scaffold protein, regulates vesicle transport in C. elegans. Neuron, 32(5), 787-800. [PubMed:11738026] [WorldCat] [DOI] - ↑ 5.0 5.1
Bowman, A.B., Kamal, A., Ritchings, B.W., Philp, A.V., McGrail, M., Gindhart, J.G., & Goldstein, L.S. (2000).
Kinesin-dependent axonal transport is mediated by the sunday driver (SYD) protein. Cell, 103(4), 583-94. [PubMed:11106729] [WorldCat] [DOI] - ↑ 6.0 6.1
Verhey, K.J., Meyer, D., Deehan, R., Blenis, J., Schnapp, B.J., Rapoport, T.A., & Margolis, B. (2001).
Cargo of kinesin identified as JIP scaffolding proteins and associated signaling molecules. The Journal of cell biology, 152(5), 959-70. [PubMed:11238452] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1 7.2 7.3 7.4
Yasuda, J., Whitmarsh, A.J., Cavanagh, J., Sharma, M., & Davis, R.J. (1999).
The JIP group of mitogen-activated protein kinase scaffold proteins. Molecular and cellular biology, 19(10), 7245-54. [PubMed:10490659] [PMC] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2 8.3
Ito, M., Yoshioka, K., Akechi, M., Yamashita, S., Takamatsu, N., Sugiyama, K., ..., & Yamamoto, K.I. (1999).
JSAP1, a novel jun N-terminal protein kinase (JNK)-binding protein that functions as a Scaffold factor in the JNK signaling pathway. Molecular and cellular biology, 19(11), 7539-48. [PubMed:10523642] [PMC] [WorldCat] [DOI] - ↑ 9.0 9.1 9.2 9.3 9.4
Bonny, C., Nicod, P., & Waeber, G. (1998).
IB1, a JIP-1-related nuclear protein present in insulin-secreting cells. The Journal of biological chemistry, 273(4), 1843-6. [PubMed:9442013] [WorldCat] [DOI] - ↑ 10.0 10.1
Kelkar, N., Gupta, S., Dickens, M., & Davis, R.J. (2000).
Interaction of a mitogen-activated protein kinase signaling module with the neuronal protein JIP3. Molecular and cellular biology, 20(3), 1030-43. [PubMed:10629060] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1 11.2
Lee, C.M., Onésime, D., Reddy, C.D., Dhanasekaran, N., & Reddy, E.P. (2002).
JLP: A scaffolding protein that tethers JNK/p38MAPK signaling modules and transcription factors. Proceedings of the National Academy of Sciences of the United States of America, 99(22), 14189-94. [PubMed:12391307] [PMC] [WorldCat] [DOI] - ↑ 12.0 12.1
Jagadish, N., Rana, R., Mishra, D., Kumar, M., & Suri, A. (2005).
Sperm associated antigen 9 (SPAG9): a new member of c-Jun NH2 -terminal kinase (JNK) interacting protein exclusively expressed in testis. The Keio journal of medicine, 54(2), 66-71. [PubMed:16077255] [WorldCat] [DOI] - ↑ 13.0 13.1 13.2 13.3 13.4 13.5
Kelkar, N., Standen, C.L., & Davis, R.J. (2005).
Role of the JIP4 scaffold protein in the regulation of mitogen-activated protein kinase signaling pathways. Molecular and cellular biology, 25(7), 2733-43. [PubMed:15767678] [PMC] [WorldCat] [DOI] - ↑
Matsuda, S., Yasukawa, T., Homma, Y., Ito, Y., Niikura, T., Hiraki, T., ..., & Nishimoto, I. (2001).
c-Jun N-terminal kinase (JNK)-interacting protein-1b/islet-brain-1 scaffolds Alzheimer's amyloid precursor protein with JNK. The Journal of neuroscience : the official journal of the Society for Neuroscience, 21(17), 6597-607. [PubMed:11517249] [PMC] [WorldCat] [DOI] - ↑
Stockinger, W., Brandes, C., Fasching, D., Hermann, M., Gotthardt, M., Herz, J., ..., & Nimpf, J. (2000).
The reelin receptor ApoER2 recruits JNK-interacting proteins-1 and -2. The Journal of biological chemistry, 275(33), 25625-32. [PubMed:10827199] [WorldCat] [DOI] - ↑ 16.0 16.1
Fu, M.M., & Holzbaur, E.L. (2013).
JIP1 regulates the directionality of APP axonal transport by coordinating kinesin and dynein motors. The Journal of cell biology, 202(3), 495-508. [PubMed:23897889] [PMC] [WorldCat] [DOI] - ↑ 17.0 17.1 17.2
Celestino, R., Gama, J.B., Castro-Rodrigues, A.F., Barbosa, D.J., Rocha, H., d'Amico, E.A., ..., & Gassmann, R. (2022).
JIP3 interacts with dynein and kinesin-1 to regulate bidirectional organelle transport. The Journal of cell biology, 221(8). [PubMed:35829703] [PMC] [WorldCat] [DOI] - ↑ 18.0 18.1 18.2 18.3
Gowrishankar, S., Lyons, L., Rafiq, N.M., Roczniak-Ferguson, A., De Camilli, P., & Ferguson, S.M. (2021).
Overlapping roles of JIP3 and JIP4 in promoting axonal transport of lysosomes in human iPSC-derived neurons. Molecular biology of the cell, 32(11), 1094-1103. [PubMed:33788575] [PMC] [WorldCat] [DOI] - ↑ 19.0 19.1 19.2
Cason, S.E., & Holzbaur, E.L.F. (2023).
Axonal transport of autophagosomes is regulated by dynein activators JIP3/JIP4 and ARF/RAB GTPases. The Journal of cell biology, 222(12). [PubMed:37909920] [PMC] [WorldCat] [DOI] - ↑
Whitmarsh, A.J., Kuan, C.Y., Kennedy, N.J., Kelkar, N., Haydar, T.F., Mordes, J.P., ..., & Davis, R.J. (2001).
Requirement of the JIP1 scaffold protein for stress-induced JNK activation. Genes & development, 15(18), 2421-32. [PubMed:11562351] [PMC] [WorldCat] [DOI] - ↑
Jaeschke, A., Czech, M.P., & Davis, R.J. (2004).
An essential role of the JIP1 scaffold protein for JNK activation in adipose tissue. Genes & development, 18(16), 1976-80. [PubMed:15314024] [PMC] [WorldCat] [DOI] - ↑
Standen, C.L., Kennedy, N.J., Flavell, R.A., & Davis, R.J. (2009).
Signal transduction cross talk mediated by Jun N-terminal kinase-interacting protein and insulin receptor substrate scaffold protein complexes. Molecular and cellular biology, 29(17), 4831-40. [PubMed:19564410] [PMC] [WorldCat] [DOI] - ↑
Kelkar, N., Delmotte, M.H., Weston, C.R., Barrett, T., Sheppard, B.J., Flavell, R.A., & Davis, R.J. (2003).
Morphogenesis of the telencephalic commissure requires scaffold protein JNK-interacting protein 3 (JIP3). Proceedings of the National Academy of Sciences of the United States of America, 100(17), 9843-8. [PubMed:12897243] [PMC] [WorldCat] [DOI] - ↑
Iwanaga, A., Wang, G., Gantulga, D., Sato, T., Baljinnyam, T., Shimizu, K., ..., & Yoshioka, K. (2008).
Ablation of the scaffold protein JLP causes reduced fertility in male mice. Transgenic research, 17(6), 1045-58. [PubMed:18574703] [WorldCat] [DOI] - ↑
Wang, H.M., Yan, Q., Yang, T., Cheng, H., Du, J., Yoshioka, K., ..., & Ding, G.H. (2015).
Scaffold protein JLP is critical for CD40 signaling in B lymphocytes. The Journal of biological chemistry, 290(9), 5256-66. [PubMed:25586186] [PMC] [WorldCat] [DOI] - ↑
Helbecque, N., Abderrahamani, A., Meylan, L., Riederer, B., Mooser, V., Miklossy, J., ..., & Waeber, G. (2003).
Islet-brain1/C-Jun N-terminal kinase interacting protein-1 (IB1/JIP-1) promoter variant is associated with Alzheimer's disease. Molecular psychiatry, 8(4), 413-22, 363. [PubMed:12740599] [WorldCat] [DOI] - ↑
Waeber, G., Delplanque, J., Bonny, C., Mooser, V., Steinmann, M., Widmann, C., ..., & Froguel, P. (2000).
The gene MAPK8IP1, encoding islet-brain-1, is a candidate for type 2 diabetes. Nature genetics, 24(3), 291-5. [PubMed:10700186] [WorldCat] [DOI] - ↑
Platzer, K., Sticht, H., Edwards, S.L., Allen, W., Angione, K.M., Bonati, M.T., ..., & Jamra, R. (2019).
De Novo Variants in MAPK8IP3 Cause Intellectual Disability with Variable Brain Anomalies. American journal of human genetics, 104(2), 203-212. [PubMed:30612693] [PMC] [WorldCat] [DOI]