「小胞モノアミントランスポーター」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| 19行目: | 19行目: | ||
VMATは、小胞内外のH<sup>+</sup>の電気化学的勾配を駆動力としてモノアミンを小胞内に輸送し、開口放出に備えて貯蔵している。VMAT1とVMAT2の場合、1分子のモノアミンを取り込むために、2分子のH<sup>+</sup>が必要となる。H<sup>+</sup>は、V型ATPアーゼのATP加水分解によって産生され、小胞内に移動される。これにより膜内外でpHの勾配が生じるため、VMATはH<sup>+</sup>とモノアミンを対向輸送することで、小胞内にモノアミンを取り込んでいる(図2)<ref name=ref1><pubmed>19259829</pubmed></ref>。また、ClC-3やClC-7などのCl<sup>-</sup>チャネルにより流入したCl<sup>-</sup>イオンが小胞膜を脱分極し、膜内外における電荷のバランスを維持している。これは、正に帯電したモノアミンを取り込む際の反発力を抑制するため、膜電位を負ないし中性に維持する必要があるためと考えられる。 | VMATは、小胞内外のH<sup>+</sup>の電気化学的勾配を駆動力としてモノアミンを小胞内に輸送し、開口放出に備えて貯蔵している。VMAT1とVMAT2の場合、1分子のモノアミンを取り込むために、2分子のH<sup>+</sup>が必要となる。H<sup>+</sup>は、V型ATPアーゼのATP加水分解によって産生され、小胞内に移動される。これにより膜内外でpHの勾配が生じるため、VMATはH<sup>+</sup>とモノアミンを対向輸送することで、小胞内にモノアミンを取り込んでいる(図2)<ref name=ref1><pubmed>19259829</pubmed></ref>。また、ClC-3やClC-7などのCl<sup>-</sup>チャネルにより流入したCl<sup>-</sup>イオンが小胞膜を脱分極し、膜内外における電荷のバランスを維持している。これは、正に帯電したモノアミンを取り込む際の反発力を抑制するため、膜電位を負ないし中性に維持する必要があるためと考えられる。 | ||
[[Image:モノアミン貯蔵の仕組み.jpg|thumb|250px|'''図2.VMATによる小胞内へのモノアミン取り込み機構'''<br>文献<ref name=ref1 />から改変]] | [[Image:モノアミン貯蔵の仕組み.jpg|thumb|250px|'''図2.VMATによる小胞内へのモノアミン取り込み機構'''<br>文献<ref name=ref1 />から改変]] | ||
モノアミンの合成と小胞輸送は従来、それぞれ独立した過程と考えられていたが、小胞輸送の効率化のため、これらは一連の過程であるとする説がある。例えば、シナプス小胞膜上のVMAT2は、ドーパミン合成酵素であるチロシンヒドロキシラーゼや芳香族アミノ酸脱炭酸酵素、シャペロンタンパク質であるHsc70と複合体を形成しており、合成されたドーパミンを素早く効率的に小胞内に取り込んでいる、というモデルが提示されている<ref><pubmed>21797260</pubmed></ref> | モノアミンの合成と小胞輸送は従来、それぞれ独立した過程と考えられていたが、小胞輸送の効率化のため、これらは一連の過程であるとする説がある。例えば、シナプス小胞膜上のVMAT2は、ドーパミン合成酵素であるチロシンヒドロキシラーゼや芳香族アミノ酸脱炭酸酵素、シャペロンタンパク質であるHsc70と複合体を形成しており、合成されたドーパミンを素早く効率的に小胞内に取り込んでいる、というモデルが提示されている<ref><pubmed>21797260</pubmed></ref>。これは神経保護作用の点で重要であり、合成されたモノアミンの細胞質への拡散を最小限に抑え、酸化やそれに伴う毒性発現を抑制すると考えられる。 | ||
| 27行目: | 27行目: | ||
ドーパミン神経において、メタンフェタミンは、直接VMAT2に作用してシナプス小胞内への取り込みを阻害するだけでなく、貯蔵されているドーパミンを細胞質へ放出させることにより、小胞内のドーパミン量を減少させる。この細胞質への放出は、メタンフェタミンが小胞膜を透過して小胞内に拡散しpHの勾配を減少させることで、モノアミン貯蔵に必要なエネルギーが失われるために起こる<ref><pubmed>17233532</pubmed></ref>。 | ドーパミン神経において、メタンフェタミンは、直接VMAT2に作用してシナプス小胞内への取り込みを阻害するだけでなく、貯蔵されているドーパミンを細胞質へ放出させることにより、小胞内のドーパミン量を減少させる。この細胞質への放出は、メタンフェタミンが小胞膜を透過して小胞内に拡散しpHの勾配を減少させることで、モノアミン貯蔵に必要なエネルギーが失われるために起こる<ref><pubmed>17233532</pubmed></ref>。 | ||
上述の精神刺激薬以外に、VMAT阻害剤としては、レセルピンとテトラベナジン、ロベリン等がある。レセルピンは、VMATのモノアミン認識部位に結合し、モノアミンの小胞輸送を阻害する。一方で、テトラベナジンは、レセルピンの作用部位とは異なる部位に結合して阻害作用を発揮すると考えられている。 | |||
2012年4月20日 (金) 12:30時点における版
英:Vesicular Monoamine Transporter、英略語:VMAT
小胞モノアミントランスポーター(Vesicular monoamine transporter、以下VMAT)は、4種類ある小胞神経伝達物質輸送体タンパク質(トランスポーター)のうちの1つであり、神経終末にあるシナプス小胞や、副腎のクロム親和性細胞の有芯小胞に存在する。細胞膜モノアミントランスポーターにより細胞質に取り込まれたモノアミン神経伝達物質を、電気化学的勾配を利用して小胞内に輸送、貯蔵する。
サブタイプ
哺乳類では、Slc18a1遺伝子にコードされるVMAT1と、Slc18a2遺伝子にコードされるVMAT2の、2つのサブタイプが存在する。これらVMAT1とVMAT2は、小胞アセチルコリントランスポーター(VAChT)とともにSLC(solute carrier)トランスポータースーパーファミリーの1つ、SLC18ファミリーを形成している[1]。
VMAT1は、主に副腎髄質のクロム親和性細胞や腸管の腸クロム親和性細胞など、さまざまな神経内分泌細胞の有芯小胞の膜上に存在する。一方で、VMAT2は、主に中枢神経系や交感神経系のモノアミン作動性神経終末にあるシナプス小胞の膜上に存在するが、VMAT1と同様に副腎髄質のクロム親和性細胞の有芯小胞にも存在する。
構造と機能
VMATの構造
上述したように、VMAT1とVMAT2は別々の遺伝子によりコードされているが、両者の配列相同性および構造は極めて類似している。細胞膜モノアミントランスポーターと同じく、12個の膜貫通ドメイン(TMD1~12)をもつ膜タンパク質で、アミノ末端(N末端)とカルボキシ末端(C末端)は細胞質側に位置する(図1)。1番目と2番目の膜貫通ドメイン(TMD1~2)の間には、小胞内に面するループ構造をもつ。膜貫通領域の予測法であるハイドロパシーモデルでは、このループ構造に数個のグリコシル化部位が存在すると予測されている[2]。
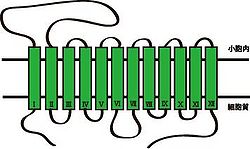
文献[3]から改変
VMATによる小胞へのモノアミン輸送
VMATは、小胞内外のH+の電気化学的勾配を駆動力としてモノアミンを小胞内に輸送し、開口放出に備えて貯蔵している。VMAT1とVMAT2の場合、1分子のモノアミンを取り込むために、2分子のH+が必要となる。H+は、V型ATPアーゼのATP加水分解によって産生され、小胞内に移動される。これにより膜内外でpHの勾配が生じるため、VMATはH+とモノアミンを対向輸送することで、小胞内にモノアミンを取り込んでいる(図2)[4]。また、ClC-3やClC-7などのCl-チャネルにより流入したCl-イオンが小胞膜を脱分極し、膜内外における電荷のバランスを維持している。これは、正に帯電したモノアミンを取り込む際の反発力を抑制するため、膜電位を負ないし中性に維持する必要があるためと考えられる。
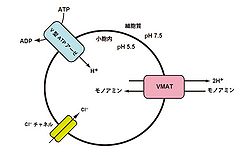
文献[4]から改変
モノアミンの合成と小胞輸送は従来、それぞれ独立した過程と考えられていたが、小胞輸送の効率化のため、これらは一連の過程であるとする説がある。例えば、シナプス小胞膜上のVMAT2は、ドーパミン合成酵素であるチロシンヒドロキシラーゼや芳香族アミノ酸脱炭酸酵素、シャペロンタンパク質であるHsc70と複合体を形成しており、合成されたドーパミンを素早く効率的に小胞内に取り込んでいる、というモデルが提示されている[5]。これは神経保護作用の点で重要であり、合成されたモノアミンの細胞質への拡散を最小限に抑え、酸化やそれに伴う毒性発現を抑制すると考えられる。
依存性薬物とVMAT
覚せい剤であるコカイン、メチルフェニデート、メタンフェタミンは、モノアミントランスポーターを標的分子としている。コカインやメチルフェニデートが細胞膜モノアミントランスポーターの阻害により薬理効果を生じる一方、メタンフェタミンはシナプス小胞膜上のVMAT2にも作用する[6]。

文献[6]から改変
ドーパミン神経において、メタンフェタミンは、直接VMAT2に作用してシナプス小胞内への取り込みを阻害するだけでなく、貯蔵されているドーパミンを細胞質へ放出させることにより、小胞内のドーパミン量を減少させる。この細胞質への放出は、メタンフェタミンが小胞膜を透過して小胞内に拡散しpHの勾配を減少させることで、モノアミン貯蔵に必要なエネルギーが失われるために起こる[7]。
上述の精神刺激薬以外に、VMAT阻害剤としては、レセルピンとテトラベナジン、ロベリン等がある。レセルピンは、VMATのモノアミン認識部位に結合し、モノアミンの小胞輸送を阻害する。一方で、テトラベナジンは、レセルピンの作用部位とは異なる部位に結合して阻害作用を発揮すると考えられている。
関連項目
- モノアミン
- 小胞アセチルコリントランスポーター
- 小胞グルタミン酸トランスポーター
- 小胞GABAトランスポーター
- ドーパミントランスポーター
- セロトニントランスポーター
- ノルエピネフリントランスポーター
- 薬物依存
- 精神刺激薬
- 覚醒剤
参考文献
- ↑
Gether, U., Andersen, P.H., Larsson, O.M., & Schousboe, A. (2006).
Neurotransmitter transporters: molecular function of important drug targets. Trends in pharmacological sciences, 27(7), 375-83. [PubMed:16762425] [WorldCat] [DOI] - ↑
Wimalasena, K. (2011).
Vesicular monoamine transporters: structure-function, pharmacology, and medicinal chemistry. Medicinal research reviews, 31(4), 483-519. [PubMed:20135628] [PMC] [WorldCat] [DOI] - ↑
Eiden, L.E., Schäfer, M.K., Weihe, E., & Schütz, B. (2004).
The vesicular amine transporter family (SLC18): amine/proton antiporters required for vesicular accumulation and regulated exocytotic secretion of monoamines and acetylcholine. Pflugers Archiv : European journal of physiology, 447(5), 636-40. [PubMed:12827358] [WorldCat] [DOI] - ↑ 4.0 4.1
Guillot, T.S., & Miller, G.W. (2009).
Protective actions of the vesicular monoamine transporter 2 (VMAT2) in monoaminergic neurons. Molecular neurobiology, 39(2), 149-70. [PubMed:19259829] [WorldCat] [DOI] - ↑
Sager, J.J., & Torres, G.E. (2011).
Proteins interacting with monoamine transporters: current state and future challenges. Biochemistry, 50(34), 7295-310. [PubMed:21797260] [WorldCat] [DOI] - ↑ 6.0 6.1
Howell, L.L., & Kimmel, H.L. (2008).
Monoamine transporters and psychostimulant addiction. Biochemical pharmacology, 75(1), 196-217. [PubMed:17825265] [WorldCat] [DOI] - ↑
Zheng, G., Dwoskin, L.P., & Crooks, P.A. (2006).
Vesicular monoamine transporter 2: role as a novel target for drug development. The AAPS journal, 8(4), E682-92. [PubMed:17233532] [PMC] [WorldCat] [DOI]