「CREB制御転写コアクチベーター」の版間の差分
細編集の要約なし |
細 →機能 |
||
| (同じ利用者による、間の4版が非表示) | |||
| 1行目: | 1行目: | ||
<div align="right"> | |||
<font size="+1">[https://researchmap.jp/yukinorihirano 平野 恭敬]</font><br> | |||
''香港科学技術大学''<br> | |||
DOI:<selfdoi /> 原稿受付日:2025年12月27日 原稿完成日:2026年1月6日<br> | |||
担当編集委員:[http://researchmap.jp/read0192882 古屋敷 智之](東京科学大学大学院 医歯学総合研究科 薬理学分野)<br> | |||
</div> | |||
英語名:CREB-regulated transcriptional coactivator<br> | 英語名:CREB-regulated transcriptional coactivator<br> | ||
英略語:CRTC | 英略語:CRTC | ||
| 6行目: | 13行目: | ||
==発見== | ==発見== | ||
CRTCファミリータンパクである[[哺乳類]][[CRTC1]]と[[CRTC2]]は、[[cAMP応答配列結合タンパク質]] ([[CREB]])結合配列である[[cAMP応答配列]]の下流で[[ルシフェラーゼ]]を発現するレポーターを用い、CRE依存的な転写を活性化させる因子として同定された。さらにアミノ酸の相同性から[[CRTC3]]も報告された<ref name=Conkright2003><pubmed>14536081</pubmed></ref>。その後、[[ショウジョウバエ]]と[[線虫]]でもCRTCが同定されたことから、進化的に保存されたCREB活性化因子だと考えられる<ref name=Altarejos2011><pubmed>21346730</pubmed></ref>。CREB活性化因子として他にも、CREBのリン酸化を介してCREBに結合する[[ヒストンアセチル化酵素]][[CREB-binding protein]], | CRTCファミリータンパクである[[哺乳類]][[CRTC1]]と[[CRTC2]]は、[[cAMP応答配列結合タンパク質]] ([[CREB]])結合配列である[[cAMP応答配列]]の下流で[[ルシフェラーゼ]]を発現するレポーターを用い、CRE依存的な転写を活性化させる因子として同定された。さらにアミノ酸の相同性から[[CRTC3]]も報告された<ref name=Conkright2003><pubmed>14536081</pubmed></ref>。その後、[[ショウジョウバエ]]と[[線虫]]でもCRTCが同定されたことから、進化的に保存されたCREB活性化因子だと考えられる<ref name=Altarejos2011><pubmed>21346730</pubmed></ref>。CREB活性化因子として他にも、CREBのリン酸化を介してCREBに結合する[[ヒストンアセチル化酵素]][[CREB-binding protein]], | ||
[[CBP]])および[[p300]]タンパク質が知られているが、CBP/p300が[[ヒストンアセチル化]] | [[CBP]])および[[p300]]タンパク質が知られているが、CBP/p300が[[ヒストンアセチル化]]を介してCREB依存的遺伝子発現を誘導する一方、CRTCは脱リン酸化をトリガーとして核内に移行し、CREBと結合して転写複合体を形成することで遺伝子発現を誘導する。 | ||
[[ファイル:Hirano CRTC Fig.png|サムネイル|'''図1. CRTCのドメイン構造とリン酸化セリン'''<br> | |||
A. N末のCBDを介してCREBと結合し、C末のTADを介して転写を活性化させる。<br> | |||
B. 定常状態ではセリン残基のリン酸化によりCRTCは細胞質に局在し、脱リン酸化後、核内に移行して遺伝子発現を活性化させる。]] | |||
==構造== | ==構造== | ||
CRTCファミリータンパクは共通して、N末端にCREB結合ドメインを持ち、C末端に[[transcription factor IID]] ([[TFIID]])転写複合体サブユニットである[[TATA-box binding protein–associated factor 4]] ([[TAF4]])と結合する転写活性化ドメインを持つ<ref name=Conkright2003><pubmed>14536081</pubmed></ref>。CRTCのN末端ドメインおよびC末端ドメイン以外の領域は制御領域として考えられ、特に[[セリン]]・[[スレオニン]]が豊富で、これら[[アミノ酸]]がリン酸化されることで核外移行し、CRTCを負に制御している。マウスCRTC2に関しては構造解析が行われ、CRTC2のN末ドメインがCREBの[[dZipドメイン]]と結合し、CREB/CRTC2複合体が二量体になってCRE配列と結合することがわかっている<ref name=Song2018><pubmed>29733854</pubmed></ref>。 | CRTCファミリータンパクは共通して、N末端にCREB結合ドメインを持ち、C末端に[[transcription factor IID]] ([[TFIID]])転写複合体サブユニットである[[TATA-box binding protein–associated factor 4]] ([[TAF4]])と結合する転写活性化ドメインを持つ<ref name=Conkright2003><pubmed>14536081</pubmed></ref>。CRTCのN末端ドメインおよびC末端ドメイン以外の領域は制御領域として考えられ、特に[[セリン]]・[[スレオニン]]が豊富で、これら[[アミノ酸]]がリン酸化されることで核外移行し、CRTCを負に制御している。マウスCRTC2に関しては構造解析が行われ、CRTC2のN末ドメインがCREBの[[dZipドメイン]]と結合し、CREB/CRTC2複合体が二量体になってCRE配列と結合することがわかっている<ref name=Song2018><pubmed>29733854</pubmed></ref>。 | ||
| 17行目: | 26行目: | ||
==機能== | ==機能== | ||
CRTCが[[核]]移行すると、CREBと結合することでCREBを活性化し、遺伝子発現を誘導する。CBPはCREBの[[リン酸化]]を必要とする一方、CRTCには必要ない。CREB/CBPとCREB/CRTC経路の下流因子の一部は共通であるものの、それぞれに特異的な標的遺伝子も存在する<ref name=Kasper2010><pubmed>20859256</pubmed></ref>。CBPとCRTCの活性化の時間軸が異なる例も報告され<ref name=Hirano2016><pubmed>27841260</pubmed></ref>、さらにCBPとCRTCによるCREBを介した記憶制御にも異なる役割が報告されている<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。CRTCのクロマチン結合領域はCREBとほぼ共局在することから<ref name=Hirano2016><pubmed>27841260</pubmed></ref>、CRTCは主にCREBを介して転写制御に関与すると考えられる。 | |||
===翻訳後修飾=== | ===翻訳後修飾=== | ||
CRTCの調節にはリン酸化及びアセチル化による翻訳後修飾が関わっている。 | CRTCの調節にはリン酸化及びアセチル化による翻訳後修飾が関わっている。 | ||
| 33行目: | 42行目: | ||
===生体での機能=== | ===生体での機能=== | ||
神経で特に発現するCRTC1について、[[視床下部]]における[[食欲]]制御、また[[扁桃体]]および[[海馬]]における記憶制御に関わることが報告されている。視床下部でのCREB/CRTC1は[[レプチン]]の下流で機能し、レプチンシグナル下流である[[食欲抑制因子]]、[[プレプロコカイン・アンフェタミン調節性転写産物]]遺伝子[[CART prepropeptide]] ([[CARTPT]])および[[Kiss1]]の発現を誘導することにより、食欲を減衰させる機能がある<ref name=Altarejos2008><pubmed>18758446</pubmed></ref>。扁桃体と海馬においてCREBが記憶固定化に重要な転写制御因子として古くから知られてきたのと一致して、CRTC1は海馬[[後期長期増強]]([[L-LTP]])に必須であること<ref name=Ch'ng2012><pubmed>22770221</pubmed></ref><ref name=Zhou2006><pubmed>17183642</pubmed></ref>、扁桃体および海馬CRTC1は[[ | 神経で特に発現するCRTC1について、[[視床下部]]における[[食欲]]制御、また[[扁桃体]]および[[海馬]]における記憶制御に関わることが報告されている。視床下部でのCREB/CRTC1は[[レプチン]]の下流で機能し、レプチンシグナル下流である[[食欲抑制因子]]、[[プレプロコカイン・アンフェタミン調節性転写産物]]遺伝子[[CART prepropeptide]] ([[CARTPT]])および[[Kiss1]]の発現を誘導することにより、食欲を減衰させる機能がある<ref name=Altarejos2008><pubmed>18758446</pubmed></ref>。扁桃体と海馬においてCREBが記憶固定化に重要な転写制御因子として古くから知られてきたのと一致して、CRTC1は海馬[[後期長期増強]]([[L-LTP]])に必須であること<ref name=Ch'ng2012><pubmed>22770221</pubmed></ref><ref name=Zhou2006><pubmed>17183642</pubmed></ref>、扁桃体および海馬CRTC1は[[恐怖条件づけ]]学習における[[記憶固定化]]に重要であることが示された<ref name=Nonaka2014><pubmed>25277455</pubmed></ref> <ref name=Uchida2017><pubmed>28076781</pubmed></ref>。CRTC1下流制御遺伝子について[[脳由来神経栄養因子]] ([[brain-derived neurotrophic factor]] ([[BDNF]]))、[[核内受容体サブファミリー4A]] ([[Nr4a]])、[[c-fos]]、[[線維芽細胞増殖因子1b]] ([[fibroblast growth factor 1b]], [[Fgf1b]])等遺伝子が報告されており、これらはCBP下流遺伝子と共通であることから、CBPとCRTC1は協調的に働くこと、またCRTC1とCBPのCREB制御における使い分けが提案されてきた。 | ||
ショウジョウバエにおいては飢餓状態の低[[インスリン]]状態がCRTCの脱リン酸化を誘導してCRTCを活性化させ、CBP非依存的に記憶能力を高めることが示された<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。また、ショウジョウバエ[[匂い嫌悪学習]]において長期記憶の固定化そのものにはCRTCは必要なく、CBPが重要な役割を果たしている<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。しかし、長期記憶が形成された1日後からCRTCをノックダウンするとその後の記憶の保持や消失に影響が生じる。これらより、ショウジョウバエではCBPとCRTCに記憶過程における時間軸で使い分けがあり、CBPは長期記憶固定化に、CRTCは固定化1日後以降の長期記憶の維持、および消失といった記憶の柔軟性を司ると考えられる<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。マウスでもCBP依存的CREB活性化が一過的な遺伝子発現を誘導し、CRTC1依存的CREB活性化はより持続的な遺伝子発現を制御することが示唆されている<ref name=Uchida2017><pubmed>28076781</pubmed></ref>。CRTC2に関しては、マウス胚由来[[線維芽細胞]]においてCRTC2とCBPが独立に制御する遺伝子が報告されていることから<ref name=Kasper2010><pubmed>20859256</pubmed></ref>、CRTC1の下流遺伝子についてもCRTC1とCBPが独立に制御する下流遺伝子が存在する可能性がある。 | ショウジョウバエにおいては飢餓状態の低[[インスリン]]状態がCRTCの脱リン酸化を誘導してCRTCを活性化させ、CBP非依存的に記憶能力を高めることが示された<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。また、ショウジョウバエ[[匂い嫌悪学習]]において長期記憶の固定化そのものにはCRTCは必要なく、CBPが重要な役割を果たしている<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。しかし、長期記憶が形成された1日後からCRTCをノックダウンするとその後の記憶の保持や消失に影響が生じる。これらより、ショウジョウバエではCBPとCRTCに記憶過程における時間軸で使い分けがあり、CBPは長期記憶固定化に、CRTCは固定化1日後以降の長期記憶の維持、および消失といった記憶の柔軟性を司ると考えられる<ref name=Hirano2013><pubmed>23349290</pubmed></ref>。マウスでもCBP依存的CREB活性化が一過的な遺伝子発現を誘導し、CRTC1依存的CREB活性化はより持続的な遺伝子発現を制御することが示唆されている<ref name=Uchida2017><pubmed>28076781</pubmed></ref>。CRTC2に関しては、マウス胚由来[[線維芽細胞]]においてCRTC2とCBPが独立に制御する遺伝子が報告されていることから<ref name=Kasper2010><pubmed>20859256</pubmed></ref>、CRTC1の下流遺伝子についてもCRTC1とCBPが独立に制御する下流遺伝子が存在する可能性がある。 | ||
| 61行目: | 70行目: | ||
CRTCファミリータンパク質と[[肥満]]および[[生活習慣病]]との関連も示唆されている。上述の[[視床下部]]におけるCRTC1の[[食欲]]減衰作用、および肝臓CRTC2の糖新生を介した血糖値の制御、褐色脂肪細胞CRTC3による脂肪量の調節が肥満および生活習慣病治療の標的となりうると考えられる。それらに加え、慢性高血糖下では血中グルコースに応答してマウス肝臓においてCRTC2の[[O-グリコシル化]]が起きる。これによりCRTC2の過剰な活性化が起きることで血糖値が高く保たれることが示唆され、CRTC2のO-グリコシル化を阻害することで慢性高血糖における耐糖能異常を改善しうることが提案された<ref name=Dentin2008><pubmed>18323454</pubmed></ref>。 | CRTCファミリータンパク質と[[肥満]]および[[生活習慣病]]との関連も示唆されている。上述の[[視床下部]]におけるCRTC1の[[食欲]]減衰作用、および肝臓CRTC2の糖新生を介した血糖値の制御、褐色脂肪細胞CRTC3による脂肪量の調節が肥満および生活習慣病治療の標的となりうると考えられる。それらに加え、慢性高血糖下では血中グルコースに応答してマウス肝臓においてCRTC2の[[O-グリコシル化]]が起きる。これによりCRTC2の過剰な活性化が起きることで血糖値が高く保たれることが示唆され、CRTC2のO-グリコシル化を阻害することで慢性高血糖における耐糖能異常を改善しうることが提案された<ref name=Dentin2008><pubmed>18323454</pubmed></ref>。 | ||
==関連項目== | |||
* [[サイクリックAMP応答配列結合タンパク質]] | |||
* [[p300]] | |||
==参考文献== | ==参考文献== | ||
2026年1月19日 (月) 12:09時点における最新版
平野 恭敬
香港科学技術大学
DOI:10.14931/bsd.11464 原稿受付日:2025年12月27日 原稿完成日:2026年1月6日
担当編集委員:古屋敷 智之(東京科学大学大学院 医歯学総合研究科 薬理学分野)
英語名:CREB-regulated transcriptional coactivator
英略語:CRTC
CREB制御転写コアクチベーター (CREB-Regulated Transcriptional Coactivators, CRTC)は、cAMP応答配列(cAMP Response Element, CRE)を認識するcAMP応答配列結合タンパク質(cAMP response element-binding protein, CREB)と結合し、転写を活性化させる因子として機能する。CRTCファミリータンパクはリン酸化されることにより細胞質に局在して不活化状態にあり、脱リン酸化されることで核内に移行し転写を活性化させることから、遺伝子発現のダイナミックな変化に寄与する[1][2][3]。神経では記憶、食欲、うつ病態、および神経変性疾患に関与する。サブファミリーごとに発現が異なり、神経で機能する以外にも、肝臓で飢餓応答、また褐色脂肪細胞では低温耐性に関与する。
発見
CRTCファミリータンパクである哺乳類CRTC1とCRTC2は、cAMP応答配列結合タンパク質 (CREB)結合配列であるcAMP応答配列の下流でルシフェラーゼを発現するレポーターを用い、CRE依存的な転写を活性化させる因子として同定された。さらにアミノ酸の相同性からCRTC3も報告された[4]。その後、ショウジョウバエと線虫でもCRTCが同定されたことから、進化的に保存されたCREB活性化因子だと考えられる[5]。CREB活性化因子として他にも、CREBのリン酸化を介してCREBに結合するヒストンアセチル化酵素CREB-binding protein, CBP)およびp300タンパク質が知られているが、CBP/p300がヒストンアセチル化を介してCREB依存的遺伝子発現を誘導する一方、CRTCは脱リン酸化をトリガーとして核内に移行し、CREBと結合して転写複合体を形成することで遺伝子発現を誘導する。
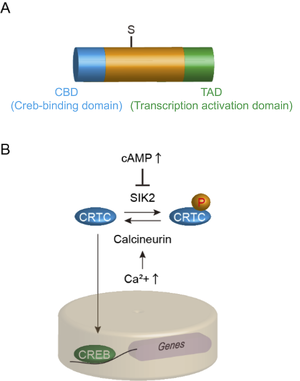
A. N末のCBDを介してCREBと結合し、C末のTADを介して転写を活性化させる。
B. 定常状態ではセリン残基のリン酸化によりCRTCは細胞質に局在し、脱リン酸化後、核内に移行して遺伝子発現を活性化させる。
構造
CRTCファミリータンパクは共通して、N末端にCREB結合ドメインを持ち、C末端にtranscription factor IID (TFIID)転写複合体サブユニットであるTATA-box binding protein–associated factor 4 (TAF4)と結合する転写活性化ドメインを持つ[4]。CRTCのN末端ドメインおよびC末端ドメイン以外の領域は制御領域として考えられ、特にセリン・スレオニンが豊富で、これらアミノ酸がリン酸化されることで核外移行し、CRTCを負に制御している。マウスCRTC2に関しては構造解析が行われ、CRTC2のN末ドメインがCREBのdZipドメインと結合し、CREB/CRTC2複合体が二量体になってCRE配列と結合することがわかっている[6]。
CRTC2のN末はCREBと結合するとともにDNAとも接しており、CREBがDNA二重らせんの主溝を認識する一方、CRTC2が副溝を認識し、CREB/DNAの結合を安定化させる役割があると考えられる[6]。DNA配列が異なると主溝と副溝の距離が変わるため、CRE配列でもその配列次第でCREB/CRTCの結合能が変わりうることが想定される[6]。
発現
CRTCは種を超えて全身で発現している[7] [8]。哺乳類ではアイソフォームによって発現に違いがあり、CRTC1が特に神経で[9][10]、CRTC2は中枢神経以外にも脾臓と肝臓で[11]、またCRTC3は褐色脂肪組織で高発現が見られ[12]、その他、複数組織で発現が認められる。
機能
CRTCが核移行すると、CREBと結合することでCREBを活性化し、遺伝子発現を誘導する。CBPはCREBのリン酸化を必要とする一方、CRTCには必要ない。CREB/CBPとCREB/CRTC経路の下流因子の一部は共通であるものの、それぞれに特異的な標的遺伝子も存在する[13]。CBPとCRTCの活性化の時間軸が異なる例も報告され[14]、さらにCBPとCRTCによるCREBを介した記憶制御にも異なる役割が報告されている[1]。CRTCのクロマチン結合領域はCREBとほぼ共局在することから[14]、CRTCは主にCREBを介して転写制御に関与すると考えられる。
翻訳後修飾
CRTCの調節にはリン酸化及びアセチル化による翻訳後修飾が関わっている。
リン酸化
CRTCファミリータンパクのリン酸化による制御は肝臓で発現するCRTC2について先行して解析が進んだ。CRTC2はAMP活性化タンパク質リン酸化酵素 (AMP-activated protein kinase, AMPK)およびAMPK関連リン酸化酵素 (AMPK-related kinase)であるSalt-inducible kinase2 (SIK2)により定常状態ではリン酸化されている[15][16]。複数のリン酸化部位の中でもマウスCRTC2では171番目のセリンがリン酸化されると14-3-3タンパク質と結合し、その結果、定常状態ではCRTC2が細胞質に局在することで下流遺伝子の発現は抑えられている[16]。上流シグナルであるグルカゴンによりCRTC2の脱リン酸化が誘導されると、細胞質から核へ移行しCREBと結合しそれを活性化する。その結果、糖新生に関与する遺伝子の発現が誘導される。CRTC2の脱リン酸化は、グルカゴン受容体を介したcAMP上昇によるSIK2阻害、および細胞内カルシウムの上昇によるカルシウム依存性脱リン酸化酵素カルシニューリンの活性化を介している[16][11]。
マウスCRTC1についても151番目セリンのリン酸化[9]、CRTC3では162番目セリンのリン酸化[12]が重要である。異なる脱リン酸化酵素(カルシニューリンおよびタンパク質脱リン酸化酵素2A (protein phosphatase 2A, PP2A)ファミリータンパク)がそれぞれのCRTCタンパクを脱リン酸化することから[17]、CRTCの活性制御機構は活性化される脱リン酸化酵素に違いがあると考えられる。
ショウジョウバエのCRTCは157番目のセリンのリン酸化により細胞質に局在し、同様の機構で脱リン酸化され[7]、線虫でも同様である[8]。
アセチル化
マウス肝臓においてCRTC2の628番目のリジン残基がアセチル化酵素p300にアセチル化され、SIRT1による脱アセチル化を受ける[18]。このリジン残基はタンパク分解を誘導するユビキチン化が起きる部位であることから、CRTC2の628番目のリジン残基のアセチル化はタンパク分解を抑制することで遺伝子発現を誘導すると考えられる[18]。
アセチル化の負の作用も報告されており、マウスCRTC1は13番目のリジン残基がアセチル化され、SIRT1による脱アセチル化を受けることにより遺伝子発現を誘導する[19]。N末端のCREB結合ドメイン内の13番目リジン残基のアセチル化は、CREB/DNAとの複合体形成に抑制的に働くことが推測される[19]。CRTC2の70および171番目のセリンのO-グリコシル化は14-3-3タンパク質との結合を阻害することで、CRTC2の核移行を誘導し、遺伝子発現を誘導する[20]。マウスCRTC1の216番目のセリン残基はS-ニトロシル化を受け、N末端CREB結合ドメイン(アミノ酸1-55)よりもC末側に位置するものの、CREBとの結合に阻害的に機能する[21]。
生体での機能
神経で特に発現するCRTC1について、視床下部における食欲制御、また扁桃体および海馬における記憶制御に関わることが報告されている。視床下部でのCREB/CRTC1はレプチンの下流で機能し、レプチンシグナル下流である食欲抑制因子、プレプロコカイン・アンフェタミン調節性転写産物遺伝子CART prepropeptide (CARTPT)およびKiss1の発現を誘導することにより、食欲を減衰させる機能がある[9]。扁桃体と海馬においてCREBが記憶固定化に重要な転写制御因子として古くから知られてきたのと一致して、CRTC1は海馬後期長期増強(L-LTP)に必須であること[22][23]、扁桃体および海馬CRTC1は恐怖条件づけ学習における記憶固定化に重要であることが示された[2] [3]。CRTC1下流制御遺伝子について脳由来神経栄養因子 (brain-derived neurotrophic factor (BDNF))、核内受容体サブファミリー4A (Nr4a)、c-fos、線維芽細胞増殖因子1b (fibroblast growth factor 1b, Fgf1b)等遺伝子が報告されており、これらはCBP下流遺伝子と共通であることから、CBPとCRTC1は協調的に働くこと、またCRTC1とCBPのCREB制御における使い分けが提案されてきた。
ショウジョウバエにおいては飢餓状態の低インスリン状態がCRTCの脱リン酸化を誘導してCRTCを活性化させ、CBP非依存的に記憶能力を高めることが示された[1]。また、ショウジョウバエ匂い嫌悪学習において長期記憶の固定化そのものにはCRTCは必要なく、CBPが重要な役割を果たしている[1]。しかし、長期記憶が形成された1日後からCRTCをノックダウンするとその後の記憶の保持や消失に影響が生じる。これらより、ショウジョウバエではCBPとCRTCに記憶過程における時間軸で使い分けがあり、CBPは長期記憶固定化に、CRTCは固定化1日後以降の長期記憶の維持、および消失といった記憶の柔軟性を司ると考えられる[1]。マウスでもCBP依存的CREB活性化が一過的な遺伝子発現を誘導し、CRTC1依存的CREB活性化はより持続的な遺伝子発現を制御することが示唆されている[3]。CRTC2に関しては、マウス胚由来線維芽細胞においてCRTC2とCBPが独立に制御する遺伝子が報告されていることから[13]、CRTC1の下流遺伝子についてもCRTC1とCBPが独立に制御する下流遺伝子が存在する可能性がある。
CRTC2とCRTC3に関しては神経以外での機能が報告されている。肝臓におけるCRTC2は飢餓時に分泌されるグルカゴンにより活性化し、糖新生に関わる遺伝子発現を誘導することで血糖値の制御に関わる[24] [25]。褐色脂肪細胞でのCRTC3のノックアウトマウスは、脂肪細胞での脂肪酸β酸化が亢進しており、体重低下および脂肪量の低下がみられ、かつ低温耐性が増強する[12]。CRTC3は褐色脂肪細胞での血管内皮増殖因子A(VEGFA)の発現に関与することから、CRTC3は分泌シグナルを介して褐色脂肪細胞の活性を制御していると提案されている[12]。
ショウジョウバエCRTCについても脂肪量の調節機能、および酸化ストレス応答に重要であることが報告されており[7]、線虫crtc-1変異体はおそらく脂肪等のエネルギー恒常性を介して寿命を延長させることも知られている[8]。
疾患との関わり
神経系で発現するCRTCファミリータンパクが神経可塑性を制御することから、その機能は神経関連疾患と深くかかわりがあると考えられる。
精神疾患
CRTC1ノックアウトマウスでは海馬と前頭葉においてCREB下流遺伝子が発現の低下が起き、社会性行動の低下、および攻撃行動の増大が認められる[26]。このことから、CREB/CRTC1依存的な遺伝子発現誘導とうつ病態との関連が示唆された[26]。
神経変性疾患
CREB/CRTC依存的な遺伝子発現の活性化は神経変性疾患に対して有効であることが報告されている。
Aβ42オリゴマー(早期アルツハイマー病脳で認められる、42アミノ酸からなるAβペプチドが重合した可溶性複合体)により培養神経でCRTC1のS-ニトロシル化が起き、CREB依存的遺伝子発現が阻害される[21]。CRTC1のS-ニトロシル化を阻害するとCREB依存的遺伝子発現が回復し、家族性アルツハイマー病原因遺伝子をもつヒトiPS細胞由来の神経における神経突起伸長が促進され、アルツハイマー病モデルマウスでのシナプス前部や長期増強の障害が抑えられる[21]。行動レベルでもアルツハイマー病モデルマウスの記憶障害がCRTC1の過剰発現により改善されることが示された[27]。
ハンチントン病モデルマウスにおいては、SIRT1を過剰発現させるとCRTC1の13番目リジン残基の抑制的アセチル化が脱アセチル化され、その結果CREB/CRTC1依存的な遺伝子発現が誘導され、神経毒性が軽減されることが示されている[19]。
パーキンソン病モデルとして用いられる6-ヒドロキシドーパミン (6-OHDA)処理ラットにおいても、CRTC1の活性化がドーパミン神経の細胞死に対して保護的に作用することが報告された[28]。
薬物依存
神経変性疾患以外では、CRTC1はコカインに対する動機づけ行動を抑制することから[29]、薬物依存に対するCRTC活性化の有効性が示唆されている。他にも、上流の抑制キナーゼであるSIK2をノックアウトすることでCRTC1を活性化させることにより、無酸素無糖負荷による神経死が軽減されることが示されており、CRTC1の活性化は脳虚血後の神経保護作用を有することが提案されている[15]。
生活習慣病
CRTCファミリータンパク質と肥満および生活習慣病との関連も示唆されている。上述の視床下部におけるCRTC1の食欲減衰作用、および肝臓CRTC2の糖新生を介した血糖値の制御、褐色脂肪細胞CRTC3による脂肪量の調節が肥満および生活習慣病治療の標的となりうると考えられる。それらに加え、慢性高血糖下では血中グルコースに応答してマウス肝臓においてCRTC2のO-グリコシル化が起きる。これによりCRTC2の過剰な活性化が起きることで血糖値が高く保たれることが示唆され、CRTC2のO-グリコシル化を阻害することで慢性高血糖における耐糖能異常を改善しうることが提案された[20]。
関連項目
参考文献
- ↑ 1.0 1.1 1.2 1.3 1.4
Hirano, Y., Masuda, T., Naganos, S., Matsuno, M., Ueno, K., Miyashita, T., ..., & Saitoe, M. (2013).
Fasting launches CRTC to facilitate long-term memory formation in Drosophila. Science (New York, N.Y.), 339(6118), 443-6. [PubMed:23349290] [WorldCat] [DOI] - ↑ 2.0 2.1
Nonaka, M., Kim, R., Fukushima, H., Sasaki, K., Suzuki, K., Okamura, M., ..., & Bito, H. (2014).
Region-specific activation of CRTC1-CREB signaling mediates long-term fear memory. Neuron, 84(1), 92-106. [PubMed:25277455] [WorldCat] [DOI] - ↑ 3.0 3.1 3.2
Uchida, S., Teubner, B.J.W., Hevi, C., Hara, K., Kobayashi, A., Dave, R.M., ..., & Shumyatsky, G.P. (2017).
CRTC1 Nuclear Translocation Following Learning Modulates Memory Strength via Exchange of Chromatin Remodeling Complexes on the Fgf1 Gene. Cell reports, 18(2), 352-366. [PubMed:28076781] [PMC] [WorldCat] [DOI] - ↑ 4.0 4.1
Conkright, M.D., Canettieri, G., Screaton, R., Guzman, E., Miraglia, L., Hogenesch, J.B., & Montminy, M. (2003).
TORCs: transducers of regulated CREB activity. Molecular cell, 12(2), 413-23. [PubMed:14536081] [WorldCat] [DOI] - ↑
Altarejos, J.Y., & Montminy, M. (2011).
CREB and the CRTC co-activators: sensors for hormonal and metabolic signals. Nature reviews. Molecular cell biology, 12(3), 141-51. [PubMed:21346730] [PMC] [WorldCat] [DOI] - ↑ 6.0 6.1 6.2
Song, Y., Zhai, L., Valencia Swain, J., Chen, Y., Wang, P., Chen, L., ..., & Xiang, S. (2018).
Structural Insights into the CRTC2-CREB Complex Assembly on CRE. Journal of molecular biology, 430(13), 1926-1939. [PubMed:29733854] [WorldCat] [DOI] - ↑ 7.0 7.1 7.2
Wang, B., Goode, J., Best, J., Meltzer, J., Schilman, P.E., Chen, J., ..., & Montminy, M. (2008).
The insulin-regulated CREB coactivator TORC promotes stress resistance in Drosophila. Cell metabolism, 7(5), 434-44. [PubMed:18460334] [PMC] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2
Mair, W., Morantte, I., Rodrigues, A.P., Manning, G., Montminy, M., Shaw, R.J., & Dillin, A. (2011).
Lifespan extension induced by AMPK and calcineurin is mediated by CRTC-1 and CREB. Nature, 470(7334), 404-8. [PubMed:21331044] [PMC] [WorldCat] [DOI] - ↑ 9.0 9.1 9.2
Altarejos, J.Y., Goebel, N., Conkright, M.D., Inoue, H., Xie, J., Arias, C.M., ..., & Montminy, M. (2008).
The Creb1 coactivator Crtc1 is required for energy balance and fertility. Nature medicine, 14(10), 1112-7. [PubMed:18758446] [PMC] [WorldCat] [DOI] - ↑
Sekeres, M.J., Mercaldo, V., Richards, B., Sargin, D., Mahadevan, V., Woodin, M.A., ..., & Josselyn, S.A. (2012).
Increasing CRTC1 function in the dentate gyrus during memory formation or reactivation increases memory strength without compromising memory quality. The Journal of neuroscience : the official journal of the Society for Neuroscience, 32(49), 17857-68. [PubMed:23223304] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Wang, Y., Li, G., Goode, J., Paz, J.C., Ouyang, K., Screaton, R., ..., & Montminy, M. (2012).
Inositol-1,4,5-trisphosphate receptor regulates hepatic gluconeogenesis in fasting and diabetes. Nature, 485(7396), 128-32. [PubMed:22495310] [PMC] [WorldCat] [DOI] - ↑ 12.0 12.1 12.2 12.3
Yoon, Y.S., Tsai, W.W., Van de Velde, S., Chen, Z., Lee, K.F., Morgan, D.A., ..., & Montminy, M. (2018).
cAMP-inducible coactivator CRTC3 attenuates brown adipose tissue thermogenesis. Proceedings of the National Academy of Sciences of the United States of America, 115(23), E5289-E5297. [PubMed:29784793] [PMC] [WorldCat] [DOI] - ↑ 13.0 13.1
Kasper, L.H., Lerach, S., Wang, J., Wu, S., Jeevan, T., & Brindle, P.K. (2010).
CBP/p300 double null cells reveal effect of coactivator level and diversity on CREB transactivation. The EMBO journal, 29(21), 3660-72. [PubMed:20859256] [PMC] [WorldCat] [DOI] - ↑ 14.0 14.1
Hirano, Y., Ihara, K., Masuda, T., Yamamoto, T., Iwata, I., Takahashi, A., ..., & Saitoe, M. (2016).
Shifting transcriptional machinery is required for long-term memory maintenance and modification in Drosophila mushroom bodies. Nature communications, 7, 13471. [PubMed:27841260] [PMC] [WorldCat] [DOI] - ↑ 15.0 15.1
Sasaki, T., Takemori, H., Yagita, Y., Terasaki, Y., Uebi, T., Horike, N., ..., & Kitagawa, K. (2011).
SIK2 is a key regulator for neuronal survival after ischemia via TORC1-CREB. Neuron, 69(1), 106-19. [PubMed:21220102] [WorldCat] [DOI] - ↑ 16.0 16.1 16.2
Screaton, R.A., Conkright, M.D., Katoh, Y., Best, J.L., Canettieri, G., Jeffries, S., ..., & Montminy, M. (2004).
The CREB coactivator TORC2 functions as a calcium- and cAMP-sensitive coincidence detector. Cell, 119(1), 61-74. [PubMed:15454081] [WorldCat] [DOI] - ↑
Sonntag, T., Ostojić, J., Vaughan, J.M., Moresco, J.J., Yoon, Y.S., Yates, J.R., & Montminy, M. (2019).
Mitogenic Signals Stimulate the CREB Coactivator CRTC3 through PP2A Recruitment. iScience, 11, 134-145. [PubMed:30611118] [PMC] [WorldCat] [DOI] - ↑ 18.0 18.1
Liu, Y., Dentin, R., Chen, D., Hedrick, S., Ravnskjaer, K., Schenk, S., ..., & Montminy, M. (2008).
A fasting inducible switch modulates gluconeogenesis via activator/coactivator exchange. Nature, 456(7219), 269-73. [PubMed:18849969] [PMC] [WorldCat] [DOI] - ↑ 19.0 19.1 19.2
Jeong, H., Cohen, D.E., Cui, L., Supinski, A., Savas, J.N., Mazzulli, J.R., ..., & Krainc, D. (2011).
Sirt1 mediates neuroprotection from mutant huntingtin by activation of the TORC1 and CREB transcriptional pathway. Nature medicine, 18(1), 159-65. [PubMed:22179316] [PMC] [WorldCat] [DOI] - ↑ 20.0 20.1
Dentin, R., Hedrick, S., Xie, J., Yates, J., & Montminy, M. (2008).
Hepatic glucose sensing via the CREB coactivator CRTC2. Science (New York, N.Y.), 319(5868), 1402-5. [PubMed:18323454] [WorldCat] [DOI] - ↑ 21.0 21.1 21.2
Zhang, X., Vlkolinsky, R., Wu, C., Dolatabadi, N., Scott, H., Prikhodko, O., ..., & Lipton, S.A. (2025).
S-Nitrosylation of CRTC1 in Alzheimer's disease impairs CREB-dependent gene expression induced by neuronal activity. Proceedings of the National Academy of Sciences of the United States of America, 122(9), e2418179122. [PubMed:40014571] [PMC] [WorldCat] [DOI] - ↑
Ch'ng, T.H., Uzgil, B., Lin, P., Avliyakulov, N.K., O'Dell, T.J., & Martin, K.C. (2012).
Activity-dependent transport of the transcriptional coactivator CRTC1 from synapse to nucleus. Cell, 150(1), 207-21. [PubMed:22770221] [PMC] [WorldCat] [DOI] - ↑
Zhou, Y., Wu, H., Li, S., Chen, Q., Cheng, X.W., Zheng, J., ..., & Xiong, Z.Q. (2006).
Requirement of TORC1 for late-phase long-term potentiation in the hippocampus. PloS one, 1(1), e16. [PubMed:17183642] [PMC] [WorldCat] [DOI] - ↑
Wang, Y., Inoue, H., Ravnskjaer, K., Viste, K., Miller, N., Liu, Y., ..., & Montminy, M. (2010).
Targeted disruption of the CREB coactivator Crtc2 increases insulin sensitivity. Proceedings of the National Academy of Sciences of the United States of America, 107(7), 3087-92. [PubMed:20133702] [PMC] [WorldCat] [DOI] - ↑
Han, H.S., Choi, B.H., Kim, J.S., Kang, G., & Koo, S.H. (2017).
Hepatic Crtc2 controls whole body energy metabolism via a miR-34a-Fgf21 axis. Nature communications, 8(1), 1878. [PubMed:29192248] [PMC] [WorldCat] [DOI] - ↑ 26.0 26.1
Breuillaud, L., Rossetti, C., Meylan, E.M., Mérinat, C., Halfon, O., Magistretti, P.J., & Cardinaux, J.R. (2012).
Deletion of CREB-regulated transcription coactivator 1 induces pathological aggression, depression-related behaviors, and neuroplasticity genes dysregulation in mice. Biological psychiatry, 72(7), 528-36. [PubMed:22592058] [WorldCat] [DOI] - ↑
Parra-Damas, A., Valero, J., Chen, M., España, J., Martín, E., Ferrer, I., ..., & Saura, C.A. (2014).
Crtc1 activates a transcriptional program deregulated at early Alzheimer's disease-related stages. The Journal of neuroscience : the official journal of the Society for Neuroscience, 34(17), 5776-87. [PubMed:24760838] [PMC] [WorldCat] [DOI] - ↑
Won, S.Y., Park, M.H., You, S.T., Choi, S.W., Kim, H.K., McLean, C., ..., & Kim, E.G. (2016).
Nigral dopaminergic PAK4 prevents neurodegeneration in rat models of Parkinson's disease. Science translational medicine, 8(367), 367ra170. [PubMed:27903866] [WorldCat] [DOI] - ↑
Hollander, J.A., Im, H.I., Amelio, A.L., Kocerha, J., Bali, P., Lu, Q., ..., & Kenny, P.J. (2010).
Striatal microRNA controls cocaine intake through CREB signalling. Nature, 466(7303), 197-202. [PubMed:20613834] [PMC] [WorldCat] [DOI]