「ノーダル」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| 5行目: | 5行目: | ||
== ノーダルとは == | == ノーダルとは == | ||
ノーダルは、原腸陥入に異常を来す変異マウスの原因遺伝子として同定され、初期胚の一過的構造であるノード (胚結節、node) で発現することからその名が付けられた<ref name=Zhou1993><pubmed>8429908</pubmed></ref>。その後、ニワトリ、マウス、アフリカツメガエル胚などの初期体節期において左右非対称に発現することが明らかになった<ref name=Collignon1996><pubmed>8610012</pubmed></ref><ref name=Levin1995><pubmed>7671308</pubmed></ref><ref name=Lowe1996><pubmed>8610013</pubmed></ref>。ノーダル変異マウスの表現型の重要性から、アフリカツメガエルで6種のノーダル関連遺伝子 (Xnr1–6) が、ゼブラフィッシュでは3種のノーダル関連遺伝子 (cyclops, squint, southpaw) が同定された<ref name=Shen2007><pubmed>17287255</pubmed></ref>。ノーダルは胚発生を制御する重要因子として着目され、シグナル経路や機能の解析が進められた。 | ノーダルは、原腸陥入に異常を来す変異マウスの原因遺伝子として同定され、初期胚の一過的構造であるノード (胚結節、node) で発現することからその名が付けられた<ref name=Zhou1993><pubmed>8429908</pubmed></ref>。その後、ニワトリ、マウス、アフリカツメガエル胚などの初期体節期において左右非対称に発現することが明らかになった<ref name=Collignon1996><pubmed>8610012</pubmed></ref><ref name=Levin1995><pubmed>7671308</pubmed></ref><ref name=Lowe1996><pubmed>8610013</pubmed></ref>。ノーダル変異マウスの表現型の重要性から、アフリカツメガエルで6種のノーダル関連遺伝子 (Xnr1–6) が、ゼブラフィッシュでは3種のノーダル関連遺伝子 (cyclops, squint, southpaw) が同定された<ref name=Shen2007><pubmed>17287255</pubmed></ref>。ノーダルは胚発生を制御する重要因子として着目され、シグナル経路や機能の解析が進められた。 | ||
[[ファイル:Meno Nodal Fig1.png|サムネイル|'''図1. ノーダルの一次構造'''<br> C末端側 (図右) に存在するシステイン残基は、システインノット構造の形成 (黒色) とダイマー形成 (褐色) に関与する。FurinやPACE4はRQRRを認識して切断し、C末端側が成熟ドメインとなる。 | |||
]] | |||
== 構造 == | == 構造 == | ||
ノーダルはプレプロタンパク質として翻訳され、分泌後にFurinや paired basic amino acid cleaving enzyme 4 (PACE4)などのプロタンパク質変換酵素によって切断を受けることで、C末端側が活性タンパクとして機能する<ref name=Beck2002><pubmed>12447384</pubmed></ref>。C末端側にはTGF-βファミリーに特徴的なシステイン残基が保存されており<ref name=Zhou1993><pubmed>8429908</pubmed></ref>、これらは分子内および分子間のジスルフィド結合を介して、システインノット構造の形成とダイマー形成に関与する (図1)。一方、プロドメインは、ノーダルの活性や組織内での拡散性を制御していると考えられている<ref name=LeGood2005><pubmed>15649361</pubmed></ref>。 | ノーダルはプレプロタンパク質として翻訳され、分泌後にFurinや paired basic amino acid cleaving enzyme 4 (PACE4)などのプロタンパク質変換酵素によって切断を受けることで、C末端側が活性タンパクとして機能する<ref name=Beck2002><pubmed>12447384</pubmed></ref>。C末端側にはTGF-βファミリーに特徴的なシステイン残基が保存されており<ref name=Zhou1993><pubmed>8429908</pubmed></ref>、これらは分子内および分子間のジスルフィド結合を介して、システインノット構造の形成とダイマー形成に関与する ('''図1''')。一方、プロドメインは、ノーダルの活性や組織内での拡散性を制御していると考えられている<ref name=LeGood2005><pubmed>15649361</pubmed></ref>。 | ||
== オルソログ == | == オルソログ == | ||
ノーダルは後生動物に高度に保存されており、刺胞動物、螺旋卵割動物 (軟体動物、環形動物など) および後口動物 (脊索動物、半索動物や棘皮動物など) の多くの系統で存在が確認されている<ref name=Grande2014><pubmed>25690967</pubmed></ref><ref name=Namigai2014><pubmed>24510729</pubmed></ref><ref name=Watanabe2014><pubmed>25156256</pubmed></ref>。一方、脱皮動物 (節足動物や線形動物など) では、共通先祖でノーダルが失われたと推察されている<ref name=Grande2014><pubmed>25690967</pubmed></ref>。脊椎動物のモデル生物では、ゼブラフィッシュやアフリカツメガエルにおいて、種固有の全ゲノム重複を経てノーダル関連遺伝子が多重化している。 | ノーダルは後生動物に高度に保存されており、刺胞動物、螺旋卵割動物 (軟体動物、環形動物など) および後口動物 (脊索動物、半索動物や棘皮動物など) の多くの系統で存在が確認されている<ref name=Grande2014><pubmed>25690967</pubmed></ref><ref name=Namigai2014><pubmed>24510729</pubmed></ref><ref name=Watanabe2014><pubmed>25156256</pubmed></ref>。一方、脱皮動物 (節足動物や線形動物など) では、共通先祖でノーダルが失われたと推察されている<ref name=Grande2014><pubmed>25690967</pubmed></ref>。脊椎動物のモデル生物では、ゼブラフィッシュやアフリカツメガエルにおいて、種固有の全ゲノム重複を経てノーダル関連遺伝子が多重化している。 | ||
[[ファイル:Meno Nodal Fig2.png|サムネイル|'''図2. ノーダルシグナル'''<br> ノーダルシグナルの主要な構成因子を示す模式図。ノーダルはCrypticなどのEGF-CFCファミリーに依存してActivin受容体に結合する。リン酸化Smad2/3は核に移行し、FoxH1などと協調して標的遺伝子 (ノーダル, Lefty2, Pitx2など) の発現を誘導する。これらの遺伝子に描かれた青色楕円は、FoxH1が結合するエンハンサーASEを表している。ノーダルはポジティブフィードバックループとLeftyを介したネガティブフィードバックループを構成する。]] | |||
== ノーダルシグナルとその制御 == | == ノーダルシグナルとその制御 == | ||
ノーダルはActivin受容体 (タイプIIとしてActRIIA/B、タイプIとしてALK4/7) と複合体を形成するが、この複合体形成にはGPIアンカー型膜タンパク質であるEGF-CFCファミリー (Cripto, Cryptic, FRL1, Oepなど) を必要とする<ref name=Shen2007><pubmed>17287255</pubmed></ref>。ノーダルの結合によって活性化されたタイプI受容体はSmad2/3をリン酸化し、これらはSmad4と複合体を形成して核内に移行する。この複合体はFoxH1やEomesなどの転写因子と協調して標的遺伝子の発現を制御する。また、ノーダルはFoxH1を介したポジティブフィードバックループを形成しており、自らの発現を誘導する (図2)<ref name=Norris2002><pubmed>12091315</pubmed></ref><ref name=Saijoh2000><pubmed>10678167</pubmed></ref><ref name=Yamamoto2003><pubmed>12642485</pubmed></ref>。 | ノーダルはActivin受容体 (タイプIIとしてActRIIA/B、タイプIとしてALK4/7) と複合体を形成するが、この複合体形成にはGPIアンカー型膜タンパク質であるEGF-CFCファミリー (Cripto, Cryptic, FRL1, Oepなど) を必要とする<ref name=Shen2007><pubmed>17287255</pubmed></ref>。ノーダルの結合によって活性化されたタイプI受容体はSmad2/3をリン酸化し、これらはSmad4と複合体を形成して核内に移行する。この複合体はFoxH1やEomesなどの転写因子と協調して標的遺伝子の発現を制御する。また、ノーダルはFoxH1を介したポジティブフィードバックループを形成しており、自らの発現を誘導する ('''図2''')<ref name=Norris2002><pubmed>12091315</pubmed></ref><ref name=Saijoh2000><pubmed>10678167</pubmed></ref><ref name=Yamamoto2003><pubmed>12642485</pubmed></ref>。 | ||
ノーダルシグナルは、細胞外のアンタゴニストによって厳密に制御されている (図2)。TGF-β ファミリーのLefty1とLefty2はノーダルのフィードバック阻害因子であり<ref name=Meno1999><pubmed>10518210</pubmed></ref><ref name=Saijoh2000><pubmed>10678167</pubmed></ref><ref name=Yamamoto2003><pubmed>12642485</pubmed></ref>、ノーダルに直接結合する他、ActRIIやEGF-CFCファミリーとの競合的な結合によってノーダルシグナルを抑制するメカニズムが報告されている<ref name=Chen2004><pubmed>15062104</pubmed></ref><ref name=Sakuma2002><pubmed>11952836</pubmed></ref>。また、CerberusファミリーのCerl (Cer1) やCerl2 (Dand5) などはノーダルと結合することでノーダルシグナルを抑制する<ref name=Hashimoto2004><pubmed>15084459</pubmed></ref><ref name=Marques2004><pubmed>15466485</pubmed></ref><ref name=Shen2007><pubmed>17287255</pubmed></ref>。 | ノーダルシグナルは、細胞外のアンタゴニストによって厳密に制御されている (図2)。TGF-β ファミリーのLefty1とLefty2はノーダルのフィードバック阻害因子であり<ref name=Meno1999><pubmed>10518210</pubmed></ref><ref name=Saijoh2000><pubmed>10678167</pubmed></ref><ref name=Yamamoto2003><pubmed>12642485</pubmed></ref>、ノーダルに直接結合する他、ActRIIやEGF-CFCファミリーとの競合的な結合によってノーダルシグナルを抑制するメカニズムが報告されている<ref name=Chen2004><pubmed>15062104</pubmed></ref><ref name=Sakuma2002><pubmed>11952836</pubmed></ref>。また、CerberusファミリーのCerl (Cer1) やCerl2 (Dand5) などはノーダルと結合することでノーダルシグナルを抑制する<ref name=Hashimoto2004><pubmed>15084459</pubmed></ref><ref name=Marques2004><pubmed>15466485</pubmed></ref><ref name=Shen2007><pubmed>17287255</pubmed></ref>。 | ||
| 36行目: | 37行目: | ||
=== 前後軸形成 === | === 前後軸形成 === | ||
着床したマウス胚は、エピブラストおよび隣接した胚体外外胚葉が胚盤胞腔側へ成長し、両者が臓側内胚葉に覆われた円筒胚を形成する。円筒胚の近位は胎盤を形成し、遠位には遠位臓側内胚葉 (distal visceral endoderm: DVE) が出現する。このDVEは将来の前方 (頭側) へ移動して前方臓側内胚葉 (anterior visceral endoderm: AVE) を形成し、その反対側に原条が形成されることで、胚に明確な前後非対称性が確立される<ref name=Arnold2009><pubmed>19129791</pubmed></ref>。ノーダルは、PEEやASEなどのエンハンサーによりエピブラストで発現し、そのシグナルはDVEにおけるLefty1、Cerl、Dkk1の発現を誘導する<ref name=Brennan2001><pubmed>11418863</pubmed></ref>。AVEから分泌されるこれらの因子は、隣接するエピブラストにおけるノーダルポジティブフィードバックループとWntシグナルを抑制し、エピブラストのノーダル発現をAVEと反対側、すなわち胚後方に限局させる<ref name=Perea-Gomez2002><pubmed>12431380</pubmed></ref>。この結果、胚前方には神経外胚葉が、胚後方には原条が形成される。 | 着床したマウス胚は、エピブラストおよび隣接した胚体外外胚葉が胚盤胞腔側へ成長し、両者が臓側内胚葉に覆われた円筒胚を形成する。円筒胚の近位は胎盤を形成し、遠位には遠位臓側内胚葉 (distal visceral endoderm: DVE) が出現する。このDVEは将来の前方 (頭側) へ移動して前方臓側内胚葉 (anterior visceral endoderm: AVE) を形成し、その反対側に原条が形成されることで、胚に明確な前後非対称性が確立される<ref name=Arnold2009><pubmed>19129791</pubmed></ref>。ノーダルは、PEEやASEなどのエンハンサーによりエピブラストで発現し、そのシグナルはDVEにおけるLefty1、Cerl、Dkk1の発現を誘導する<ref name=Brennan2001><pubmed>11418863</pubmed></ref>。AVEから分泌されるこれらの因子は、隣接するエピブラストにおけるノーダルポジティブフィードバックループとWntシグナルを抑制し、エピブラストのノーダル発現をAVEと反対側、すなわち胚後方に限局させる<ref name=Perea-Gomez2002><pubmed>12431380</pubmed></ref>。この結果、胚前方には神経外胚葉が、胚後方には原条が形成される。 | ||
[[ファイル:Meno Nodal Fig3.png|サムネイル|'''図3. マウスにおける左右軸形成'''<br>胚遠位から観察したマウス初期体節期胚の模式図 (図上が前方、下が後方)。左右軸形成は①から④の順に進行する。<br>① 左右オーガナイザーであるノードの腹側に左向きの流れ (ノーダル flow) が発生する。<br>② ノード周縁部 (クラウン細胞) では、NotchシグナルによってノーダルやCerl2などの左右軸関連遺伝子が発現するが、流れにより左側のCerl2 mRNAが分解される (褐色はCerl2 mRNAを表す)。<br>③ Cerl2は右側でノーダルを強く抑制することにより、左側でのノーダル活性が高くなる (緑色はノードにおけるノーダル活性を表す)。ノードから拡散したノーダルは、近傍の左側側板中胚葉 (lateral plate mesoderm, lpm) に自らの発現を誘導する (紺色はノーダル発現を示す)。<br>④ ノーダルはポジティブフィードバックループによって発現域を拡張するとともに、転写因子Pitx2の発現を誘導する (紺色はノーダルおよびPitx2発現を示す)。これらの左右非対称な発現は、その後の臓器の左右非対称な形態形成を制御する。]] | |||
=== 左右軸形成 === | === 左右軸形成 === | ||
脊椎動物では、初期体節期にノーダルが左側側板中胚葉で発現する。ノーダルはFoxH1を介して転写因子Pitx2の発現を誘導し (図2)<ref name=Shiratori2001><pubmed>11172719</pubmed></ref>、臓器の左右非対称な形態形成を制御する。脊椎動物以外でも、ノーダルを保有する動物系統ではPitxがノーダルと同側に非対称に発現することが確認されており、進化の過程でPitxはノーダルシグナルと連結することで非対称な形態形成の役割を獲得したと推察されている<ref name=Grande2014><pubmed>25690967</pubmed></ref>。例えば、ノーダル-Pitx発現の左右非対称性は、軟体動物の巻貝では貝殻の巻き方向を決定し<ref name=Grande2009><pubmed>19098895</pubmed></ref>、棘皮動物のウニではプルテウス幼生におけるウニ原基の左右非対称な形成を制御する (右側のノーダルシグナルはウニ原基形成を抑制する) <ref name=Duboc2005><pubmed>15992548</pubmed></ref>。 | 脊椎動物では、初期体節期にノーダルが左側側板中胚葉で発現する。ノーダルはFoxH1を介して転写因子Pitx2の発現を誘導し ('''図2''')<ref name=Shiratori2001><pubmed>11172719</pubmed></ref>、臓器の左右非対称な形態形成を制御する。脊椎動物以外でも、ノーダルを保有する動物系統ではPitxがノーダルと同側に非対称に発現することが確認されており、進化の過程でPitxはノーダルシグナルと連結することで非対称な形態形成の役割を獲得したと推察されている<ref name=Grande2014><pubmed>25690967</pubmed></ref>。例えば、ノーダル-Pitx発現の左右非対称性は、軟体動物の巻貝では貝殻の巻き方向を決定し<ref name=Grande2009><pubmed>19098895</pubmed></ref>、棘皮動物のウニではプルテウス幼生におけるウニ原基の左右非対称な形成を制御する (右側のノーダルシグナルはウニ原基形成を抑制する) <ref name=Duboc2005><pubmed>15992548</pubmed></ref>。 | ||
脊椎動物でノーダルを左側の側板中胚葉で発現させる装置が左右オーガナイザー (マウスのノード、ニワトリのヘンゼン結節、アフリカツメガエルの原腸蓋板、ゼブラフィッシュのクッパー胞) である。ニワトリを除くこれらの左右オーガナイザーでは、線毛の回転運動によって左向きの水流が形成される (図3)。この物理現象により、Cerl2などのノーダル阻害因子が右側で優位となり (マウスでは左側のCerl2 mRNAが分解される)<ref name=Marques2004><pubmed>15466485</pubmed></ref><ref name=Nakamura2012><pubmed>23271656</pubmed></ref><ref name=Sampaio2014><pubmed>24930722</pubmed></ref><ref name=Schweickert2010><pubmed>20381352</pubmed></ref>、左側のノーダル活性が右側に比べて相対的に高まる(図3)<ref name=Hamada2014><pubmed>25580264</pubmed></ref>。左右オーガナイザーから拡散したノーダルは、近傍の左側側板中胚葉に自らの発現を誘導する (図3)<ref name=Oki2007><pubmed>17913787</pubmed></ref>。ノーダルのポジティブフィードバックループとLeftyによるネガティブフィードバックループは、チューリングの反応拡散モデルの基本条件を満たしており、左右オーガナイザーにおける僅かなノーダル活性差を側板中胚葉における顕著な左右非対称性へと増幅する<ref name=Hamada2002><pubmed>11836504</pubmed></ref><ref name=Nakamura2006><pubmed>17011489</pubmed></ref>。左側側板中胚葉のノーダル発現域は、拡散とポジティブフィードバックループによって心臓形成領域まで拡張するが (図3)<ref name=Yamamoto2003><pubmed>12642485</pubmed></ref>、Leftyによりその発現域は左側に限局され、最終的にノーダル発現は終息する<ref name=Meno1998><pubmed>9708731</pubmed></ref><ref name=Meno2001><pubmed>11703930</pubmed></ref>。 | 脊椎動物でノーダルを左側の側板中胚葉で発現させる装置が左右オーガナイザー (マウスのノード、ニワトリのヘンゼン結節、アフリカツメガエルの原腸蓋板、ゼブラフィッシュのクッパー胞) である。ニワトリを除くこれらの左右オーガナイザーでは、線毛の回転運動によって左向きの水流が形成される ('''図3''')。この物理現象により、Cerl2などのノーダル阻害因子が右側で優位となり (マウスでは左側のCerl2 mRNAが分解される)<ref name=Marques2004><pubmed>15466485</pubmed></ref><ref name=Nakamura2012><pubmed>23271656</pubmed></ref><ref name=Sampaio2014><pubmed>24930722</pubmed></ref><ref name=Schweickert2010><pubmed>20381352</pubmed></ref>、左側のノーダル活性が右側に比べて相対的に高まる('''図3''')<ref name=Hamada2014><pubmed>25580264</pubmed></ref>。左右オーガナイザーから拡散したノーダルは、近傍の左側側板中胚葉に自らの発現を誘導する (図3)<ref name=Oki2007><pubmed>17913787</pubmed></ref>。ノーダルのポジティブフィードバックループとLeftyによるネガティブフィードバックループは、チューリングの反応拡散モデルの基本条件を満たしており、左右オーガナイザーにおける僅かなノーダル活性差を側板中胚葉における顕著な左右非対称性へと増幅する<ref name=Hamada2002><pubmed>11836504</pubmed></ref><ref name=Nakamura2006><pubmed>17011489</pubmed></ref>。左側側板中胚葉のノーダル発現域は、拡散とポジティブフィードバックループによって心臓形成領域まで拡張するが (図3)<ref name=Yamamoto2003><pubmed>12642485</pubmed></ref>、Leftyによりその発現域は左側に限局され、最終的にノーダル発現は終息する<ref name=Meno1998><pubmed>9708731</pubmed></ref><ref name=Meno2001><pubmed>11703930</pubmed></ref>。 | ||
左側側板中胚葉でノーダルによって誘導されたPitx2は、その細胞系譜で発現を維持する<ref name=Shiratori2001><pubmed>11172719</pubmed></ref>。マウスでは、このメカニズムにより確立された左右軸情報が、心臓形態形成、刺激伝導系の発生、肺の分葉パターン、腸ループ回転などの非対称な形態形成を制御する<ref name=Franco2017><pubmed>29367545</pubmed></ref><ref name=Hamada2002><pubmed>11836504</pubmed></ref><ref name=Joo2026><pubmed>41734036</pubmed></ref><ref name=Yashiro2007><pubmed>17994097</pubmed></ref>。ゼブラフィッシュでは、左側間脳におけるノーダルシグナルが、副松果体と手綱核の左右非対称な発生を制御している<ref name=Concha2000><pubmed>11144351</pubmed></ref><ref name=Gamse2005><pubmed>16207761</pubmed></ref><ref name=Gobbo2025><pubmed>39906337</pubmed></ref>。 | 左側側板中胚葉でノーダルによって誘導されたPitx2は、その細胞系譜で発現を維持する<ref name=Shiratori2001><pubmed>11172719</pubmed></ref>。マウスでは、このメカニズムにより確立された左右軸情報が、心臓形態形成、刺激伝導系の発生、肺の分葉パターン、腸ループ回転などの非対称な形態形成を制御する<ref name=Franco2017><pubmed>29367545</pubmed></ref><ref name=Hamada2002><pubmed>11836504</pubmed></ref><ref name=Joo2026><pubmed>41734036</pubmed></ref><ref name=Yashiro2007><pubmed>17994097</pubmed></ref>。ゼブラフィッシュでは、左側間脳におけるノーダルシグナルが、副松果体と手綱核の左右非対称な発生を制御している<ref name=Concha2000><pubmed>11144351</pubmed></ref><ref name=Gamse2005><pubmed>16207761</pubmed></ref><ref name=Gobbo2025><pubmed>39906337</pubmed></ref>。 | ||
| 54行目: | 55行目: | ||
* [[内臓錯位症候群]] | * [[内臓錯位症候群]] | ||
* [[全前脳胞症]] | * [[全前脳胞症]] | ||
== 参考文献 == | == 参考文献 == | ||
<references /> | <references /> | ||
2026年4月15日 (水) 22:04時点における版
英語名:Nodal
ノーダルは、transforming growth factor-β (TGF-β)ファミリーに属する分泌因子であり、多くの動物系統の初期胚発生において重要な役割を果たす。ノーダルシグナルは、体軸形成 (前後・左右軸)、中・内胚葉系譜の形成、原腸形成などの基本的プロセスを制御する。ノーダルシグナルの異常は内臓錯位症候群 (heterotaxy) や全前脳胞症 (holoprosencephaly) などの疾患を引き起こすことが知られている。
ノーダルとは
ノーダルは、原腸陥入に異常を来す変異マウスの原因遺伝子として同定され、初期胚の一過的構造であるノード (胚結節、node) で発現することからその名が付けられた[1]。その後、ニワトリ、マウス、アフリカツメガエル胚などの初期体節期において左右非対称に発現することが明らかになった[2][3][4]。ノーダル変異マウスの表現型の重要性から、アフリカツメガエルで6種のノーダル関連遺伝子 (Xnr1–6) が、ゼブラフィッシュでは3種のノーダル関連遺伝子 (cyclops, squint, southpaw) が同定された[5]。ノーダルは胚発生を制御する重要因子として着目され、シグナル経路や機能の解析が進められた。
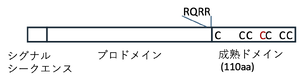
C末端側 (図右) に存在するシステイン残基は、システインノット構造の形成 (黒色) とダイマー形成 (褐色) に関与する。FurinやPACE4はRQRRを認識して切断し、C末端側が成熟ドメインとなる。
構造
ノーダルはプレプロタンパク質として翻訳され、分泌後にFurinや paired basic amino acid cleaving enzyme 4 (PACE4)などのプロタンパク質変換酵素によって切断を受けることで、C末端側が活性タンパクとして機能する[6]。C末端側にはTGF-βファミリーに特徴的なシステイン残基が保存されており[1]、これらは分子内および分子間のジスルフィド結合を介して、システインノット構造の形成とダイマー形成に関与する (図1)。一方、プロドメインは、ノーダルの活性や組織内での拡散性を制御していると考えられている[7]。
オルソログ
ノーダルは後生動物に高度に保存されており、刺胞動物、螺旋卵割動物 (軟体動物、環形動物など) および後口動物 (脊索動物、半索動物や棘皮動物など) の多くの系統で存在が確認されている[8][9][10]。一方、脱皮動物 (節足動物や線形動物など) では、共通先祖でノーダルが失われたと推察されている[8]。脊椎動物のモデル生物では、ゼブラフィッシュやアフリカツメガエルにおいて、種固有の全ゲノム重複を経てノーダル関連遺伝子が多重化している。
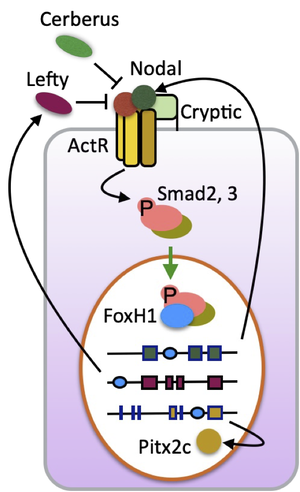
ノーダルシグナルの主要な構成因子を示す模式図。ノーダルはCrypticなどのEGF-CFCファミリーに依存してActivin受容体に結合する。リン酸化Smad2/3は核に移行し、FoxH1などと協調して標的遺伝子 (ノーダル, Lefty2, Pitx2など) の発現を誘導する。これらの遺伝子に描かれた青色楕円は、FoxH1が結合するエンハンサーASEを表している。ノーダルはポジティブフィードバックループとLeftyを介したネガティブフィードバックループを構成する。
ノーダルシグナルとその制御
ノーダルはActivin受容体 (タイプIIとしてActRIIA/B、タイプIとしてALK4/7) と複合体を形成するが、この複合体形成にはGPIアンカー型膜タンパク質であるEGF-CFCファミリー (Cripto, Cryptic, FRL1, Oepなど) を必要とする[5]。ノーダルの結合によって活性化されたタイプI受容体はSmad2/3をリン酸化し、これらはSmad4と複合体を形成して核内に移行する。この複合体はFoxH1やEomesなどの転写因子と協調して標的遺伝子の発現を制御する。また、ノーダルはFoxH1を介したポジティブフィードバックループを形成しており、自らの発現を誘導する (図2)[11][12][13]。
ノーダルシグナルは、細胞外のアンタゴニストによって厳密に制御されている (図2)。TGF-β ファミリーのLefty1とLefty2はノーダルのフィードバック阻害因子であり[14][12][13]、ノーダルに直接結合する他、ActRIIやEGF-CFCファミリーとの競合的な結合によってノーダルシグナルを抑制するメカニズムが報告されている[15][16]。また、CerberusファミリーのCerl (Cer1) やCerl2 (Dand5) などはノーダルと結合することでノーダルシグナルを抑制する[17][18][5]。
発現部位
マウスでは、ノーダルは着床して間もない時期のエピブラストと臓側内胚葉、ノードの辺縁、左側側板中胚葉で順次発現する。これらの部位での発現制御は詳細に解析され、エピブラスト近位での発現を担うPEE (proximal epiblast enhancer)、ノードでの発現を制御するNDE (node-specific enhancer)、ポジティブフィードバックループを担うASE (asymmetric enhancer) などの特異的エンハンサーが同定されている[19][11][12]。
ゼブラフィッシュでは、Squint (ndr1) とCyclops (ndr2) が胚盤縁全周で発現する[20][21][22]。Cyclopsは、原腸陥入期には胚盾、脊索、脊索前板で発現し、体節形成期になると左側側板中胚葉の前方と左側間脳で発現する[21][22]。Southpaw (ndr3) は、マウスのノードに該当するクッパー胞の周囲で発現し、Cyclopsに先立って左側側板中胚葉で発現する[23]。
アフリカツメガエルでは、Xnr1とXnr2が胞胚期の植物極側と原腸陥入期の帯域 (特に原口背唇部)[24]、Xnr4が原口背唇部や脊索など[25]、Xnr5とXnr6は胞胚期の背側植物極側で発現する[26]。加えて、Xnr1はマウスのノードに該当する原腸蓋板 (gastrocoel roof plate) に次いで左側側板中胚葉で発現する[4]。
脊椎動物以外でも、脱皮動物を除く多くの動物系統でノーダルの非対称な発現が確認されている。例えば、刺胞動物のヒドラでは、出芽領域で非対称に発現する[10]。棘皮動物のウニ胚では、口側の外胚葉で発現した後[27]、右側の外胚葉と原腸の一部で発現する[28]。軟体動物の巻貝では、右巻貝で胚の右側、左巻貝で胚の左側に発現する[29][30]。半索動物や腕足動物の胚でも、調べられた種では右側にノーダルが発現することが確認されている[8]。これらのことから、左右相称動物におけるノーダル発現は右側が基本であったが、脊索動物の先祖に生じたと推察される背腹反転により、脊索動物では胚の左側にノーダルが発現するようになったと考えられている[8][9]。
個体における機能
中・内胚葉系譜の形成
脊椎動物においてノーダルは中・内胚葉の誘導を行う。マウスでは、ノーダル hypomorphic変異胚で胚体内胚葉 (definitive endoderm) を欠き[31]、ノーダル null変異胚では原条の欠損により中胚葉がほとんど形成されない[32]。アフリカツメガエルでは、植物極に局在する転写因子VegTおよび背側のβ-cateninによってノーダルが植物極で転写され、中・内胚葉の誘導および中胚葉のパターン化を制御する[33][24][25][26]。さらに、高いノーダルシグナルは内胚葉とオーガナイザーを含む背側中胚葉を、低いノーダルシグナルは腹側中胚葉を誘導することが知られている。ゼブラフィッシュのsquint;cyclops二重変異体は、中胚葉と内胚葉がほぼ消失し、オーガナイザーである胚盾が形成されない[20]。また、マウスのノーダル null変異胚では、エピブラストが早期に神経上皮化する[34]。primed型多能性幹細胞 (ヒトES細胞やマウスエピブラスト幹細胞) の樹立・維持にはActivin/ノーダルシグナルが必要であるが、これはエピブラストの多能性維持におけるノーダルシグナルの重要性を示している。
神経外胚葉のパターン化
ノーダルシグナルの欠損は、オーガナイザーおよび前方正中中胚葉の形成不全により、神経外胚葉のパターン化に影響を及ぼす。ゼブラフィッシュのcyclops変異体では、脊索前板や神経底板が形成されず、同領域のShh発現が消失する[35][36][22]。その結果、前脳の正中構造の形成不全により単眼症が生じる。同様に、マウスでもノーダル hypomorphic変異胚やSmad2変異胚において、前方中胚葉および前脳正中部の形成不全に起因する全前脳胞症 (holoprosencephaly) が観察される[31][37]。
前後軸形成
着床したマウス胚は、エピブラストおよび隣接した胚体外外胚葉が胚盤胞腔側へ成長し、両者が臓側内胚葉に覆われた円筒胚を形成する。円筒胚の近位は胎盤を形成し、遠位には遠位臓側内胚葉 (distal visceral endoderm: DVE) が出現する。このDVEは将来の前方 (頭側) へ移動して前方臓側内胚葉 (anterior visceral endoderm: AVE) を形成し、その反対側に原条が形成されることで、胚に明確な前後非対称性が確立される[38]。ノーダルは、PEEやASEなどのエンハンサーによりエピブラストで発現し、そのシグナルはDVEにおけるLefty1、Cerl、Dkk1の発現を誘導する[39]。AVEから分泌されるこれらの因子は、隣接するエピブラストにおけるノーダルポジティブフィードバックループとWntシグナルを抑制し、エピブラストのノーダル発現をAVEと反対側、すなわち胚後方に限局させる[40]。この結果、胚前方には神経外胚葉が、胚後方には原条が形成される。
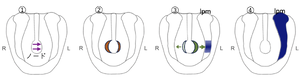
胚遠位から観察したマウス初期体節期胚の模式図 (図上が前方、下が後方)。左右軸形成は①から④の順に進行する。
① 左右オーガナイザーであるノードの腹側に左向きの流れ (ノーダル flow) が発生する。
② ノード周縁部 (クラウン細胞) では、NotchシグナルによってノーダルやCerl2などの左右軸関連遺伝子が発現するが、流れにより左側のCerl2 mRNAが分解される (褐色はCerl2 mRNAを表す)。
③ Cerl2は右側でノーダルを強く抑制することにより、左側でのノーダル活性が高くなる (緑色はノードにおけるノーダル活性を表す)。ノードから拡散したノーダルは、近傍の左側側板中胚葉 (lateral plate mesoderm, lpm) に自らの発現を誘導する (紺色はノーダル発現を示す)。
④ ノーダルはポジティブフィードバックループによって発現域を拡張するとともに、転写因子Pitx2の発現を誘導する (紺色はノーダルおよびPitx2発現を示す)。これらの左右非対称な発現は、その後の臓器の左右非対称な形態形成を制御する。
左右軸形成
脊椎動物では、初期体節期にノーダルが左側側板中胚葉で発現する。ノーダルはFoxH1を介して転写因子Pitx2の発現を誘導し (図2)[41]、臓器の左右非対称な形態形成を制御する。脊椎動物以外でも、ノーダルを保有する動物系統ではPitxがノーダルと同側に非対称に発現することが確認されており、進化の過程でPitxはノーダルシグナルと連結することで非対称な形態形成の役割を獲得したと推察されている[8]。例えば、ノーダル-Pitx発現の左右非対称性は、軟体動物の巻貝では貝殻の巻き方向を決定し[29]、棘皮動物のウニではプルテウス幼生におけるウニ原基の左右非対称な形成を制御する (右側のノーダルシグナルはウニ原基形成を抑制する) [28]。
脊椎動物でノーダルを左側の側板中胚葉で発現させる装置が左右オーガナイザー (マウスのノード、ニワトリのヘンゼン結節、アフリカツメガエルの原腸蓋板、ゼブラフィッシュのクッパー胞) である。ニワトリを除くこれらの左右オーガナイザーでは、線毛の回転運動によって左向きの水流が形成される (図3)。この物理現象により、Cerl2などのノーダル阻害因子が右側で優位となり (マウスでは左側のCerl2 mRNAが分解される)[18][42][43][44]、左側のノーダル活性が右側に比べて相対的に高まる(図3)[45]。左右オーガナイザーから拡散したノーダルは、近傍の左側側板中胚葉に自らの発現を誘導する (図3)[46]。ノーダルのポジティブフィードバックループとLeftyによるネガティブフィードバックループは、チューリングの反応拡散モデルの基本条件を満たしており、左右オーガナイザーにおける僅かなノーダル活性差を側板中胚葉における顕著な左右非対称性へと増幅する[47][48]。左側側板中胚葉のノーダル発現域は、拡散とポジティブフィードバックループによって心臓形成領域まで拡張するが (図3)[13]、Leftyによりその発現域は左側に限局され、最終的にノーダル発現は終息する[49][50]。
左側側板中胚葉でノーダルによって誘導されたPitx2は、その細胞系譜で発現を維持する[41]。マウスでは、このメカニズムにより確立された左右軸情報が、心臓形態形成、刺激伝導系の発生、肺の分葉パターン、腸ループ回転などの非対称な形態形成を制御する[51][47][52][53]。ゼブラフィッシュでは、左側間脳におけるノーダルシグナルが、副松果体と手綱核の左右非対称な発生を制御している[54][55][56]。
ヒト疾患との関わり
臓器の左右性に異常を来す先天異常には、完全内臓逆位や内臓錯位症候群などがある。内臓錯位症候群は出生10,000人に約0.8人と稀な疾患であるが、手術介入が必要な重度の先天性心疾患や不整脈を伴うことが多い[57]。マウスでは、ノーダルを始めとする左右軸関連遺伝子の変異によって、ヒト完全内臓逆位や内臓錯位症候群に類似した表現型が再現される (引用文献はその一例) [51][31][18][49][50][37][11][13]。ヒト内臓錯位症候群の遺伝子解析では、ノーダルを含む左右軸関連遺伝子の変異が多数同定されている[58]。さらに、内臓錯位症候群を伴わない先天性心疾患や全前脳胞症でもノーダルの変異が同定されることがある[59][60]。内臓錯位症候群は、遺伝要因のみならず糖尿病合併妊娠で発症リスクが亢進することが知られている。マウスの糖尿病モデルでは、高血糖環境がノードにおけるノーダル発現を変化させる結果、左右軸を確立できないことが明らかになっている[61]。
関連語
参考文献
- ↑ 1.0 1.1
Zhou, X., Sasaki, H., Lowe, L., Hogan, B.L., & Kuehn, M.R. (1993).
Nodal is a novel TGF-beta-like gene expressed in the mouse node during gastrulation. Nature, 361(6412), 543-7. [PubMed:8429908] [WorldCat] [DOI] - ↑
Collignon, J., Varlet, I., & Robertson, E.J. (1996).
Relationship between asymmetric nodal expression and the direction of embryonic turning. Nature, 381(6578), 155-8. [PubMed:8610012] [WorldCat] [DOI] - ↑
Levin, M., Johnson, R.L., Stern, C.D., Kuehn, M., & Tabin, C. (1995).
A molecular pathway determining left-right asymmetry in chick embryogenesis. Cell, 82(5), 803-14. [PubMed:7671308] [WorldCat] [DOI] - ↑ 4.0 4.1
Lowe, L.A., Supp, D.M., Sampath, K., Yokoyama, T., Wright, C.V., Potter, S.S., ..., & Kuehn, M.R. (1996).
Conserved left-right asymmetry of nodal expression and alterations in murine situs inversus. Nature, 381(6578), 158-61. [PubMed:8610013] [WorldCat] [DOI] - ↑ 5.0 5.1 5.2
Shen, M.M. (2007).
Nodal signaling: developmental roles and regulation. Development (Cambridge, England), 134(6), 1023-34. [PubMed:17287255] [WorldCat] [DOI] - ↑
Beck, S., Le Good, J.A., Guzman, M., Ben Haim, N., Roy, K., Beermann, F., & Constam, D.B. (2002).
Extraembryonic proteases regulate Nodal signalling during gastrulation. Nature cell biology, 4(12), 981-5. [PubMed:12447384] [WorldCat] [DOI] - ↑
Le Good, J.A., Joubin, K., Giraldez, A.J., Ben-Haim, N., Beck, S., Chen, Y., ..., & Constam, D.B. (2005).
Nodal stability determines signaling range. Current biology : CB, 15(1), 31-6. [PubMed:15649361] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2 8.3 8.4
Grande, C., Martín-Durán, J.M., Kenny, N.J., Truchado-García, M., & Hejnol, A. (2014).
Evolution, divergence and loss of the Nodal signalling pathway: new data and a synthesis across the Bilateria. The International journal of developmental biology, 58(6-8), 521-32. [PubMed:25690967] [WorldCat] [DOI] - ↑ 9.0 9.1
Namigai, E.K., Kenny, N.J., & Shimeld, S.M. (2014).
Right across the tree of life: the evolution of left-right asymmetry in the Bilateria. Genesis (New York, N.Y. : 2000), 52(6), 458-70. [PubMed:24510729] [WorldCat] [DOI] - ↑ 10.0 10.1
Watanabe, H., Schmidt, H.A., Kuhn, A., Höger, S.K., Kocagöz, Y., Laumann-Lipp, N., ..., & Holstein, T.W. (2014).
Nodal signalling determines biradial asymmetry in Hydra. Nature, 515(7525), 112-5. [PubMed:25156256] [WorldCat] [DOI] - ↑ 11.0 11.1 11.2
Norris, D.P., Brennan, J., Bikoff, E.K., & Robertson, E.J. (2002).
The Foxh1-dependent autoregulatory enhancer controls the level of Nodal signals in the mouse embryo. Development (Cambridge, England), 129(14), 3455-68. [PubMed:12091315] [WorldCat] [DOI] - ↑ 12.0 12.1 12.2
Saijoh, Y., Adachi, H., Sakuma, R., Yeo, C.Y., Yashiro, K., Watanabe, M., ..., & Hamada, H. (2000).
Left-right asymmetric expression of lefty2 and nodal is induced by a signaling pathway that includes the transcription factor FAST2. Molecular cell, 5(1), 35-47. [PubMed:10678167] [WorldCat] [DOI] - ↑ 13.0 13.1 13.2 13.3
Yamamoto, M., Mine, N., Mochida, K., Sakai, Y., Saijoh, Y., Meno, C., & Hamada, H. (2003).
Nodal signaling induces the midline barrier by activating Nodal expression in the lateral plate. Development (Cambridge, England), 130(9), 1795-804. [PubMed:12642485] [WorldCat] [DOI] - ↑
Meno, C., Gritsman, K., Ohishi, S., Ohfuji, Y., Heckscher, E., Mochida, K., ..., & Hamada, H. (1999).
Mouse Lefty2 and zebrafish antivin are feedback inhibitors of nodal signaling during vertebrate gastrulation. Molecular cell, 4(3), 287-98. [PubMed:10518210] [WorldCat] [DOI] - ↑
Chen, C., & Shen, M.M. (2004).
Two modes by which Lefty proteins inhibit nodal signaling. Current biology : CB, 14(7), 618-24. [PubMed:15062104] [WorldCat] [DOI] - ↑
Sakuma, R., Ohnishi Yi, Y., Meno, C., Fujii, H., Juan, H., Takeuchi, J., ..., & Hamada, H. (2002).
Inhibition of Nodal signalling by Lefty mediated through interaction with common receptors and efficient diffusion. Genes to cells : devoted to molecular & cellular mechanisms, 7(4), 401-12. [PubMed:11952836] [WorldCat] [DOI] - ↑
Hashimoto, H., Rebagliati, M., Ahmad, N., Muraoka, O., Kurokawa, T., Hibi, M., & Suzuki, T. (2004).
The Cerberus/Dan-family protein Charon is a negative regulator of Nodal signaling during left-right patterning in zebrafish. Development (Cambridge, England), 131(8), 1741-53. [PubMed:15084459] [WorldCat] [DOI] - ↑ 18.0 18.1 18.2
Marques, S., Borges, A.C., Silva, A.C., Freitas, S., Cordenonsi, M., & Belo, J.A. (2004).
The activity of the Nodal antagonist Cerl-2 in the mouse node is required for correct L/R body axis. Genes & development, 18(19), 2342-7. [PubMed:15466485] [PMC] [WorldCat] [DOI] - ↑
Krebs, L.T., Iwai, N., Nonaka, S., Welsh, I.C., Lan, Y., Jiang, R., ..., & Gridley, T. (2003).
Notch signaling regulates left-right asymmetry determination by inducing Nodal expression. Genes & development, 17(10), 1207-12. [PubMed:12730124] [PMC] [WorldCat] [DOI] - ↑ 20.0 20.1
Feldman, B., Gates, M.A., Egan, E.S., Dougan, S.T., Rennebeck, G., Sirotkin, H.I., ..., & Talbot, W.S. (1998).
Zebrafish organizer development and germ-layer formation require nodal-related signals. Nature, 395(6698), 181-5. [PubMed:9744277] [WorldCat] [DOI] - ↑ 21.0 21.1
Rebagliati, M.R., Toyama, R., Fricke, C., Haffter, P., & Dawid, I.B. (1998).
Zebrafish nodal-related genes are implicated in axial patterning and establishing left-right asymmetry. Developmental biology, 199(2), 261-72. [PubMed:9698446] [WorldCat] [DOI] - ↑ 22.0 22.1 22.2
Sampath, K., Rubinstein, A.L., Cheng, A.M., Liang, J.O., Fekany, K., Solnica-Krezel, L., ..., & Wright, C.V. (1998).
Induction of the zebrafish ventral brain and floorplate requires cyclops/nodal signalling. Nature, 395(6698), 185-9. [PubMed:9744278] [WorldCat] [DOI] - ↑
Long, S., Ahmad, N., & Rebagliati, M. (2003).
The zebrafish nodal-related gene southpaw is required for visceral and diencephalic left-right asymmetry. Development (Cambridge, England), 130(11), 2303-16. [PubMed:12702646] [WorldCat] [DOI] - ↑ 24.0 24.1
Jones, C.M., Kuehn, M.R., Hogan, B.L., Smith, J.C., & Wright, C.V. (1995).
Nodal-related signals induce axial mesoderm and dorsalize mesoderm during gastrulation. Development (Cambridge, England), 121(11), 3651-62. [PubMed:8582278] [WorldCat] [DOI] - ↑ 25.0 25.1
Joseph, E.M., & Melton, D.A. (1997).
Xnr4: a Xenopus nodal-related gene expressed in the Spemann organizer. Developmental biology, 184(2), 367-72. [PubMed:9133442] [WorldCat] [DOI] - ↑ 26.0 26.1
Takahashi, S., Yokota, C., Takano, K., Tanegashima, K., Onuma, Y., Goto, J., & Asashima, M. (2000).
Two novel nodal-related genes initiate early inductive events in Xenopus Nieuwkoop center. Development (Cambridge, England), 127(24), 5319-29. [PubMed:11076754] [WorldCat] [DOI] - ↑
Duboc, V., Röttinger, E., Besnardeau, L., & Lepage, T. (2004).
Nodal and BMP2/4 signaling organizes the oral-aboral axis of the sea urchin embryo. Developmental cell, 6(3), 397-410. [PubMed:15030762] [WorldCat] [DOI] - ↑ 28.0 28.1
Duboc, V., Röttinger, E., Lapraz, F., Besnardeau, L., & Lepage, T. (2005).
Left-right asymmetry in the sea urchin embryo is regulated by nodal signaling on the right side. Developmental cell, 9(1), 147-58. [PubMed:15992548] [WorldCat] [DOI] - ↑ 29.0 29.1
Grande, C., & Patel, N.H. (2009).
Nodal signalling is involved in left-right asymmetry in snails. Nature, 457(7232), 1007-11. [PubMed:19098895] [PMC] [WorldCat] [DOI] - ↑
Kuroda, R., Endo, B., Abe, M., & Shimizu, M. (2009).
Chiral blastomere arrangement dictates zygotic left-right asymmetry pathway in snails. Nature, 462(7274), 790-4. [PubMed:19940849] [WorldCat] [DOI] - ↑ 31.0 31.1 31.2
Lowe, L.A., Yamada, S., & Kuehn, M.R. (2001).
Genetic dissection of nodal function in patterning the mouse embryo. Development (Cambridge, England), 128(10), 1831-43. [PubMed:11311163] [WorldCat] [DOI] - ↑
Conlon, F.L., Lyons, K.M., Takaesu, N., Barth, K.S., Kispert, A., Herrmann, B., & Robertson, E.J. (1994).
A primary requirement for nodal in the formation and maintenance of the primitive streak in the mouse. Development (Cambridge, England), 120(7), 1919-28. [PubMed:7924997] [WorldCat] [DOI] - ↑
Agius, E., Oelgeschläger, M., Wessely, O., Kemp, C., & De Robertis, E.M. (2000).
Endodermal Nodal-related signals and mesoderm induction in Xenopus. Development (Cambridge, England), 127(6), 1173-83. [PubMed:10683171] [PMC] [WorldCat] [DOI] - ↑
Camus, A., Perea-Gomez, A., Moreau, A., & Collignon, J. (2006).
Absence of Nodal signaling promotes precocious neural differentiation in the mouse embryo. Developmental biology, 295(2), 743-55. [PubMed:16678814] [WorldCat] [DOI] - ↑
Krauss, S., Concordet, J.P., & Ingham, P.W. (1993).
A functionally conserved homolog of the Drosophila segment polarity gene hh is expressed in tissues with polarizing activity in zebrafish embryos. Cell, 75(7), 1431-44. [PubMed:8269519] [WorldCat] [DOI] - ↑
Rebagliati, M.R., Toyama, R., Haffter, P., & Dawid, I.B. (1998).
cyclops encodes a nodal-related factor involved in midline signaling. Proceedings of the National Academy of Sciences of the United States of America, 95(17), 9932-7. [PubMed:9707578] [PMC] [WorldCat] [DOI] - ↑ 37.0 37.1
Nomura, M., & Li, E. (1998).
Smad2 role in mesoderm formation, left-right patterning and craniofacial development. Nature, 393(6687), 786-90. [PubMed:9655392] [WorldCat] [DOI] - ↑
Arnold, S.J., & Robertson, E.J. (2009).
Making a commitment: cell lineage allocation and axis patterning in the early mouse embryo. Nature reviews. Molecular cell biology, 10(2), 91-103. [PubMed:19129791] [WorldCat] [DOI] - ↑
Brennan, J., Lu, C.C., Norris, D.P., Rodriguez, T.A., Beddington, R.S., & Robertson, E.J. (2001).
Nodal signalling in the epiblast patterns the early mouse embryo. Nature, 411(6840), 965-9. [PubMed:11418863] [WorldCat] [DOI] - ↑
Perea-Gomez, A., Vella, F.D., Shawlot, W., Oulad-Abdelghani, M., Chazaud, C., Meno, C., ..., & Ang, S.L. (2002).
Nodal antagonists in the anterior visceral endoderm prevent the formation of multiple primitive streaks. Developmental cell, 3(5), 745-56. [PubMed:12431380] [WorldCat] [DOI] - ↑ 41.0 41.1
Shiratori, H., Sakuma, R., Watanabe, M., Hashiguchi, H., Mochida, K., Sakai, Y., ..., & Hamada, H. (2001).
Two-step regulation of left-right asymmetric expression of Pitx2: initiation by nodal signaling and maintenance by Nkx2. Molecular cell, 7(1), 137-49. [PubMed:11172719] [WorldCat] [DOI] - ↑
Nakamura, T., Saito, D., Kawasumi, A., Shinohara, K., Asai, Y., Takaoka, K., ..., & Hamada, H. (2012).
Fluid flow and interlinked feedback loops establish left-right asymmetric decay of Cerl2 mRNA. Nature communications, 3, 1322. [PubMed:23271656] [WorldCat] [DOI] - ↑
Sampaio, P., Ferreira, R.R., Guerrero, A., Pintado, P., Tavares, B., Amaro, J., ..., & Lopes, S.S. (2014).
Left-right organizer flow dynamics: how much cilia activity reliably yields laterality? Developmental cell, 29(6), 716-28. [PubMed:24930722] [WorldCat] [DOI] - ↑
Schweickert, A., Vick, P., Getwan, M., Weber, T., Schneider, I., Eberhardt, M., ..., & Blum, M. (2010).
The nodal inhibitor Coco is a critical target of leftward flow in Xenopus. Current biology : CB, 20(8), 738-43. [PubMed:20381352] [WorldCat] [DOI] - ↑
Hamada, H., & Tam, P.P. (2014).
Mechanisms of left-right asymmetry and patterning: driver, mediator and responder. F1000prime reports, 6, 110. [PubMed:25580264] [PMC] [WorldCat] [DOI] - ↑
Oki, S., Hashimoto, R., Okui, Y., Shen, M.M., Mekada, E., Otani, H., ..., & Hamada, H. (2007).
Sulfated glycosaminoglycans are necessary for Nodal signal transmission from the node to the left lateral plate in the mouse embryo. Development (Cambridge, England), 134(21), 3893-904. [PubMed:17913787] [WorldCat] [DOI] - ↑ 47.0 47.1
Hamada, H., Meno, C., Watanabe, D., & Saijoh, Y. (2002).
Establishment of vertebrate left-right asymmetry. Nature reviews. Genetics, 3(2), 103-13. [PubMed:11836504] [WorldCat] [DOI] - ↑
Nakamura, T., Mine, N., Nakaguchi, E., Mochizuki, A., Yamamoto, M., Yashiro, K., ..., & Hamada, H. (2006).
Generation of robust left-right asymmetry in the mouse embryo requires a self-enhancement and lateral-inhibition system. Developmental cell, 11(4), 495-504. [PubMed:17011489] [WorldCat] [DOI] - ↑ 49.0 49.1
Meno, C., Shimono, A., Saijoh, Y., Yashiro, K., Mochida, K., Ohishi, S., ..., & Hamada, H. (1998).
lefty-1 is required for left-right determination as a regulator of lefty-2 and nodal. Cell, 94(3), 287-97. [PubMed:9708731] [WorldCat] [DOI] - ↑ 50.0 50.1
Meno, C., Takeuchi, J., Sakuma, R., Koshiba-Takeuchi, K., Ohishi, S., Saijoh, Y., ..., & Hamada, H. (2001).
Diffusion of nodal signaling activity in the absence of the feedback inhibitor Lefty2. Developmental cell, 1(1), 127-38. [PubMed:11703930] [WorldCat] [DOI] - ↑ 51.0 51.1
Franco, D., Sedmera, D., & Lozano-Velasco, E. (2017).
Multiple Roles of Pitx2 in Cardiac Development and Disease. Journal of cardiovascular development and disease, 4(4). [PubMed:29367545] [PMC] [WorldCat] [DOI] - ↑
Joo, K., Matsuoka, R., Kitajima, K., Yashiro, K., Shiose, A., Tominaga, R., ..., & Meno, C. (2026).
Cardiac conduction system malformations in heterotaxy result from dysregulated Pitx2 expression. JCI insight, 11(6). [PubMed:41734036] [PMC] [WorldCat] [DOI] - ↑
Yashiro, K., Shiratori, H., & Hamada, H. (2007).
Haemodynamics determined by a genetic programme govern asymmetric development of the aortic arch. Nature, 450(7167), 285-8. [PubMed:17994097] [WorldCat] [DOI] - ↑
Concha, M.L., Burdine, R.D., Russell, C., Schier, A.F., & Wilson, S.W. (2000).
A nodal signaling pathway regulates the laterality of neuroanatomical asymmetries in the zebrafish forebrain. Neuron, 28(2), 399-409. [PubMed:11144351] [WorldCat] [DOI] - ↑
Gamse, J.T., Kuan, Y.S., Macurak, M., Brösamle, C., Thisse, B., Thisse, C., & Halpern, M.E. (2005).
Directional asymmetry of the zebrafish epithalamus guides dorsoventral innervation of the midbrain target. Development (Cambridge, England), 132(21), 4869-81. [PubMed:16207761] [WorldCat] [DOI] - ↑
Gobbo, A., Messina, A., & Vallortigara, G. (2025).
Swimming through asymmetry: zebrafish as a model for brain and behavior lateralization. Frontiers in behavioral neuroscience, 19, 1527572. [PubMed:39906337] [PMC] [WorldCat] [DOI] - ↑
Smith, A., Ho, S.Y., Anderson, R.H., Connell, M.G., Arnold, R., Wilkinson, J.L., & Cook, A.C. (2006).
The diverse cardiac morphology seen in hearts with isomerism of the atrial appendages with reference to the disposition of the specialised conduction system. Cardiology in the young, 16(5), 437-54. [PubMed:16984696] [WorldCat] [DOI] - ↑
Wells, J.R., Padua, M.B., & Ware, S.M. (2022).
The genetic landscape of cardiovascular left-right patterning defects. Current opinion in genetics & development, 75, 101937. [PubMed:35777348] [PMC] [WorldCat] [DOI] - ↑
Dardas, Z., Fatih, J.M., Jolly, A., Dawood, M., Du, H., Grochowski, C.M., ..., & Morris, S.A. (2024).
NODAL variants are associated with a continuum of laterality defects from simple D-transposition of the great arteries to heterotaxy. Genome medicine, 16(1), 53. [PubMed:38570875] [PMC] [WorldCat] [DOI] - ↑
Roessler, E., Pei, W., Ouspenskaia, M.V., Karkera, J.D., Veléz, J.I., Banerjee-Basu, S., ..., & Muenke, M. (2009).
Cumulative ligand activity of NODAL mutations and modifiers are linked to human heart defects and holoprosencephaly. Molecular genetics and metabolism, 98(1-2), 225-34. [PubMed:19553149] [PMC] [WorldCat] [DOI] - ↑
Matsuoka, R., Kitajima, K., Nii, T., Zou, Z., Tanaka, K., Joo, K., ..., & Meno, C. (2025).
Hyperglycaemia induces diet-dependent defects of the left-right axis by lowering intracellular pH. Biochimica et biophysica acta. Molecular basis of disease, 1871(1), 167550. [PubMed:39442590] [WorldCat] [DOI]