グルタミン酸受容体相互作用タンパク質
緑川良介、髙宮考悟
宮崎大学医学部 機能制御学講座 統合生理学分野
DOI:10.14931/bsd.11505 原稿受付日:2025年6月18日 原稿完成日:2025年8月15日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
英:glutamate receptor interacting protein
英略語:GRIP
GRIPは、多PDZドメインを有する足場タンパク質群であり、AMPA型グルタミン酸受容体の局在や輸送を制御することで興奮性シナプスの機能と可塑性に寄与する。哺乳類ではGRIP1とGRIP2の2つの相同タンパク質が知られる。
イントロダクション
GRIP1は、1997年にDongらによって初めて同定されたAMPA受容体結合タンパク質であり[1] (Dong et al., 1997)、その後の研究でGRIP1と高い相同性を有するGRIP2がクローニングされた[2] (Dong et al., 1999)。またGRIP2遺伝子座由来のスプライシングバリアントとしてABP (AMPA receptor-binding protein) が報告された[3](Wyszynski et al., 1999)[注釈1 1]。現在では、これらはGRIPファミリーに属する多PDZドメイン足場タンパク質群として理解されている。
GRIPは、シナプス後膜においてAMPA受容体の局在や安定化に寄与し、記憶・学習を支える長期増強(LTP)や長期抑圧(LTD)といった可塑性機構に関与する。また、PICK1や他のPDZタンパク質と相互作用しながら、受容体のトラフィッキングや分解、リサイクリングの制御にも関わる。GRIPファミリーは、PDZドメインを介してシナプス受容体複合体を組織化する代表的な足場タンパク質として広く研究されている。
- ↑ ABPはGRIP2のスプライシングバリアントの一部を指す歴史的名称であり、文献によってはABP/GRIP2と併記、もしくはGRIP2をABP (ABP-L)と呼称することもある
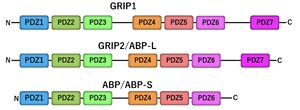
GRIP1およびGRIP2はそれぞれ7個のPDZドメインをもち、N末端側から順に番号が付けられる。
ABPはGRIP2遺伝子座由来のスプライシングバリアントの一つであり、N末端領域の一部およびPDZ7ドメインを欠く短縮型として報告されている。
構造
GRIP1, GRIP2はいずれも7つのPDZドメインを持つ(図1)。これらのドメインを介して他のシナプス構成因子や足場タンパクとの複合体を形成する。現在までのところ、GRIP全長のX線結晶構造は未報告である。一方、PDZドメイン断片(例:PDZ12タンデム)については結晶構造解析の報告があるが、GRIP PDZドメインとGluA2/3 C末端との高解像度X線結晶構造は報告されていない
サブファミリー
GRIPには主に以下の2つのサブタイプが存在する:
GRIP1
最も広く研究されているサブタイプで、AMPARの輸送と固定に特に重要な働きを持つ。さらに計5つのスプライシングバリアント(GRIP1a-e)の存在が報告される[4] [5] [6](Yamazaki et al., 2001)( Charych et al., 2004)( Charych 2006)。
GRIP2/ABP
GRIP1と高い相同性を持ち、類似の機能を果たすと考えられている。スプライシングバリアントとしてABP-L, pABP-L, ABP-Sの存在が報告される[3] [7](Wyszynski et al., 1999) (Desouza et al., 2002)。
発現
組織分布
GRIPは中枢神経系において広く発現しており、特に海馬、大脳皮質、嗅球で高い発現がみられる[2][3] (Dong et al., 1999) (Wyszynski et al., 1998)。細胞種としては、GRIP1は大脳皮質の錐体細胞、海馬CA1錐体細胞、小脳のプルキンエ細胞において高い発現が確認されている。
細胞内分布
細胞内では、主に細胞体-樹状突起、シナプス後膜近傍の樹状突起スパインに局在し、AMPARと共局在する[2][3] (Dong et al., 1999)(Wyszynski et al., 1999)。
特に樹状突起スパインにおいては、N末端にパルミトイル化配列をもつGRIP1bおよびpABP-Lが、パルミトイル化を介して高い割合で局在すると考えられている[7](Desouza et al., 2002)。
結合タンパク質
これまでに報告されているGRIP結合タンパクの多くはPDZドメインを介して結合する。GRIPが認識するリガンドの多くはclassⅡ型(–X–Φ–X–Φ)に分類されるC末端配列を有するが、非典型的配列を認識するケースも報告されている[注釈2 1]※。
- ↑ PDZの項目参照。PDZドメインは一般に結合タンパクのC末端配列を介して相互作用し、その配列に基づいてclassⅠ~Ⅲに分類される。classⅡはC末端配列が–X–Φ–X–Φ(Xは任意のアミノ酸、Φは疎水性アミノ酸)であるタンパクと結合する傾向を示す。
GRIP1結合タンパク
これまでに報告されている、GRIP1の各PDZドメインに結合する代表的なタンパクを以下に示す:
| PDZ ドメイン | 結合タンパク | 結合タンパクのC末端配列 | 参考文献 |
|---|---|---|---|
| PDZ1-3 | Fras1 | G-T-E-V | [8]et al., 2004 |
| PDZ4-5 | GluA2, GluA3 (short form) | S-V-K-I | [1]Dong et al., 1997 |
| PDZ6 | EphB2 | S-V-E-V | [9]Torres et al., 1998 |
| PDZ6 | EphA7 | G-I-Q-V | [9]Torres et al., 1998 |
| PDZ6 | EphrinB1 | Y-Y-K-V | [10]Brückner K et al., 1999 |
| PDZ6 | Liprin-α | T-Y-S-C | [11]Wyszynski et al., 2002 |
| PDZ7 | GRASP-1 NG2 |
Q-Y-W-V | [12]Feng et al., 2002 |
文献[13]Stegmüller et al., 2003[14]Sheng et al., 2001を参考に再構成
GRIP2結合タンパク
GluA2/3[2] (Dong et al., 1999)、 ephrinB[10] (Brückner et al., 1999) 系タンパク、GRASP-1[15](Ye et al., 2000)、[13]NG2(Stegmüller et al., 2003)等との相互作用が報告されており、GRIP1 のホモログとして類似の足場機能を担うと考えられている。ただし、これらのタンパクとの相互作用に関して、GRIP1との機能分担の詳細は明らかにされていない。
文献[16]を参考に再構成。
機能
タンパク質機能
シナプス後膜へのAMPA受容体の輸送及びアンカリング
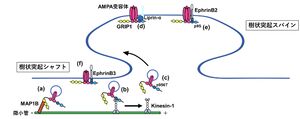
GRIP1はGluA2/3のC末端PDZ結合配列への結合を介し、他のGRIP結合タンパクと協調してAMPA受容体の輸送およびシナプス後膜局在を制御する(図2)
- MAP1Bとの相互作用は微小管依存的なAMPA受容体輸送の調節に関与する(a) [17] (Palenzuela et al., 2017)。
- Kinesin-1(KIF5)との直接結合はAMPA受容体の樹状突起方向への選択的輸送に寄与する(b) [18] (Setou et al., 2002)。
- GRIP1のThr956リン酸化はGluA2との結合を低下させ、AMPA受容体の動的再分布に関与する(c) [19] (Geiger et al., 2014)。
- GRIP1はLiprin-αとの結合等を介し、AMPA受容体のシナプス後膜での安定化に寄与する(d) [11] (Wyszinski et al., 2002)。
- ephrinB2およびephrinB3はGRIP1とPDZ依存的に結合し、AMPA受容体の表面安定化に関与する。ephrinB2は主にスパインに、ephrinB3は樹状突起シャフトに多く分布することから、それぞれの部位でAMPA受容体安定化を担う可能性が示唆されている(e,f)。
文献[10][20][21] (Brückner et al., 1999; Essmann et al., 2008; Aoto et al., 2007)。 図3. GRIP, PICK1を介した小脳プルキンエ細胞におけるLTD分子機構
GRIP–PICK1競合によるAMPA受容体の内在化制御とシナプス可塑性
GRIPは同じくPDZドメインをもつPICK1との競合的相互作用により、AMPA受容体の内在化およびリサイクリングへの分子スイッチとして機能する。これによりLTDを代表とするシナプス可塑性機構の制御を担っている[22][23][24][25][26][27](Chung et al., 2000; Perez et al., 2001; Lu et al., 2005; Steinberg et al., 2006; Takamiya et al., 2008; Mao et al., 2010 )。小脳プルキンエ細胞におけるGRIPおよびPICK1を介したLTD分子機構を図3に示す。
定常時には、GRIPを足場としてAMPA受容体は樹状突起スパインに安定化されている。
↓
LTD誘発刺激によりmGluR1活性化および電位依存性カルシウムチャンネル(VDCC)からのCa²⁺流入を介して細胞内Ca²⁺濃度が上昇し、PKCαが活性化される。
↓
PICK1は活性型PKCαと結合し、活性型PKCαをGluA2近傍へリクルートする。
↓
PKCαはGluA2のSer880をリン酸化し、これによりGRIPとの結合が低下する。
↓
リン酸化GluA2はPICK1と結合し、クラスリン依存性エンドサイトーシスを介して細胞内へ取り込まれる。
↓
その結果、スパインにおけるAMPA受容体発現が減少し、LTDが発現する。また、エンドサイトーシス後のAMPA受容体のリサイクリング過程には、GRIP1がExocyst構成因子Sec8と相互作用し、リサイクリングエンドソームを介した受容体再輸送に関与することが報告されている[27](Mao et al., 2010)。
上皮細胞におけるFras1輸送の制御
GRIP1はPDZ1–3タンデムドメインを介してFras1のC末端配列に結合し、Fras1の基底膜側への輸送および分泌を制御する。分泌されたFras1はFrem1やFrem2などと巨大な細胞外マトリクス複合体を形成し、特に胚発生期における表皮と真皮の接着を安定化する[8](Takamiya et al., 2004)。このことから、GRIP1は神経系における受容体輸送のみならず、上皮組織の形態形成にも重要な役割を果たすことが示されている。その他GRIP1ノックアウトマウスの解析から、腎臓の形成初期にも重要な働きを担っていることが示されている。
個体機能
GRIPファミリーは小脳プルキンエ細胞におけるLTD発現に必須であることが示されており[26](Takamiya et al., 2008)、さらにGRIP1条件付きノックアウトマウスでは海馬シナプス可塑性異常とともに学習・記憶障害が認められる[28](Tan et al., 2020)。これらの知見は、GRIPが個体レベルの神経機能に重要な役割を果たすことを示している。
疾患との関わり
GRIP1の機能獲得型変異が自閉スペクトラム症(ASD)患者で報告されており、AMPAR輸送異常を介した神経発達障害への関与が示唆されている[29](Mejias et al., 2011)。さらに、GRIP1欠損マウスではFras1の基底膜側への輸送障害により表皮と真皮の接着が維持できず、Frasier症候群様の表現型を示すことが報告されている[8](Takamiya et al., 2004)。ヒトにおいてもGRIP1変異がFrasier症候群の原因となることが示されており、GRIP1はその原因遺伝子の一つとされている。
参考文献
- ↑ 1.0 1.1
Dong, H., O'Brien, R.J., Fung, E.T., Lanahan, A.A., Worley, P.F., & Huganir, R.L. (1997).
GRIP: a synaptic PDZ domain-containing protein that interacts with AMPA receptors. Nature, 386(6622), 279-84. [PubMed:9069286] [WorldCat] [DOI] - ↑ 2.0 2.1 2.2 2.3
Dong, H., Zhang, P., Song, I., Petralia, R.S., Liao, D., & Huganir, R.L. (1999).
Characterization of the glutamate receptor-interacting proteins GRIP1 and GRIP2. The Journal of neuroscience : the official journal of the Society for Neuroscience, 19(16), 6930-41. [PubMed:10436050] [PMC] [WorldCat] [DOI] - ↑ 3.0 3.1 3.2 3.3
Wyszynski, M., Valtschanoff, J.G., Naisbitt, S., Dunah, A.W., Kim, E., Standaert, D.G., ..., & Sheng, M. (1999).
Association of AMPA receptors with a subset of glutamate receptor-interacting protein in vivo. The Journal of neuroscience : the official journal of the Society for Neuroscience, 19(15), 6528-37. [PubMed:10414981] [PMC] [WorldCat] [DOI] - ↑
Yamazaki, M., Fukaya, M., Abe, M., Ikeno, K., Kakizaki, T., Watanabe, M., & Sakimura, K. (2001).
Differential palmitoylation of two mouse glutamate receptor interacting protein 1 forms with different N-terminal sequences. Neuroscience letters, 304(1-2), 81-4. [PubMed:11335060] [WorldCat] [DOI] - ↑
Charych, E.I., Yu, W., Li, R., Serwanski, D.R., Miralles, C.P., Li, X., ..., & De Blas, A.L. (2004).
A four PDZ domain-containing splice variant form of GRIP1 is localized in GABAergic and glutamatergic synapses in the brain. The Journal of biological chemistry, 279(37), 38978-90. [PubMed:15226318] [WorldCat] [DOI] - ↑
Charych, E.I., Li, R., Serwanski, D.R., Li, X., Miralles, C.P., Pinal, N., & De Blas, A.L. (2006).
Identification and characterization of two novel splice forms of GRIP1 in the rat brain. Journal of neurochemistry, 97(3), 884-98. [PubMed:16539648] [WorldCat] [DOI] - ↑ 7.0 7.1
DeSouza, S., Fu, J., States, B.A., & Ziff, E.B. (2002).
Differential palmitoylation directs the AMPA receptor-binding protein ABP to spines or to intracellular clusters. The Journal of neuroscience : the official journal of the Society for Neuroscience, 22(9), 3493-503. [PubMed:11978826] [PMC] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2
Takamiya, K., Kostourou, V., Adams, S., Jadeja, S., Chalepakis, G., Scambler, P.J., ..., & Adams, R.H. (2004).
A direct functional link between the multi-PDZ domain protein GRIP1 and the Fraser syndrome protein Fras1. Nature genetics, 36(2), 172-7. [PubMed:14730302] [WorldCat] [DOI] - ↑ 9.0 9.1
Torres, R., Firestein, B.L., Dong, H., Staudinger, J., Olson, E.N., Huganir, R.L., ..., & Yancopoulos, G.D. (1998).
PDZ proteins bind, cluster, and synaptically colocalize with Eph receptors and their ephrin ligands. Neuron, 21(6), 1453-63. [PubMed:9883737] [WorldCat] [DOI] - ↑ 10.0 10.1 10.2
Brückner, K., Pablo Labrador, J., Scheiffele, P., Herb, A., Seeburg, P.H., & Klein, R. (1999).
EphrinB ligands recruit GRIP family PDZ adaptor proteins into raft membrane microdomains. Neuron, 22(3), 511-24. [PubMed:10197531] [WorldCat] [DOI] - ↑ 11.0 11.1
Wyszynski, M., Kim, E., Dunah, A.W., Passafaro, M., Valtschanoff, J.G., Serra-Pagès, C., ..., & Sheng, M. (2002).
Interaction between GRIP and liprin-alpha/SYD2 is required for AMPA receptor targeting. Neuron, 34(1), 39-52. [PubMed:11931740] [WorldCat] [DOI] - ↑
Feng, W., Fan, J.S., Jiang, M., Shi, Y.W., & Zhang, M. (2002).
PDZ7 of glutamate receptor interacting protein binds to its target via a novel hydrophobic surface area. The Journal of biological chemistry, 277(43), 41140-6. [PubMed:12196542] [WorldCat] [DOI] - ↑ 13.0 13.1
Stegmüller, J., Werner, H., Nave, K.A., & Trotter, J. (2003).
The proteoglycan NG2 is complexed with alpha-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid (AMPA) receptors by the PDZ glutamate receptor interaction protein (GRIP) in glial progenitor cells. Implications for glial-neuronal signaling. The Journal of biological chemistry, 278(6), 3590-8. [PubMed:12458226] [WorldCat] [DOI] - ↑
Sheng, M., & Sala, C. (2001).
PDZ domains and the organization of supramolecular complexes. Annual review of neuroscience, 24, 1-29. [PubMed:11283303] [WorldCat] [DOI] - ↑
Ye, B., Liao, D., Zhang, X., Zhang, P., Dong, H., & Huganir, R.L. (2000).
GRASP-1: a neuronal RasGEF associated with the AMPA receptor/GRIP complex. Neuron, 26(3), 603-17. [PubMed:10896157] [WorldCat] [DOI] - ↑
Bissen, D., Foss, F., & Acker-Palmer, A. (2019).
AMPA receptors and their minions: auxiliary proteins in AMPA receptor trafficking. Cellular and molecular life sciences : CMLS, 76(11), 2133-2169. [PubMed:30937469] [PMC] [WorldCat] [DOI] - ↑
Palenzuela, R., Gutiérrez, Y., Draffin, J.E., Lario, A., Benoist, M., & Esteban, J.A. (2017).
MAP1B Light Chain Modulates Synaptic Transmission via AMPA Receptor Intracellular Trapping. The Journal of neuroscience : the official journal of the Society for Neuroscience, 37(41), 9945-9963. [PubMed:28904092] [PMC] [WorldCat] [DOI] - ↑
Setou, M., Seog, D.H., Tanaka, Y., Kanai, Y., Takei, Y., Kawagishi, M., & Hirokawa, N. (2002).
Glutamate-receptor-interacting protein GRIP1 directly steers kinesin to dendrites. Nature, 417(6884), 83-7. [PubMed:11986669] [WorldCat] [DOI] - ↑
Geiger, J.C., Lipka, J., Segura, I., Hoyer, S., Schlager, M.A., Wulf, P.S., ..., & Acker-Palmer, A. (2014).
The GRIP1/14-3-3 pathway coordinates cargo trafficking and dendrite development. Developmental cell, 28(4), 381-93. [PubMed:24576423] [WorldCat] [DOI] - ↑
Essmann, C.L., Martinez, E., Geiger, J.C., Zimmer, M., Traut, M.H., Stein, V., ..., & Acker-Palmer, A. (2008).
Serine phosphorylation of ephrinB2 regulates trafficking of synaptic AMPA receptors. Nature neuroscience, 11(9), 1035-43. [PubMed:19160501] [WorldCat] [DOI] - ↑
Aoto, J., Ting, P., Maghsoodi, B., Xu, N., Henkemeyer, M., & Chen, L. (2007).
Postsynaptic ephrinB3 promotes shaft glutamatergic synapse formation. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(28), 7508-19. [PubMed:17626212] [PMC] [WorldCat] [DOI] - ↑
Chung, H.J., Xia, J., Scannevin, R.H., Zhang, X., & Huganir, R.L. (2000).
Phosphorylation of the AMPA receptor subunit GluR2 differentially regulates its interaction with PDZ domain-containing proteins. The Journal of neuroscience : the official journal of the Society for Neuroscience, 20(19), 7258-67. [PubMed:11007883] [PMC] [WorldCat] [DOI] - ↑
Perez, J.L., Khatri, L., Chang, C., Srivastava, S., Osten, P., & Ziff, E.B. (2001).
PICK1 targets activated protein kinase Calpha to AMPA receptor clusters in spines of hippocampal neurons and reduces surface levels of the AMPA-type glutamate receptor subunit 2. The Journal of neuroscience : the official journal of the Society for Neuroscience, 21(15), 5417-28. [PubMed:11466413] [PMC] [WorldCat] [DOI] - ↑
Lu, W., & Ziff, E.B. (2005).
PICK1 interacts with ABP/GRIP to regulate AMPA receptor trafficking. Neuron, 47(3), 407-21. [PubMed:16055064] [WorldCat] [DOI] - ↑
Steinberg, J.P., Takamiya, K., Shen, Y., Xia, J., Rubio, M.E., Yu, S., ..., & Huganir, R.L. (2006).
Targeted in vivo mutations of the AMPA receptor subunit GluR2 and its interacting protein PICK1 eliminate cerebellar long-term depression. Neuron, 49(6), 845-60. [PubMed:16543133] [WorldCat] [DOI] - ↑ 26.0 26.1
Takamiya, K., Mao, L., Huganir, R.L., & Linden, D.J. (2008).
The glutamate receptor-interacting protein family of GluR2-binding proteins is required for long-term synaptic depression expression in cerebellar Purkinje cells. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(22), 5752-5. [PubMed:18509036] [PMC] [WorldCat] [DOI] - ↑ 27.0 27.1
Mao, L., Takamiya, K., Thomas, G., Lin, D.T., & Huganir, R.L. (2010).
GRIP1 and 2 regulate activity-dependent AMPA receptor recycling via exocyst complex interactions. Proceedings of the National Academy of Sciences of the United States of America, 107(44), 19038-43. [PubMed:20956289] [PMC] [WorldCat] [DOI] - ↑
Tan, H.L., Chiu, S.L., Zhu, Q., & Huganir, R.L. (2020).
GRIP1 regulates synaptic plasticity and learning and memory. Proceedings of the National Academy of Sciences of the United States of America, 117(40), 25085-25091. [PubMed:32948689] [PMC] [WorldCat] [DOI] - ↑
Mejias, R., Adamczyk, A., Anggono, V., Niranjan, T., Thomas, G.M., Sharma, K., ..., & Wang, T. (2011).
Gain-of-function glutamate receptor interacting protein 1 variants alter GluA2 recycling and surface distribution in patients with autism. Proceedings of the National Academy of Sciences of the United States of America, 108(12), 4920-5. [PubMed:21383172] [PMC] [WorldCat] [DOI]