ヒストン
英語名:Histone 独:Histon 仏:Histone
真核生物のクロマチン(染色質)の基本単位であるヌクレオソーム(nucleosome)を構成する塩基性タンパク質。DNA を核内に収納する役割を担う。通常の細胞を構成しているタンパク質中でヒストンは最も多量に存在しているタンパク質であり、ヌクレオソームはほぼ等量のDNA(200bp(130kDa))とヒストンタンパク質(132kDa)により構成されている。ヒストンとDNAの相互作用は遺伝子発現の最初の段階である転写に大きな影響を及ぼす[1]。
分類
ヒストンはH1、H2A、H2B、H3、H4の5種類に分類される。このうちH2A、H2B、H3、H4の4種は、コアヒストンと呼ばれ、それぞれ二分子ずつが集合し、ヒストン八量体を形成する。一つのヒストン八量体には、146 bp の DNA が左巻きに約1.65回巻き付いている[2]。この構造がクロマチン構造の最小単位であるヌクレオソームである。H1 はリンカーヒストンと呼ばれ、ヌクレオソーム間の DNA に結合する。コアヒストンは比較的小さく11~15kDa、H1ヒストンはやや大きく約21kDaであり、ヌクレオソーム内ではそれぞれのコアヒストンが二分子ずつ存在するのに対して、H1ヒストンは一分子含まれる [3]。ヒストンは正の電荷をもつアミノ酸の含有量が高く、各ヒストンのアミノ酸残基の少なくとも20%がリジンまたはアルギニンであるため、負の電荷をもったDNA分子に強く結合する。ヒストンの塩基性アミノ酸含量またはリジン/アルギニン比に従い、H1は高リジン型ヒストン、H2A、H2Bはリジン型ヒストン、H3、H4はアルギニン型ヒストンと呼ばれている[4]。
構造

ヌクレアソームはヒストン八量体に146 bp の DNA が左巻きに約1.65回巻き付いた構造である。ヒストン八量体はコアヒストンであるH2A、H2B、H3、H4から形成され、H3-H4四量体がDNAに結合し、そこに2個のH2A・H2Bが結合することによってヌクレオソームが完成する。
ヌクレオソームを構成するヒストンにはどのコアヒストンにも保存されている領域が存在し、ヒストン型折りたたみドメイン(histone-fold domain)と呼ばれる。この領域はヒストンの中間体の集合に関与し、間に短いループを2つ(L1、L2)もつ3つのαヘリックス(α1、α2、α3)で構成されている。この領域を介して特定の組み合わせのヒストンが結合する。H3とH4はまずヘテロ二量体を形成し、この二量体同士が結合し、H3、H4各2分子からなる四量体(H3・H4)を形成する。H2A、H2Bは溶液中でヘテロ二量体は形成するが、四量体は形成しない。その後、H3-H4四量体がDNAに結合し、そこに2個のH2A・H2Bが結合することによってヌクレオソームが完成する(図1) 。コアヒストンとヌクレオソームの分子構成 ヌクレアソームはヒストン八量体に146 bp の DNA が左巻きに約1.65回巻き付いた構造である。ヒストン八量体はコアヒストンであるH2A、H2B、H3、H4から形成され、H3-H4四量体がDNAに結合し、そこに2個のH2A・H2Bが結合することによってヌクレオソームが完成する。]]ヌクレオソームヒストンの構造は球形のカルボキシル末端部分と、直鎖状のアミノ末端部分(ヒストンテール)からなる[2][5][6]。 ヒストンテールのセリン、リジン、アルギニン残基などはリン酸化、アセチル化、メチル化、ユビキチン化といった化学修飾を受けることが知られている。これらの化学修飾は、遺伝子発現等、数々のクロマチン機能の制御に関わっている(機能の項参照)。ヒストンは多くの翻訳後修飾可能な残基を持っており、複数の修飾の組み合わせがそれぞれ特異的な機能を引き出すという仮説は、ヒストンコード仮説と呼ばれている[7][8]。
機能
DNA鎖の核内への収納
真核生物のクロマチンの基本単位であるヌクレオソームを構成するヒストンは円柱形で、146bpのDNAがその表面に1.65回巻き付けられている[2]。ヒストンは真核生物の大きなゲノムを細胞核にはめ込むのに必要な圧縮を可能にし、DNA鎖の核内への収納に関与している。最終的に約2mのDNAは10μm程度の核内に収納される。
クロマチンの制御
ヒストンのアミノ末端部分は、さまざまな修飾を受けることによりクロマチンの機能を制御している。遺伝子の発現もそのうちのひとつで、このようにゲノムの塩基配列の変化を起こさずに遺伝子の機能を調節する仕組みをエピジェネティクスという。ヒストン修飾は遺伝子発現制御にとどまらずDNA修復や染色体凝縮(有糸分裂)、精子形成(減数分裂)などの多様な生物学的プロセスに関与していることが知られている[9]が、ここでは転写を調節するヒストン修飾の例を以下に示す。
ヒストンの修飾(表1、表2、図2)
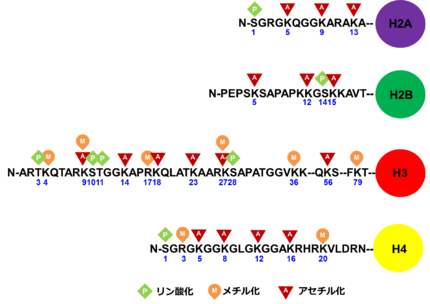
それぞれのヒストンコアタンパク質におけるヒストンテールの修飾のうち代表的なものを示した。左端がN末端を示す。ヒストンテールは多様な修飾を受け、その影響は修飾の種類や部位によって決まる(表1)。ヒストン修飾は遺伝子の発現制御などに重要な役割を果たしている。
ヒストンのアセチル化
ヒストンのアセチル化は細胞内のヒストンアセチル基転移酵素(Histone Acetyl Transferase:HAT)により行われる。HATはヒストン中の特定のリジン残基のアミノ基(-NH2(-NH3+))をアミド(-NHCOCH3)に変換することにより電荷を中和し、ヒストン-DNA間の結合を部分的に弱める。これにより、ヌクレオソーム同士をつないでいるDNA鎖(リンカーDNA)に対して転写因子やRNAポリメラーゼがより結合しやすい状態になり、結果として転写が活性化される。ヒストンの脱アセチル化では、このアセチル基が加水分解により除去され、元のアミノ基に戻ることによりヒストンへのDNAの巻きつきが強められ転写が抑制される。ヒストンの脱アセチル化はヒストン脱アセチル化酵素(Histone Deacetylase:HDAC)によって行われる。
ヒストンのメチル化
ヒストンのメチル化は主にリジン残基に見られ、ヒストンH3ではK4、K9、K27、K36、K79が、ヒストンH4ではK20がメチル化されることが知られている。これらのメチル化の数は1~3つ(mono~tri)存在し、またそれぞれリン酸化される残基の位置によって転写の活性化に関与するものと抑制に関与するものが存在する。一般的にH3K4、K36、K79は転写活性化に関与し、H3K9、K27、H4K20は転写抑制に関与している。またリジン残基だけでなくアルギニン残基もメチル化され、転写制御に関わることが報告されている[10][11]。
| ヒストン | サイト | 修飾 | 機能 |
| H2A | S1 | リン酸化 | 有糸分裂、転写抑制 |
| K5 | アセチル化 | 転写活性化 | |
| K9 | アセチル化 | 転写活性化 | |
| K13 | アセチル化 | 転写活性化 | |
| H2B | K5 | アセチル化 | 転写活性化 |
| K12 | アセチル化 | 転写活性化 | |
| S14 | リン酸化 | アポトーシス | |
| K15 | アセチル化 | 転写活性化 | |
| H3 | T3 | リン酸化 | 減数分裂 |
| K4 | アセチル化 | 転写活性化 | |
| メチル化 | ユークロマチン形成 | ||
| K9 | アセチル化 | 転写活性化 | |
| メチル化 | 転写抑制 | ||
| S10 | リン酸化 | 転写活性化 | |
| T11 | リン酸化 | 有糸分裂 | |
| K14 | アセチル化 | 転写活性化(伸長) | |
| R17 | メチル化 | 転写活性化 | |
| K18 | アセチル化 | 転写活性化、DNA修復 | |
| K23 | アセチル化 | 転写活性化、DNA修復 | |
| K27 | アセチル化 | 転写サイレンシング | |
| メチル化 | 転写サイレンシング | ||
| S28 | リン酸化 | 有糸分裂 | |
| K36 | メチル化 | 転写伸長 | |
| K56 | アセチル化 | DNA修復 | |
| K79 | メチル化 | 転写伸長 | |
| H4 | S1 | リン酸化 | 有糸分裂 |
| R3 | メチル化 | 転写活性化 | |
| K5 | アセチル化 | ヒストンのDNAへの結合 | |
| K8 | アセチル化 | ヒストンのDNAへの結合、 テロメアサイレンシング | |
| K12 | アセチル化 | 転写活性化、DNA修復 | |
| K16 | アセチル化 | 転写サイレンシング | |
| K20 | メチル化 | 転写活性化 |
| ヒストン修飾 | ヒストン修飾酵素 |
| アセチル化 | CBP /p300、PCAF、GCN5、 TIP60、SAGA、NuA3、NuA4 |
| 脱アセチル化 | HDAC、SIRT、NuRD、SIR2複合体、 Rpd3大、Rpd3小 |
| メチル化 | SUV39H1、G9a、Ezh2、SET1、 SET2、SET7/9、MLL、DOT1、 CARM1、PRMT |
| 脱メチル化 | LSD1、KDM2、KDM4 |
| リン酸化 | Aurora Kinase、MSK1 |
| ユビキチン化 | RING2、RING1B |
| SUMO化 | UBC9 |
神経系細胞分化におけるヒストンの修飾の役割
哺乳類の中枢神経系は、発生段階において共通の神経幹細胞から分化・産生されるニューロン、アストロサイト、オリゴデンドロサイトによって構成され、互いに精妙に相互作用することで高度な神経活動が維持されている[13]。
アセチル化
前述のように、ヒストンのアセチル化と脱アセチル化は、それぞれHAT及びHDACにより行われている。代表的なHATとしてCBP(CREB binding protein)やp300が知られている(表2)。p300の欠損マウスやヘテロ欠損マウス、p300とCBP両方のヘテロ欠損マウスでは細胞の増殖や神経管形成、心臓の発達が起こらずに胎生致死となる[14]。また、CBPは神経系遺伝子のプローター領域のヒストンのアセチル化増進を介して神経発生を制御していることが報告されており、CBPのヘテロ欠損マウスでは胎生期の神経発生異常に起因すると考えられるルビンシュタイン・テイビ症候群を引き起こすことが知られている[15]。神経幹細胞からニューロンへの分化においてはNRSF(neuron restrictive silencing factor, 別名 repressor for element-1 silencing transcription factor(REST))と呼ばれる転写因子がニューロン特異的遺伝子の発現を制御していることが知られている。NRSFはニューロン特異的遺伝子のプロモーター上のNRSE(neuron restrictive silencing element)と呼ばれる配列に特異的に結合し、そこでHDACやメチル化DNA結合タンパク質であるMeCP2(methyl CpG binding protein 2)、CoREST(co-repressor for REST)とよばれるコリプレッサーの複合体を形成することにより、ニューロン特異的遺伝子の発現を負に制御している[16]。ヒストンのアセチル化は神経幹細胞からオリゴデンドロサイトの分化にも関与し、その分化はHDACにより大きく影響を受ける。HDACは転写因子YY1(Yin Yang1)と強調してオリゴデンドロサイトの発現を抑制する転写調節因子Id4(inhibition of differentiation 4)およびTCF(T-cell factor)を抑制することでオリゴデンドロサイトへの分化を促進させることが報告されている[17]。さらにHDACはWntの下流のβ-カテニンと拮抗的にTCFと結合し、オリゴデンドロサイト分化を抑制するId2(inhibition of differentiation 2)やId4の発現を阻害することによってもオリゴデンドロサイトの分化を促進させている[18]。
その他にも、成体ラット海馬由来の神経幹細胞に、HDAC阻害剤としての活性を有し、抗てんかん薬として知られるバルプロ酸を作用させると、アストロサイト、オリゴデンドロサイトへの分化が抑制され、ニューロンへの分化が促進することが報告されている[19]。このニューロン分化促進は、HDACによりその発現が抑制されているニューロン分化を促進する転写因子NeuroD(neurogenic differentiation)の発現抑制がHDAC阻害剤であるバルプロ酸により解除されることに起因すると考えられている[19]。最近では、このようなHDAC阻害剤によるニューロン分化促進作用を利用した脊髄損傷の治療への応用的研究や、HDAC阻害剤を中枢神経系の疾患(ルビンシュタイン・テイビ症候群、レット症候群、フリードリッヒ運動失調症、ハンチントン病、多発性硬化症 など)の治療に利用しようとした試みもなされている[20] [21]。
メチル化
中枢神経系の発生過程において、神経幹細胞は胎生中期にはニューロンへのみ分化し、胎生後期以降にはアストロサイトへの分化能を獲得し、優位にアストロサイトへと分化することが知られている[22]。この神経幹細胞の発生段階依存的なアストロサイトへの分化能獲得には、DNAのメチル化やヒストンのメチル化などのエピジェネティックなクロマチン修飾が関与することが報告されている[23][24]。
神経幹細胞からアストロサイト特異的タンパク質glial fibrillary acidic protein(GFAP)を発現するアストロサイトへの分化は、アストロサイト分化誘導性サイトカインである(ciliary neurotrophic factor:CNTF)や白血病抑制因子(leukemia inhibitory factor:LIF)などのIL-6 ファミリーサイトカインが重要な役割を果たしており、これらの下流の転写因子であるSTAT3(single transducer and activator of transcription 3)がGFAPのプロモーターに結合することにより誘導される[26]。これらCNTFやLIFによるアストロサイト分化誘導は線維芽細胞増殖因子2(fibroblast growth factor 2:FGF2)により促進されることが知られている。このFGF2によるアストロサイト分化促進はヒストンのメチル化に起因し、GFAPのプロモーター領域のSTAT3結合領域の近傍でH3K9の脱メチル化かつH3K4のメチル化が誘導されることでクロマチン構造が緩み、CNTFにより活性化されたSTAT3がGFAPのプロモーター領域に結合しやすくなるためであると考えられている[24]。上述したように、神経幹細胞は胎生中期でニューロンに分化する性質を獲得し、発生段階が進むにつれ、アストロサイトに分化するように性質が変化する。この神経幹細胞の発生段階依存的であるニューロン分化期からアストロサイトへの分化期の転換にヒストンのメチル化が関与することが報告されており、これはポリコーム群(PcG)やトリソラックス群(TrxG)と呼ばれるヒストンのメチル化酵素を含んだタンパク質複合体を介して行われている。PcGは主に遺伝子の抑制に関わるヒストン修飾、TrxGは遺伝子の活性化に関わるヒストンの修飾に関わっており、互いに拮抗することで遺伝子の発現を制御している。これらPcG、TrxGによる遺伝子の発現制御は神経幹細胞を含む多種の幹細胞の維持と分化調節の共通メカニズムのひとつであると考えられている[25]。
胎生中期の神経幹細胞では、Wnt-β-カテニン経路の活性化によりニューロン分化を促進するNeurogenin1(Neurog1)の発現が誘導されることによりニューロン分化が促進されることが報告されている。アストロサイト分化が優位に起こる胎生後期神経幹細胞においてもWntの作用は受けているが、この時にはNeurog1の発現は誘導されず、ニューロン分化も起こらない。この胎生中期と胎生後期でのWntに対する応答性の違いは、PcGの異なる二つの複合体であるPRC1(polycomb repressor complex1)、PRC2により行われるヒストンのメチル化修飾に起因している[26]。具体的には、発生段階依存的にNeurog1のプロモーター領域でPRC2の必須構成因子でありH3K27 のメチル化酵素であるEzh2(enhancer of homolog 2)によるH3K27のトリメチル化修飾が亢進され、さらにPRC1の構成因子であるRing1BがH3K27me3を認識して結合することによってNeurog1の発現が抑制されることが明らかになっている[26]。Neurog1はアストロサイトの分化を抑制していることが知られているため、Neurog1の抑制によってアストロサイトの分化は誘導される。このように、ヒストンのメチル化修飾は神経幹細胞のニューロンへの分化の抑制、アストサイトへの分化能の獲得に重要な役割を果たしている。
また、ヒストンのメチル化やメチル化酵素、脱メチル化酵素の働きが脳機能や多くの精神疾患に関与していることが報告されている[27][28]。H3K4のメチル化酵素であるMLL1(mixed-lineage leukemia 1)の変異マウスでは海馬の可塑性やシグナルの異常に伴い、学習能力と記憶形成能の低下がみられることが報告されている[29][30]。MLLによるH3K4のメチル化の調節は精神疾患の治療に潜在的な役割を果たすことが示唆されている。非定型抗精神病薬クロザピンは統合失調症の治療に使われ、ヒトの前頭前野においてGABA合成酵素遺伝子のGad1/GAD1プロモーター領域でH3K4のトリメチル化を増加させる。MLL1のヘテロマウスでは脳のGad1でのH3K4のメチル化は減少し[31]、統合失調症患者の脳においてもMLL1の発現量が減少していることが知られている。これらのことから、統合失調症などの精神疾患において、MLL1は新たな治療のターゲットとなりうると考えられている。
H3K9のメチル化酵素であるG9a も神経系において重要な役割を果たしていることが報告されている。GLP(G9a-like protein)/G9aの複合体は成熟ニューロンにおいて非神経性遺伝子やニューロン前駆遺伝子の働きを抑制しており、この複合体の欠損は、学習や意欲、環境への適応などの脳の高次機能に影響を与えることが報告されている[32]。その他にも、コカインは中毒性の薬物であり脳内の遺伝子の発現を変化させ、マウスの行動やニューロンの形態に影響を与えることが知られている。このコカインに対する中毒状態のマウスにおいてG9aが抑制されることにより、グローバルなH3K9のメチル化が抑制されることが報告されている。G9aの発現低下は脳の側坐核ニューロンの樹状突起スパイン密度を増加させており、これがコカインの嗜好性を増強させている。G9aはコカインに対する嗜好性を低下させ、コカイン中毒を抑制するという点で重要な役割を果たすことが明らかとなっているため、G9aの抑制の解除はコカインへの渇望を抑制するための効果的治療法となりうると考えられている[33]。
H3K27のメチル化は、うつ様行動の発生に関与することが知られている。マウスに社会的ストレスを繰り返し与えることによりヒトのうつ患者と同様な行動や神経化学的変化を引き起こす。うつモデルマウスでは海馬の脳由来神経栄養因子遺伝子(brain-derived neurotrophic factor:BDNF)プロモーターでのH3K27のメチル化が増加しており、これはうつモデルマウスがストレスのない環境へ移されたとしても持続することが知られている。抗うつ薬であるイミプラミンを投与すると、うつ様行動の解消に加え、BDNFプロモーターのH3K27のメチル化状態がH3K4のメチル化状態やH3のアセチル化に置換される。このクロマチン状態の変化はイミプラミン投与の副産物やうつ様行動が解消された結果生じるものではなく、イミプラミンによるうつ症状改善のメカニズムのひとつであると考えられている[34]。そのため、うつ病治療においてもヒストンのメチル化制御は重要な要因のひとつであるといえる。
ここに示した例以外にも多くのヒストンメチル化状態やメチル化酵素、脱メチル化酵素が脳機能や精神疾患に関わることが報告されている[27][28]。
これらから、メチル化やアセチル化などのヒストン修飾は脳の発達や機能にさまざまな役割を果たしており、脳において重要な機構であるといえる。
- ↑ 八杉龍一、小関治男、古谷雅樹、日高敏隆
岩波生物学辞典 第4版
岩波書店:1996 - ↑ 2.0 2.1 2.2 2.3 2.4
Luger, K., Mäder, A.W., Richmond, R.K., Sargent, D.F., & Richmond, T.J. (1997).
Crystal structure of the nucleosome core particle at 2.8 A resolution. Nature, 389(6648), 251-60. [PubMed:9305837] [WorldCat] [DOI] - ↑ 大場義樹
クロマチン
東京大学出版会:1986 - ↑ James D. Watson, T. A. Baker, S. P. Bell、訳 中村桂子監fckLR
ワトソン 遺伝子の分子生物学【第5版】
東京電機大学出版局:2006 - ↑
Arents, G., & Moudrianakis, E.N. (1995).
The histone fold: a ubiquitous architectural motif utilized in DNA compaction and protein dimerization. Proceedings of the National Academy of Sciences of the United States of America, 92(24), 11170-4. [PubMed:7479959] [PMC] [WorldCat] [DOI] - ↑
Zlatanova, J., Bishop, T.C., Victor, J.M., Jackson, V., & van Holde, K. (2009).
The nucleosome family: dynamic and growing. Structure (London, England : 1993), 17(2), 160-71. [PubMed:19217387] [WorldCat] [DOI] - ↑
Strahl, B.D., & Allis, C.D. (2000).
The language of covalent histone modifications. Nature, 403(6765), 41-5. [PubMed:10638745] [WorldCat] [DOI] - ↑
Jenuwein, T., & Allis, C.D. (2001).
Translating the histone code. Science (New York, N.Y.), 293(5532), 1074-80. [PubMed:11498575] [WorldCat] [DOI] - ↑
Song, N., Liu, J., An, S., Nishino, T., Hishikawa, Y., & Koji, T. (2011).
Immunohistochemical Analysis of Histone H3 Modifications in Germ Cells during Mouse Spermatogenesis. Acta histochemica et cytochemica, 44(4), 183-90. [PubMed:21927517] [PMC] [WorldCat] [DOI] - ↑
Fabbrizio, E., El Messaoudi, S., Polanowska, J., Paul, C., Cook, J.R., Lee, J.H., ..., & Sardet, C. (2002).
Negative regulation of transcription by the type II arginine methyltransferase PRMT5. EMBO reports, 3(7), 641-5. [PubMed:12101096] [PMC] [WorldCat] [DOI] - ↑
Bauer, U.M., Daujat, S., Nielsen, S.J., Nightingale, K., & Kouzarides, T. (2002).
Methylation at arginine 17 of histone H3 is linked to gene activation. EMBO reports, 3(1), 39-44. [PubMed:11751582] [PMC] [WorldCat] [DOI] - ↑
Inche, A.G., & La Thangue, N.B. (2006).
Chromatin control and cancer-drug discovery: realizing the promise. Drug discovery today, 11(3-4), 97-109. [PubMed:16533707] [WorldCat] [DOI]
(執筆者:村尾直哉、中島欽一 担当編集委員:村上富士夫)