「有髄線維」の版間の差分
細 (→脱髄性疾患) |
細 (→脱髄性疾患) |
||
| 232行目: | 232行目: | ||
中枢性脱髄疾患の中では[[多発性硬化症]](multiple sclerosis, MS)が最も多くみられる。日本での有病率は2006年では10万人あたり8 - 9人程度と推定されている。若年成人での神経障害の主な原因である。約80-90%のMS患者が二十代後半で再発-[[寛解]]型になり、寛解期には共通して、ある一定程度神経障害が一過的に回復する。発病から数年後、多くの患者が実質上機能回復はなくなり第二ステージに移り、病状は進行型になる。そして、あとの残り10-20%の患者は初めから寛解を経験することのない進行型である<ref name=ref10><pubmed>22189514</pubmed></ref>。[[カルシウムチャネル]]ブロッカーである[[Fampridine]](Fampyra)はMS治療において初めて機能回復に成功した経口投与薬であるが、転倒する、背中が痛む、[[めまい]]がする、[[不眠]]、[[疲労感]]、[[悪心]]、[[平衡障害]]などの副作用を伴うことが知られている<ref><pubmed>7354839</pubmed></ref> <ref><pubmed>6631441</pubmed></ref> <ref><pubmed>3001584</pubmed></ref> <ref><pubmed>2435223</pubmed></ref>。[[wikipedia:ja:インターフェロン|インターフェロン]]β(Interferon β)と[[wikipedia:ja:グラチマラー酢酸塩|グラチマラー酢酸塩]](glatiramer acetate)が現在もっともよく用いられている。これらの薬剤は根本治療法であるが、おもに再発-寛解型の患者に用いられている<ref name=ref10 />。 | 中枢性脱髄疾患の中では[[多発性硬化症]](multiple sclerosis, MS)が最も多くみられる。日本での有病率は2006年では10万人あたり8 - 9人程度と推定されている。若年成人での神経障害の主な原因である。約80-90%のMS患者が二十代後半で再発-[[寛解]]型になり、寛解期には共通して、ある一定程度神経障害が一過的に回復する。発病から数年後、多くの患者が実質上機能回復はなくなり第二ステージに移り、病状は進行型になる。そして、あとの残り10-20%の患者は初めから寛解を経験することのない進行型である<ref name=ref10><pubmed>22189514</pubmed></ref>。[[カルシウムチャネル]]ブロッカーである[[Fampridine]](Fampyra)はMS治療において初めて機能回復に成功した経口投与薬であるが、転倒する、背中が痛む、[[めまい]]がする、[[不眠]]、[[疲労感]]、[[悪心]]、[[平衡障害]]などの副作用を伴うことが知られている<ref><pubmed>7354839</pubmed></ref> <ref><pubmed>6631441</pubmed></ref> <ref><pubmed>3001584</pubmed></ref> <ref><pubmed>2435223</pubmed></ref>。[[wikipedia:ja:インターフェロン|インターフェロン]]β(Interferon β)と[[wikipedia:ja:グラチマラー酢酸塩|グラチマラー酢酸塩]](glatiramer acetate)が現在もっともよく用いられている。これらの薬剤は根本治療法であるが、おもに再発-寛解型の患者に用いられている<ref name=ref10 />。 | ||
また、末梢神経系では[[ギラン・バレー症候群]]([[Guillain-Barré syndrome]])や[[ | また、末梢神経系では[[ギラン・バレー症候群]]([[Guillain-Barré syndrome]])や[[慢性炎症脱髄性多発神経炎]]([[chronic inflammatory demyelinating polyneuropathy]]; [[CIDP]])、などがある。また、最近の研究により[[統合失調症]]との関連が示唆されている<ref><pubmed>18538868</pubmed></ref> <ref><pubmed>20216548</pubmed></ref> <ref><pubmed>21196354</pubmed></ref>。髄鞘形成が不完全な[[髄鞘形成不全疾患]](dysmyelinating disease)とは区別される。 | ||
2021年6月17日 (木) 12:13時点における版
清水 崇弘
University College London (Wolfson Institute for Biomedical Research)
池中 一裕
自然科学研究機構 生理学研究所 分子生理研究系・分子神経生理
DOI:10.14931/bsd.816 原稿受付日:2012年8月29日 原稿完成日:2012年11月20日 原稿更新日:2013年8月21日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
英語名: myelinated nerve, medullated nerve 独:myelinisierte Nervenfaser 仏:fibres myélinisées
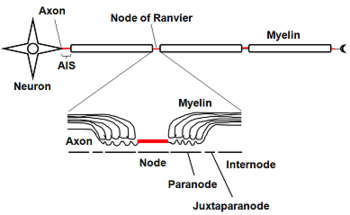
髄鞘(ミエリン)を有する軸索のことを有髄線維あるいは有髄神経線維という。髄鞘は中枢神経系では稀突起膠細胞(あるいはオリゴデンドロサイト[oligodendrocyte])、末梢神経系ではシュワン細胞(Schwann cell)というグリア細胞が形成する。軸索は樹状突起と比べると細く平滑な細胞突起である。ミエリン鞘は等間隔にあるランヴィエ絞輪(node of Ranvier)によって区切られており、軸索中の電位依存性ナトリウムチャネルはランヴィエ絞輪に集積している。
髄鞘はリン脂質に富んだタンパク質で層構造を形成しているため、非常に良い絶縁体の役割を果たす。さらに、活動電位を発生させる電位依存性ナトリウムチャネルがランヴィエ絞輪に集積しているために、活動電位を軸索に沿って跳躍伝導させることができる。また、単に絶縁体としての働きだけではなく、軸索との間に物質交換を行うことによって神経軸索の栄養・保護などさまざまな神経機能を調節している。主要構成タンパク質はミエリン塩基性タンパク質(myelin basic protein; MBP)、ミエリンプロテオリピドプロテイン(myelin proteolipid protein; PLP)であり、その他にミエリン関連糖タンパク質(myelin associated glycoprotein; MAG)、ミエリンオリゴデンドロサイト糖タンパク質(myelin oligodendrocyte glycoprotein; MOG)、2',3'-環状ヌクレオチドホスホジエステラーゼ(2',3'-cyclic-nucleotide phosphodiesterase; CNPase)などを含む。
神経の分類と髄鞘の有無
末梢神経の神経線維は伝導速度によって大きくA,B,C線維と分類される。A線維はさらに速度の速い順にalpha,beta,gamma, deltaと分類される。例えばAalphaは固有知覚を求心性に伝えるとともに体性運動を遠心性に伝える。一方、感覚神経では太さに応じてI,II,III,IV線維と分類される。筋からの求心線維には慣用的にI-IVの分類が主に用いられ、皮膚からの求心線維にはA-Cの分類が用いられる。また、この伝導速度は髄鞘の有無や神経線維の直径の大小の組み合わせで規定される。同じ直径の有髄線維と無髄線維では有髄線維が、同じ種類の線維間では神経線維の直径の大きい方が伝導速度が速い。前者は跳躍伝導により、後者の電気緊張電位の広がりを利用した伝導よりも速い伝導速度を得ている。一般に骨格筋運動と付随する固有感覚、部位のはっきりした皮膚感覚は伝導速度の速い線維を、交感神経活動や鈍痛などは伝導速度の遅い線維を利用して伝えられる。
| 筋からの求心性感覚神経線維(太さから分類) | 線維直径(μm) | 皮膚からの求心性感覚神経線維(速度から分類) | 伝導速度(m/s) | |
| 有髄神経 | I | 12-20 | Aα | 72-120 |
| II | 6-12 | Aβ | 36-72 | |
| III | 1-6 | Aδ | 4-36 | |
| - | ≦3 | B(注1) | 3-15 | |
| 無髄神経 | IV | 0.2-1.5 | C | 0.4-2.0 |
(注1)B繊維は一般的に自律神経系前繊維を指す。
| 受容器の種類 | 伝達速度からの分類 | 太さあるいは機能からの名称 | 様式 |
| 皮膚と皮下の機械受容器 | 触覚 | ||
| マイスナー小体 | Aα、β | RA1 (注2) | なでる、粗動 |
| メルケル細胞 | Aα、β | SA1 (注3) | 圧力、触感 |
| パチニ小体 | Aα、β | RA2 (注2) | 振動 |
| ルフィニ終末 | Aα、β | SA2 (注3) | 皮膚の伸縮 |
| Hair-tylotrich, hair-guard | Aα、β | G1、G2 | なでる、粗動 |
| Hair-down | Aδ | D | 軽くなでる |
| Field | Aα、β | F | 皮膚の伸縮 |
| C機械受容器 | C | なでる、erotic touch | |
| 温度受容器 | 温度 | ||
| 冷覚受容器 | Aδ | III | 皮膚冷感(<25℃[77℉]) |
| 温覚受容器 | C | IV | 皮膚温感(>35℃[95℉]) |
| 高熱侵害受容器 | Aδ | III | 高温(>45℃[113℉]) |
| 寒冷侵害受容器 | C | IV | 低温(<5℃[41℉]) |
| 侵害受容器 | 痛み | ||
| 機械的 | Aδ | III | 鋭く穿刺するような痛み |
| 温度機械的(熱) | Aδ | III | 焼けるような痛み |
| 温度機械的(寒冷) | C | IV | 凍てつく痛み |
| 多様式的 | C | IV | 鈍い焼けるような痛み |
| 筋・骨格の機械受容器 | 四肢の固有受容性感覚 | ||
| 筋紡錘(第一) | Aα | Ia | 筋肉の長さとスピード |
| 筋紡錘(第二) | Aβ | II | 筋肉の伸展 |
| ゴルジ腱器官 | Aα | Ib | 筋肉の収縮 |
| 間接嚢受容器 | Aβ | II | 筋肉の角度 |
| 伸縮感応性自由終末 | Aδ | III | 過剰な伸展あるいは力 |
(注2)Rapidly adapting type 1 あるいは 2
(注3)Slowly adapting type1 あるいは 2
有髄線維の構造
髄鞘は細胞形質膜の多層構造体であるため、細胞形質膜や細胞内小胞膜などの他の多くの細胞と比べてタンパク質成分が少なく、脂質が約8割程度を占め、残りがタンパク質である。髄鞘を構成する主な脂質は糖脂質ガラクトセレブロシド(Galactocerebroside)とその硫酸化誘導体スルファチド(Sulfatide)である[2]。神経軸索の髄鞘と髄鞘の隙間は特別な名称がつけられており、非常に特異な構造をしている。ノード(node)に電位作動型ナトリウムチャネルNav1.2やNav1.6、アンキリンG(Ankyrin G)などが、パラノード(paranode)にはCasprなど、ジャクスタパラノード(jaxtaparanode)にはKv1.2などのカリウムチャネルなどが分布する[3]。発達とともにこれらのチャネルやそのアイソフォームの分布が変化する[4]。また、病態時にもチャネルの分布は変化する[5] [6]。
中枢神経系(オリゴデンドロサイト)と末梢神経系(シュワン細胞)で髄鞘の巻き方が異なる。オリゴデンドロサイトは離れた複数の軸索個々に髄鞘を形成するのに対し、シュワン細胞はいくつかの軸索を抱え込むようにして包んだ後、1本の軸索を選別して、その周りに髄鞘を形成する[7]。髄鞘を構成するタンパク質も異なる。中枢神経系では髄鞘の主要構成タンパク質はPLP,MBPである。一方、末梢神経系ではP0(ピーゼロ)とP2が主要構成タンパク質である。その他のタンパク質は中枢神経系ではCNPase、MOG、MAGなどがあり、末梢神経系ではPMP22、MAG、MOGなどが発現している。
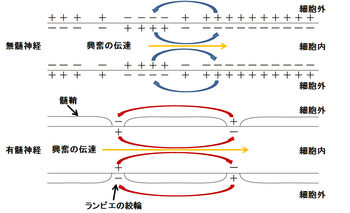
跳躍伝導
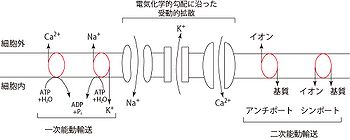
それぞれのイオンが受動的に流失し、電気化学的平衡が失われた場合、それを補償する能動的輸送が必要となる。この能動的輸送にはエネルギーが必要とされる。一般的には一次と二次能動輸送という二種類の重要な能動輸送がある(図2)。 神経軸索の起始部で髄鞘に覆われていない部分は初節(axon initial segment; AISと略される)とよばれ、電位依存性ナトリウムチャネルが高密度に集積しており、通常活動電位が最初に発火する[9]。AISで発現するチャネルは発達に伴い、あるいは病態時にその発現や分布が変化する[10]。AIS以降の軸索では、ほぼ等間隔にランヴィエ絞輪が現れる。AISやランヴィエ絞輪で発生した活動電位は、受動的伝播(電気緊張電位)によって次のランヴィエ絞輪に伝わる。髄鞘の絶縁性が高いために電位変化の減衰度合いは小さく押さえられる。そのため無髄軸索よりも離れた距離でも臨界脱分極を越える。またランヴィエ絞輪では電位依存性ナトリウムチャネルが集積しているため、活動電位が発生しやすい。この2つの効果によって跳躍伝導(saltatory conduction)が起こる。跳躍伝導は、活動電位の伝導速度を速く保つとともに、活動電位発生がランヴィエ絞輪に限局されるために、代謝エネルギーの節約にもなる。
脱髄性疾患
正常な発生における髄鞘形成がなされたのち、神経軸索から髄鞘が脱落することを脱髄という[11]。脱髄性疾患(demyelinating disease)では、髄鞘の消失により神経伝導速度が遅くなり、さまざまな神経症状が引き起こされる。脱髄が起こる場所により症状はさまざまである。運動麻痺、感覚麻痺、視力障害などが起こる。
中枢性脱髄疾患の中では多発性硬化症(multiple sclerosis, MS)が最も多くみられる。日本での有病率は2006年では10万人あたり8 - 9人程度と推定されている。若年成人での神経障害の主な原因である。約80-90%のMS患者が二十代後半で再発-寛解型になり、寛解期には共通して、ある一定程度神経障害が一過的に回復する。発病から数年後、多くの患者が実質上機能回復はなくなり第二ステージに移り、病状は進行型になる。そして、あとの残り10-20%の患者は初めから寛解を経験することのない進行型である[12]。カルシウムチャネルブロッカーであるFampridine(Fampyra)はMS治療において初めて機能回復に成功した経口投与薬であるが、転倒する、背中が痛む、めまいがする、不眠、疲労感、悪心、平衡障害などの副作用を伴うことが知られている[13] [14] [15] [16]。インターフェロンβ(Interferon β)とグラチマラー酢酸塩(glatiramer acetate)が現在もっともよく用いられている。これらの薬剤は根本治療法であるが、おもに再発-寛解型の患者に用いられている[12]。
また、末梢神経系ではギラン・バレー症候群(Guillain-Barré syndrome)や慢性炎症脱髄性多発神経炎(chronic inflammatory demyelinating polyneuropathy; CIDP)、などがある。また、最近の研究により統合失調症との関連が示唆されている[17] [18] [19]。髄鞘形成が不完全な髄鞘形成不全疾患(dysmyelinating disease)とは区別される。
| 中枢神経系 | 原発性 | 多発性硬化症 | 同心円硬化症(Balo病) |
| 急性散在性脳脊髄炎(ADEM) | |||
| 炎症性広汎性硬化症(Schilder病) | |||
| 感染性 | 亜急性硬化症全脳炎(SSPE) | ||
| 進行性多巣性白質脳症(PML) | |||
| 中毒・代謝性 | 低酸素脳症 | ||
| 橋中心髄鞘破壊症 | |||
| ビタミンB12欠乏症 | |||
| 血管性 | Binswanger病 | ||
| 末梢神経系 | ギラン・バレー症候群 | フィッシャー症候群 | |
| 慢性炎症性脱髄性多発神経炎 | |||
表3.代表的な脱髄性疾患
大きく分けて中枢神経系と末梢神経系の疾患がある。
関連語
参考文献
- ↑ 1.0 1.1 Eric R. Kandel et al.
Principles of neural science fifth edition p475-480
McGraw-Hill Professional, New York, 2012 - ↑
Coetzee, T., Suzuki, K., & Popko, B. (1998).
New perspectives on the function of myelin galactolipids. Trends in neurosciences, 21(3), 126-30. [PubMed:9530920] [WorldCat] [DOI] - ↑
Salzer, J.L., Brophy, P.J., & Peles, E. (2008).
Molecular domains of myelinated axons in the peripheral nervous system. Glia, 56(14), 1532-40. [PubMed:18803321] [WorldCat] [DOI] - ↑
Vabnick, I., Trimmer, J.S., Schwarz, T.L., Levinson, S.R., Risal, D., & Shrager, P. (1999).
Dynamic potassium channel distributions during axonal development prevent aberrant firing patterns. The Journal of neuroscience : the official journal of the Society for Neuroscience, 19(2), 747-58. [PubMed:9880595] [PMC] [WorldCat] - ↑
Rasband, M.N., Kagawa, T., Park, E.W., Ikenaka, K., & Trimmer, J.S. (2003).
Dysregulation of axonal sodium channel isoforms after adult-onset chronic demyelination. Journal of neuroscience research, 73(4), 465-70. [PubMed:12898531] [WorldCat] [DOI] - ↑
Rasband, M.N., Trimmer, J.S., Peles, E., Levinson, S.R., & Shrager, P. (2000).
K+ channel distribution and clustering in developing and hypomyelinated axons of the optic nerve. Journal of neurocytology, 28(4-5), 319-31. [PubMed:10739574] [WorldCat] [DOI] - ↑
Pereira, J.A., Lebrun-Julien, F., & Suter, U. (2012).
Molecular mechanisms regulating myelination in the peripheral nervous system. Trends in neurosciences, 35(2), 123-34. [PubMed:22192173] [WorldCat] [DOI] - ↑ ニューロンの生理学 D. Tritsch, D.Chenoy-Marchais, A.Feltz
- ↑
Rasband, M.N. (2010).
The axon initial segment and the maintenance of neuronal polarity. Nature reviews. Neuroscience, 11(8), 552-62. [PubMed:20631711] [WorldCat] [DOI] - ↑
Buffington, S.A., & Rasband, M.N. (2011).
The axon initial segment in nervous system disease and injury. The European journal of neuroscience, 34(10), 1609-19. [PubMed:22103418] [PMC] [WorldCat] [DOI] - ↑
Nave, K.A., & Trapp, B.D. (2008).
Axon-glial signaling and the glial support of axon function. Annual review of neuroscience, 31, 535-61. [PubMed:18558866] [WorldCat] [DOI] - ↑ 12.0 12.1
Nakahara, J., Maeda, M., Aiso, S., & Suzuki, N. (2012).
Current concepts in multiple sclerosis: autoimmunity versus oligodendrogliopathy. Clinical reviews in allergy & immunology, 42(1), 26-34. [PubMed:22189514] [WorldCat] [DOI] - ↑
Sherratt, R.M., Bostock, H., & Sears, T.A. (1980).
Effects of 4-aminopyridine on normal and demyelinated mammalian nerve fibres. Nature, 283(5747), 570-2. [PubMed:7354839] [WorldCat] [DOI] - ↑
Jones, R.E., Heron, J.R., Foster, D.H., Snelgar, R.S., & Mason, R.J. (1983).
Effects of 4-aminopyridine in patients with multiple sclerosis. Journal of the neurological sciences, 60(3), 353-62. [PubMed:6631441] [WorldCat] [DOI] - ↑
Kocsis, J.D., Bowe, C.M., & Waxman, S.G. (1986).
Different effects of 4-aminopyridine on sensory and motor fibers: pathogenesis of paresthesias. Neurology, 36(1), 117-20. [PubMed:3001584] [WorldCat] [DOI] - ↑
Stefoski, D., Davis, F.A., Faut, M., & Schauf, C.L. (1987).
4-Aminopyridine improves clinical signs in multiple sclerosis. Annals of neurology, 21(1), 71-7. [PubMed:2435223] [WorldCat] [DOI] - ↑
Fields, R.D. (2008).
White matter in learning, cognition and psychiatric disorders. Trends in neurosciences, 31(7), 361-70. [PubMed:18538868] [PMC] [WorldCat] [DOI] - ↑
Nave, K.A. (2010).
Myelination and the trophic support of long axons. Nature reviews. Neuroscience, 11(4), 275-83. [PubMed:20216548] [WorldCat] [DOI] - ↑
Herring, N.R., & Konradi, C. (2011).
Myelin, copper, and the cuprizone model of schizophrenia. Frontiers in bioscience (Scholar edition), 3, 23-40. [PubMed:21196354] [PMC] [WorldCat]