「視床下部」の版間の差分
Ayumuinutsuka (トーク | 投稿記録) 細編集の要約なし |
Ayumuinutsuka (トーク | 投稿記録) 細編集の要約なし |
||
| 15行目: | 15行目: | ||
=== 室傍核(Paraventricular nucleus: PVN) === | === 室傍核(Paraventricular nucleus: PVN) === | ||
視床下部前方の背側部において第三脳室壁近くにある明瞭な核で視交叉上核とおなじく構成する細胞は大きい。下垂体後葉にオキシトシンを分泌している。また、室傍核にはストレスホルモンとも呼ばれる副腎皮質刺激ホルモン放出ホルモン(corticotropin-releasing hormone: CRH)を神経分泌によって放出する神経細胞が存在する。視床下部からのCRHの放出は下垂体前葉における副腎皮質刺激ホルモン(adrenocorticotropic hormone: ACTH)産生細胞を刺激し、ACTHやβ-リポトロピン、β―エンドルフィンの産生と放出とが促される。ACTHは副腎皮質を刺激し、副腎皮質ホルモンである糖質コルチコイド(主にコルチゾール)の産生と分泌とを高める。このコルチゾールが循環器機能やエネルギー代謝を高め、ストレスに対する全身の防御にはたらく。ヒトを含めた哺乳動物ではストレスに対する防御システムとして内分泌系および自律神経系が最も重要な役割を担っており、両者を制御する中枢が視床下部であり、視床下部―下垂体―副腎皮質の一連のホルモン伝達系はストレス応答の重要な経路となっている<ref> | 視床下部前方の背側部において第三脳室壁近くにある明瞭な核で視交叉上核とおなじく構成する細胞は大きい。下垂体後葉にオキシトシンを分泌している。また、室傍核にはストレスホルモンとも呼ばれる副腎皮質刺激ホルモン放出ホルモン(corticotropin-releasing hormone: CRH)を神経分泌によって放出する神経細胞が存在する。視床下部からのCRHの放出は下垂体前葉における副腎皮質刺激ホルモン(adrenocorticotropic hormone: ACTH)産生細胞を刺激し、ACTHやβ-リポトロピン、β―エンドルフィンの産生と放出とが促される。ACTHは副腎皮質を刺激し、副腎皮質ホルモンである糖質コルチコイド(主にコルチゾール)の産生と分泌とを高める。このコルチゾールが循環器機能やエネルギー代謝を高め、ストレスに対する全身の防御にはたらく。ヒトを含めた哺乳動物ではストレスに対する防御システムとして内分泌系および自律神経系が最も重要な役割を担っており、両者を制御する中枢が視床下部であり、視床下部―下垂体―副腎皮質の一連のホルモン伝達系はストレス応答の重要な経路となっている<ref><pubmed> 21663538</pubmed></ref>。 | ||
=== 視交叉上核(Suprachiasmatic nucleus: SCN) === | === 視交叉上核(Suprachiasmatic nucleus: SCN) === | ||
視床下部の底部、視交叉のすぐ上に位置する一対の神経核で、密集した大型の神経細胞から構成されている(一般に視床下部の神経核は主として散在性の小細胞から構成されている)。視交叉上核には神経ホルモンであるバゾプレシンあるいはオキシトシンを含む神経分泌ニューロンの細胞体が存在し、そこから延びる軸索は下垂体後葉に投射して毛細血管に神経分泌している。視交叉上核は体内時計の中枢として知られている<ref> | 視床下部の底部、視交叉のすぐ上に位置する一対の神経核で、密集した大型の神経細胞から構成されている(一般に視床下部の神経核は主として散在性の小細胞から構成されている)。視交叉上核には神経ホルモンであるバゾプレシンあるいはオキシトシンを含む神経分泌ニューロンの細胞体が存在し、そこから延びる軸索は下垂体後葉に投射して毛細血管に神経分泌している。視交叉上核は体内時計の中枢として知られている<ref><pubmed> 20148688 </pubmed></ref>。視交叉上核を破壊された動物では、規則正しい睡眠・覚醒リズムが消失してしまうだけではなく、視交叉上核の細胞は、体内から取り出され外界からの刺激がない状態で培養されても、自律的にリズムを刻み続けることができる<ref><pubmed> 7718233 </pubmed></ref>。同時に、視交叉上核は外部環境である日長の情報を網膜から受け取り、他の情報と統合し、松果体へ送信している<ref><pubmed> 16337005 </pubmed></ref>。松果体ではこの情報に応答して睡眠を制御するホルモンであるメラトニンを分泌する。メラトニン分泌は夜間に高く昼間に低い。 | ||
=== 結節乳頭体核(Tuberomammillary nucleus: TMN) === | === 結節乳頭体核(Tuberomammillary nucleus: TMN) === | ||
| 25行目: | 25行目: | ||
=== 背内側核(Dorsomedial hypothalamic nucleus: DMN) === | === 背内側核(Dorsomedial hypothalamic nucleus: DMN) === | ||
脳弓の外側にあり小型または中型の細胞から構成されている。摂食行動<ref> | 脳弓の外側にあり小型または中型の細胞から構成されている。摂食行動<ref><pubmed> 12117580 </pubmed></ref>や概日リズムに合わせたコルチコイド分泌とそれに付随した覚醒、運動などに関与していることが知られている<ref><pubmed> 14627654 </pubmed></ref>。 | ||
=== 腹内側核(Ventromedial hypothalamic nucleus: VMN) === | === 腹内側核(Ventromedial hypothalamic nucleus: VMN) === | ||
腹内側核は視床下部の中で最も大きく明瞭な核であり、小型または中型の細胞から構成されている。満腹中枢としての機能は1940年代におこなわれた腹内側核の除去が動物に肥満をもたらすという様々な実験結果から提唱されたものであり、1970年代に肥満をもたらしているのは室傍核など腹内側核の周辺組織の受けた損傷であるというGoldらによる異論<ref> | 腹内側核は視床下部の中で最も大きく明瞭な核であり、小型または中型の細胞から構成されている。満腹中枢としての機能は1940年代におこなわれた腹内側核の除去が動物に肥満をもたらすという様々な実験結果から提唱されたものであり、1970年代に肥満をもたらしているのは室傍核など腹内側核の周辺組織の受けた損傷であるというGoldらによる異論<ref><pubmed> 4795550 </pubmed></ref>があったものの、現在でも有効である<ref><pubmed> 16412483 </pubmed></ref>。 | ||
== 視床下部の機能について == | == 視床下部の機能について == | ||
| 34行目: | 34行目: | ||
=== 摂食行動と代謝の調節 === | === 摂食行動と代謝の調節 === | ||
多くの動物にとって生存にかかわる最も大きな問題は飢えである。エネルギーを適切に管理するため、視床下部は摂食行動と代謝レベルを調節している。エネルギーに余裕があるときには糖質から脂肪への変換を行い、エネルギーが欠乏しているときにはタンパク質を分解するという一連の代謝システムは視床下部の自律神経と内分泌をコントロールする機能によって管理されている。この機能に関しては、弓状核が主にその役割を担っており、腹内側核、背内側核、室傍核などが協調してはたらいている<ref> | 多くの動物にとって生存にかかわる最も大きな問題は飢えである。エネルギーを適切に管理するため、視床下部は摂食行動と代謝レベルを調節している。エネルギーに余裕があるときには糖質から脂肪への変換を行い、エネルギーが欠乏しているときにはタンパク質を分解するという一連の代謝システムは視床下部の自律神経と内分泌をコントロールする機能によって管理されている。この機能に関しては、弓状核が主にその役割を担っており、腹内側核、背内側核、室傍核などが協調してはたらいている<ref><pubmed> 16988703 </pubmed></ref>。 | ||
=== 生殖行動の調節 === | === 生殖行動の調節 === | ||
哺乳動物のメスにおいては、視床下部は繁殖期のサイクルを調節している。生殖行動には十分なエネルギーの蓄えが必要であり、多くの動物にとってそれは一年のうち一定の時期に限定されている。弓状核の神経細胞はホルモン分泌を介して生殖行動を調節しており、性行動は背内側核や視索前野、乳頭体核などといった領域にも管理されている<ref> | 哺乳動物のメスにおいては、視床下部は繁殖期のサイクルを調節している。生殖行動には十分なエネルギーの蓄えが必要であり、多くの動物にとってそれは一年のうち一定の時期に限定されている。弓状核の神経細胞はホルモン分泌を介して生殖行動を調節しており、性行動は背内側核や視索前野、乳頭体核などといった領域にも管理されている<ref><pubmed> 12052919 </pubmed></ref>。生殖行動はエネルギー代謝、胎児への血液供給を含めた循環器系、体温調節などのシステムと協調している。 | ||
=== ストレス応答の調節 === | === ストレス応答の調節 === | ||
動物が攻撃を受けた時には覚醒水準や代謝を高め、闘争や逃走にリソースを集中する必要が生じる。こうしたストレス応答に際しては心理的ストレスも身体的ストレスも共に視床下部の室傍核に伝えられる。この室傍核から下垂体、そして副腎へと伝えられるシグナル伝達はストレス応答にとって非常に重要であり、この回路はHPA axis (Hypothalamic-pituitary-adrenal axis)と呼ばれている。視床下部の室傍核からストレスホルモンとも呼ばれる副腎皮質刺激ホルモン放出ホルモンが放出され、それによって刺激された下垂体前葉から副腎皮質刺激ホルモンが産生・放出され、それによって刺激された副腎皮質は副腎皮質ホルモンとして知られる糖質コルチコイドの分泌を高める。このコルチゾールが循環器機能やエネルギー代謝を高め、ストレスに対して全身の防御反応を引き起こすのである<ref> | 動物が攻撃を受けた時には覚醒水準や代謝を高め、闘争や逃走にリソースを集中する必要が生じる。こうしたストレス応答に際しては心理的ストレスも身体的ストレスも共に視床下部の室傍核に伝えられる。この室傍核から下垂体、そして副腎へと伝えられるシグナル伝達はストレス応答にとって非常に重要であり、この回路はHPA axis (Hypothalamic-pituitary-adrenal axis)と呼ばれている。視床下部の室傍核からストレスホルモンとも呼ばれる副腎皮質刺激ホルモン放出ホルモンが放出され、それによって刺激された下垂体前葉から副腎皮質刺激ホルモンが産生・放出され、それによって刺激された副腎皮質は副腎皮質ホルモンとして知られる糖質コルチコイドの分泌を高める。このコルチゾールが循環器機能やエネルギー代謝を高め、ストレスに対して全身の防御反応を引き起こすのである<ref><pubmed> 21663538 </pubmed></ref>。ストレスは睡眠や性行動を抑制する。 | ||
=== 睡眠・覚醒の調節 === | === 睡眠・覚醒の調節 === | ||
視床下部が睡眠・覚醒を司っていることは古くから知られており、嗜眠性脳炎の研究などから視床下部の前方部には睡眠中枢が、後方部には覚醒中枢が存在することが提起された。視床下部前方部に存在する腹外側視索前野(Ventrolateral preoptic nucleus: VLPO)におけるGABA作動性ニューロンが睡眠中枢として中心的な役割を果たしており、VLPOの神経細胞は睡眠時に活動を増加させることで睡眠の開始と維持を行っている<ref> | 視床下部が睡眠・覚醒を司っていることは古くから知られており、嗜眠性脳炎の研究などから視床下部の前方部には睡眠中枢が、後方部には覚醒中枢が存在することが提起された。視床下部前方部に存在する腹外側視索前野(Ventrolateral preoptic nucleus: VLPO)におけるGABA作動性ニューロンが睡眠中枢として中心的な役割を果たしており、VLPOの神経細胞は睡眠時に活動を増加させることで睡眠の開始と維持を行っている<ref><pubmed> 12401341 </pubmed></ref>。一方、視床下部後方部に存在する結節乳頭体核はヒスタミン神経の起始核であり、覚醒中枢の一つと考えられている。ヒスタミン神経細胞はここから脳内のほとんどの領域に軸索を投射しており、ヒスタミン神経細胞の活動が高まると覚醒レベルが上昇する。VLPOとTMNは互いに軸索を投射してその活動を抑制し合っており、TMNからVLPOへの抑制が優位になると覚醒が、VLPOからTMNへの抑制が優位になると睡眠が開始されることで迅速な睡眠・覚醒の相転移が行われている(フリップ・フロップ)<ref><pubmed> 16251950 </pubmed></ref>。 | ||
== 最近の知見について == | == 最近の知見について == | ||
このように生理的に重要な機能を多く併せ持つ視床下部ではあるが、その神経回路の機能に関してはいまだに不明な点が多い。形態学的に分類、記載されてきた神経核ではあるが、細胞に発現しているペプチドの染色結果などにより、同じ種類の神経細胞が複数の領域にまたがって存在していたり、一つの神経核の中でも多数の異なる種類の神経細胞が共存していたりすることが分かってきた。そのため、神経細胞が形成する回路としての機能単位を正確に捉えるには新しい実験手法が必要とされている。例えば、神経ペプチドであるオレキシンを産生するオレキシンニューロンは睡眠に関与することが知られていたが、少数の細胞が散在しているため古典的な手法では特異的にその機能を調べることは困難であった。しかし、オレキシンのプロモーター下流でチャネルロドプシンやハロロドプシンを発現させ、それを光刺激することによってin vivoでオレキシン神経細胞特異的に活動を制御する、といった光遺伝学的手法によって現在ではその機能が次第に明らかになりつつある<ref> | このように生理的に重要な機能を多く併せ持つ視床下部ではあるが、その神経回路の機能に関してはいまだに不明な点が多い。形態学的に分類、記載されてきた神経核ではあるが、細胞に発現しているペプチドの染色結果などにより、同じ種類の神経細胞が複数の領域にまたがって存在していたり、一つの神経核の中でも多数の異なる種類の神経細胞が共存していたりすることが分かってきた。そのため、神経細胞が形成する回路としての機能単位を正確に捉えるには新しい実験手法が必要とされている。例えば、神経ペプチドであるオレキシンを産生するオレキシンニューロンは睡眠に関与することが知られていたが、少数の細胞が散在しているため古典的な手法では特異的にその機能を調べることは困難であった。しかし、オレキシンのプロモーター下流でチャネルロドプシンやハロロドプシンを発現させ、それを光刺激することによってin vivoでオレキシン神経細胞特異的に活動を制御する、といった光遺伝学的手法によって現在ではその機能が次第に明らかになりつつある<ref><pubmed> 17943086 </pubmed></ref><ref><pubmed> 21775598 </pubmed></ref>。 | ||
== 関連項目 == | == 関連項目 == | ||
2012年4月17日 (火) 16:09時点における版
英:Hypothalamus
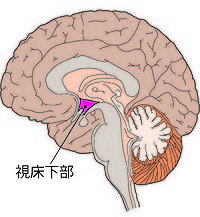
視床下部とは、間脳に位置し、内分泌や自律機能の調節を行う総合中枢である。ヒトの場合は脳重量のわずか0.3%程度を占めるにすぎない小さな組織であるが、多くの神経核から構成されており、体温維持や摂食行動、性行動や睡眠覚醒など多様な機能を協調して管理することで生体の恒常性維持に重要な役割を果たしている。中脳以下の自律機能を司る中枢がそれぞれ呼吸運動や血管運動などの個別の自律機能を調節するのに対して、視床下部は交感神経・副交感神経機能や内分泌を統合的に調節している。系統発生的には古い脳領域であり、摂食行動、性行動、睡眠といった本能行動や怒りや不安などの情動行動の中枢である。
視床下部の構造
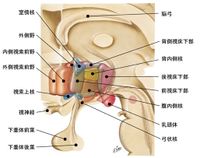
視床下部を構成する灰白質は第三脳室と接している視床下部脳室周囲層、その外側の視床下部内側野、視床下部の最も外側に位置する視床下部外側野の3領域に分けられ、それぞれに核群が存在している。また、視床下部は下垂体門脈と呼ばれる血管系を介して下垂体とつながっている。下垂体は甲状腺、副腎皮質、性腺といった下位の内分泌腺を刺激するホルモンを分泌する上位の内分泌器官であるが、視床下部で産生される視床下部ホルモンは下垂体門脈を経由して下垂体からのホルモン分泌を調節している。視床下部の毛細血管の内皮細胞には小さな孔が開いているため神経細胞は常に直接血液に接しており、視床下部内側領域には血液および脳脊髄液を連結する小管系も存在する。こうした視床下部の組織学的特徴は、視床下部の神経細胞が血液、脳脊髄液中の生理活性分子の濃度変化を感知するのに役立っている。以下、視床下部に存在する多くの神経核のうち、主なものを記す。
弓状核(Arcuate nucleus: ARC)
ホメオスタシスは自律神経系とホルモン系との協調作用によって保たれており、視床下部はこのホルモン系の制御を行っている。ホルモン系調節の中心は視床下部と下垂体をつなげる漏斗と呼ばれる部位に存在する弓状核(別名を漏斗核)である。弓状核は下垂体前葉からのホルモン分泌を促進させる放出ホルモン(成長ホルモン放出ホルモン、甲状腺刺激ホルモン放出ホルモン、副腎皮質刺激ホルモン放出ホルモン、性腺刺激ホルモン放出ホルモン、プロラクチン放出ホルモン)あるいは分泌を抑制する放出抑制ホルモン(成長ホルモン抑制ホルモン、プロラクチン抑制ホルモン)を分泌している。摂食行動とも関連が深い。
室傍核(Paraventricular nucleus: PVN)
視床下部前方の背側部において第三脳室壁近くにある明瞭な核で視交叉上核とおなじく構成する細胞は大きい。下垂体後葉にオキシトシンを分泌している。また、室傍核にはストレスホルモンとも呼ばれる副腎皮質刺激ホルモン放出ホルモン(corticotropin-releasing hormone: CRH)を神経分泌によって放出する神経細胞が存在する。視床下部からのCRHの放出は下垂体前葉における副腎皮質刺激ホルモン(adrenocorticotropic hormone: ACTH)産生細胞を刺激し、ACTHやβ-リポトロピン、β―エンドルフィンの産生と放出とが促される。ACTHは副腎皮質を刺激し、副腎皮質ホルモンである糖質コルチコイド(主にコルチゾール)の産生と分泌とを高める。このコルチゾールが循環器機能やエネルギー代謝を高め、ストレスに対する全身の防御にはたらく。ヒトを含めた哺乳動物ではストレスに対する防御システムとして内分泌系および自律神経系が最も重要な役割を担っており、両者を制御する中枢が視床下部であり、視床下部―下垂体―副腎皮質の一連のホルモン伝達系はストレス応答の重要な経路となっている[1]。
視交叉上核(Suprachiasmatic nucleus: SCN)
視床下部の底部、視交叉のすぐ上に位置する一対の神経核で、密集した大型の神経細胞から構成されている(一般に視床下部の神経核は主として散在性の小細胞から構成されている)。視交叉上核には神経ホルモンであるバゾプレシンあるいはオキシトシンを含む神経分泌ニューロンの細胞体が存在し、そこから延びる軸索は下垂体後葉に投射して毛細血管に神経分泌している。視交叉上核は体内時計の中枢として知られている[2]。視交叉上核を破壊された動物では、規則正しい睡眠・覚醒リズムが消失してしまうだけではなく、視交叉上核の細胞は、体内から取り出され外界からの刺激がない状態で培養されても、自律的にリズムを刻み続けることができる[3]。同時に、視交叉上核は外部環境である日長の情報を網膜から受け取り、他の情報と統合し、松果体へ送信している[4]。松果体ではこの情報に応答して睡眠を制御するホルモンであるメラトニンを分泌する。メラトニン分泌は夜間に高く昼間に低い。
結節乳頭体核(Tuberomammillary nucleus: TMN)
視床下部の後部に位置する結節乳頭体核は乳頭体の内部にある核で、さらに小細胞性で乳頭体の主部をなす乳頭体内側核と大細胞性で外側をしめる小さい乳頭体外側核とに分けられる。嗅覚と自律神経とに関係する重要な神経核である。大脳辺緑系と連絡、感情形成に関与している。ヒスタミン神経系の起始核であり、ここから上行性および下行性に伸び、脳の広領域に投射している。
背内側核(Dorsomedial hypothalamic nucleus: DMN)
脳弓の外側にあり小型または中型の細胞から構成されている。摂食行動[5]や概日リズムに合わせたコルチコイド分泌とそれに付随した覚醒、運動などに関与していることが知られている[6]。
腹内側核(Ventromedial hypothalamic nucleus: VMN)
腹内側核は視床下部の中で最も大きく明瞭な核であり、小型または中型の細胞から構成されている。満腹中枢としての機能は1940年代におこなわれた腹内側核の除去が動物に肥満をもたらすという様々な実験結果から提唱されたものであり、1970年代に肥満をもたらしているのは室傍核など腹内側核の周辺組織の受けた損傷であるというGoldらによる異論[7]があったものの、現在でも有効である[8]。
視床下部の機能について
視床下部は摂食行動、睡眠・覚醒、ストレス応答、生殖行動など多様な行動を調節している。それらは単独で機能しているわけではなく互いの活動を促進、抑制することで全体的なモードを規定している。例えば、ストレス応答の際は生存確率を高めるために代謝レベルを高めるが、その際には体温や血圧を上昇させ、睡眠は抑制し、生殖行動のスイッチをオフにするような統合的な調節が行われている。以下に代表的な機能について記す。
摂食行動と代謝の調節
多くの動物にとって生存にかかわる最も大きな問題は飢えである。エネルギーを適切に管理するため、視床下部は摂食行動と代謝レベルを調節している。エネルギーに余裕があるときには糖質から脂肪への変換を行い、エネルギーが欠乏しているときにはタンパク質を分解するという一連の代謝システムは視床下部の自律神経と内分泌をコントロールする機能によって管理されている。この機能に関しては、弓状核が主にその役割を担っており、腹内側核、背内側核、室傍核などが協調してはたらいている[9]。
生殖行動の調節
哺乳動物のメスにおいては、視床下部は繁殖期のサイクルを調節している。生殖行動には十分なエネルギーの蓄えが必要であり、多くの動物にとってそれは一年のうち一定の時期に限定されている。弓状核の神経細胞はホルモン分泌を介して生殖行動を調節しており、性行動は背内側核や視索前野、乳頭体核などといった領域にも管理されている[10]。生殖行動はエネルギー代謝、胎児への血液供給を含めた循環器系、体温調節などのシステムと協調している。
ストレス応答の調節
動物が攻撃を受けた時には覚醒水準や代謝を高め、闘争や逃走にリソースを集中する必要が生じる。こうしたストレス応答に際しては心理的ストレスも身体的ストレスも共に視床下部の室傍核に伝えられる。この室傍核から下垂体、そして副腎へと伝えられるシグナル伝達はストレス応答にとって非常に重要であり、この回路はHPA axis (Hypothalamic-pituitary-adrenal axis)と呼ばれている。視床下部の室傍核からストレスホルモンとも呼ばれる副腎皮質刺激ホルモン放出ホルモンが放出され、それによって刺激された下垂体前葉から副腎皮質刺激ホルモンが産生・放出され、それによって刺激された副腎皮質は副腎皮質ホルモンとして知られる糖質コルチコイドの分泌を高める。このコルチゾールが循環器機能やエネルギー代謝を高め、ストレスに対して全身の防御反応を引き起こすのである[11]。ストレスは睡眠や性行動を抑制する。
睡眠・覚醒の調節
視床下部が睡眠・覚醒を司っていることは古くから知られており、嗜眠性脳炎の研究などから視床下部の前方部には睡眠中枢が、後方部には覚醒中枢が存在することが提起された。視床下部前方部に存在する腹外側視索前野(Ventrolateral preoptic nucleus: VLPO)におけるGABA作動性ニューロンが睡眠中枢として中心的な役割を果たしており、VLPOの神経細胞は睡眠時に活動を増加させることで睡眠の開始と維持を行っている[12]。一方、視床下部後方部に存在する結節乳頭体核はヒスタミン神経の起始核であり、覚醒中枢の一つと考えられている。ヒスタミン神経細胞はここから脳内のほとんどの領域に軸索を投射しており、ヒスタミン神経細胞の活動が高まると覚醒レベルが上昇する。VLPOとTMNは互いに軸索を投射してその活動を抑制し合っており、TMNからVLPOへの抑制が優位になると覚醒が、VLPOからTMNへの抑制が優位になると睡眠が開始されることで迅速な睡眠・覚醒の相転移が行われている(フリップ・フロップ)[13]。
最近の知見について
このように生理的に重要な機能を多く併せ持つ視床下部ではあるが、その神経回路の機能に関してはいまだに不明な点が多い。形態学的に分類、記載されてきた神経核ではあるが、細胞に発現しているペプチドの染色結果などにより、同じ種類の神経細胞が複数の領域にまたがって存在していたり、一つの神経核の中でも多数の異なる種類の神経細胞が共存していたりすることが分かってきた。そのため、神経細胞が形成する回路としての機能単位を正確に捉えるには新しい実験手法が必要とされている。例えば、神経ペプチドであるオレキシンを産生するオレキシンニューロンは睡眠に関与することが知られていたが、少数の細胞が散在しているため古典的な手法では特異的にその機能を調べることは困難であった。しかし、オレキシンのプロモーター下流でチャネルロドプシンやハロロドプシンを発現させ、それを光刺激することによってin vivoでオレキシン神経細胞特異的に活動を制御する、といった光遺伝学的手法によって現在ではその機能が次第に明らかになりつつある[14][15]。
関連項目
ストレス応答、睡眠
参考文献
- ↑
Tasker, J.G., & Herman, J.P. (2011).
Mechanisms of rapid glucocorticoid feedback inhibition of the hypothalamic-pituitary-adrenal axis. Stress (Amsterdam, Netherlands), 14(4), 398-406. [PubMed:21663538] [PMC] [WorldCat] [DOI] - ↑
Welsh, D.K., Takahashi, J.S., & Kay, S.A. (2010).
Suprachiasmatic nucleus: cell autonomy and network properties. Annual review of physiology, 72, 551-77. [PubMed:20148688] [PMC] [WorldCat] [DOI] - ↑
Welsh, D.K., Logothetis, D.E., Meister, M., & Reppert, S.M. (1995).
Individual neurons dissociated from rat suprachiasmatic nucleus express independently phased circadian firing rhythms. Neuron, 14(4), 697-706. [PubMed:7718233] [WorldCat] [DOI] - ↑
Morin, L.P., & Allen, C.N. (2006).
The circadian visual system, 2005. Brain research reviews, 51(1), 1-60. [PubMed:16337005] [WorldCat] [DOI] - ↑
Bellinger, L.L., & Bernardis, L.L. (2002).
The dorsomedial hypothalamic nucleus and its role in ingestive behavior and body weight regulation: lessons learned from lesioning studies. Physiology & behavior, 76(3), 431-42. [PubMed:12117580] [WorldCat] [DOI] - ↑
Chou, T.C., Scammell, T.E., Gooley, J.J., Gaus, S.E., Saper, C.B., & Lu, J. (2003).
Critical role of dorsomedial hypothalamic nucleus in a wide range of behavioral circadian rhythms. The Journal of neuroscience : the official journal of the Society for Neuroscience, 23(33), 10691-702. [PubMed:14627654] [PMC] [WorldCat] - ↑
Gold, R.M. (1973).
Hypothalamic obesity: the myth of the ventromedial nucleus. Science (New York, N.Y.), 182(4111), 488-90. [PubMed:4795550] [WorldCat] [DOI] - ↑
King, B.M. (2006).
The rise, fall, and resurrection of the ventromedial hypothalamus in the regulation of feeding behavior and body weight. Physiology & behavior, 87(2), 221-44. [PubMed:16412483] [WorldCat] [DOI] - ↑
Morton, G.J., Cummings, D.E., Baskin, D.G., Barsh, G.S., & Schwartz, M.W. (2006).
Central nervous system control of food intake and body weight. Nature, 443(7109), 289-95. [PubMed:16988703] [WorldCat] [DOI] - ↑
Simerly, R.B. (2002).
Wired for reproduction: organization and development of sexually dimorphic circuits in the mammalian forebrain. Annual review of neuroscience, 25, 507-36. [PubMed:12052919] [WorldCat] [DOI] - ↑
Tasker, J.G., & Herman, J.P. (2011).
Mechanisms of rapid glucocorticoid feedback inhibition of the hypothalamic-pituitary-adrenal axis. Stress (Amsterdam, Netherlands), 14(4), 398-406. [PubMed:21663538] [PMC] [WorldCat] [DOI] - ↑
Gaus, S.E., Strecker, R.E., Tate, B.A., Parker, R.A., & Saper, C.B. (2002).
Ventrolateral preoptic nucleus contains sleep-active, galaninergic neurons in multiple mammalian species. Neuroscience, 115(1), 285-94. [PubMed:12401341] [WorldCat] [DOI] - ↑
Saper, C.B., Scammell, T.E., & Lu, J. (2005).
Hypothalamic regulation of sleep and circadian rhythms. Nature, 437(7063), 1257-63. [PubMed:16251950] [WorldCat] [DOI] - ↑
Adamantidis, A.R., Zhang, F., Aravanis, A.M., Deisseroth, K., & de Lecea, L. (2007).
Neural substrates of awakening probed with optogenetic control of hypocretin neurons. Nature, 450(7168), 420-4. [PubMed:17943086] [PMC] [WorldCat] [DOI] - ↑
Tsunematsu, T., Kilduff, T.S., Boyden, E.S., Takahashi, S., Tominaga, M., & Yamanaka, A. (2011).
Acute optogenetic silencing of orexin/hypocretin neurons induces slow-wave sleep in mice. The Journal of neuroscience : the official journal of the Society for Neuroscience, 31(29), 10529-39. [PubMed:21775598] [PMC] [WorldCat] [DOI]
(執筆者: 担当編集委員:)