「Signal Transducers and Activator of Transcription 3」の版間の差分
Kinichinakashima (トーク | 投稿記録) 細編集の要約なし |
|||
| 3行目: | 3行目: | ||
英:Signal Transducers and Activator of Transcription3、英略語:STAT3 | 英:Signal Transducers and Activator of Transcription3、英略語:STAT3 | ||
シグナル伝達と転写活性化を行うことで、分化や生存、増殖などを調節するタンパク質の一群、STATファミリーの一つ。STATファミリー分子として報告されているのはSTAT1、STAT2、STAT3、STAT4、STAT5A、STAT5B、STAT6の7種類<ref><pubmed> 8608586 </pubmed></ref><ref><pubmed> 9418183 </pubmed></ref>。STAT3は非活性化状態時では細胞質に局在するが、Janus kinase(JAK)が活性化されることによってリン酸化を受け、核内移行し目的遺伝子を活性化する転写因子となる。この活性化経路はJAK-STAT経路と呼ばれている。悪性腫瘍形成の初期の過程などにおいて、JAK-STAT経路の制御不全が見られており、免疫抑制や腫瘍の生存延長、血管新生などを引き起こす。 | |||
== STATファミリー == | == STATファミリー == | ||
免疫系に作用するサイトカインとして同定された、L-6ファミリーサイトカイン(LIFなど)が細胞膜上のサイトカイン受容体複合体中のサイトカイン特異的結合鎖と結合することで、膜たんぱく質gp130を含む信号伝達鎖の二量体化がおこり、信号伝達鎖の細胞内領域に会合するJAKが活性化され、信号伝達鎖の細胞内領域中のチロシン残基をリン酸化する。リン酸化されたチロシン残基に、転写因子STAT3が自身のSH2(src homology 2)ドメインを介して会合、近接したJAKによりチロシンリン酸化(チロシン705)を受けることで活性化する<ref><pubmed> 9685167 </pubmed></ref>。チロシンリン酸化されたSTAT3分子はホモないしヘテロ二量体を形成し核へ移行した後、目的遺伝子の転写を制御する。 | |||
== 脳内での働き == | == 脳内での働き == | ||
| 13行目: | 13行目: | ||
STAT3をシグナル経路下流の転写因子とするLIFなどのサイトカイン群と、smadをシグナル経路下流の転写因子とするBMP2などのサイトカイン群(TGF-βスーパーファミリー)。両者は別々の受容体システムを介し、互いに協調的にクロストークして分化誘導<ref name="ref1"><pubmed> 10205054 </pubmed></ref>することが明らかにされている。 | STAT3をシグナル経路下流の転写因子とするLIFなどのサイトカイン群と、smadをシグナル経路下流の転写因子とするBMP2などのサイトカイン群(TGF-βスーパーファミリー)。両者は別々の受容体システムを介し、互いに協調的にクロストークして分化誘導<ref name="ref1"><pubmed> 10205054 </pubmed></ref>することが明らかにされている。 | ||
また免疫・造血系制御に重要な役割を持つ、TGF-βスーパーファミリー(BMP2など)に属するサイトカインが、セリン/スレオニンキナーゼドメインを細胞内領域に持つタイプⅠとタイプⅡ受容体の二分子ずつのヘテロ四量体に結合し、受容体を活性化する。活性化受容体は、特異的転写因子群smadのセリン残基をリン酸化し、それらを活性化する。BMPの刺激で活性化される特異型smad(smad1,5,8)は共有型smadであるsmad4とヘテロオリゴマーを形成、核へ移行し、目的遺伝子の転写を制御する<ref><pubmed> 9393997 </pubmed></ref><ref><pubmed> 10733523 </pubmed></ref>。 | また免疫・造血系制御に重要な役割を持つ、TGF-βスーパーファミリー(BMP2など)に属するサイトカインが、セリン/スレオニンキナーゼドメインを細胞内領域に持つタイプⅠとタイプⅡ受容体の二分子ずつのヘテロ四量体に結合し、受容体を活性化する。活性化受容体は、特異的転写因子群smadのセリン残基をリン酸化し、それらを活性化する。BMPの刺激で活性化される特異型smad(smad1,5,8)は共有型smadであるsmad4とヘテロオリゴマーを形成、核へ移行し、目的遺伝子の転写を制御する<ref><pubmed> 9393997 </pubmed></ref><ref><pubmed> 10733523 </pubmed></ref>。 | ||
2012年7月12日 (木) 11:06時点における版
STAT3
英:Signal Transducers and Activator of Transcription3、英略語:STAT3
シグナル伝達と転写活性化を行うことで、分化や生存、増殖などを調節するタンパク質の一群、STATファミリーの一つ。STATファミリー分子として報告されているのはSTAT1、STAT2、STAT3、STAT4、STAT5A、STAT5B、STAT6の7種類[1][2]。STAT3は非活性化状態時では細胞質に局在するが、Janus kinase(JAK)が活性化されることによってリン酸化を受け、核内移行し目的遺伝子を活性化する転写因子となる。この活性化経路はJAK-STAT経路と呼ばれている。悪性腫瘍形成の初期の過程などにおいて、JAK-STAT経路の制御不全が見られており、免疫抑制や腫瘍の生存延長、血管新生などを引き起こす。
STATファミリー
免疫系に作用するサイトカインとして同定された、L-6ファミリーサイトカイン(LIFなど)が細胞膜上のサイトカイン受容体複合体中のサイトカイン特異的結合鎖と結合することで、膜たんぱく質gp130を含む信号伝達鎖の二量体化がおこり、信号伝達鎖の細胞内領域に会合するJAKが活性化され、信号伝達鎖の細胞内領域中のチロシン残基をリン酸化する。リン酸化されたチロシン残基に、転写因子STAT3が自身のSH2(src homology 2)ドメインを介して会合、近接したJAKによりチロシンリン酸化(チロシン705)を受けることで活性化する[3]。チロシンリン酸化されたSTAT3分子はホモないしヘテロ二量体を形成し核へ移行した後、目的遺伝子の転写を制御する。
脳内での働き
STAT3をシグナル経路下流の転写因子とするLIFなどのサイトカイン群と、smadをシグナル経路下流の転写因子とするBMP2などのサイトカイン群(TGF-βスーパーファミリー)。両者は別々の受容体システムを介し、互いに協調的にクロストークして分化誘導[4]することが明らかにされている。
また免疫・造血系制御に重要な役割を持つ、TGF-βスーパーファミリー(BMP2など)に属するサイトカインが、セリン/スレオニンキナーゼドメインを細胞内領域に持つタイプⅠとタイプⅡ受容体の二分子ずつのヘテロ四量体に結合し、受容体を活性化する。活性化受容体は、特異的転写因子群smadのセリン残基をリン酸化し、それらを活性化する。BMPの刺激で活性化される特異型smad(smad1,5,8)は共有型smadであるsmad4とヘテロオリゴマーを形成、核へ移行し、目的遺伝子の転写を制御する[5][6]。
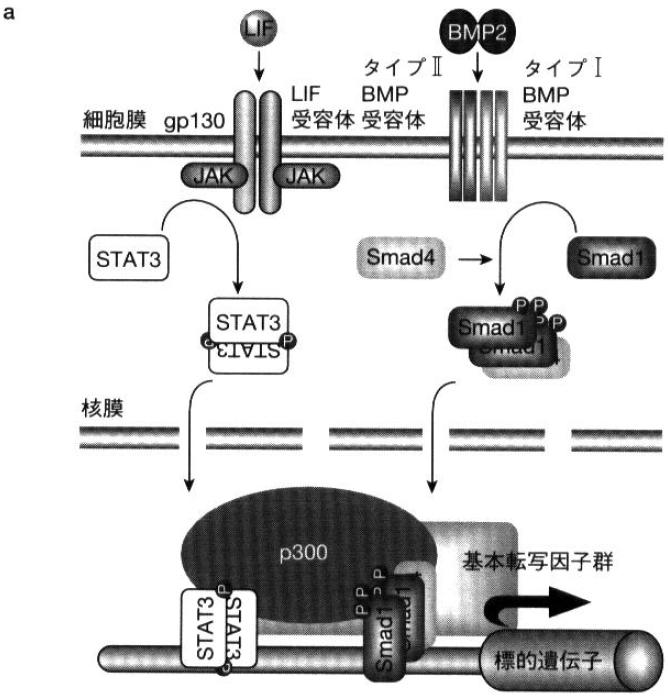
上記の通り、STATとsmadは別々のサイトカイン受容体システムを通じて活性化を受ける転写因子である。しかし、それらの協調作用により、神経幹細胞のアストロサイトへの分化が劇的に誘導される[4]。転写活性化の補助的役割を果たす核内転写共役因子p300がサイトカイン刺激に応答して、自身のN末端側を二量体化したSTAT3と、自身のC末端側をヘテロオリゴマー化したsmad1と、それぞれ同時に結合しSTAT3/p300/smad1複合体が形成される。これにより二種類サイトカインシグナルが核内で統合され、目的遺伝子GFAPの相乗的発現が起こる[4]。そしてGFAPの発現によりアストロサイトへの分化が誘導される。(図a参照[7])
参考文献
- ↑
Ihle, J.N. (1996).
STATs: signal transducers and activators of transcription. Cell, 84(3), 331-4. [PubMed:8608586] [WorldCat] [DOI] - ↑
O'Shea, J.J., Notarangelo, L.D., Johnston, J.A., & Candotti, F. (1997).
Advances in the understanding of cytokine signal transduction: the role of Jaks and STATs in immunoregulation and the pathogenesis of immunodeficiency. Journal of clinical immunology, 17(6), 431-47. [PubMed:9418183] [WorldCat] [DOI] - ↑
Nakashima, K., & Taga, T. (1998).
gp130 and the IL-6 family of cytokines: signaling mechanisms and thrombopoietic activities. Seminars in hematology, 35(3), 210-21. [PubMed:9685167] [WorldCat] - ↑ 4.0 4.1 4.2
Nakashima, K., Yanagisawa, M., Arakawa, H., Kimura, N., Hisatsune, T., Kawabata, M., ..., & Taga, T. (1999).
Synergistic signaling in fetal brain by STAT3-Smad1 complex bridged by p300. Science (New York, N.Y.), 284(5413), 479-82. [PubMed:10205054] [WorldCat] [DOI] - ↑
Heldin, C.H., Miyazono, K., & ten Dijke, P. (1997).
TGF-beta signalling from cell membrane to nucleus through SMAD proteins. Nature, 390(6659), 465-71. [PubMed:9393997] [WorldCat] [DOI] - ↑
Massagué, J., & Chen, Y.G. (2000).
Controlling TGF-beta signaling. Genes & development, 14(6), 627-44. [PubMed:10733523] [WorldCat] - ↑ 中島欽一、滝沢琢己
免疫2000・01 P88-97
中山書店:2000