ケージド試薬
ケージド試薬とは、生理活性分子に光分解性保護基が結合したもので、結合状態では生理活性を持たないが、これに光照射することによって、保護基の解離が起こり、生理活性分子が放出される合成試薬である。
特徴
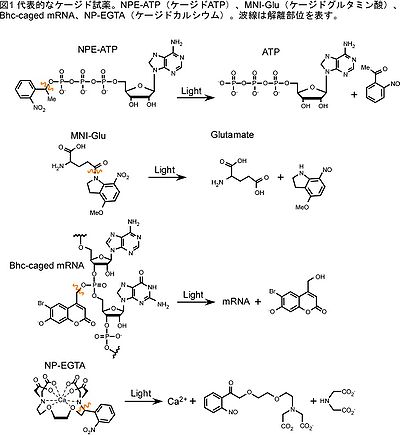
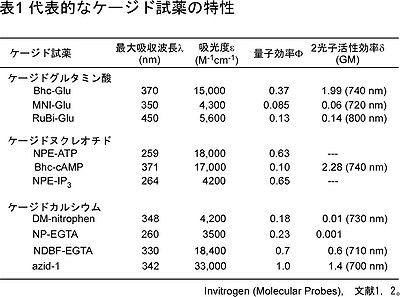
励起波長は主にUV領域であり350 nm付近の励起光を用いることが多い。ケージド試薬に使われる生理活性分子としては、神経伝達物質、ヌクレオチド(IP3, ATP, cAMP, cGMP)、DNA, mRNA、カルシウム、ペプチド、タンパク質などがある。ケージドカルシウム以外では生理活性分子と保護基は共有結合しており、光照射によって、この共有結合が解離する。代表的な光分解性保護基としては、o-ニトロベンジル基、2-(o-ニトロフェニル)エチル基(NPE)、(クマリン-4-イル)メチル基(Bhc)、7-ニトロインドリニル基が存在する(図、表)[1][2]。ケージド試薬のモル吸光係数と量子効率を掛け合わせた値が高いほど光励起されやすく、100 M-1cm-1以上が目安となる[2]。
光照射によって瞬時に生理活性を上昇させることが可能であるため、生理活性上昇からの細胞・分子応答を高い時間解像度で計測できることに利点がある。従って神経科学の分野では、反応速度が速い神経伝達物質受容体反応の誘発や、細胞内カルシウム濃度上昇に広く用いられている。また光照射部位を対物レンズによって局在させることが可能であるため局所的に一過的に活性を上げることができる。
ケージド神経伝達物質
最初のケージド神経伝達物質アゴニストは、1986年に報告されたケージドカルバミルコリンで、UV照射によってアセチルコリン受容体を活性化することに成功した[3]。最も広く用いられているものは、興奮性シナプス後部の主たる神経伝達物質に保護基が結合したケージドグルタミン酸であるが、他の多くの神経伝達物質のアゴニスト・アンタゴニストでもケージド試薬が開発されている。受容体の反応性を調べるために用いるだけでなく、ケージドグルタミン酸のUV照射によって、神経細胞の細胞膜上の多数のグルタミン酸受容体を活性化することで、活動電位を誘発することが可能であり、脳スライス標本において光照射部位を走査することによって、シナプス結合マッピングを行なう方法が確立されている[4]。一方で、シナプスのような微細構造における受容体反応を単一シナプスレベルで光誘導するためには、励起領域を1fl (1 μm3)以下にする必要があり、このためには焦点領域でのみ励起することができる2光子顕微鏡が適用可能である。しかし一般に蛍光分子に比べケージド分子は2光子励起されにくく、細胞障害を起こさずに活性化するためには、試薬の吸収断面積と量子効率を掛け合わせた数値(2光子活性効率)が0.1 GM (1 GM = 10-50 cm4 s )を超えることが目安となる。また実際のシナプス伝達を模倣しようとすると、数mMのケージドグルタミン酸を投与する必要があり、高い水溶性、pH7付近の溶液中での自発的加水分解の起こりにくさ、反応速度定数が数百μ秒以下であることが要求される。生理的条件下で使用できるものとして現在、MNI-Glutamate、CDNI-Glutamate、Rubi-Glutamateなどが報告されている(表)[5][6][7]。MNI-Glutamateを用いてシナプス後部の樹状突起スパインでのグルタミン酸受容体の応答マッピングや機能・構造可塑性を誘発できることが報告されており、単一樹状突起スパインにおける可塑性の解明に大いに役立っている[5][8]。また2光子励起可能なケージドGABAも報告されている[9]。これらのいくつかについてはTOCRIS、INVITORGENから購入可能である。
ケージドヌクレオチド
NPE-ATP、NPE-cAMPはケージド試薬として最初に合成され生細胞へ適用された(図)[10][11]。ケージドIP3を含め、生物学研究で広範囲に使用されている。
ケージドカルシウム
カルシウムイオンは保護基と共有結合できないため、高親和性のカルシウムキレート剤(BAPTA、EDTA、EGTA)に保護基が結合したケージド試薬が合成されている。保護基が結合した状態はカルシウムイオンに高親和性を持つが、保護基の解離によってキレート剤内の共有結合がはずれ低親和性(Kd = 5-300 nM)となり、カルシウムイオンを放出する。しかし解離したキレーターは低親和性ながらも結合能(Kd = 0.006-3 mM)を有すること、光解離しなかったケージドカルシウムは放出されたカルシウムイオンと速やかに結合するため、カルシウムイオン濃度の時空間制御法には、注意を払う必要がある[1]。一方で全視野照射によって細胞全体にステップ状の活性上昇を与えることも可能であるため、通常では計測困難な、例えばカルシウムチャネル直下で起こる一過的なカルシウム濃度上昇による細胞内現象を、細胞全体の均一な濃度上昇によって誘導することが可能であり、カルシウム蛍光指示薬と併用することでカルシウム濃度上昇の定量計測が可能である。この方法は特に分泌現象の解明に役立っており[12]、またプルキンエ細胞の樹状突起においては、長期抑圧の誘導に必要な細胞内カルシウム濃度上昇の時空間パターンが詳細に明らかにされている[13]。2光子励起可能なケージドカルシウム、NDBF-EGTA (0.6 GM)やazid-1 (1 .4 GM)も報告されている(表)[1]。
ケージドペプチド・ケージドタンパク質
G-アクチンが最初にケージド化されたタンパク質であり[14]、コフィリンなどもケージド化されてそれを瞬時に光照射することでその機能が明らかにされている[15]。市販の試薬を使うことでケージド化することも可能である。
ケージドmRNA
ゼブラフィッシュにおいて、mRNAのリン酸骨格部位をBhc基し、これをマイクロインジェクションによりゼブラフィッシュに導入後、光照射部位特異的にタンパク質を発現させることが実現している(図)[16]。
投与方法
細胞内に負荷する場合には主としてガラスピペットからの負荷と、AM体のケージド試薬を細胞外液に投与する方法がある。前者の場合は、ある程度濃度を調整することが可能であるが、細胞内環境はガラスピペット内液による細胞内還流によって変化する。後者は、細胞外液に投与することで細胞膜を透過し、細胞内において脱エステル化される。非侵襲的に細胞内に負荷することができるが、その濃度を調節することや細胞内濃度を高くすることは難しい。マイクロインジェクションによって負荷する方法もあり、高濃度の試薬を細胞内環境の変化を最小にして導入することが可能であるが、熟練した実験技術を要する。ケージド神経伝達物質のような細胞外に投与するものに関しては、細胞外液に直接溶かすか、ガラスピペットなどを用いて局所的に投与する方法が用いられる。
光照射方法
一過的に強い光照射を行なうことに利点があるため、光源としては主にフラッシュランプやレーザーが用いられる。フラッシュランプ(パルスキセノン・水銀アークランプ)は安価で効率的に活性化可能である。2光子励起の場合には700-800 nmの波長の近赤外超短パルスレーザーが用いられ、高い開口数の対物レンズを通して集光する。照射時間の制御には機械式シャッター、より高速な制御を必要とする場合は、AOTF、EOMなどの光学素子が用いられる。
最近ではUV波長領域よりも長波長側の400 nm付近でも分解できるケージド試薬(Rubi-Glutamateなど)が開発されており[7]、可視光を用いても、より細胞障害が低く、より深部での光分解が可能になりつつある。また光可逆的に活性をオンオフできるケージド試薬の開発が期待されている。
- ↑ 1.0 1.1 1.2
Ellis-Davies, G.C. (2007).
Caged compounds: photorelease technology for control of cellular chemistry and physiology. Nature methods, 4(8), 619-28. [PubMed:17664946] [PMC] [WorldCat] [DOI] - ↑ 2.0 2.1
Furuta, T., & Suzuki, A. (2011).
[Use of caged compounds for the study of transient complexes]. Seikagaku. The Journal of Japanese Biochemical Society, 83(10), 966-74. [PubMed:22184890] [WorldCat] - ↑
Walker, J.W., McCray, J.A., & Hess, G.P. (1986).
Photolabile protecting groups for an acetylcholine receptor ligand. Synthesis and photochemistry of a new class of o-nitrobenzyl derivatives and their effects on receptor function. Biochemistry, 25(7), 1799-805. [PubMed:3707910] [WorldCat] [DOI] - ↑
Callaway, E.M., & Katz, L.C. (1993).
Photostimulation using caged glutamate reveals functional circuitry in living brain slices. Proceedings of the National Academy of Sciences of the United States of America, 90(16), 7661-5. [PubMed:7689225] [PMC] [WorldCat] [DOI] - ↑ 5.0 5.1
Matsuzaki, M., Ellis-Davies, G.C., Nemoto, T., Miyashita, Y., Iino, M., & Kasai, H. (2001).
Dendritic spine geometry is critical for AMPA receptor expression in hippocampal CA1 pyramidal neurons. Nature neuroscience, 4(11), 1086-92. [PubMed:11687814] [PMC] [WorldCat] [DOI] - ↑
Ellis-Davies, G.C., Matsuzaki, M., Paukert, M., Kasai, H., & Bergles, D.E. (2007).
4-Carboxymethoxy-5,7-dinitroindolinyl-Glu: an improved caged glutamate for expeditious ultraviolet and two-photon photolysis in brain slices. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(25), 6601-4. [PubMed:17581946] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1
Fino, E., Araya, R., Peterka, D.S., Salierno, M., Etchenique, R., & Yuste, R. (2009).
RuBi-Glutamate: Two-Photon and Visible-Light Photoactivation of Neurons and Dendritic spines. Frontiers in neural circuits, 3, 2. [PubMed:19506708] [PMC] [WorldCat] [DOI] - ↑
Matsuzaki, M., Honkura, N., Ellis-Davies, G.C., & Kasai, H. (2004).
Structural basis of long-term potentiation in single dendritic spines. Nature, 429(6993), 761-6. [PubMed:15190253] [PMC] [WorldCat] [DOI] - ↑
Matsuzaki, M., Hayama, T., Kasai, H., & Ellis-Davies, G.C.R. (2010).
Two-photon uncaging of gamma-aminobutyric acid in intact brain tissue. Nature chemical biology, 6(4), 255-257. [PubMed:20173751] [PMC] [WorldCat] [DOI] - ↑
Kaplan, J.H., Forbush, B., & Hoffman, J.F. (1978).
Rapid photolytic release of adenosine 5'-triphosphate from a protected analogue: utilization by the Na:K pump of human red blood cell ghosts. Biochemistry, 17(10), 1929-35. [PubMed:148906] [WorldCat] [DOI] - ↑
Engels, J., & Schlaeger, E.J. (1977).
Synthesis, structure, and reactivity of adenosine cyclic 3',5'-phosphate benzyl triesters. Journal of medicinal chemistry, 20(7), 907-11. [PubMed:195057] [WorldCat] [DOI] - ↑
Kasai, H. (1999).
Comparative biology of Ca2+-dependent exocytosis: implications of kinetic diversity for secretory function. Trends in neurosciences, 22(2), 88-93. [PubMed:10092049] [WorldCat] [DOI] - ↑
Tanaka, K., Khiroug, L., Santamaria, F., Doi, T., Ogasawara, H., Ellis-Davies, G.C., ..., & Augustine, G.J. (2007).
Ca2+ requirements for cerebellar long-term synaptic depression: role for a postsynaptic leaky integrator. Neuron, 54(5), 787-800. [PubMed:17553426] [WorldCat] [DOI] - ↑
Marriott, G. (1994).
Caged protein conjugates and light-directed generation of protein activity: preparation, photoactivation, and spectroscopic characterization of caged G-actin conjugates. Biochemistry, 33(31), 9092-7. [PubMed:8049211] [WorldCat] [DOI] - ↑
Ghosh, M., Song, X., Mouneimne, G., Sidani, M., Lawrence, D.S., & Condeelis, J.S. (2004).
Cofilin promotes actin polymerization and defines the direction of cell motility. Science (New York, N.Y.), 304(5671), 743-6. [PubMed:15118165] [WorldCat] [DOI] - ↑
Ando, H., Furuta, T., Tsien, R.Y., & Okamoto, H. (2001).
Photo-mediated gene activation using caged RNA/DNA in zebrafish embryos. Nature genetics, 28(4), 317-25. [PubMed:11479592] [WorldCat] [DOI]