「シナプトタグミン」の版間の差分
細編集の要約なし |
Yasunorimori (トーク | 投稿記録) |
||
| (3人の利用者による、間の9版が非表示) | |||
| 4行目: | 4行目: | ||
<font size="+1">[http://researchmap.jp/read0210534 福田 光則]</font><br> | <font size="+1">[http://researchmap.jp/read0210534 福田 光則]</font><br> | ||
''東北大学 大学院生命科学研究科 生命機能科学専攻''<br> | ''東北大学 大学院生命科学研究科 生命機能科学専攻''<br> | ||
DOI XXXX/XXXX 原稿受付日:2012年5月9日 原稿完成日:XXXX年X月X日<br> | |||
担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | 担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | ||
</div> | </div> | ||
| 11行目: | 11行目: | ||
| Symbol = C2 | | Symbol = C2 | ||
| Name = Human Synaptotagmin 1 C2 domains. | | Name = Human Synaptotagmin 1 C2 domains. | ||
| image = | | image = Synaptotagmin_C2_domain.png | ||
| width = 200 | | width = 200 | ||
| caption = | | caption = Human Synaptotagmin 1 C2A and C2B domains. Based on 2R83. | ||
| Pfam = PF00168 | | Pfam = PF00168 | ||
| InterPro = IPR000008 | | InterPro = IPR000008 | ||
| 25行目: | 25行目: | ||
| PDB = {{PDB3|1a25}}B:173-260 {{PDB3|1bci}}A:20-106 {{PDB3|1byn}}A:158-244 {{PDB3|1cjy}}A:20-106 {{PDB3|1djg}}B:631-720 {{PDB3|1djh}}B:631-720 {{PDB3|1dji}}B:631-720 {{PDB3|1djw}}B:631-720 {{PDB3|1djx}}A:631-720 {{PDB3|1djy}}A:631-720 {{PDB3|1djz}}B:631-720 {{PDB3|1dqv}}A:314-400 {{PDB3|1dsy}}A:173-260 {{PDB3|1gmi}}A:8-99 {{PDB3|1k5w}}A:289-377 {{PDB3|1qas}}B:631-720 {{PDB3|1qat}}B:631-720 {{PDB3|1rh8}}A:4654-4752 {{PDB3|1rlw}}A:20-106 {{PDB3|1tjm}}A:289-377 {{PDB3|1tjx}}A:289-377 {{PDB3|1ugk}}A:170-258 {{PDB3|1uov}}A:289-377 {{PDB3|1uow}}A:289-377 {{PDB3|1v27}}A:822-913 {{PDB3|1w15}}A:304-392 {{PDB3|1w16}}A:304-392 {{PDB3|1wfj}}A:6-87 {{PDB3|1wfm}}A:189-259 {{PDB3|2b3r}}A:1574-1662 {{PDB3|2bwq}}A:760-851 {{PDB3|2isd}}B:631-720 {{PDB3|3rpb}}A:557-645 | | PDB = {{PDB3|1a25}}B:173-260 {{PDB3|1bci}}A:20-106 {{PDB3|1byn}}A:158-244 {{PDB3|1cjy}}A:20-106 {{PDB3|1djg}}B:631-720 {{PDB3|1djh}}B:631-720 {{PDB3|1dji}}B:631-720 {{PDB3|1djw}}B:631-720 {{PDB3|1djx}}A:631-720 {{PDB3|1djy}}A:631-720 {{PDB3|1djz}}B:631-720 {{PDB3|1dqv}}A:314-400 {{PDB3|1dsy}}A:173-260 {{PDB3|1gmi}}A:8-99 {{PDB3|1k5w}}A:289-377 {{PDB3|1qas}}B:631-720 {{PDB3|1qat}}B:631-720 {{PDB3|1rh8}}A:4654-4752 {{PDB3|1rlw}}A:20-106 {{PDB3|1tjm}}A:289-377 {{PDB3|1tjx}}A:289-377 {{PDB3|1ugk}}A:170-258 {{PDB3|1uov}}A:289-377 {{PDB3|1uow}}A:289-377 {{PDB3|1v27}}A:822-913 {{PDB3|1w15}}A:304-392 {{PDB3|1w16}}A:304-392 {{PDB3|1wfj}}A:6-87 {{PDB3|1wfm}}A:189-259 {{PDB3|2b3r}}A:1574-1662 {{PDB3|2bwq}}A:760-851 {{PDB3|2isd}}B:631-720 {{PDB3|3rpb}}A:557-645 | ||
}} | }} | ||
英語名:Synaptotagmin 独:Synaptotagmine | |||
{{box | {{box | ||
| 38行目: | 38行目: | ||
これらの過程の中で、特にシナプス小胞と細胞膜の融合は細胞外からの[[カルシウム]]イオン流入によって厳密に制御されていることから、シナプス小胞上にはカルシウムイオン上昇を感知するカルシウムセンサー(カルシウムイオンを結合し膜融合を促進する分子で、膜融合の装置そのものではない)の存在が提唱されてきた<ref name=ref8><pubmed>11399430</pubmed></ref>。 | これらの過程の中で、特にシナプス小胞と細胞膜の融合は細胞外からの[[カルシウム]]イオン流入によって厳密に制御されていることから、シナプス小胞上にはカルシウムイオン上昇を感知するカルシウムセンサー(カルシウムイオンを結合し膜融合を促進する分子で、膜融合の装置そのものではない)の存在が提唱されてきた<ref name=ref8><pubmed>11399430</pubmed></ref>。 | ||
シナプトタグミン1は1981年にシナプス小胞や内[[分泌]]細胞の[[有芯小胞]]上に豊富に存在する分子量65,000のシナプス小胞抗原タンパク質(p65)として報告され<ref name=ref9><pubmed>7298720</pubmed></ref>、1990年にその構造が明らかにされた<ref name=ref1><pubmed>2333096</pubmed></ref>。遺伝学、生化学などを駆使した近年の目覚ましい研究成果により、現在ではシナプス小胞上に存在するシナプトタグミン1分子が主要なカルシウムセンサー(唯一ではなく、主に低親和性カルシウムセンサーとして機能)であると考えられている<ref name=ref4><pubmed>15217342</pubmed></ref><ref name=ref5></ref><ref name=ref6></ref><ref name=ref7><pubmed>18275379</pubmed></ref>。 | シナプトタグミン1は1981年にシナプス小胞や内[[分泌]]細胞の[[有芯小胞]]上に豊富に存在する分子量65,000のシナプス小胞抗原タンパク質(p65)として報告され<ref name=ref9><pubmed>7298720</pubmed></ref>、1990年にその構造が明らかにされた<ref name=ref1><pubmed>2333096</pubmed></ref>。遺伝学、生化学などを駆使した近年の目覚ましい研究成果により、現在ではシナプス小胞上に存在するシナプトタグミン1分子が主要なカルシウムセンサー(唯一ではなく、主に低親和性カルシウムセンサーとして機能)であると考えられている<ref name=ref4><pubmed>15217342</pubmed></ref><ref name=ref5>'''Fukuda, M.'''<br>Molecular mechanism of Exocytosis.<br>Landes Bioscience, Austin, TX, (2006) 42-61</ref><ref name=ref6><pubmed>16698267</pubmed></ref><ref name=ref7><pubmed>18275379</pubmed></ref>。 | ||
また、シナプス小胞以外のカルシウム依存的な小胞輸送過程に他のシナプトタグミンアイソフォームの関与も相次いで報告され、シナプトタグミンファミリーがかなり普遍的なカルシウムセンサーではないかという概念が定着しつつある。 | また、シナプス小胞以外のカルシウム依存的な小胞輸送過程に他のシナプトタグミンアイソフォームの関与も相次いで報告され、シナプトタグミンファミリーがかなり普遍的なカルシウムセンサーではないかという概念が定着しつつある。 | ||
| 46行目: | 46行目: | ||
[[image:シナプトタグミン図2.jpg|thumb|300px|'''図2 シナプトタグミンの構造'''<br>シナプトタグミンはN末端側に膜貫通領域を持つ1回膜貫通型の膜タンパク質で、C末端側の細胞質領域にはC2領域と呼ばれるタンパク質モチーフを2つ持っている(N末端側から、内腔領域、膜貫通領域、スペーサー領域、C2A領域、C2B領域と命名)。]] | [[image:シナプトタグミン図2.jpg|thumb|300px|'''図2 シナプトタグミンの構造'''<br>シナプトタグミンはN末端側に膜貫通領域を持つ1回膜貫通型の膜タンパク質で、C末端側の細胞質領域にはC2領域と呼ばれるタンパク質モチーフを2つ持っている(N末端側から、内腔領域、膜貫通領域、スペーサー領域、C2A領域、C2B領域と命名)。]] | ||
シナプトタグミンはN末端側に膜貫通領域を持つ1回膜貫通型の膜タンパク質で、C末端側の細胞質領域にはC2領域と呼ばれる[[プロテインキナーゼC]] | シナプトタグミンはN末端側に膜貫通領域を持つ1回膜貫通型の膜タンパク質で、C末端側の細胞質領域にはC2領域と呼ばれる[[プロテインキナーゼC]]のC2調節領域に由来するタンパク質モチーフを2つ持っている(N末端側から、内腔領域、膜貫通領域、スペーサー領域、C2A領域、C2B領域と命名)(図2)。 | ||
==ファミリー== | ==ファミリー== | ||
[[image:シナプトタグミン図3.jpg|thumb|300px|'''図3 シナプトタグミンファミリーの系統樹'''<br>CLUSTALWプログラムにより作成したシナプトタグミン1から15までの系統樹を示す。シナプトタグミンファミリーはアミノ酸配列の相同性からシナプトタグミン1/2/9(赤)、シナプトタグミン4/11(緑)、シナプトタグミン3/5/6/10(青)、およびそれ以外のシナプトタグミンに分類される。カルシウム結合能を持つアイソフォームを青色の四角で囲った。なお、シナプトタグミン4はカルシウム非結合型に分類されることが多いが、アストロサイトなど一部の細胞でカルシウムセンサーとして機能することが報告されている(点線の四角)。]] | [[image:シナプトタグミン図3.jpg|thumb|300px|'''図3 シナプトタグミンファミリーの系統樹'''<br>CLUSTALWプログラムにより作成したシナプトタグミン1から15までの系統樹を示す。シナプトタグミンファミリーはアミノ酸配列の相同性からシナプトタグミン1/2/9(赤)、シナプトタグミン4/11(緑)、シナプトタグミン3/5/6/10(青)、およびそれ以外のシナプトタグミンに分類される。カルシウム結合能を持つアイソフォームを青色の四角で囲った。なお、シナプトタグミン4はカルシウム非結合型に分類されることが多いが、アストロサイトなど一部の細胞でカルシウムセンサーとして機能することが報告されている(点線の四角)。]] | ||
ほ乳類には少なくとも17種類のアイソフォームが存在し、このうち[[シナプトタグミン1]], [[シナプトタグミン4|4]], [[シナプトタグミン7|7]], [[シナプトタグミン12|12]], [[シナプトタグミン14|14]]は[[ショウジョウバエ]]から[[wikipedia:ja:ほ乳類|ほ乳類]]に至るまで進化的に保存されている<ref name=ref2><pubmed>12801916</pubmed></ref><ref name=ref3><pubmed>20078875</pubmed></ref>。シナプトタグミンファミリーはアミノ酸配列の相同性からシナプトタグミン1/2/9、シナプトタグミン4/11、シナプトタグミン3/5/6/10、およびそれ以外のシナプトタグミンに分類される<ref name=ref10><pubmed>10531343</pubmed></ref>(図3)。なお、[[シナプトタグミン16]](元々の名称はStrep14)および[[シナプトタグミン17]](元々の名称はB/K)は膜貫通領域が欠損しているため、厳密にはシナプトタグミンファミリーの範疇には属さない<ref name=ref2><pubmed>12801916</pubmed></ref> | ほ乳類には少なくとも17種類のアイソフォームが存在し、このうち[[シナプトタグミン1]], [[シナプトタグミン4|4]], [[シナプトタグミン7|7]], [[シナプトタグミン12|12]], [[シナプトタグミン14|14]]は[[ショウジョウバエ]]から[[wikipedia:ja:ほ乳類|ほ乳類]]に至るまで進化的に保存されている<ref name=ref2><pubmed>12801916</pubmed></ref><ref name=ref3><pubmed>20078875</pubmed></ref>。シナプトタグミンファミリーはアミノ酸配列の相同性からシナプトタグミン1/2/9、シナプトタグミン4/11、シナプトタグミン3/5/6/10、およびそれ以外のシナプトタグミンに分類される<ref name=ref10><pubmed>10531343</pubmed></ref>(図3)。なお、[[シナプトタグミン16]](元々の名称はStrep14)および[[シナプトタグミン17]](元々の名称はB/K)は膜貫通領域が欠損しているため、厳密にはシナプトタグミンファミリーの範疇には属さない<ref name=ref2><pubmed>12801916</pubmed></ref>。アミノ酸の相同性とは別に、カルシウム結合能の有無で機能的にカルシウム結合型とカルシウム非結合型に分類されることもある(図3)。シナプトタグミンファミリー間で機能領域と考えられているC2A領域およびC2B領域は高度に保存されているが、他の領域(内腔領域、膜貫通領域およびスペーサー領域)ではほとんど相同性を示さない。シナプトタグミン1, [[シナプトタグミン2|2]]では、細胞外に位置する内腔領域で[[N結合型糖鎖]]および[[O結合型糖鎖]]の修飾を受けている。また、多くのアイソフォームで膜貫通領域の近傍で[[アシル化]]による修飾([[システイン]]残基への[[脂肪酸]]の付加)を受け、オリゴマー形成が促進される<ref name=ref9><pubmed>11514560</pubmed></ref>。なお、シナプトタグミン3/5/6/10はN末端側の内腔領域に保存されたシステイン残基を持ち、ジスルフィド結合を介してオリゴマーを形成する<ref name=ref10><pubmed>10531343</pubmed></ref>。シナプトタグミン1の二つのC2領域はアミノ酸レベルで40%以上の相同性を示すため、基本的には同様な立体構造を取り(8本の[[wikipedia:ja:βストランド|βストランド]]と3本のカルシウム結合ループにより構成)共にカルシウム結合能を示すが<ref name=ref11><pubmed>7697723</pubmed></ref><ref name=ref12><pubmed>11754837</pubmed></ref>、互いに異なる生化学的性質も示す。一例を挙げると、C2B領域にはカルシウム非依存的に[[イノシトールポリリン酸]]、[[アダプター複合体]]AP-2、[[ニューレキシン]](neurexin)などが結合し、またカルシウム依存的にC2B領域同士が結合し多量体を形成するが<ref name=ref13><pubmed>7961887</pubmed></ref><ref name=ref14><pubmed>9830048</pubmed></ref>、これらの性質はC2A領域には見られない(図2)。カルシウム依存的にC2領域に結合する分子とシナプトタグミン1の結合に必要なカルシウム濃度は5-100μMであり、この濃度は神経細胞で開口放出に必要とされるカルシウムイオン濃度とほぼ一致している<ref name=ref8><pubmed>11399430</pubmed></ref>。 | ||
なお、シナプトタグミンファミリーと同様にC末端側に2つのC2領域を持つタンパク質ファミリーとして[[Doc2]]/[[rabphilin]]ファミリーやシナプトタグミン様タンパク質(synaptotagmin-like protein, Slp)ファミリーが知られており、一部のものではシナプトタグミンとは異なるタイプのカルシウムセンサー(神経伝達物質放出の際の高親和性カルシウムセンサーなど)としての機能が提唱されている<ref name=ref16><pubmed>18726178</pubmed></ref><ref name=ref17><pubmed> 20150444</pubmed></ref>。 | なお、シナプトタグミンファミリーと同様にC末端側に2つのC2領域を持つタンパク質ファミリーとして[[Doc2]]/[[rabphilin]]ファミリーやシナプトタグミン様タンパク質(synaptotagmin-like protein, Slp)ファミリーが知られており、一部のものではシナプトタグミンとは異なるタイプのカルシウムセンサー(神経伝達物質放出の際の高親和性カルシウムセンサーなど)としての機能が提唱されている<ref name=ref16><pubmed>18726178</pubmed></ref><ref name=ref17><pubmed> 20150444</pubmed></ref>。 | ||
| 69行目: | 65行目: | ||
|style="background-color:#d3d3d3; text-align:center" |細胞内局在 | |style="background-color:#d3d3d3; text-align:center" |細胞内局在 | ||
|- | |- | ||
| | |シナプトタグミン 1 | ||
| | |大脳、嗅球などの神経細胞 | ||
| | |シナプス小胞、成長円錐小胞 | ||
|- | |- | ||
| | |シナプトタグミン 2 | ||
| | |小脳、脳幹などの神経細胞 | ||
|シナプス小胞 | |シナプス小胞 | ||
|- | |- | ||
| | |シナプトタグミン 4 | ||
| | |脳組織全般の神経細胞、アストロサイト(グリア細胞) | ||
| | |ゴルジ体、有芯小胞 | ||
|- | |- | ||
| | |シナプトタグミン 7 | ||
| | |脳組織全般、交感神経細胞 | ||
| | |前シナプス膜、リソソーム | ||
|- | |- | ||
| | |シナプトタグミン 9 | ||
| | |大脳辺縁系、線条体の神経細胞 | ||
|シナプス小胞、有芯小胞 | |シナプス小胞、有芯小胞 | ||
|- | |- | ||
| | |シナプトタグミン 10 | ||
|嗅球の神経細胞 | |嗅球の神経細胞 | ||
|有芯小胞 | |有芯小胞 | ||
|- | |- | ||
| | |シナプトタグミン 12 | ||
|脳組織全般 | |脳組織全般 | ||
|シナプス小胞 | |シナプス小胞 | ||
|- | |- | ||
|} | |} | ||
==機能== | ==機能== | ||
| 108行目: | 103行目: | ||
これに対して、C2B領域はシナプス小胞の融合促進だけではなく<ref name=ref26><pubmed>12110842</pubmed></ref><ref name=ref27><pubmed>15456828</pubmed></ref>、シナプス小胞の[[エンドサイトーシス]]やドッキングなどの過程<ref name=ref28><pubmed>11114192</pubmed></ref><ref name=ref29><pubmed>19716167</pubmed></ref>にも関与するものと考えられている。例えば、[[wikipedia:ja:ヤリイカ|ヤリイカ]]巨大[[軸索]]ではC2B領域に対する機能阻害抗体の導入により、シナプス小胞の融合過程には全く影響がなく、シナプス小胞のリサイクリングの過程が特異的に阻害される(恐らくはAP-2との結合を阻害)<ref name=ref30><pubmed>15591349</pubmed></ref>。一方、C2Bドメインに特異的に結合するイノシトールポリリン酸([[イノシトール1,3,4,5-四リン酸]](IP<SUB>4</SUB>)など)をシナプス前部に導入すると、C2B領域に結合することによりシナプス小胞の融合過程が顕著に阻害される<ref name=ref31><pubmed>7809161</pubmed></ref>。 | これに対して、C2B領域はシナプス小胞の融合促進だけではなく<ref name=ref26><pubmed>12110842</pubmed></ref><ref name=ref27><pubmed>15456828</pubmed></ref>、シナプス小胞の[[エンドサイトーシス]]やドッキングなどの過程<ref name=ref28><pubmed>11114192</pubmed></ref><ref name=ref29><pubmed>19716167</pubmed></ref>にも関与するものと考えられている。例えば、[[wikipedia:ja:ヤリイカ|ヤリイカ]]巨大[[軸索]]ではC2B領域に対する機能阻害抗体の導入により、シナプス小胞の融合過程には全く影響がなく、シナプス小胞のリサイクリングの過程が特異的に阻害される(恐らくはAP-2との結合を阻害)<ref name=ref30><pubmed>15591349</pubmed></ref>。一方、C2Bドメインに特異的に結合するイノシトールポリリン酸([[イノシトール1,3,4,5-四リン酸]](IP<SUB>4</SUB>)など)をシナプス前部に導入すると、C2B領域に結合することによりシナプス小胞の融合過程が顕著に阻害される<ref name=ref31><pubmed>7809161</pubmed></ref>。 | ||
さらに、C2B領域(特にC2Bエフェクタードメインと呼ばれるβ4ストランド上の塩基性クラスター<ref name= | さらに、C2B領域(特にC2Bエフェクタードメインと呼ばれるβ4ストランド上の塩基性クラスター<ref name=ref13><pubmed>7961887</pubmed></ref><ref name=ref14><pubmed>9830048</pubmed></ref>)はカルシウム刺激がないときには融合を抑制するようなクランプ的な機能を併せ持つと想定されており<ref name=ref32><pubmed>8990201</pubmed></ref><ref name=ref33><pubmed>21338883</pubmed></ref>、ショウジョウバエなどのシナプトタグミン1変異体では自発的な神経伝達物質放出が増大することが知られている<ref name=ref34><pubmed>12467593</pubmed></ref>。このようなC2B領域の機能の多様性は、C2B領域に複数のエフェクター結合領域が存在することに起因するものと考えられている<ref name=ref5>'''Fukuda, M.'''<br>Molecular mechanism of exocytosis.<br>Landes Bioscience, Austin, TX, (2006) 42-61</ref>。また、C2B領域は必ずしも単独で機能するのではなく、一部C2A領域と協調して小胞の融合を促進するモデルも提唱されている<ref name=ref35><pubmed>10811903</pubmed></ref><ref name=ref36><pubmed>15046725</pubmed></ref>。 | ||
シナプトタグミンによるカルシウム依存的な小胞融合の促進メカニズムとして現在最も有力な仮説は、膜の融合装置と考えられる[[SNAREタンパク質]]とシナプトタグミンとのカルシウム依存的な相互作用により小胞膜と細胞膜の融合が促進されるというモデルである。実際、精製したSNAREタンパク質を組み込んだ2種類のリポソーム([[v-SNARE]][[シナプトブレビン]]を組み込んだリポソームおよび[[t-SNARE]][[シンタキシン]]と[[SNAP-25]]を組み込んだリポソーム)にカルシウムイオンとシナプトタグミン1の細胞質領域を加えることにより2種類のリポソームの膜融合が顕著に促進される<ref name=ref37><pubmed>15044754</pubmed></ref>。一方、シナプトタグミンのC2領域のカルシウム依存的なリン脂質の結合が小胞の融合を促進するという仮説や、C2B領域同士のカルシウム依存的なオリゴマー化がシナプス小胞と細胞膜の融合により生じた孔を拡大させるという仮説も提唱されている<ref name=ref38><pubmed>12931189</pubmed></ref>。 | シナプトタグミンによるカルシウム依存的な小胞融合の促進メカニズムとして現在最も有力な仮説は、膜の融合装置と考えられる[[SNAREタンパク質]]とシナプトタグミンとのカルシウム依存的な相互作用により小胞膜と細胞膜の融合が促進されるというモデルである。実際、精製したSNAREタンパク質を組み込んだ2種類のリポソーム([[v-SNARE]][[シナプトブレビン]]を組み込んだリポソームおよび[[t-SNARE]][[シンタキシン]]と[[SNAP-25]]を組み込んだリポソーム)にカルシウムイオンとシナプトタグミン1の細胞質領域を加えることにより2種類のリポソームの膜融合が顕著に促進される<ref name=ref37><pubmed>15044754</pubmed></ref>。一方、シナプトタグミンのC2領域のカルシウム依存的なリン脂質の結合が小胞の融合を促進するという仮説や、C2B領域同士のカルシウム依存的なオリゴマー化がシナプス小胞と細胞膜の融合により生じた孔を拡大させるという仮説も提唱されている<ref name=ref38><pubmed>12931189</pubmed></ref>。 | ||
2013年8月21日 (水) 19:20時点における版
森 靖典
University of Bristol, UK
福田 光則
東北大学 大学院生命科学研究科 生命機能科学専攻
DOI XXXX/XXXX 原稿受付日:2012年5月9日 原稿完成日:XXXX年X月X日
担当編集委員:林 康紀(独立行政法人理化学研究所 脳科学総合研究センター)
| Human Synaptotagmin 1 C2 domains. | |||||||||
|---|---|---|---|---|---|---|---|---|---|
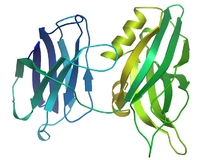 Human Synaptotagmin 1 C2A and C2B domains. Based on 2R83. | |||||||||
| Identifiers | |||||||||
| Symbol | C2 | ||||||||
| Pfam | PF00168 | ||||||||
| InterPro | IPR000008 | ||||||||
| SMART | C2 | ||||||||
| PROSITE | PDOC00380 | ||||||||
| SCOP | 1qas | ||||||||
| SUPERFAMILY | 1qas | ||||||||
| OPM superfamily | 47 | ||||||||
| OPM protein | 1ugk | ||||||||
| CDD | cd00030 | ||||||||
| |||||||||
英語名:Synaptotagmin 独:Synaptotagmine
シナプトタグミンはシナプス小胞上に豊富に存在するカルシウム・リン脂質結合分子として同定された膜タンパク質である[1]。シナプトタグミンは植物・動物を含め様々な生物種に存在することが現在では知られており、ヒトやマウスでは17種類のアイソフォームの存在が報告されている[2][3]。N末端側に膜貫通領域を1カ所持ち、C末端側の細胞質領域に存在する二つのC2領域でカルシウムイオンやリン脂質を結合することが知られている[4][5][6][7]。このカルシウムイオンの結合能を利用して、シナプトタグミンファミリーはシナプス小胞からの神経伝達物質放出をはじめ、開口放出(エクソサイトーシス:exocytosis)の際の主要な「カルシウムセンサー」として機能するものと考えられている。
シナプトタグミンとは
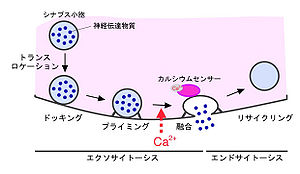
神経伝達物質の放出は、シナプス小胞が細胞膜の近傍まで運ばれるトランスロケーションのステップ、標的となる膜に結合するドッキングのステップ、準備期間としてのプライミングのステップ、そして、融合のステップより構成されている(これらのステップを総称してエクソサイトーシスと呼ぶ)。融合した小胞はエンドサイトーシスにより細胞内に回収され、再利用される(リサイクリングのステップ)。融合のステップは細胞内カルシウム濃度の上昇に伴って起こることから、何らかのカルシウムセンサーの存在が提唱されている。
神経細胞間の情報伝達は、主にシナプス部における神経伝達物質のやり取りによって行われている。神経伝達物質はシナプス前部に存在するシナプス小胞に貯蔵されており、開口放出によってシナプス間隙へと放出される。この開口放出機構は、小胞のシナプス前部膜付近への移動(トランスロケーション:translocation)、細胞膜との繋留/接着(テザリング/ドッキング:tethering/docking)、プライミングと呼ばれる融合可能な状態への準備(priming)を経て、小胞膜と細胞膜の融合(fusion)に至る一連の過程から構成されている(図1)。開口放出によって細胞膜に移行した小胞のタンパク質は、その後エンドサイトーシスによって選択的に回収(リサイクリング:recycling)される。
これらの過程の中で、特にシナプス小胞と細胞膜の融合は細胞外からのカルシウムイオン流入によって厳密に制御されていることから、シナプス小胞上にはカルシウムイオン上昇を感知するカルシウムセンサー(カルシウムイオンを結合し膜融合を促進する分子で、膜融合の装置そのものではない)の存在が提唱されてきた[8]。
シナプトタグミン1は1981年にシナプス小胞や内分泌細胞の有芯小胞上に豊富に存在する分子量65,000のシナプス小胞抗原タンパク質(p65)として報告され[9]、1990年にその構造が明らかにされた[1]。遺伝学、生化学などを駆使した近年の目覚ましい研究成果により、現在ではシナプス小胞上に存在するシナプトタグミン1分子が主要なカルシウムセンサー(唯一ではなく、主に低親和性カルシウムセンサーとして機能)であると考えられている[4][5][6][7]。
また、シナプス小胞以外のカルシウム依存的な小胞輸送過程に他のシナプトタグミンアイソフォームの関与も相次いで報告され、シナプトタグミンファミリーがかなり普遍的なカルシウムセンサーではないかという概念が定着しつつある。
構造
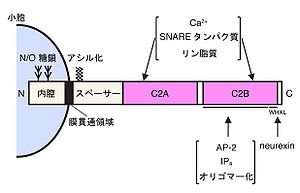
シナプトタグミンはN末端側に膜貫通領域を持つ1回膜貫通型の膜タンパク質で、C末端側の細胞質領域にはC2領域と呼ばれるタンパク質モチーフを2つ持っている(N末端側から、内腔領域、膜貫通領域、スペーサー領域、C2A領域、C2B領域と命名)。
シナプトタグミンはN末端側に膜貫通領域を持つ1回膜貫通型の膜タンパク質で、C末端側の細胞質領域にはC2領域と呼ばれるプロテインキナーゼCのC2調節領域に由来するタンパク質モチーフを2つ持っている(N末端側から、内腔領域、膜貫通領域、スペーサー領域、C2A領域、C2B領域と命名)(図2)。
ファミリー
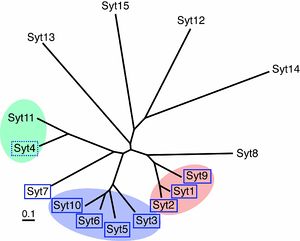
CLUSTALWプログラムにより作成したシナプトタグミン1から15までの系統樹を示す。シナプトタグミンファミリーはアミノ酸配列の相同性からシナプトタグミン1/2/9(赤)、シナプトタグミン4/11(緑)、シナプトタグミン3/5/6/10(青)、およびそれ以外のシナプトタグミンに分類される。カルシウム結合能を持つアイソフォームを青色の四角で囲った。なお、シナプトタグミン4はカルシウム非結合型に分類されることが多いが、アストロサイトなど一部の細胞でカルシウムセンサーとして機能することが報告されている(点線の四角)。
ほ乳類には少なくとも17種類のアイソフォームが存在し、このうちシナプトタグミン1, 4, 7, 12, 14はショウジョウバエからほ乳類に至るまで進化的に保存されている[2][3]。シナプトタグミンファミリーはアミノ酸配列の相同性からシナプトタグミン1/2/9、シナプトタグミン4/11、シナプトタグミン3/5/6/10、およびそれ以外のシナプトタグミンに分類される[10](図3)。なお、シナプトタグミン16(元々の名称はStrep14)およびシナプトタグミン17(元々の名称はB/K)は膜貫通領域が欠損しているため、厳密にはシナプトタグミンファミリーの範疇には属さない[2]。アミノ酸の相同性とは別に、カルシウム結合能の有無で機能的にカルシウム結合型とカルシウム非結合型に分類されることもある(図3)。シナプトタグミンファミリー間で機能領域と考えられているC2A領域およびC2B領域は高度に保存されているが、他の領域(内腔領域、膜貫通領域およびスペーサー領域)ではほとんど相同性を示さない。シナプトタグミン1, 2では、細胞外に位置する内腔領域でN結合型糖鎖およびO結合型糖鎖の修飾を受けている。また、多くのアイソフォームで膜貫通領域の近傍でアシル化による修飾(システイン残基への脂肪酸の付加)を受け、オリゴマー形成が促進される[9]。なお、シナプトタグミン3/5/6/10はN末端側の内腔領域に保存されたシステイン残基を持ち、ジスルフィド結合を介してオリゴマーを形成する[10]。シナプトタグミン1の二つのC2領域はアミノ酸レベルで40%以上の相同性を示すため、基本的には同様な立体構造を取り(8本のβストランドと3本のカルシウム結合ループにより構成)共にカルシウム結合能を示すが[11][12]、互いに異なる生化学的性質も示す。一例を挙げると、C2B領域にはカルシウム非依存的にイノシトールポリリン酸、アダプター複合体AP-2、ニューレキシン(neurexin)などが結合し、またカルシウム依存的にC2B領域同士が結合し多量体を形成するが[13][14]、これらの性質はC2A領域には見られない(図2)。カルシウム依存的にC2領域に結合する分子とシナプトタグミン1の結合に必要なカルシウム濃度は5-100μMであり、この濃度は神経細胞で開口放出に必要とされるカルシウムイオン濃度とほぼ一致している[8]。
なお、シナプトタグミンファミリーと同様にC末端側に2つのC2領域を持つタンパク質ファミリーとしてDoc2/rabphilinファミリーやシナプトタグミン様タンパク質(synaptotagmin-like protein, Slp)ファミリーが知られており、一部のものではシナプトタグミンとは異なるタイプのカルシウムセンサー(神経伝達物質放出の際の高親和性カルシウムセンサーなど)としての機能が提唱されている[15][16]。
発現
神経系においてこれまで解析がなされている主なシナプトタグミンアイソフォームの脳組織における分布および細胞内局在を以下にまとめた(表1)
| アイソフォーム | 組織分布 | 細胞内局在 |
| シナプトタグミン 1 | 大脳、嗅球などの神経細胞 | シナプス小胞、成長円錐小胞 |
| シナプトタグミン 2 | 小脳、脳幹などの神経細胞 | シナプス小胞 |
| シナプトタグミン 4 | 脳組織全般の神経細胞、アストロサイト(グリア細胞) | ゴルジ体、有芯小胞 |
| シナプトタグミン 7 | 脳組織全般、交感神経細胞 | 前シナプス膜、リソソーム |
| シナプトタグミン 9 | 大脳辺縁系、線条体の神経細胞 | シナプス小胞、有芯小胞 |
| シナプトタグミン 10 | 嗅球の神経細胞 | 有芯小胞 |
| シナプトタグミン 12 | 脳組織全般 | シナプス小胞 |
機能
神経伝達物質放出
シナプトタグミン1ノックアウトマウスを用いた解析の結果、海馬神経細胞における開口放出のうちカルシウム依存的な活動電位と同調した速い放出(synchronous release)に重要であることが明らかとなった[17]。同様な活動電位と同調した速い放出成分の減少は、ショウジョウバエのシナプトタグミン1変異体でも観察されたことから[18]、シナプトタグミン1は活動電位と同調した低親和性のカルシウムセンサーとして機能すると一般的に考えられている。一方で、線虫やショウジョウバエのシナプトタグミン1変異体では開口放出の過程だけではなく、シナプス小胞のリサイクリングの過程にも異常があることが報告されており[19][20]、シナプトタグミン1が単なるカルシウムセンサーではなく、シナプス小胞輸送の様々なステップの制御にも関与する可能性が示唆されている。
このようなシナプトタグミン1の機能の多様性は、それぞれのC2領域の固有の機能と密接な関連があるものと考えられている。例えば、C2A領域のリン脂質結合能が減少している変異型シナプトタグミン1(R233Q)をノックインしたマウス由来の神経細胞では神経伝達物質の放出が抑制されるが[21]、逆にC2A領域のカルシウム依存的なシンタキシンへの結合が増加している優勢変異型シナプトタグミン1(D232N)をノックインしたマウス由来の神経細胞では神経伝達物質の放出が増加する[22]。一方で、C2A領域へのカルシウムイオン結合能は神経伝達物質放出に必須ではないという報告もあり混沌としているが[23]、シナプトタグミン1のC2A領域に対する機能阻害抗体によりシナプス小胞の融合過程が著しく阻害されることから[24]、C2A領域の機能はやはりシナプス小胞の融合促進に重要と考えられている。
これに対して、C2B領域はシナプス小胞の融合促進だけではなく[25][26]、シナプス小胞のエンドサイトーシスやドッキングなどの過程[27][28]にも関与するものと考えられている。例えば、ヤリイカ巨大軸索ではC2B領域に対する機能阻害抗体の導入により、シナプス小胞の融合過程には全く影響がなく、シナプス小胞のリサイクリングの過程が特異的に阻害される(恐らくはAP-2との結合を阻害)[29]。一方、C2Bドメインに特異的に結合するイノシトールポリリン酸(イノシトール1,3,4,5-四リン酸(IP4)など)をシナプス前部に導入すると、C2B領域に結合することによりシナプス小胞の融合過程が顕著に阻害される[30]。
さらに、C2B領域(特にC2Bエフェクタードメインと呼ばれるβ4ストランド上の塩基性クラスター[13][14])はカルシウム刺激がないときには融合を抑制するようなクランプ的な機能を併せ持つと想定されており[31][32]、ショウジョウバエなどのシナプトタグミン1変異体では自発的な神経伝達物質放出が増大することが知られている[33]。このようなC2B領域の機能の多様性は、C2B領域に複数のエフェクター結合領域が存在することに起因するものと考えられている[5]。また、C2B領域は必ずしも単独で機能するのではなく、一部C2A領域と協調して小胞の融合を促進するモデルも提唱されている[34][35]。
シナプトタグミンによるカルシウム依存的な小胞融合の促進メカニズムとして現在最も有力な仮説は、膜の融合装置と考えられるSNAREタンパク質とシナプトタグミンとのカルシウム依存的な相互作用により小胞膜と細胞膜の融合が促進されるというモデルである。実際、精製したSNAREタンパク質を組み込んだ2種類のリポソーム(v-SNAREシナプトブレビンを組み込んだリポソームおよびt-SNAREシンタキシンとSNAP-25を組み込んだリポソーム)にカルシウムイオンとシナプトタグミン1の細胞質領域を加えることにより2種類のリポソームの膜融合が顕著に促進される[36]。一方、シナプトタグミンのC2領域のカルシウム依存的なリン脂質の結合が小胞の融合を促進するという仮説や、C2B領域同士のカルシウム依存的なオリゴマー化がシナプス小胞と細胞膜の融合により生じた孔を拡大させるという仮説も提唱されている[37]。
シナプス小胞上での他のシナプトタグミンファミリーの機能
シナプトタグミン1以外にシナプス小胞上に存在するシナプトタグミンとしてはシナプトタグミン2, 9, 12などが報告されている[38]。このうちシナプトタグミン2およびシナプトタグミン9は、シナプトタグミン1とは脳内において異なる発現パターンを示す[39]。シナプトタグミン2は小脳や脳幹部での発現が高く、そのノックアウトマウスにおいては例えば神経筋接合部における活動電位に依存した放出過程に異常が生じる[40]。一方、シナプトタグミン9の神経系における発現パターンは大脳辺縁系や線条体などに限られており、そのノックアウトマウスにおいては線条体由来の神経細胞における活動電位に依存した放出過程に異常が生じる[39]。
シナプトタグミン2およびシナプトタグミン9は系統樹上シナプトタグミン1に最も近縁で同等の機能を有すると考えられており[41]、実際これらのシナプトタグミンの発現によりシナプトタグミン1を欠損する海馬神経細胞からの活動電位に依存した放出が回復することが示されている(ただし、シナプトタグミン1, 2, 9の間では放出速度に違いがある)[39]。シナプトタグミン12(元々の名称はSrg1)は脳組織に広範囲に発現しているが、カルシウムイオンの結合能力がなく、活動電位に依存した放出過程ではなく自発的放出(spontaneous release)の促進に関与することが報告されている[42]。
シナプス小胞輸送以外
シナプス小胞の輸送以外の神経機能に関わるシナプトタグミンファミリーとしては、シナプトタグミン4、7、10、14などが挙げられる。シナプトタグミン4の局在や機能に関してはこれまで様々な報告があるが、最近の知見ではシナプス小胞ではなくペプチド性分泌因子などの放出に関与する有芯小胞(LDCV: large dense-core vesicle)への局在が有力視されている[43]。例えば、視床下部におけるオキシトシンやバソプレシンの分泌[44][45]や海馬神経細胞における脳由来神経栄養因子(BDNF)の放出制御に関与することが明らかになっている[46]。
また、シナプトタグミン4は神経細胞以外にアストロサイトにも発現しており、アストロサイトからのグルタミン酸やATPの放出に関与することが報告されている[47]。さらに、ショウジョウバエにおいては、シナプトタグミン4はシナプス前部ではなくシナプス後部におけるカルシウムセンサーとして機能することが報告されている[48][49]。なお、シナプトタグミン4は動物種、細胞種やカルシウム濃度の条件によって開口放出を正に制御する場合と負に制御する場合があることから、その機能については今後さらなる解析が必要と考えられている[43]。
シナプトタグミン10も嗅球の神経細胞において有芯小胞に局在し、インスリン様成長因子1(IGF-1)の放出を制御することで嗅球の神経発生に関与することが最近明らかになっている[50]。シナプトタグミン7は海馬神経細胞におけるシナプス小胞の開口放出には関与しないが、交感神経細胞の神経突起の伸長過程を制御することが報告されている[51]。また、シナプトタグミン14のC2B領域のアミノ酸変異により遺伝性の脊髄小脳変性症が発症することから[52]、このアイソフォームの小脳発達過程での重要性が示唆されているが、詳細な機能は明らかになっていない。
他のシナプトタグミンアイソフォームの神経細胞における局在や機能に関しては現時点では不明であるが、海馬神経細胞に蛍光タンパク質を融合したシナプトタグミンアイソフォームを1つずつ発現させ、その機能部位の同定が現在試みられている[53]。それぞれのシナプトタグミンアイソフォームが神経系において独自の機能を果たしている可能性が高く、今後のさらなる機能解析が期待されている。
関連項目
参考文献
- ↑ 1.0 1.1
Perin, M.S., Fried, V.A., Mignery, G.A., Jahn, R., & Südhof, T.C. (1990).
Phospholipid binding by a synaptic vesicle protein homologous to the regulatory region of protein kinase C. Nature, 345(6272), 260-3. [PubMed:2333096] [WorldCat] [DOI] - ↑ 2.0 2.1 2.2
Fukuda, M. (2003).
Molecular cloning, expression, and characterization of a novel class of synaptotagmin (Syt XIV) conserved from Drosophila to humans. Journal of biochemistry, 133(5), 641-9. [PubMed:12801916] [WorldCat] [DOI] - ↑ 3.0 3.1
Craxton, M. (2010).
A manual collection of Syt, Esyt, Rph3a, Rph3al, Doc2, and Dblc2 genes from 46 metazoan genomes--an open access resource for neuroscience and evolutionary biology. BMC genomics, 11, 37. [PubMed:20078875] [PMC] [WorldCat] [DOI] - ↑ 4.0 4.1
Sudhof, T.C. (2004).
The synaptic vesicle cycle. Annual review of neuroscience, 27, 509-47. [PubMed:15217342] [WorldCat] [DOI] - ↑ 5.0 5.1 5.2 Fukuda, M.
Molecular mechanism of Exocytosis.
Landes Bioscience, Austin, TX, (2006) 42-61 引用エラー: 無効な<ref>タグ; name "ref5"が異なる内容で複数回定義されています - ↑ 6.0 6.1
Rizo, J., Chen, X., & Araç, D. (2006).
Unraveling the mechanisms of synaptotagmin and SNARE function in neurotransmitter release. Trends in cell biology, 16(7), 339-50. [PubMed:16698267] [WorldCat] [DOI] - ↑ 7.0 7.1
Chapman, E.R. (2008).
How does synaptotagmin trigger neurotransmitter release? Annual review of biochemistry, 77, 615-41. [PubMed:18275379] [WorldCat] [DOI] - ↑ 8.0 8.1
Augustine, G.J. (2001).
How does calcium trigger neurotransmitter release? Current opinion in neurobiology, 11(3), 320-6. [PubMed:11399430] [WorldCat] [DOI] - ↑ 9.0 9.1
Matthew, W.D., Tsavaler, L., & Reichardt, L.F. (1981).
Identification of a synaptic vesicle-specific membrane protein with a wide distribution in neuronal and neurosecretory tissue. The Journal of cell biology, 91(1), 257-69. [PubMed:7298720] [PMC] [WorldCat] [DOI] 引用エラー: 無効な<ref>タグ; name "ref9"が異なる内容で複数回定義されています - ↑ 10.0 10.1
Fukuda, M., Kanno, E., & Mikoshiba, K. (1999).
Conserved N-terminal cysteine motif is essential for homo- and heterodimer formation of synaptotagmins III, V, VI, and X. The Journal of biological chemistry, 274(44), 31421-7. [PubMed:10531343] [WorldCat] [DOI] - ↑
Sutton, R.B., Davletov, B.A., Berghuis, A.M., Südhof, T.C., & Sprang, S.R. (1995).
Structure of the first C2 domain of synaptotagmin I: a novel Ca2+/phospholipid-binding fold. Cell, 80(6), 929-38. [PubMed:7697723] [WorldCat] [DOI] - ↑
Fernandez, I., Araç, D., Ubach, J., Gerber, S.H., Shin, O., Gao, Y., ..., & Rizo, J. (2001).
Three-dimensional structure of the synaptotagmin 1 C2B-domain: synaptotagmin 1 as a phospholipid binding machine. Neuron, 32(6), 1057-69. [PubMed:11754837] [WorldCat] [DOI] - ↑ 13.0 13.1
Fukuda, M., Aruga, J., Niinobe, M., Aimoto, S., & Mikoshiba, K. (1994).
Inositol-1,3,4,5-tetrakisphosphate binding to C2B domain of IP4BP/synaptotagmin II. The Journal of biological chemistry, 269(46), 29206-11. [PubMed:7961887] [WorldCat] - ↑ 14.0 14.1
Chapman, E.R., Desai, R.C., Davis, A.F., & Tornehl, C.K. (1998).
Delineation of the oligomerization, AP-2 binding, and synprint binding region of the C2B domain of synaptotagmin. The Journal of biological chemistry, 273(49), 32966-72. [PubMed:9830048] [WorldCat] [DOI] - ↑
Fukuda, M. (2008).
Regulation of secretory vesicle traffic by Rab small GTPases. Cellular and molecular life sciences : CMLS, 65(18), 2801-13. [PubMed:18726178] [WorldCat] [DOI] - ↑
Groffen, A.J., Martens, S., Díez Arazola, R., Cornelisse, L.N., Lozovaya, N., de Jong, A.P., ..., & Verhage, M. (2010).
Doc2b is a high-affinity Ca2+ sensor for spontaneous neurotransmitter release. Science (New York, N.Y.), 327(5973), 1614-8. [PubMed:20150444] [PMC] [WorldCat] [DOI] - ↑
Littleton, J.T., Stern, M., Schulze, K., Perin, M., & Bellen, H.J. (1993).
Mutational analysis of Drosophila synaptotagmin demonstrates its essential role in Ca(2+)-activated neurotransmitter release. Cell, 74(6), 1125-34. [PubMed:8104705] [WorldCat] [DOI] - ↑
Geppert, M., Goda, Y., Hammer, R.E., Li, C., Rosahl, T.W., Stevens, C.F., & Südhof, T.C. (1994).
Synaptotagmin I: a major Ca2+ sensor for transmitter release at a central synapse. Cell, 79(4), 717-27. [PubMed:7954835] [WorldCat] [DOI] - ↑
Jorgensen, E.M., Hartwieg, E., Schuske, K., Nonet, M.L., Jin, Y., & Horvitz, H.R. (1995).
Defective recycling of synaptic vesicles in synaptotagmin mutants of Caenorhabditis elegans. Nature, 378(6553), 196-9. [PubMed:7477324] [WorldCat] [DOI] - ↑
Poskanzer, K.E., Marek, K.W., Sweeney, S.T., & Davis, G.W. (2003).
Synaptotagmin I is necessary for compensatory synaptic vesicle endocytosis in vivo. Nature, 426(6966), 559-63. [PubMed:14634669] [WorldCat] [DOI] - ↑
Fernández-Chacón, R., Königstorfer, A., Gerber, S.H., García, J., Matos, M.F., Stevens, C.F., ..., & Südhof, T.C. (2001).
Synaptotagmin I functions as a calcium regulator of release probability. Nature, 410(6824), 41-9. [PubMed:11242035] [WorldCat] [DOI] - ↑
Pang, Z.P., Shin, O.H., Meyer, A.C., Rosenmund, C., & Südhof, T.C. (2006).
A gain-of-function mutation in synaptotagmin-1 reveals a critical role of Ca2+-dependent soluble N-ethylmaleimide-sensitive factor attachment protein receptor complex binding in synaptic exocytosis. The Journal of neuroscience : the official journal of the Society for Neuroscience, 26(48), 12556-65. [PubMed:17135417] [PMC] [WorldCat] [DOI] - ↑
Robinson, I.M., Ranjan, R., & Schwarz, T.L. (2002).
Synaptotagmins I and IV promote transmitter release independently of Ca(2+) binding in the C(2)A domain. Nature, 418(6895), 336-40. [PubMed:12110845] [WorldCat] [DOI] - ↑
Mikoshiba, K., Fukuda, M., Moreira, J.E., Lewis, F.M., Sugimori, M., Niinobe, M., & Llinás, R. (1995).
Role of the C2A domain of synaptotagmin in transmitter release as determined by specific antibody injection into the squid giant synapse preterminal. Proceedings of the National Academy of Sciences of the United States of America, 92(23), 10703-7. [PubMed:7479868] [PMC] [WorldCat] [DOI] - ↑
Mackler, J.M., Drummond, J.A., Loewen, C.A., Robinson, I.M., & Reist, N.E. (2002).
The C(2)B Ca(2+)-binding motif of synaptotagmin is required for synaptic transmission in vivo. Nature, 418(6895), 340-4. [PubMed:12110842] [WorldCat] [DOI] - ↑
Nishiki, T., & Augustine, G.J. (2004).
Dual roles of the C2B domain of synaptotagmin I in synchronizing Ca2+-dependent neurotransmitter release. The Journal of neuroscience : the official journal of the Society for Neuroscience, 24(39), 8542-50. [PubMed:15456828] [PMC] [WorldCat] [DOI] - ↑
Fukuda, M., Moreira, J.E., Liu, V., Sugimori, M., Mikoshiba, K., & Llinás, R.R. (2000).
Role of the conserved WHXL motif in the C terminus of synaptotagmin in synaptic vesicle docking. Proceedings of the National Academy of Sciences of the United States of America, 97(26), 14715-9. [PubMed:11114192] [PMC] [WorldCat] [DOI] - ↑
de Wit, H., Walter, A.M., Milosevic, I., Gulyás-Kovács, A., Riedel, D., Sørensen, J.B., & Verhage, M. (2009).
Synaptotagmin-1 docks secretory vesicles to syntaxin-1/SNAP-25 acceptor complexes. Cell, 138(5), 935-46. [PubMed:19716167] [WorldCat] [DOI] - ↑
Llinás, R.R., Sugimori, M., Moran, K.A., Moreira, J.E., & Fukuda, M. (2004).
Vesicular reuptake inhibition by a synaptotagmin I C2B domain antibody at the squid giant synapse. Proceedings of the National Academy of Sciences of the United States of America, 101(51), 17855-60. [PubMed:15591349] [PMC] [WorldCat] [DOI] - ↑
Llinás, R., Sugimori, M., Lang, E.J., Morita, M., Fukuda, M., Niinobe, M., & Mikoshiba, K. (1994).
The inositol high-polyphosphate series blocks synaptic transmission by preventing vesicular fusion: a squid giant synapse study. Proceedings of the National Academy of Sciences of the United States of America, 91(26), 12990-3. [PubMed:7809161] [PMC] [WorldCat] [DOI] - ↑
Ohara-Imaizumi, M., Fukuda, M., Niinobe, M., Misonou, H., Ikeda, K., Murakami, T., ..., & Kumakura, K. (1997).
Distinct roles of C2A and C2B domains of synaptotagmin in the regulation of exocytosis in adrenal chromaffin cells. Proceedings of the National Academy of Sciences of the United States of America, 94(1), 287-91. [PubMed:8990201] [PMC] [WorldCat] [DOI] - ↑
Kochubey, O., & Schneggenburger, R. (2011).
Synaptotagmin increases the dynamic range of synapses by driving Ca²+-evoked release and by clamping a near-linear remaining Ca²+ sensor. Neuron, 69(4), 736-48. [PubMed:21338883] [WorldCat] [DOI] - ↑
Yoshihara, M., & Littleton, J.T. (2002).
Synaptotagmin I functions as a calcium sensor to synchronize neurotransmitter release. Neuron, 36(5), 897-908. [PubMed:12467593] [WorldCat] [DOI] - ↑
García, R.A., Forde, C.E., & Godwin, H.A. (2000).
Calcium triggers an intramolecular association of the C2 domains in synaptotagmin. Proceedings of the National Academy of Sciences of the United States of America, 97(11), 5883-8. [PubMed:10811903] [PMC] [WorldCat] [DOI] - ↑
Bai, J., Wang, C.T., Richards, D.A., Jackson, M.B., & Chapman, E.R. (2004).
Fusion pore dynamics are regulated by synaptotagmin*t-SNARE interactions. Neuron, 41(6), 929-42. [PubMed:15046725] [WorldCat] [DOI] - ↑
Tucker, W.C., Weber, T., & Chapman, E.R. (2004).
Reconstitution of Ca2+-regulated membrane fusion by synaptotagmin and SNAREs. Science (New York, N.Y.), 304(5669), 435-8. [PubMed:15044754] [WorldCat] [DOI] - ↑
Wang, C.T., Lu, J.C., Bai, J., Chang, P.Y., Martin, T.F., Chapman, E.R., & Jackson, M.B. (2003).
Different domains of synaptotagmin control the choice between kiss-and-run and full fusion. Nature, 424(6951), 943-7. [PubMed:12931189] [WorldCat] [DOI] - ↑
Takamori, S., Holt, M., Stenius, K., Lemke, E.A., Grønborg, M., Riedel, D., ..., & Jahn, R. (2006).
Molecular anatomy of a trafficking organelle. Cell, 127(4), 831-46. [PubMed:17110340] [WorldCat] [DOI] - ↑ 39.0 39.1 39.2
Xu, J., Mashimo, T., & Südhof, T.C. (2007).
Synaptotagmin-1, -2, and -9: Ca(2+) sensors for fast release that specify distinct presynaptic properties in subsets of neurons. Neuron, 54(4), 567-81. [PubMed:17521570] [WorldCat] [DOI] - ↑
Pang, Z.P., Melicoff, E., Padgett, D., Liu, Y., Teich, A.F., Dickey, B.F., ..., & Südhof, T.C. (2006).
Synaptotagmin-2 is essential for survival and contributes to Ca2+ triggering of neurotransmitter release in central and neuromuscular synapses. The Journal of neuroscience : the official journal of the Society for Neuroscience, 26(52), 13493-504. [PubMed:17192432] [PMC] [WorldCat] [DOI] - ↑
Fukuda, M., Kowalchyk, J.A., Zhang, X., Martin, T.F., & Mikoshiba, K. (2002).
Synaptotagmin IX regulates Ca2+-dependent secretion in PC12 cells. The Journal of biological chemistry, 277(7), 4601-4. [PubMed:11751925] [WorldCat] [DOI] - ↑
Maximov, A., Shin, O.H., Liu, X., & Südhof, T.C. (2007).
Synaptotagmin-12, a synaptic vesicle phosphoprotein that modulates spontaneous neurotransmitter release. The Journal of cell biology, 176(1), 113-24. [PubMed:17190793] [PMC] [WorldCat] [DOI] - ↑ 43.0 43.1
Mori, Y., & Fukuda, M. (2011).
Synaptotagmin IV acts as a multi-functional regulator of Ca2+-dependent exocytosis. Neurochemical research, 36(7), 1222-7. [PubMed:21153436] [WorldCat] [DOI] - ↑
Zhang, Z., Bhalla, A., Dean, C., Chapman, E.R., & Jackson, M.B. (2009).
Synaptotagmin IV: a multifunctional regulator of peptidergic nerve terminals. Nature neuroscience, 12(2), 163-71. [PubMed:19136969] [PMC] [WorldCat] [DOI] - ↑
Zhang, G., Bai, H., Zhang, H., Dean, C., Wu, Q., Li, J., ..., & Cai, D. (2011).
Neuropeptide exocytosis involving synaptotagmin-4 and oxytocin in hypothalamic programming of body weight and energy balance. Neuron, 69(3), 523-35. [PubMed:21315262] [PMC] [WorldCat] [DOI] - ↑
Dean, C., Liu, H., Dunning, F.M., Chang, P.Y., Jackson, M.B., & Chapman, E.R. (2009).
Synaptotagmin-IV modulates synaptic function and long-term potentiation by regulating BDNF release. Nature neuroscience, 12(6), 767-76. [PubMed:19448629] [PMC] [WorldCat] [DOI] - ↑
Zhang, Q., Fukuda, M., Van Bockstaele, E., Pascual, O., & Haydon, P.G. (2004).
Synaptotagmin IV regulates glial glutamate release. Proceedings of the National Academy of Sciences of the United States of America, 101(25), 9441-6. [PubMed:15197251] [PMC] [WorldCat] [DOI] - ↑
Yoshihara, M., Adolfsen, B., Galle, K.T., & Littleton, J.T. (2005).
Retrograde signaling by Syt 4 induces presynaptic release and synapse-specific growth. Science (New York, N.Y.), 310(5749), 858-63. [PubMed:16272123] [WorldCat] [DOI] - ↑
Barber, C.F., Jorquera, R.A., Melom, J.E., & Littleton, J.T. (2009).
Postsynaptic regulation of synaptic plasticity by synaptotagmin 4 requires both C2 domains. The Journal of cell biology, 187(2), 295-310. [PubMed:19822673] [PMC] [WorldCat] [DOI] - ↑
Cao, P., Maximov, A., & Südhof, T.C. (2011).
Activity-dependent IGF-1 exocytosis is controlled by the Ca(2+)-sensor synaptotagmin-10. Cell, 145(2), 300-11. [PubMed:21496647] [PMC] [WorldCat] [DOI] - ↑
Arantes, R.M., & Andrews, N.W. (2006).
A role for synaptotagmin VII-regulated exocytosis of lysosomes in neurite outgrowth from primary sympathetic neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 26(17), 4630-7. [PubMed:16641243] [PMC] [WorldCat] [DOI] - ↑
Doi, H., Yoshida, K., Yasuda, T., Fukuda, M., Fukuda, Y., Morita, H., ..., & Matsumoto, N. (2011).
Exome sequencing reveals a homozygous SYT14 mutation in adult-onset, autosomal-recessive spinocerebellar ataxia with psychomotor retardation. American journal of human genetics, 89(2), 320-7. [PubMed:21835308] [PMC] [WorldCat] [DOI] - ↑
Dean, C., Dunning, F.M., Liu, H., Bomba-Warczak, E., Martens, H., Bharat, V., ..., & Chapman, E.R. (2012).
Axonal and dendritic synaptotagmin isoforms revealed by a pHluorin-syt functional screen. Molecular biology of the cell, 23(9), 1715-27. [PubMed:22398727] [PMC] [WorldCat] [DOI]