|
|
| (3人の利用者による、間の34版が非表示) |
| 1行目: |
1行目: |
| <div align="right">
| | 英:Signal Transducers and Activator of Transcription、英略語:STAT |
| <font size="+1">赤土 正一、[http://researchmap.jp/kinichinakashima 中島 欽一]</font><br>
| |
| ''奈良先端科学技術大学院大学 バイオサイエンス研究科''<br>
| |
| DOI:<selfdoi /> 原稿受付日:2012年11月26日 原稿完成日:2013年3月20日<br>
| |
| 担当編集委員:[http://researchmap.jp/noriko1128 大隅 典子](東北大学 大学院医学系研究科 附属創生応用医学研究センター 脳神経科学コアセンター 発生発達神経科学分野)<br>
| |
| </div>
| |
|
| |
|
| {{PBB|geneid=6774}} 英:Signal Transducers and Activator of Transcription 3、英略語:STAT3
| | シグナル伝達と転写活性化を行うことで、分化や生存、増殖などを調節するタンパク質である。STATは非活性化状態時では細胞質に局在するが、Janus kinase(JAK)が活性化されることによってリン酸化を受け、核内移行し目的遺伝子を活性化する転写因子となる。この活性化経路はJAK-STAT経路と呼ばれている。悪性腫瘍形成の初期の過程などにおいて、JAK-STAT経路の制御不全が見られており、免疫抑制や腫瘍の生存延長、血管新生などを引き起こす。 |
|
| |
|
| {{box|text=
| | == STATファミリー == |
| [[シグナル伝達]]と[[wikipedia:ja:転写|転写]]活性化を行うことで、[[分化]]や生存、[[増殖]]などを調節するタンパク質の一群、Signal Transducers and Activator of Transcription(STAT)ファミリー分子の一つ。STAT3は非活性化状態時では[[細胞質]]に局在するが、活性化した[[Janusキナーゼ]]([[JAK]])によって[[チロシンリン酸化]]を受け、核内移行し標的遺伝子を活性化する[[転写因子]]として働く。この活性化経路は[[JAK/STAT経路]]と呼ばれている<ref><pubmed> 15225360 </pubmed></ref>。
| |
| }}
| |
|
| |
|
| == ファミリー ==
| | STATファミリー分子として報告されているのはSTAT1、STAT2、STAT3、STAT4、STAT5A、STAT5B、STAT6の7種類<ref><pubmed> 8608586 </pubmed></ref><ref><pubmed> 9418183 </pubmed></ref>。これらの全ての分子はホモ二量体を形成することができ、またいずれもシグナル伝達に関与している。いずれの分子もその構造内に、SH2ドメイン(JAKによるリン酸化を受けた受容体との結合部位)DNA結合ドメインを持ち、C末端側で保存されたチロシン残基がSTAT二量体の形成に関与している。 |
|
| |
|
| これまでSTATファミリー分子としては、[[STAT1]]、[[STAT2]]、STAT3、[[STAT4]]、[[STAT5A]]、[[STAT5B]]、[[STAT6]]の7種類が報告されている<ref><pubmed> 8608586 </pubmed></ref><ref><pubmed> 9418183 </pubmed></ref>。
| | == 脳内での働き == |
|
| |
|
| == 構造 == | | STATをシグナル経路下流の転写因子とするIL6やIFNγなどのサイトカイン群と、smadをシグナル経路下流の転写因子とするBMP2などのサイトカイン群(TGF-βスーパーファミリー)。両者は別々の受容体システムを介し、互いに協調的または拮抗的にクロストークして分化誘導<ref name="ref1"><pubmed> 10205054 </pubmed></ref>ないし転写抑制<ref name="ref2"><pubmed> 10067896 </pubmed></ref>することが明らかにされている。 |
|
| |
|
| [[Image:STAT3-1.jpg|thumb|350px|'''図1.STAT3の構造'''<br>SH2ドメインは信号伝達鎖内のリン酸化チロシン残基を認識、結合する機能を持つ。コイルド-コイルドメインは4つのα-ヘリックスから成り、STAT3がSH2ドメインを介して信号伝達鎖と結合し、活性化されるために必須な領域として知られる<ref><pubmed> 12746441 </pubmed></ref>。核局在化シグナル(NLS)は細胞質内で二量体化したSTAT3が核内に輸送されるために必要な配列である。DNA結合ドメインは活性化STAT3が標的DNA配列に結合する役割を有する。]]
| | 免疫系に作用するサイトカインとして同定された、L-6ファミリーサイトカイン(LIFなど)やインターフェロン(IFN)が細胞膜上のサイトカイン受容体複合体中のサイトカイン特異的結合鎖と結合することで、膜たんぱく質gp130を含む信号伝達鎖の二量体化がおこり、信号伝達鎖の細胞内領域に会合するJAKが活性化され、信号伝達鎖の細胞内領域中のチロシン残基をリン酸化する。リン酸化されたチロシン残基に、転写因子STATファミリー(STAT3など)が自身のSH2(src homology 2)ドメインを介して会合、近接したJAKによりチロシンリン酸化(チロシン705)を受けることで活性化する<ref><pubmed> 9685167 </pubmed></ref>。チロシンリン酸化されたSTAT分子はホモないし別のSTATファミリー分子間にてヘテロ二量体を形成し核へ移行した後、目的遺伝子の転写を制御する。 |
|
| |
|
| STAT3は[[wikipedia:ja:マウス|マウス]]では770アミノ酸残基から構成される。[[wikipedia:ja:SH2ドメイン|SH2ドメイン]]は信号伝達鎖内のリン酸化チロシン残基を認識、結合する機能を持つ。[[wikipedia:ja:コイルド-コイルドメイン|コイルド-コイルドメイン]]は4つの[[wikipedia:ja:α-ヘリックス|α-ヘリックス]]から成り、STAT3がSH2ドメインを介して信号伝達鎖と結合し、活性化されるために必須な領域として知られる。[[wikipedia:ja:核局在化シグナル|核局在化シグナル]](nuclear localization signal, NLS)は[[wikipedia:ja:細胞質|細胞質]]内で二量体化したSTAT3が核内に輸送されるために必要な配列である。DNA結合ドメインは活性化STAT3が標的[[wikipedia:ja:DNA|DNA]]配列に結合する役割を有する。またリン酸化を受けることでSTAT3の活性に関わる705番目のチロシン残基と727番目のセリン残基を有する。 チロシンリン酸化されたSTAT3分子はホモ二量体あるいは異なるSTATファミリー分子間でヘテロ二量体を形成する。図1には例として、マウスSTAT3の構造を示した。
| | また免疫・造血系制御に重要な役割を持つ、TGF-βスーパーファミリー(BMP2など)に属するサイトカインが、セリン/スレオニンキナーゼドメインを細胞内領域に持つタイプⅠとタイプⅡ受容体の二分子ずつのヘテロ四量体に結合し、受容体を活性化する。活性化受容体は、特異的転写因子群smadのセリン残基をリン酸化し、それらを活性化する。BMPの刺激で活性化される特異型smad(smad1,5,8)は共有型smadであるsmad4とヘテロオリゴマーを形成、核へ移行し、目的遺伝子の転写を制御する<ref><pubmed> 9393997 </pubmed></ref><ref><pubmed> 10733523 </pubmed></ref>。 |
|
| |
|
| == 発現 == | | 上記の通り、STATとsmadは別々のサイトカイン受容体システムを通じて活性化を受ける転写因子である。しかし、それらの協調作用により、神経幹細胞のアストロサイトへの分化が劇的に誘導される<ref name="ref1" />。転写活性化の補助的役割を果たす核内転写共役因子p300がサイトカイン刺激に応答して、自身のN末端側を二量体化したSTAT3と、自身のC末端側をヘテロオリゴマー化したsmad1と、それぞれ同時に結合しSTAT3/p300/smad1複合体が形成される。これにより二種類サイトカインシグナルが核内で統合され、目的遺伝子GFAPの相乗的発現が起こる<ref name="ref1" />。そしてGFAPの発現によりアストロサイトへの分化が誘導される。(図a参照) |
|
| |
|
| [http://mouse.brain-map.org/experiment/show/2638 STAT3]は脳、[[wikipedia:ja:心臓|心臓]]、[[wikipedia:ja:肝臓|肝臓]]、[[wikipedia:ja:腎臓|腎臓]]、[[wikipedia:ja:脾臓|脾臓]]、[[wikipedia:ja:胸腺|胸腺]]など身体組織全体で広範囲に発現していることが、マウスを用いた研究により確認されている<ref><pubmed> 7545930 </pubmed></ref>。
| | <br> |
|
| |
|
| STAT3はJAKチロシンキナーゼによりリン酸化されることで活性化し、標的遺伝子の転写を誘導する(後述)。しかし実はSTAT3遺伝子自身もその標的であり、活性化したSTAT3がSTAT3の遺伝子を誘導するというポジティブフィードバックループの存在も知られている<ref><pubmed> 15852015
| | <br> |
| </pubmed></ref><ref><pubmed> 9497331 </pubmed></ref>。
| |
|
| |
|
| 神経系細胞においては、STAT3は[[アストロサイト]]内で最も強く発現しており、[[神経幹細胞]] (neural stem cell, NSC) の発現量の二倍近い。また、ニューロンとNSCにおける発現量はほぼ同じで大きな差はないことが報告されている<ref><pubmed> 22736940 </pubmed></ref>。
| | [[Image:無題1.jpg|RTENOTITLE]] |
|
| |
| [[Image:STAT3-2.jpg|thumb|350px|'''図2.IL-6ファミリーサイトカイン群と受容体'''<br>IL-6ファミリーサイトカインはそれぞれに特異的な受容体に結合し、共通信号伝達鎖gp130を含んだ受容体複合体を形成する。IL-6受容体(IL-6R)、IL-11R、CNTFRは可溶性の形態(sIL-6R、sIL-11R、sCNTFR)でも受容体複合体形成を可能とする。IL-6、IL-11はgp130同士のホモ二量体、LIF、CNTF、CT-1はgp130/LIFRとのヘテロ二量体形成を誘導する。CT-1受容体(CT-1R)はCT-1の結合によりgp130/LIFRとのヘテロ二量体を形成する。OSMはOSMRまたはLIFRとgp130とのヘテロ二量体化を誘導する。]] | |
|
| |
|
| [[Image:STAT3-3.jpg|thumb|350px|'''図3.IL-6ファミリーサイトカインシグナルによるGFAP遺伝子の発現'''<br>IL-6ファミリーのシグナルによりSTAT3がリン酸化を受け、活性化される。活性化されたSTAT3はSTAT3同士でホモ二量体または他のSTATとヘテロ二量体を形成し、核内に移行後、GFAPプロモーター中のSTAT3認識配列に結合し、転写を誘導する。IL-6ファミリーに属する全てのサイトカインはSTAT3を活性化し、GFAPの転写を誘導することが明らかになっている。ここではLIFによるものを示した。]] | | 上記の協調的クロストークの他に、STATとsmadは拮抗的クロストークもまた行う<ref name="ref2" />。サイトカインIFNγ結合により、リン酸化される活性化STAT1は二量体を形成、核へ移行し、smad7遺伝子を転写する。抑制型smadであるsmad7は受容体を介する特異型であるsmad3のセリンリン酸化を阻害し、共有型smadであるsmad4とのオリゴマー形成と核移行を阻害することでTGF-βスーパーファミリーサイトカインシグナルを負に制御する。(図b参照) [[Image:無題2.jpg|RTENOTITLE]] |
|
| |
|
| == 活性化機構 ==
| | <br> |
| ===リン酸化による制御===
| |
| [[wikipedia:ja:免疫|免疫]]系に作用する[[wikipedia:ja:サイトカイン|サイトカイン]]として同定された[[インターロイキン-6]]([[Interleukin-6]], [[IL-6]])は、信号伝達に必須な[[受容体]]コンポーネントとして[[wikipedia:ja:膜タンパク質|膜タンパク質glycoprotein]] 130([[Gp130]])を共通に利用するIL-6ファミリーサイトカインの一つである。IL-6ファミリーサイトカインには他にも、[[インターロイキン-11]](IL-11)、[[オンコスタチンM]] ([[Oncostatin M]], [[OSM]])、[[白血病抑制因子]]([[Leukemia Inhibitory Factor]], [[LIF]])、[[カルジオトロピン-1]]([[Cardiotrophin-1]], [[CT-1]])、[[毛様体神経栄養因子]]([[Ciliary Neurotrophic Factor]], [[CNTF]])などが含まれる<ref name="ref4"><pubmed> 11820727 </pubmed></ref>。IL-6ファミリーサイトカインは、[[細胞膜]]上のサイトカイン特異的受容体と結合することで、IL-6ファミリーサイトカインに共通かつ必須の信号伝達因子であるgp130を含む信号伝達鎖の二量体化を引き起こす(図2)。
| |
| | |
| その後、信号伝達鎖の細胞内領域に会合するJAKチロシンキナーゼが活性化され、信号伝達鎖の細胞内領域中のチロシン残基をリン酸化する。リン酸化されたチロシン残基に、転写因子STAT3が自身の[[Src homology 2]]([[SH2]])ドメインを介して会合、近接したJAKにより705番目の[[wikipedia:ja:チロシン|チロシン]]残基が[[リン酸化]]を受けることで活性化する<ref><pubmed> 9685167 </pubmed></ref>。
| |
| | |
| チロシンリン酸化されたSTAT3分子はホモ二量体あるいは異なるSTATファミリー分子間でヘテロ二量体を形成し核へ移行した後、標的遺伝子の転写を誘導する。JAK/STAT3経路はIL-6ファミリーや[[インスリン様成長因子-1]]([[Insulin-like growth factor-1]], [[IGF-1]])など複数のサイトカインや増殖因子の刺激により活性化することが知られている<ref name="ref1"><pubmed> 10486560 </pubmed></ref><ref name="ref2"><pubmed> 22772901 </pubmed></ref><ref name="ref3"><pubmed> 15998644 </pubmed></ref>。
| |
| | |
| ===転写による制御===
| |
| JAK/STAT経路が活性化することで、STAT3は標的遺伝子の転写を誘導する。しかし実はSTAT3遺伝子自身もその標的であり、活性化したSTAT3はSTAT3遺伝子プロモーター中のSTAT認識配列に直接結合し、転写が誘導されるというポジティブフィードバックループの存在が報告されている<ref><pubmed> 15852015 </pubmed></ref>。
| |
| | |
| == 神経系での機能 ==
| |
| | |
| === アストロサイト分化誘導 ===
| |
| | |
| IL-6ファミリーサイトカインの刺激により活性化したSTAT3は、転写活性化因子として[[グリア線維性酸性タンパク質]]([[Glial fibrillary acidic protein]], [[GFAP]])の[[プロモーター]]に結合し、転写を促進する。GFAPは[[アストロサイト]]で特異的に発現するタンパク質であり、これまで[[神経幹細胞]][[Neural stem cell]]([[NSC]])の培養系にIL-6ファミリーサイトカインを添加すると、JAK/STAT3経路を活性化することでアストロサイトへの分化が促進されることが明らかとなっている(図3)<ref name="ref4" /><ref name="ref1" />。また、STAT3をシグナル経路下流の転写因子とするIL-6ファミリーサイトカインと[[Smad]]をシグナル経路下流の転写因子とする[[骨形成因子]]([[Bone morphogenetic protein]], [[BMP]])群([[TGF-βスーパーファミリー]]に属する)の両者は別々の受容体システムを介し、相乗的にアストロサイトの分化を誘導することが明らかにされている<ref><pubmed> 10205054 </pubmed></ref>。そのメカニズムとして、転写活性化の補助的役割を果たす核内転写共役因子[[P300]]が、サイトカイン刺激に応答して活性化されたSTAT3のN末端と、Smad1のC末端に結合し、STAT3/p300/smad1複合体を形成することで、標的遺伝子GFAPの効率的な発現を誘導することが明らかにされている。
| |
| | |
| === 神経幹細胞増殖制御 ===
| |
| | |
| 通常のSTAT3[[遺伝子欠損]]([[ノックアウト]]、[[KO]])[[wikipedia:ja:マウス|マウス]]は発生の比較的初期に死に至るので、マウス脳内におけるSTAT3 KOの影響を解析することは困難である<ref><pubmed> 9108058 </pubmed></ref>。そこで、神経系細胞特異的にSTAT3遺伝子を欠損([[コンディショナルノックアウト]]、cKO)させる[[トランスジェニックマウス]]を用いて解析した結果、STAT3 cKOマウスの[[海馬歯状回]]において、NSCの数が、野生型マウスに比べ減少していることが明らかになった<ref name="ref5"><pubmed> 19023034 </pubmed></ref>。またニューロンに対して[[栄養因子]]として作用する[[CNTF]]は、gp130を介したシグナル伝達によりNSCの自己増殖を制御するという報告もなされている<ref><pubmed> 17311007 </pubmed></ref><ref><pubmed> 1542794 </pubmed></ref><ref><pubmed> 8390097 </pubmed></ref>。さらに、CNTF KOマウスの歯状回で、NSCの数が野生型マウスと比較して減少しているというSTAT3 cKOマウスと類似の結果が得られたことから、CNTFは受容体と結合し、下流のJAK/STAT3経路を活性化することで、NSCの自己増殖を制御すると考えられている<ref name="ref5" />。
| |
| | |
| === てんかん発作誘導性神経細胞死における神経保護作用 ===
| |
| | |
| 成体マウスにおいて[[興奮性アミノ酸]]の一種、[[カイニン酸]]([[Kainic acid]], [[KA]])投与による[[てんかん]]誘導に際し、[[抗てんかん薬]]として知られる[[Carbamazepine]]([[CBZ]])を投与すると、海馬の[[CA3領域]]において、ニューロン死の割合がKA投与のみの個体に比べ低いことが分かった。また、KA+CBZ投与マウスのCA3ニューロンにおいて、STAT3の発現レベルがmRNA、タンパク質においても上昇しており、活性化を表すチロシンリン酸化STAT3の増加も見られている。加えて、ニューロン保護タンパク質として知られている[[B-cell lymphoma-extra large]]([[Bcl-xl]])もまた、KA+CBZ投与マウスのCA3ニューロン内で発現レベルが高まっている上、CT-1の刺激によってSTAT3とSTAT1のヘテロ二量体がBcl-xl遺伝子に直接結合し、発現制御を行うという報告<ref><pubmed> 10866494 </pubmed></ref>から、CBZのシグナルを受けてJAK/STAT3経路が活性化し、Bcl-xlなどの抗[[アポトーシス]]分子の発現を誘導することで、てんかんによるニューロン死への保護効果が上昇することが示唆されている<ref name="ref2" />。しかし、CBZシグナルがどのようなメカニズムでJAK/STAT3経路が活性化しているかはいまだ明らかになっていない。炎症性サイトカインである[[腫瘍壊死因子]]([[Tumor necrosis factor-α]], [[TNF-α]])は神経疾患、または炎症反応中の脳で神経細胞毒性を持ち<ref><pubmed> 7507336 </pubmed></ref>、高濃度添加によりニューロン死が観察される。一方、インスリン様成長因子-1(insulin-like growth factor-1, IGF-1)は頭部外傷など、脳内の炎症反応により多量に発現し、[[神経保護作用]]を発揮する<ref><pubmed> 9246719 </pubmed></ref><ref><pubmed> 14568359 </pubmed></ref>。加えて、TNF-αのみを添加したニューロン群より、IGF-1とTNF-αを添加したニューロン群においてニューロン死の割合が低かったことから、IGF-1はTNF-αにより誘導されるニューロン死の抑制という作用を有することが明らかになった。このニューロン保護効果には、何らかのメカニズムでJAK/STAT3経路がIGF-1により活性化され、活性化されたSTAT3が[[サイトカインシグナル抑制因子]]([[Suppressors of cytokine signaling 3]], [[SOCS-3]])の転写を誘導し、誘導されたSOCS3がIL-6ファミリーサイトカイン受容体複合体の信号伝達鎖のリン酸化チロシン残基とJAKに結合し、JAKの機能を阻害することで、JAK/STAT3経路を抑制することが重要であると報告されている<ref><pubmed> 10829066 </pubmed></ref>。しかしSOCS3がJAK/STAT3経路を負に制御することにより、TNF-αシグナルをどのように抑制するのか、その詳細なメカニズムは明らかになっていない<ref name="ref3" /><ref><pubmed> 10070253 </pubmed></ref>。
| |
| | |
| === 脊髄損傷時の反応性アストロサイト分化誘導 ===
| |
| | |
| [[脊髄]]に損傷が起こると炎症反応が発生し、損傷部周辺の細胞で炎症性サイトカインの発現が亢進する。これらの刺激により損傷部周辺ではGFAP強陽性となる反応性アストロサイトの出現が観察される<ref><pubmed> 9989494 </pubmed></ref>。反応性アストロサイトは集合し[[グリア瘢痕]]を形成する<ref><pubmed> 12578228 </pubmed></ref>。グリア瘢痕は損傷部の物理的な防壁となり、損傷部を外部環境刺激から守ることで中枢神経系を再統合する役割を持つ<ref><pubmed> 9724451 </pubmed></ref>。しかし、グリア瘢痕は、chondroitin sulfate proteoglycans(CSPGs)などの軸索伸長阻害因子を分泌し、損傷部周辺ニューロンの[[軸索]]再伸長を阻害するため、これにより神経軸索再生が抑制される<ref><pubmed> 12626698 </pubmed></ref>。関連して、脊髄損傷を起こしたマウスへIL-6受容体の機能阻害抗体(MR16-1)を投与すると、損傷部の反応性アストロサイトの数が減少し、神経機能の回復が観察されるという報告がなされている。ところで、アストロサイト特異的にSTAT3遺伝子を欠損させたマウスの脊髄を損傷させても、反応性アストロサイトが出現せず、グリア瘢痕は形成されない。しかし、先に述べたようにグリア瘢痕は損傷部を外部環境刺激から守る役割を持つので、アストロサイト特異的STAT3遺伝子欠損マウスは脊髄損傷が起きた後、傷口と炎症部が広がっていき、部分的に運動機能がさらに低下する<ref><pubmed> 18614693 </pubmed></ref>。これらのことから、IL-6ファミリーサイトカイン刺激によるJAK/STAT3経路の活性化によって誘導される反応性アストロサイトには、良い作用と悪い作用が存在し、そのバランスを制御することが病態改善には重要であると考えられる<ref><pubmed> 15048924 </pubmed></ref>。
| |
| | |
| == まとめ ==
| |
| | |
| ここに紹介したもの以外にも、STAT3の神経系における働きは多岐にわたり、それらを総合すると、JAK/STAT3経路は神経系の発達、形成に重要な役割を担う情報伝達経路と言える。また、単純に神経発達や形成に重要な因子となるタンパク質の発現を誘導するのみならず、その過度な活性化による障害を防ぐために自らのシグナル経路を抑制するタンパク質発現を誘導する負のフィードバックメカニズムも備えられており<ref><pubmed> 12754507 </pubmed></ref>、正しい生体機能が発揮されるために、JAK/STAT3経路は精妙に制御されている。
| |
| | |
| == 関連項目 ==
| |
| | |
| *[[Janusキナーゼ]]
| |
| *[[チロシンリン酸化]]
| |
| *[[転写因子]]<br>
| |
|
| |
|
| == 参考文献 == | | == 参考文献 == |
|
| |
|
| <references /> | | <references /> |
英:Signal Transducers and Activator of Transcription、英略語:STAT
シグナル伝達と転写活性化を行うことで、分化や生存、増殖などを調節するタンパク質である。STATは非活性化状態時では細胞質に局在するが、Janus kinase(JAK)が活性化されることによってリン酸化を受け、核内移行し目的遺伝子を活性化する転写因子となる。この活性化経路はJAK-STAT経路と呼ばれている。悪性腫瘍形成の初期の過程などにおいて、JAK-STAT経路の制御不全が見られており、免疫抑制や腫瘍の生存延長、血管新生などを引き起こす。
STATファミリー
STATファミリー分子として報告されているのはSTAT1、STAT2、STAT3、STAT4、STAT5A、STAT5B、STAT6の7種類[1][2]。これらの全ての分子はホモ二量体を形成することができ、またいずれもシグナル伝達に関与している。いずれの分子もその構造内に、SH2ドメイン(JAKによるリン酸化を受けた受容体との結合部位)DNA結合ドメインを持ち、C末端側で保存されたチロシン残基がSTAT二量体の形成に関与している。
脳内での働き
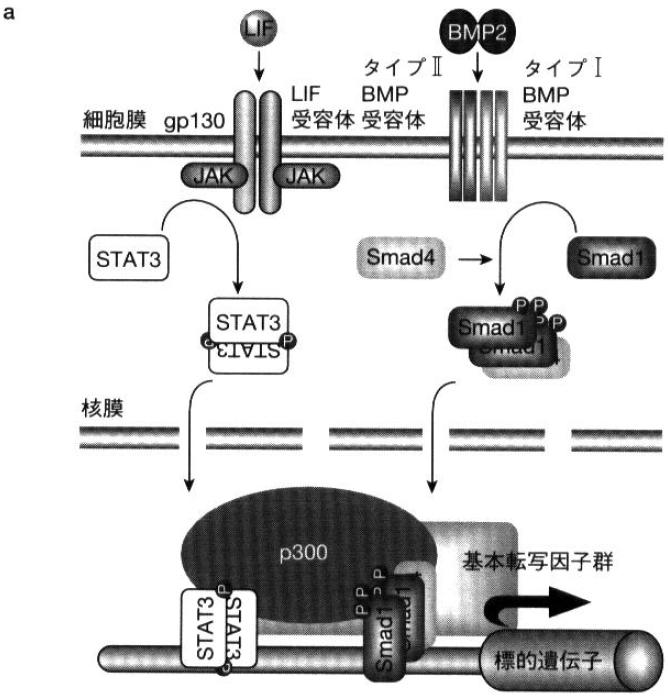
STATをシグナル経路下流の転写因子とするIL6やIFNγなどのサイトカイン群と、smadをシグナル経路下流の転写因子とするBMP2などのサイトカイン群(TGF-βスーパーファミリー)。両者は別々の受容体システムを介し、互いに協調的または拮抗的にクロストークして分化誘導[3]ないし転写抑制[4]することが明らかにされている。
免疫系に作用するサイトカインとして同定された、L-6ファミリーサイトカイン(LIFなど)やインターフェロン(IFN)が細胞膜上のサイトカイン受容体複合体中のサイトカイン特異的結合鎖と結合することで、膜たんぱく質gp130を含む信号伝達鎖の二量体化がおこり、信号伝達鎖の細胞内領域に会合するJAKが活性化され、信号伝達鎖の細胞内領域中のチロシン残基をリン酸化する。リン酸化されたチロシン残基に、転写因子STATファミリー(STAT3など)が自身のSH2(src homology 2)ドメインを介して会合、近接したJAKによりチロシンリン酸化(チロシン705)を受けることで活性化する[5]。チロシンリン酸化されたSTAT分子はホモないし別のSTATファミリー分子間にてヘテロ二量体を形成し核へ移行した後、目的遺伝子の転写を制御する。
また免疫・造血系制御に重要な役割を持つ、TGF-βスーパーファミリー(BMP2など)に属するサイトカインが、セリン/スレオニンキナーゼドメインを細胞内領域に持つタイプⅠとタイプⅡ受容体の二分子ずつのヘテロ四量体に結合し、受容体を活性化する。活性化受容体は、特異的転写因子群smadのセリン残基をリン酸化し、それらを活性化する。BMPの刺激で活性化される特異型smad(smad1,5,8)は共有型smadであるsmad4とヘテロオリゴマーを形成、核へ移行し、目的遺伝子の転写を制御する[6][7]。
上記の通り、STATとsmadは別々のサイトカイン受容体システムを通じて活性化を受ける転写因子である。しかし、それらの協調作用により、神経幹細胞のアストロサイトへの分化が劇的に誘導される[3]。転写活性化の補助的役割を果たす核内転写共役因子p300がサイトカイン刺激に応答して、自身のN末端側を二量体化したSTAT3と、自身のC末端側をヘテロオリゴマー化したsmad1と、それぞれ同時に結合しSTAT3/p300/smad1複合体が形成される。これにより二種類サイトカインシグナルが核内で統合され、目的遺伝子GFAPの相乗的発現が起こる[3]。そしてGFAPの発現によりアストロサイトへの分化が誘導される。(図a参照)
上記の協調的クロストークの他に、STATとsmadは拮抗的クロストークもまた行う[4]。サイトカインIFNγ結合により、リン酸化される活性化STAT1は二量体を形成、核へ移行し、smad7遺伝子を転写する。抑制型smadであるsmad7は受容体を介する特異型であるsmad3のセリンリン酸化を阻害し、共有型smadであるsmad4とのオリゴマー形成と核移行を阻害することでTGF-βスーパーファミリーサイトカインシグナルを負に制御する。(図b参照) 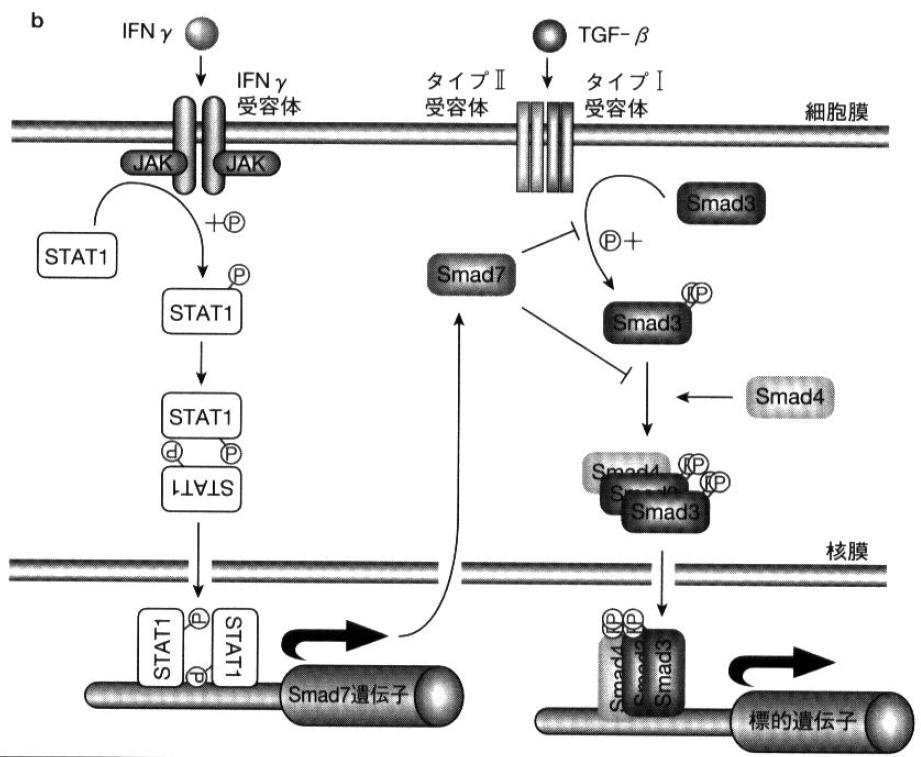
参考文献
- ↑
Ihle, J.N. (1996).
STATs: signal transducers and activators of transcription. Cell, 84(3), 331-4.
[PubMed:8608586]
[WorldCat]
[DOI]
- ↑
O'Shea, J.J., Notarangelo, L.D., Johnston, J.A., & Candotti, F. (1997).
Advances in the understanding of cytokine signal transduction: the role of Jaks and STATs in immunoregulation and the pathogenesis of immunodeficiency. Journal of clinical immunology, 17(6), 431-47.
[PubMed:9418183]
[WorldCat]
[DOI]
- ↑ 3.0 3.1 3.2
Nakashima, K., Yanagisawa, M., Arakawa, H., Kimura, N., Hisatsune, T., Kawabata, M., ..., & Taga, T. (1999).
Synergistic signaling in fetal brain by STAT3-Smad1 complex bridged by p300. Science (New York, N.Y.), 284(5413), 479-82.
[PubMed:10205054]
[WorldCat]
[DOI]
- ↑ 4.0 4.1
Ulloa, L., Doody, J., & Massagué, J. (1999).
Inhibition of transforming growth factor-beta/SMAD signalling by the interferon-gamma/STAT pathway. Nature, 397(6721), 710-3.
[PubMed:10067896]
[WorldCat]
[DOI]
- ↑
Nakashima, K., & Taga, T. (1998).
gp130 and the IL-6 family of cytokines: signaling mechanisms and thrombopoietic activities. Seminars in hematology, 35(3), 210-21.
[PubMed:9685167]
[WorldCat]
- ↑
Heldin, C.H., Miyazono, K., & ten Dijke, P. (1997).
TGF-beta signalling from cell membrane to nucleus through SMAD proteins. Nature, 390(6659), 465-71.
[PubMed:9393997]
[WorldCat]
[DOI]
- ↑
Massagué, J., & Chen, Y.G. (2000).
Controlling TGF-beta signaling. Genes & development, 14(6), 627-44.
[PubMed:10733523]
[WorldCat]

