「FM1-43」の版間の差分
Norikotakahashi (トーク | 投稿記録) 細編集の要約なし |
|||
| 61行目: | 61行目: | ||
[[Image:Takahashinoriko fig 3.jpg|thumb|250px|'''図3.(タイトル:開口放出に伴う FM 蛍光の変化''' 説明:膜融合時、細胞外色素の有無により蛍光変化の様式が異なる)]] | [[Image:Takahashinoriko fig 3.jpg|thumb|250px|'''図3.(タイトル:開口放出に伴う FM 蛍光の変化''' 説明:膜融合時、細胞外色素の有無により蛍光変化の様式が異なる)]] | ||
シナプスを刺激した時にミリ秒で起きる伝達物質放出は、活性帯にドックした小胞が開口放出すると仮想されている。この仮想的な小胞群を即時型放出プール[[Readily releasable pool]](RRP)という。[[シナプス小胞]]は開口放出後30-60秒で細胞内部に[[エンドサイトーシス]]で取り込まれる(図 3左)。更に、シナプス終末内でシナプス小胞に再生されて即時型放出プールに再び至る。これをリサイクリングと呼び、これに関係する小胞の全体をリサイクリングプール(recycling pool, 放出可能プール、TRP)という。 | |||
細胞外を FM1-43 で還流中に、長い放出刺激(例 10 Hz、900 発)を与え[[開口放出]]([[エクソサイトーシス]])した小胞の膜を染めた後、細胞外を色素を含まない溶液で還流し、細胞外膜に結合した色素を wash out | 細胞外を FM1-43 で還流中に、長い放出刺激(例 10 Hz、900 発)を与え[[開口放出]]([[エクソサイトーシス]])した小胞の膜を染めた後、細胞外を色素を含まない溶液で還流し、細胞外膜に結合した色素を wash out すると、リサイクリングプールの全体が染まる。一方、ちょうど RRP にある小胞を枯渇させる程度の短い放出刺激(例 20 Hz、30 発)を与えて負荷後に wash out すると RRP が選択的に染まる。この様な解析から、RRP はリサイクリングプールの10-30%でないかと推定されており<ref><pubmed> 15044806 </pubmed></ref>、TRP が 40程度の小さなシナプスでは RRP の小胞数は4-12個となる。 | ||
次に、リサイクリングプールを染めた小胞に刺激を与えると、シナプス小胞は細胞膜と融合し、FM1-43が細胞外液へ拡散することにより神経終末の蛍光は減弱する脱染色(destaining | 次に、リサイクリングプールを染めた小胞に刺激を与えると、シナプス小胞は細胞膜と融合し、FM1-43が細胞外液へ拡散することにより神経終末の蛍光は減弱する脱染色(destaining 図3右)。この destaining の時間経過は、小胞の開口放出確率が大きい程速い。定量的には、RRP にある小胞の数を[RRP]、その放出確率をPvとすると、一回の刺激で放出される小胞の数は平均[RRP]*Pvとなる。一方、TRP にある小胞の数を[TRP]、一回の刺激による TRP の蛍光の減弱率を kとすると、一回の刺激で放出される小胞の数は[TRP]*kとなる。よって、[RRP]*Pv = [TRP]*k となり、これからPv=k*[RRP]/[TRP] という関係式が得られ、終末ごとにRRPにある小胞の放出確率を求めることができる <ref><pubmed>23049481 </pubmed></ref>。 | ||
FM1-43によって染めることができるリサイクリングプールの小胞は、電子顕微鏡的に終末に存在する小胞の15-20%である<ref><pubmed> 15044806 </pubmed></ref>。 この電子顕微鏡的に同定されるリサイクリングされ難いシナプス小胞の群をreserve pool 或いは resting poolと言う。このプールの小胞もゆっくりとしたリサイクリングに関係していることが他の方法によって明らかとなっている<ref><pubmed>21835344 </pubmed></ref>。 | FM1-43によって染めることができるリサイクリングプールの小胞は、電子顕微鏡的に終末に存在する小胞の15-20%である<ref><pubmed> 15044806 </pubmed></ref>。 この電子顕微鏡的に同定されるリサイクリングされ難いシナプス小胞の群をreserve pool 或いは resting poolと言う。このプールの小胞もゆっくりとしたリサイクリングに関係していることが他の方法によって明らかとなっている<ref><pubmed>21835344 </pubmed></ref>。 | ||
2013年4月25日 (木) 22:59時点における版
| FM1-43 | |
|---|---|
| |
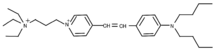
3-[4-[2-[4-(dibutylamino)phenyl]ethenyl]pyridin-1-ium-1-yl]propyl-triethylazanium dibromide | |
別称 Frie Mao 1-43, SynaptoGreen™ Reagent, SureCN1527120, N-(3-Triethylammoniumpropyl)-4-(p-dibutylaminostyryl)pyridinium, 2Br | |
| Identifiers | |
| 149838-22-2 | |
| Jmol-3D images | Image |
| PubChem | 2733618 |
| |
| Properties | |
| Molar mass | 611.53816 |
| 特記なき場合、データは常温(25 °C)・常圧(100 kPa)におけるものである。 | |
FM 色素は脂質二重膜を可逆的に染める蛍光色素で、シナプス前終末の機能や分泌現象の計測に活用されている。
FM1-43とは
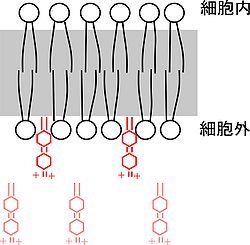
Molecular Probe 社の Fei Mao は William J Betz らとともに、細胞膜を染める一連のスチリル色素を合成した。これらを FM (Fei Mao)色素と呼び、FM1-43 はその代表格である。シナプス前終末の機能解析や、分泌小胞の動態解析に広く用いられる。
色素の特性として次の3つの性質がある。
分子構造
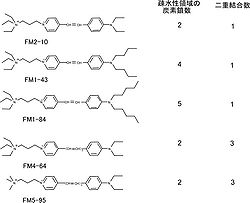
構造は、親水性領域、二重結合領域、疎水性炭素鎖領域に分けられる。
親水性領域が正の電荷をもつため、膜を通過しない。二重結合の数は蛍光波長に関連する。
二重結合が一つの FM1-43、FM1-84、FM2-10 は黄色蛍光を呈し、二重結合が二つの FM4-64、FM5-95 は赤色蛍光を呈する。
疎水性炭素鎖の長さは細胞膜の染め方に関連し、長いものほど明るく、一旦膜に組み込まれると離脱しがたい[1]。 FM1-43 の炭素鎖数は4であり、解離時定数τdissは8 msを示す。より短いFM2-10(炭素鎖数 2)は、比較的離脱しやすい(τdiss=6.4 ms)。逆に、より長い FM1-84(炭素鎖数 5)は離脱に時間がかかる(τdiss=36 ms)[2]。
蛍光特性
FM1-43の励起には1光子では波長480 nm光、2光子では波長840 nm光が頻用される。
極大蛍光波長はリポソーム中にて580 nmである。
波長480nm光の高出力励起(~150 μW)にてジアミノベンチジン(DAB)の光変換(photoconversion) を起こす。そのため、アルデヒドで固定可能な色素であるFM1-43FX と DABを細胞に与え光変換させると、共局在部位で電子密度の高い産物が作られ、電子顕微鏡観察が可能となる。FM1-43を取り込んだ小胞が、高い電子密度で描出され、微細構造解析に活用されている。
応用例
シナプス前機能の解析
シナプス前終末における小胞プールの大きさと開口放出確率の測定

シナプスを刺激した時にミリ秒で起きる伝達物質放出は、活性帯にドックした小胞が開口放出すると仮想されている。この仮想的な小胞群を即時型放出プールReadily releasable pool(RRP)という。シナプス小胞は開口放出後30-60秒で細胞内部にエンドサイトーシスで取り込まれる(図 3左)。更に、シナプス終末内でシナプス小胞に再生されて即時型放出プールに再び至る。これをリサイクリングと呼び、これに関係する小胞の全体をリサイクリングプール(recycling pool, 放出可能プール、TRP)という。
細胞外を FM1-43 で還流中に、長い放出刺激(例 10 Hz、900 発)を与え開口放出(エクソサイトーシス)した小胞の膜を染めた後、細胞外を色素を含まない溶液で還流し、細胞外膜に結合した色素を wash out すると、リサイクリングプールの全体が染まる。一方、ちょうど RRP にある小胞を枯渇させる程度の短い放出刺激(例 20 Hz、30 発)を与えて負荷後に wash out すると RRP が選択的に染まる。この様な解析から、RRP はリサイクリングプールの10-30%でないかと推定されており[3]、TRP が 40程度の小さなシナプスでは RRP の小胞数は4-12個となる。
次に、リサイクリングプールを染めた小胞に刺激を与えると、シナプス小胞は細胞膜と融合し、FM1-43が細胞外液へ拡散することにより神経終末の蛍光は減弱する脱染色(destaining 図3右)。この destaining の時間経過は、小胞の開口放出確率が大きい程速い。定量的には、RRP にある小胞の数を[RRP]、その放出確率をPvとすると、一回の刺激で放出される小胞の数は平均[RRP]*Pvとなる。一方、TRP にある小胞の数を[TRP]、一回の刺激による TRP の蛍光の減弱率を kとすると、一回の刺激で放出される小胞の数は[TRP]*kとなる。よって、[RRP]*Pv = [TRP]*k となり、これからPv=k*[RRP]/[TRP] という関係式が得られ、終末ごとにRRPにある小胞の放出確率を求めることができる [4]。
FM1-43によって染めることができるリサイクリングプールの小胞は、電子顕微鏡的に終末に存在する小胞の15-20%である[5]。 この電子顕微鏡的に同定されるリサイクリングされ難いシナプス小胞の群をreserve pool 或いは resting poolと言う。このプールの小胞もゆっくりとしたリサイクリングに関係していることが他の方法によって明らかとなっている[6]。
シナプス小胞の動態の解析
開口放出した顆粒はActive zoneの周辺から内部に取り込まれ(エンドサイトーシス)、再び放出可能となる(リサイクル)。このリサイクルにかかる時間は、海馬培養標本では 20-30秒、神経筋接合部では 60秒と見積もられた。そこでRecycling pool(= RRP + Reserve pool)の測定は、RRP 測定時よりも長い時間電気刺激を与え、色素をロードする事により達成できる(例 10Hz 900 発)。リサイクルされた小胞は、元来小胞があった領域のほぼ全域に拡散し、core(中央部)への拡散のみが軽度に少なかった。また、リサイクルした小胞は、初めて刺激を受けたプール同様の放出確率を持つことが報告された[7] 。
膜融合様式の解析
FM色素には、炭素鎖数の異なる複数種類の色素がある。これらが小胞膜を染める頻度を比較することにより、融合細孔の開放時間の長短が識別可能となる。
FM2-10やFM1-43色素を用い、小胞膜から離脱する完全融合型(full fusion)と、離脱しない不完全融合型(incomplete fusion)の識別が行われた[8] [9]。
開口放出現象の可視化
FM1-43を網膜双極性細胞のシナプス小胞に取り込ませて標識し、全反射顕微鏡で細胞膜直下(~100nm)の観察を行い、単一小胞の開口放出現象の可視化が報告された[10] 。
また、下垂体前葉細胞 (lactotrophs) や膵島細胞においても、ホルモンを含む大型有芯小胞の膜融合に伴い、開口放出部位においてFM1-43蛍光強度の上昇が報告された [11][12]。
分泌小胞の直径測定
シナプス小胞から大型有芯小胞に至るまで、小胞の直径計測に有効である [13]。
水溶性色素(赤色スルホローダミンB, SRB)とFM1-43を細胞外液に同時に与え、開口放出を誘発すると、水溶性色素は小胞内部に進入し、FM1-43は細胞外膜から小胞内膜へ拡散するため、開口放出した小胞が両色素で描出される。この際 2光子レーザー走査顕微鏡で画像を取得し、双方の色素の増加分の比を求めると小胞直径が計算される(直径=6 ΔSRB/ΔFM1-43)。本法は色素濃度やレンズ特性(点拡がり関数)によらず、シナプス小胞のような光学解像度以下の器官の計測にも応用可能である。
関連項目
参考文献
- ↑
Cochilla, A.J., Angleson, J.K., & Betz, W.J. (1999).
Monitoring secretory membrane with FM1-43 fluorescence. Annual review of neuroscience, 22, 1-10. [PubMed:10202529] [WorldCat] [DOI] - ↑
Wu, Y., Yeh, F.L., Mao, F., & Chapman, E.R. (2009).
Biophysical characterization of styryl dye-membrane interactions. Biophysical journal, 97(1), 101-9. [PubMed:19580748] [PMC] [WorldCat] [DOI] - ↑
Rizzoli, S.O., & Betz, W.J. (2004).
The structural organization of the readily releasable pool of synaptic vesicles. Science (New York, N.Y.), 303(5666), 2037-9. [PubMed:15044806] [WorldCat] [DOI] - ↑
Ermolyuk, Y.S., Alder, F.G., Henneberger, C., Rusakov, D.A., Kullmann, D.M., & Volynski, K.E. (2012).
Independent regulation of basal neurotransmitter release efficacy by variable Ca²+ influx and bouton size at small central synapses. PLoS biology, 10(9), e1001396. [PubMed:23049481] [PMC] [WorldCat] [DOI] - ↑
Rizzoli, S.O., & Betz, W.J. (2004).
The structural organization of the readily releasable pool of synaptic vesicles. Science (New York, N.Y.), 303(5666), 2037-9. [PubMed:15044806] [WorldCat] [DOI] - ↑
Hua, Z., Leal-Ortiz, S., Foss, S.M., Waites, C.L., Garner, C.C., Voglmaier, S.M., & Edwards, R.H. (2011).
v-SNARE composition distinguishes synaptic vesicle pools. Neuron, 71(3), 474-87. [PubMed:21835344] [PMC] [WorldCat] [DOI] - ↑
Betz, W.J., & Bewick, G.S. (1992).
Optical analysis of synaptic vesicle recycling at the frog neuromuscular junction. Science (New York, N.Y.), 255(5041), 200-3. [PubMed:1553547] [WorldCat] [DOI] - ↑
Klingauf, J., Kavalali, E.T., & Tsien, R.W. (1998).
Kinetics and regulation of fast endocytosis at hippocampal synapses. Nature, 394(6693), 581-5. [PubMed:9707119] [WorldCat] [DOI] - ↑
Zenisek, D., Steyer, J.A., Feldman, M.E., & Almers, W. (2002).
A membrane marker leaves synaptic vesicles in milliseconds after exocytosis in retinal bipolar cells. Neuron, 35(6), 1085-97. [PubMed:12354398] [WorldCat] [DOI] - ↑
Zenisek, D., Steyer, J.A., & Almers, W. (2000).
Transport, capture and exocytosis of single synaptic vesicles at active zones. Nature, 406(6798), 849-54. [PubMed:10972279] [WorldCat] [DOI] - ↑
Cochilla, A.J., Angleson, J.K., & Betz, W.J. (2000).
Differential regulation of granule-to-granule and granule-to-plasma membrane fusion during secretion from rat pituitary lactotrophs. The Journal of cell biology, 150(4), 839-48. [PubMed:10953007] [PMC] [WorldCat] [DOI] - ↑
Takahashi, N., Kishimoto, T., Nemoto, T., Kadowaki, T., & Kasai, H. (2002).
Fusion pore dynamics and insulin granule exocytosis in the pancreatic islet. Science (New York, N.Y.), 297(5585), 1349-52. [PubMed:12193788] [WorldCat] [DOI] - ↑
Kasai, H., Hatakeyama, H., Kishimoto, T., Liu, T.T., Nemoto, T., & Takahashi, N. (2005).
A new quantitative (two-photon extracellular polar-tracer imaging-based quantification (TEPIQ)) analysis for diameters of exocytic vesicles and its application to mouse pancreatic islets. The Journal of physiology, 568(Pt 3), 891-903. [PubMed:16150799] [PMC] [WorldCat] [DOI]
(執筆者:高橋倫子、河西春郎 担当編集委員:柚崎通介)