「ランヴィエ絞輪」の版間の差分
細編集の要約なし |
|||
| (2人の利用者による、間の3版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/hidekazutsutsui/ 筒井 秀和]、[http://researchmap.jp/yasushiokamura 岡村 康司]</font><br> | <font size="+1">[http://researchmap.jp/hidekazutsutsui/ 筒井 秀和]、[http://researchmap.jp/yasushiokamura 岡村 康司]</font><br> | ||
''大阪大学 医学系研究科''<br> | ''大阪大学 医学系研究科''<br> | ||
DOI [[XXXX]]/XXXX 原稿受付日:2013年11月2日 原稿完成日:2013年11月18日<br> | |||
担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | 担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | ||
</div> | </div> | ||
| 11行目: | 11行目: | ||
==ランヴィエ絞輪とは== | ==ランヴィエ絞輪とは== | ||
有髄神経軸索はミエリン鞘(髄鞘)で囲まれる。そこに、1-2 mmおきに周期的に存在する、髄鞘で囲まれていない1 μm程度の間隙のことをランヴィエの絞輪という。[[w: | 有髄神経軸索はミエリン鞘(髄鞘)で囲まれる。そこに、1-2 mmおきに周期的に存在する、髄鞘で囲まれていない1 μm程度の間隙のことをランヴィエの絞輪という。[[w:ランヴィエ|ランヴィエ]](L.A.Ranvier)は、フランスの組織学者で、この構造を最初に記載した。この部位を興奮が跳躍伝導することを、日本の生理学者[[wj:田崎一二|田崎一二]]が[[wj:カエル|カエル]]の[[末梢神経]]で世界にさきがけて明らかにした。 | ||
==機能== | ==機能== | ||
| 42行目: | 42行目: | ||
またランヴィエの絞輪部の軸索には[[intramembranous particles]] (IMP)と呼ばれる顆粒構造が存在し、これは[[ナトリウムチャネル|電位依存性Na<sup>+</sup>チャネル]]を含んだものだと考えられている。 | またランヴィエの絞輪部の軸索には[[intramembranous particles]] (IMP)と呼ばれる顆粒構造が存在し、これは[[ナトリウムチャネル|電位依存性Na<sup>+</sup>チャネル]]を含んだものだと考えられている。 | ||
ランヴィエの絞輪の両端には[[パラノード]] | ランヴィエの絞輪の両端には[[パラノード]](paranode)とよばれる構造が隣接する。パラノード部では髄鞘が肥大し細胞質成分が観察され、paranodal loopと呼ばれる構造を示す。パラノード部では、40個以上のparanodal loopがらせん状に軸索と[[接着分子]]を介して密着し、電気的な絶縁と、分子の拡散障壁部を形成している。この構造は、ボルト(=軸索)とナット(=paranodal loop)にもたとえられる。 | ||
パラノード部の両遠部には、[[傍パラノード]] | パラノード部の両遠部には、[[傍パラノード]]部(juxtaparanode)があり、その両遠部がインターノード部(internode)となる。 | ||
==分子== | ==分子== | ||
| 55行目: | 55行目: | ||
*[[シュワン細胞]] | *[[シュワン細胞]] | ||
*[[跳躍伝導]] | *[[跳躍伝導]] | ||
==参考文献== | ==参考文献== | ||
<references /> | <references /> | ||
2013年11月18日 (月) 14:33時点における版
筒井 秀和、岡村 康司
大阪大学 医学系研究科
DOI XXXX/XXXX 原稿受付日:2013年11月2日 原稿完成日:2013年11月18日
担当編集委員:林 康紀(独立行政法人理化学研究所 脳科学総合研究センター)
英語名 node of Ranvier、myelin sheath gap 独:Ranvier-Schnürring、Ranvier’scher Schnürring、Ranvier-Node 仏:Nœud de Ranvier
有髄神経軸索はミエリン鞘(髄鞘)で囲まれる。そこに、1-2 mmおきに周期的に存在する、髄鞘で囲まれていない1 μm程度の間隙のことをランヴィエの絞輪という。有髄線維では、この部位を興奮が跳躍伝導する事により神経伝達速度を向上させている。ランヴィエ絞輪には足場タンパク質としてスペクトリン、アンキリンG、これらを足場としてNav1.6、KCNQ等のチャネルやNa+-K+-ATPaseが集積する。パラノード部には、caspr, neurofasin などの接着分子が発現する。傍パラノードにはKv1.1、Kv1.2などの電位依存性カリウムチャネルが存在する
ランヴィエ絞輪とは
有髄神経軸索はミエリン鞘(髄鞘)で囲まれる。そこに、1-2 mmおきに周期的に存在する、髄鞘で囲まれていない1 μm程度の間隙のことをランヴィエの絞輪という。ランヴィエ(L.A.Ranvier)は、フランスの組織学者で、この構造を最初に記載した。この部位を興奮が跳躍伝導することを、日本の生理学者田崎一二がカエルの末梢神経で世界にさきがけて明らかにした。
機能
Kelvinは大西洋横断ケーブルの特性を理解するためにケーブル理論を考案した。その理論は原理的に、神経線維へも適用できる[1]。その中で、電気信号の伝達速度を規定するパラメータは、長さ定数(length constant; λ)
である。ここで、Rm:膜抵抗、Re:細胞外抵抗、Ri:細胞内抵抗である。λは、伝達速度とほぼ比例の関係にある。
捕食や逃避といった行動を考えると、神経伝達速度を上昇させることは、進化の過程で重要な選択圧であることが想像できる。
長いλを実現するためには、例えば、無脊椎動物であるイカの巨大軸索に見られるように、軸索を太くしてRiを下げる例があるが、その一方で、脊椎動物では髄鞘を巻いてRmを大きくする方法が獲得された。髄鞘で囲まれていない間隙、すなわち、ランヴィエの絞輪にはアンキリンなどのタンパク質を足場にして電位依存性チャネルが集積し、これにより跳躍伝導が起き[2]、高速(30-160 m/s)で減衰の無い信号伝達が実現されている。跳躍伝導はクルマエビなどの節足動物でも見られ、これは進化的に独立に獲得されたと考えられている[3]。
髄鞘を用いる方法は、太い軸索に比べて、
- 軸索を相対的にコンパクトにでき、集積化に適する。
- イオン環境の変動が小さく、恒常性維持のためのエネルギー消費が節約できる。また集積化した際にも、神経線維間で電気信号の混線が起きにくい。
- 髄鞘の巻き数や絞輪の間隔を制御する事で、伝達速度の微妙な調節が可能、などの利点を持つと考えられる[3]。
例えば、巨大軸索と比較した場合、スペースで1万5千倍、エネルギー消費で数千倍の節約効果があると見積もられている[4]。
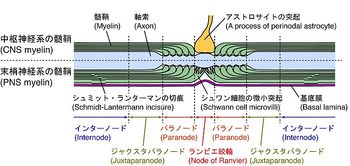
吉村 武、池中 一裕による髄鞘の項目から。
構造
ランヴィエの絞輪の長さは神経線維の種類や太さにもよるが、典型的には1-2 μm程度で、間隔は1-2 mm程度である。この間隔は、活動電位の伝播に必要最低限な間隔よりも短い。実際の間隔と必要最低限の間隔の比を安全率(safety factor)と呼ぶ。健常な線維では、安全率は5-7程度と高い[2]。
中枢神経系ではオリゴデンドロサイトが、末梢神経系ではシュワン細胞が髄鞘形成を担うが、ランヴィエの絞輪の微細構造も、中枢と末梢では大きく異なる(図1)[4]。例えば、末梢神経では、髄鞘をつくるシュワン細胞から多くの微絨毛が絞輪部まで伸び、その先端部はほぼ垂直に細胞膜近傍に位置する。これに対し、中枢神経では、アストロサイトがランヴィエの絞輪の近傍まで微細突起を伸ばしている事が多い。どちらにおいても軸索の太さは、ランヴィエの絞輪では細くなっている。
太い線維においては、ランヴィエの絞輪部では、髄鞘が被っている部分(インターノード)における軸索径に比べて1/5の程度の細さにまでなる[4]。
またランヴィエの絞輪部の軸索にはintramembranous particles (IMP)と呼ばれる顆粒構造が存在し、これは電位依存性Na+チャネルを含んだものだと考えられている。
ランヴィエの絞輪の両端にはパラノード(paranode)とよばれる構造が隣接する。パラノード部では髄鞘が肥大し細胞質成分が観察され、paranodal loopと呼ばれる構造を示す。パラノード部では、40個以上のparanodal loopがらせん状に軸索と接着分子を介して密着し、電気的な絶縁と、分子の拡散障壁部を形成している。この構造は、ボルト(=軸索)とナット(=paranodal loop)にもたとえられる。
パラノード部の両遠部には、傍パラノード部(juxtaparanode)があり、その両遠部がインターノード部(internode)となる。
分子
ランヴィエの絞輪部には足場タンパク質としてスペクトリン、アンキリンGが存在する。これらを足場としてNav1.6、KCNQ等のチャネルやNa+-K+-ATPaseが集積する。この状況は、軸索起始部と似ており、その相同性が示されている。パラノード部には、caspr, neurofasin などの接着分子が発現する。傍パラノード部にはKv1.1、Kv1.2,などの電位依存性カリウムチャネル (K+チャネル)が存在する[5][6]。Na+チャネル、K+チャネルがこのように空間的に相補的な発現をする事の生理学的意義については議論が続けられている。
関連項目
参考文献
- ↑ K.S. Cole
Membranes, ions, and impulses.
University of California Press, 1972 - ↑ 2.0 2.1 I. Tasaki
"Conduction of the nerve impulse"
Handbook of Physiology 1959, Section 1, 75 - ↑ 3.0 3.1
Hartline, D.K., & Colman, D.R. (2007).
Rapid conduction and the evolution of giant axons and myelinated fibers. Current biology : CB, 17(1), R29-35. [PubMed:17208176] [WorldCat] [DOI] - ↑ 4.0 4.1 4.2
Salzer, J.L. (1997).
Clustering sodium channels at the node of Ranvier: close encounters of the axon-glia kind. Neuron, 18(6), 843-6. [PubMed:9208851] [WorldCat] [DOI] - ↑
Rasband, M.N., & Shrager, P. (2000).
Ion channel sequestration in central nervous system axons. The Journal of physiology, 525 Pt 1, 63-73. [PubMed:10811725] [PMC] [WorldCat] [DOI] - ↑
Lai, H.C., & Jan, L.Y. (2006).
The distribution and targeting of neuronal voltage-gated ion channels. Nature reviews. Neuroscience, 7(7), 548-62. [PubMed:16791144] [WorldCat] [DOI]
