「シュワン細胞」の版間の差分
細 →神経鞘腫 |
細 →神経鞘腫 |
(相違点なし)
| |
2020年1月9日 (木) 11:22時点における最新版
村松 里衣子、山下 俊英
大阪大学大学院医学系研究科分子神経科学
DOI:10.14931/bsd.556 原稿受付日:2012年2月2日 原稿完成日:2013年6月4日
担当編集委員:林 康紀(独立行政法人理化学研究所 脳科学総合研究センター)
英語名:Schwann cell 独:Schwann Zelle 仏:Cellule de Schwann
シュワン細胞(シュヴァン細胞)は末梢神経系のグリア細胞の一つ。ドイツの生物学者Theodor Schwannにより発見された。一部の細胞はミエリンを形成する。発生期の神経細胞の生存や軸索投射、損傷後の神経回路の再生に寄与する。ミエリン形成により跳躍伝導を司る。シュワン細胞由来の腫瘍形成や脱髄疾患では、遺伝子変異が報告されている。
種類
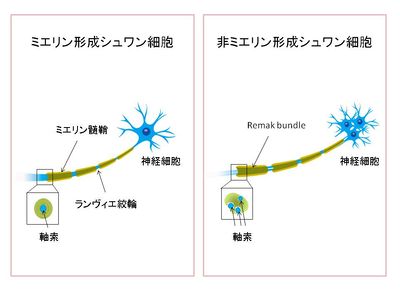
シュワン細胞は、ミエリン形成の有無で2つに大別される。
ミエリン形成シュワン細胞
すべての運動神経や一部の感覚神経を含む、大きい直径の軸索の周囲を覆う。1つのシュワン細胞は一つの軸索に付随し、ミエリンを形成する。軸索の直径や神経線維のリン酸化を制御する。ミエリンには切れ目があり、発見者 (フランスの病理学者Louis-Antoine Ranvier) の名前から、ランヴィエ絞輪と呼ばれている。末梢の有髄神経のランヴィエ絞輪の間隔は200-1500 µm程度ある(無髄神経で隣接するシュワン細胞の核の間隔は90 µm以下)。ランヴィエ絞輪部分は細胞外液にさらされており、また、高い密度でイオンチャネルが分布している (Na+チャネルは1000 µm-2) 。そのため、髄鞘に覆われている部分と比較し活動電位が発生しやすい状態であり、跳躍伝導が生じる場となっている[1]。これらの構造のため、有髄神経は同じ直径の無髄神経と比較し、活動電位の伝導がおよそ10倍早まる。
非ミエリンシュワン細胞
一部の感覚神経細胞からのC線維や交感神経節後細胞など、小さい直径 (0.5-1.5µm)の軸索ならびに神経筋接合部に関連する。1つのシュワン細胞は複数と接触する。軸索周囲で細胞体を薄く伸展させRemak bundlesを形成したり、運動神経の前シナプス終末を覆っている。成体では、ミエリン形成シュワン細胞数の4倍存在する[2]。
発生
分化過程
大部分は外胚葉の神経堤に由来し、胎生期中に細胞を成熟させながら標的となる末梢神経へ移動する。幹細胞は、シュワン前駆細胞、未成熟シュワン細胞を経て成熟シュワン細胞へ分化する。ラットでは胎生14-15日でシュワン前駆細胞、胎生15-17日で未成熟シュワン細胞へ分化する (マウスではそれぞれ胎生12-13日、13-15日)。その後、出生にかけて成熟細胞になり、生後数週間かけてミエリン形成を完成させる。
シュワン細胞の分化は、おおむね可逆的である(前駆細胞から未成熟シュワン細胞への分化は不可逆的)。最終的に分化する細胞の形態は、関連する軸索からのシグナルから決定される。一部のシュワン細胞前駆細胞は、神経細胞や線維芽細胞などグリア細胞系譜以外の細胞へも分化する。
分子メカニズム
ニューレグリン (NRG)、エンドセリン、Notch、骨形成タンパク質(Bone Morphogenetic Protein, BMP)、インスリン様成長因子 (IGF)、血小板由来成長因子(PDGF)、神経栄養因子など数多くの因子が、シュワン細胞の分化や脱分化、そして生存機構に関与すると報告されている。
各分化段階でシュワン細胞に発現するたんぱく質は変化する。幹細胞から未成熟シュワン細胞までに共通して発現する因子として、SOX10、p75神経栄養因子受容体、L1、ErbB3などが挙げられる。シュワン前駆細胞と未成熟シュワン細胞では、protein zero (P0)、GAP43、peripheral myelin protein 22-kDa (PMP22)、desert hedgehog (DHH)やbrain fatty acid-binding protein (BFABP)などが発現している[3]。
ニューレグリンは上皮成長因子(EGF)と相同性が高い分子で、受容体型チロシンキナーゼのErbBを介してシグナル伝達を行う。NRG-1ならびにErbB2/3を欠損させたマウスでは、末梢神経でシュワン前駆細胞およびシュワン細胞の欠損が観察される。このことから、NRGシグナルはシュワン細胞の発達に主要な役割を果たすと考えられており、二次的に神経細胞の発生にも影響を与える。
シュワン細胞は軸索と接することによりDNA合成が促され、細胞増殖が活発になるが、そのメカニズムには軸索由来のNRGの関与が示唆されている。発生途中に軸索を除去するとシュワン細胞は脱落するが、NRG-1処置により生存が維持される。NRGあるいはその受容体のErbB3のシグナルを中和すると、軸索シュワン細胞の増殖は低下する。このことから、軸索由来のNRGがシュワン細胞の増殖・生存の維持に寄与していると考えられている。
NGR-1、ErbB2,3、ならびにSox10欠損マウスではシュワン細胞の欠損が生じるが、さらに投射途中の後根神経節の神経細胞や運動神経細胞で神経細胞死も観察される。これは、シュワン細胞による神経細胞への栄養因子供給が欠如するためと示唆されている。
ラット胎生14日ごろの末梢神経では、シュワン前駆細胞が神経の外縁部や内部に分布し、多くの軸索を包み込もうとしている。それらは互いにシート状の突起で連絡しはじめ、胎生18日に組織間隙との交通がないコンパクトな状態となり、軸索を束状化させる。NGRシグナル欠損マウスでは、異所性に併走する軸索がしばしば観察され、これはミエリンによる囲い込みが不完全な結果と示唆されている。すなわちNRGは間接的に軸索の束状化にも寄与する[4]。
ランヴィエ絞輪部分へのNa+チャネルの集積には、ミエリン化したシュワン細胞が発現するGliomedinの関与が示唆されている[5] [6]。
病態との関連
腫瘍
神経鞘腫
神経鞘腫は全脳腫瘍の8.9%を占める。良性の腫瘍であり、成人に多く、女性は男性の1.4倍多い。頭蓋内の神経鞘腫は95%が第Ⅷ神経より発生する。第Ⅷ神経より発生する場合、ほとんどが前庭神経より発生する。Neurofibromatosis type (NF) 2遺伝子の関与が指摘されている。
神経線維腫症
神経線維腫症は皮下や筋肉などの軟部組織に発生する良性の腫瘍である。局所の圧痛が生じる。成人に見られ、男女差はない。NF1あるいはNF2が責任遺伝子と示唆されており、それぞれ神経線維腫症1型、2型に分類され、どちらも難病指定されている。2型は聴神経鞘腫悪性化がしばしば観察され、神経鞘腫と合併することがある。
脱髄疾患
シャルコー・マリー・トゥース病タイプI
シャルコー・マリー・トゥース病(Charcot-Marie-Tooth disease)タイプIは下肢の筋緊張や感覚障害を特徴とする遺伝性の末梢神経障害である。多くが若年(10-20歳)で発症し、ミエリンおよび軸索の傷害が進むにつれ広範に神経症状があらわれる。シャルコー・マリー・トゥース病タイプⅠでは、ミエリンの脱落および神経伝達速度の遅延が認められる。常染色体優性遺伝であり、中でもPMP22の変異の割合が最も高い。
ギランバレー症候群
ギランバレー症候群は急性多発性神経炎の一つで、四肢の神経障害に始まる。先行感染に伴うことから免疫系の異常な活性化が原因と考えられているが、原因は未だ不明な指定難病。脱髄に加え軸索傷害を伴う場合もある。急性・単相性の経過で、症状は4週間以内にピークを迎えた後に徐々に回復に向かうと言われているが、部分的に機能障害が残る。
神経回路の再生
中枢神経系と異なり、切断あるいは挫傷の後、細胞死を免れた末梢神経は再生する。再生能力が乏しい中枢神経であっても、移植した末梢神経組織の中では再生していく様子が、中枢神経損傷ラットの延髄と脊髄の間に坐骨神経を移植する実験から示されている[7]。このことから、末梢神経組織は中枢神経組織と比較し再生に適した環境と考えられている。
神経回路の再生は、損傷により断片化された組織が除去された後に、軸索が再伸長して完成する。損傷を受け活性化したシュワン細胞は、マクロファージの遊走性を高める。その結果、損傷部分で断片化した神経組織の貧食が進み、軸索の再生に適した場を提供する。
損傷部周囲のシュワン細胞は、脱分化し細胞増殖する。増殖したシュワン細胞は、Büngner’s bandと呼ばれる構造物を形成し、その内部を再生軸索が走行していく。ここには神経成長因子 (NGF)、グリア細胞株由来神経栄養因子(GDNF)などの成長を促す因子は豊富が発現している。また、ラミニンやフィブロネクチンなど軸索伸長の足場となる因子も発現している。これらは単独で軸索伸長を促進、あるいはNGFなど作用を増大させると考えられている[8]。
関連項目
参考文献
- ↑
Waxman, S.G., & Ritchie, J.M. (1993).
Molecular dissection of the myelinated axon. Annals of neurology, 33(2), 121-36. [PubMed:7679565] [WorldCat] [DOI] - ↑
Griffin, J.W., & Thompson, W.J. (2008).
Biology and pathology of nonmyelinating Schwann cells. Glia, 56(14), 1518-31. [PubMed:18803315] [WorldCat] [DOI] - ↑
Jessen, K.R., & Mirsky, R. (2005).
The origin and development of glial cells in peripheral nerves. Nature reviews. Neuroscience, 6(9), 671-82. [PubMed:16136171] [WorldCat] [DOI] - ↑
Birchmeier, C., & Nave, K.A. (2008).
Neuregulin-1, a key axonal signal that drives Schwann cell growth and differentiation. Glia, 56(14), 1491-7. [PubMed:18803318] [WorldCat] [DOI] - ↑
Eshed, Y., Feinberg, K., Poliak, S., Sabanay, H., Sarig-Nadir, O., Spiegel, I., ..., & Peles, E. (2005).
Gliomedin mediates Schwann cell-axon interaction and the molecular assembly of the nodes of Ranvier. Neuron, 47(2), 215-29. [PubMed:16039564] [WorldCat] [DOI] - ↑
Feinberg, K., Eshed-Eisenbach, Y., Frechter, S., Amor, V., Salomon, D., Sabanay, H., ..., & Peles, E. (2010).
A glial signal consisting of gliomedin and NrCAM clusters axonal Na+ channels during the formation of nodes of Ranvier. Neuron, 65(4), 490-502. [PubMed:20188654] [PMC] [WorldCat] [DOI] - ↑
Richardson, P.M., McGuinness, U.M., & Aguayo, A.J. (1980).
Axons from CNS neurons regenerate into PNS grafts. Nature, 284(5753), 264-5. [PubMed:7360259] [WorldCat] [DOI] - ↑
Webber, C., & Zochodne, D. (2010).
The nerve regenerative microenvironment: early behavior and partnership of axons and Schwann cells. Experimental neurology, 223(1), 51-9. [PubMed:19501085] [WorldCat] [DOI]