「筋ジストロフィー」の版間の差分
細編集の要約なし |
細 →治療 |
||
| (同じ利用者による、間の14版が非表示) | |||
| 1行目: | 1行目: | ||
<div align="right"> | |||
<font size="+1">[https://researchmap.jp/ono_hiro 小野 洋也]、[https://researchmap.jp/634?lang=ja 青木 吉嗣]</font><br> | |||
''国立研究開発法人国立精神・神経医療研究センター 神経研究所遺伝子疾患治療研究部''<br> | |||
DOI:<selfdoi /> 原稿受付日:2025年5月4日 原稿完成日:2026年4月15日<br> | |||
担当編集委員:[https://researchmap.jp/shinsuke.ishigaki 石垣 診祐](滋賀医科大学 神経難病研究センター)<br> | |||
</div> | |||
英:muscular dystrophy 独:Muskeldystrophie 仏:dystrophie musculaire <br> | |||
{{box|text= 筋ジストロフィーは、遺伝的要因により慢性進行性の筋力低下と筋萎縮を生じる疾患群の総称である。単一の疾患ではなく、原因遺伝子、遺伝形式、発症年齢、障害される筋の分布、進行速度、筋外症状の異なる多数の病型を含む。代表的病型として、デュシェンヌ型筋ジストロフィー(Duchenne muscular dystrophy)、ベッカー型筋ジストロフィー(Becker muscular dystrophy)、筋強直性ジストロフィー(myotonic dystrophy)、顔面肩甲上腕型筋ジストロフィー(facioscapulohumeral muscular dystrophy)、肢帯型筋ジストロフィー(limb-girdle muscular dystrophy)などがある<ref name=Mercuri2013><pubmed>23465426</pubmed></ref><ref name=Birnkrant2018>'''Birnkrant DJ, Bushby K, Bann CM, et al. (2018)'''<br>Diagnosis and management of Duchenne muscular dystrophy, parts 1-3. Lancet Neurol. 17:251-267.</ref><ref name=Harper2001>'''Harper PS. (2001).'''<br>Myotonic Dystrophy. 3rd ed. London: WB Saunders</ref><ref name=Tawil2015><pubmed>26215877</pubmed></ref><ref name=Straub2018><pubmed>30055862</pubmed></ref>。近年は遺伝学的検査が診断の中心となっている。また、一部の病型では変異に応じた分子病態に基づく治療や遺伝子治療が導入されている<ref name=Straub2022><pubmed>34863211</pubmed></ref><ref name=Komaki2020><pubmed>33285037</pubmed></ref><ref name=PMDA2025>Pharmaceuticals and Medical Devices Agency. Delandistrogene moxeparvovec (ELEVIDYS) for Duchenne muscular dystrophy: approval and safety information. 2025.</ref>。}} | |||
== 筋ジストロフィーとは== | |||
[[骨格筋]]の進行性[[変性]]と[[筋力]]低下を主徴とする遺伝性筋疾患群である。従来は臨床症候に基づいて分類されてきたが、分子遺伝学の進歩により、それぞれ異なる原因遺伝子と病態機序をもつ疾患の集合体であることが明らかになった<ref name=Mercuri2013/><ref name=Emery2002><pubmed>11879882</pubmed></ref>。現在では50を超える病型・病型亜分類が知られており、臨床像、遺伝形式、病理所見、遺伝学的所見を統合して分類される。 | |||
代表的病型の分子基盤として、[[デュシェンヌ型筋ジストロフィー]]/[[ベッカー型筋ジストロフィー]]では[[Dystrophin]] ([[DMD]])遺伝子、[[筋強直性ジストロフィー1型]]では[[Dystrophia myotonica protein kinase]] ([[DMPK]])遺伝子のCTGリピート伸長、[[筋強直性ジストロフィー2型]]では[[Cellular nucleic acid binding protein]] ([[CNBP]])遺伝子のCCTGリピート伸長、[[顔面肩甲上腕型筋ジストロフィー]]では[[Double homeobox 4]] ([[DUX4]])異常発現、[[肢帯型筋ジストロフィー]]では[[Calpain 3]] ([[CAPN3]])や[[Dysferlin]] ([[DYSF]])など複数遺伝子の異常が知られる<ref name=Harper2001/><ref name=Tawil2015/><ref name=Straub2018/><ref name=Richard1995><pubmed>7720071</pubmed></ref><ref name=Liu1998><pubmed>9731526</pubmed></ref>。 | |||
筋ジストロフィーは骨格筋のみの疾患ではない。デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーでは、脳内で発現するジストロフィン・アイソフォームの異常と関連して、発達、認知、行動面の変化がみられることがある。また、筋強直性ジストロフィーでは、[[認知機能]]障害、日中の過度の眠気、[[注意]]・[[遂行機能障害]]などの中枢神経症状がみられる<ref name=Udd2012><pubmed>22995693</pubmed></ref><ref name=日本神経学会>日本神経学会. 筋強直性ジストロフィー診療ガイドライン.</ref><ref name=Hendriksen2008><pubmed>18354150</pubmed></ref><ref name=Doorenweerd2017><pubmed>28974727</pubmed></ref>。代表的筋ジストロフィーの主な特徴と中枢神経系との対応を表1に示す。 | |||
{| class="wikitable" | |||
|+ 表1.代表的筋ジストロフィーの特徴と中枢神経系との関連 | |||
! 病型 | |||
! 原因遺伝子・機序 | |||
! 主な筋症状 | |||
! 中枢神経症状 | |||
! 発症時期・特徴 | |||
|- | |||
| デュシェンヌ型筋ジストロフィー | |||
| [[Dystrophin]] ([[DMD]]) 遺伝子変異 | |||
| 小児期発症、近位筋優位の進行性筋力低下、歩行・呼吸・心筋障害 | |||
| 発達遅滞、学習障害、知的機能低下、注意障害、行動面の問題 | |||
| 幼児期発症、進行が比較的速い | |||
|- | |||
| ベッカー型筋ジストロフィー | |||
| DMD遺伝子変異 | |||
| 軽症で進行が緩徐、近位筋優位、心筋障害 | |||
| 認知・行動面の変化を示す例がある | |||
| 思春期以降発症が多い | |||
|- | |||
| 筋強直性ジストロフィー1型 | |||
| [[Dystrophia myotonica protein kinase]] ([[DMPK]]) 遺伝子のCTGリピート伸長 | |||
| 筋強直、遠位筋優位の筋力低下、顔面筋障害、白内障、心伝導障害 | |||
| 認知機能障害、日中の過度の眠気、注意・遂行機能障害 | |||
| 小児期〜成人期、成人で頻度が高い | |||
|- | |||
| 筋強直性ジストロフィー2型 | |||
| [[Cellular nucleic acid binding protein]] ([[CNBP]]) 遺伝子のCCTGリピート伸長 | |||
| 筋強直、近位筋優位の筋力低下、筋痛、白内障、不整脈 | |||
| 中枢神経症状を伴うことがある | |||
| 成人期発症、1型より緩徐 | |||
|- | |||
| 顔面肩甲上腕型筋ジストロフィー(1型および2型) | |||
| D4Z4リピート短縮や[[Structural maintenance of chromosomes flexible hinge domain containing 1]] ([[SMCHD1]]) 異常などを背景とした[[Double homeobox 4]] ([[DUX4]]) 異常発現 | |||
| 顔面・肩甲帯優位の筋力低下、左右差を伴うことがある | |||
| 典型例では中枢神経症状は前景ではない、早期発症例では知的機能低下やてんかんを伴うことがある | |||
| 思春期〜成人期初期に発症することが多い | |||
|- | |||
| 肢帯型筋ジストロフィー | |||
| 複数の原因遺伝子 | |||
| 肩帯・骨盤帯筋優位の筋力低下 | |||
| 一部で知的機能低下などを伴う | |||
| 発症時期・進行速度とも多様 | |||
|- | |||
| 福山型先天性筋ジストロフィー | |||
| [[Fukutin]] ([[FKTN]]) 遺伝子変異 | |||
| | |||
| 大脳皮質形成異常、てんかん、知的機能低下 | |||
| 乳児期発症、日本で比較的多い | |||
|} | |||
''注:症状の頻度や重症度は病型および症例により異なる。'' | |||
[[ファイル:Aoki Muscular Dystrophy Fig1.png|サムネイル|'''図1. 全長型ジストロフィン・タンパク質の構造'''<br>骨格筋、心筋、大脳、小脳などで発現する全長型ジストロフィン・タンパク質の主要ドメイン構造を示す。ジストロフィン・タンパク質は、アクチン結合ドメインを介してF-アクチンに、システインリッチドメインを介して筋線維膜貫通タンパク質であるβ-ジストログリカンに結合する(詳細は図2参照)。]] | |||
[[ファイル:Aoki Muscular Dystrophy Fig2.png|サムネイル|'''図2. ジストロフィン糖タンパク質複合体の模式図'''<br>ジストロフィン糖タンパク質複合体を構成する主要分子と、その筋線維膜近傍での配置を示す。ECD( extracellular domain tower)タワー:膜外に突出した細胞外ドメイン群が形成する塔状構造。富成司博士作成図を改変。 | |||
]] | |||
[[ファイル:Aoki Muscular Dystrophy Fig3.png|サムネイル|'''図3. DMD遺伝子変異に対するエクソン53スキップ治療の模式図'''<br> | |||
DMD遺伝子から前駆体mRNAが転写され、スプライシングを受けて成熟mRNAとなり、ジストロフィン・タンパク質が合成される。変異DMD遺伝子(例:エクソン52欠失)では、アンチセンス核酸であるビルトラルセンによりエクソン53スキップを誘導することで、アウトオブフレームがインフレーム化(mRNAの読み枠が回復)した成熟mRNAから短縮型ジストロフィン・タンパク質が産生される。]] | |||
== 診断 == | |||
筋ジストロフィーの診断は、病歴、家族歴、神経学的診察、血清[[クレアチンキナーゼ]](creatine kinase: CK)測定、[[筋電図]]、筋画像、筋生検、遺伝子検査などを組み合わせて行う。進行性筋力低下の分布、発症年齢、[[筋強直]]の有無、[[心筋]]障害、呼吸障害、中枢神経症状などの筋外症状、および家族歴は、病型推定に有用である<ref name=Mercuri2013/><ref name=Emery2002/>。血清クレアチンキナーゼ値は多くの病型で上昇するが、上昇の程度は病型や病期によって異なる。近年は[[次世代シークエンス]]を含む遺伝学的検査が診断の中心であり、必要に応じて筋病理や画像所見を補助的に用いる<ref name=Straub2022/>。とくにデュシェンヌ型筋ジストロフィー/ベッカー型筋ジストロフィーでは、[[欠失]]・[[重複]]、[[点変異]]、[[スプライシング]]異常の評価が重要である。 | |||
=== 鑑別診断 === | |||
[[炎症性筋疾患]]、[[代謝性ミオパチー]]、[[ミトコンドリア病]]、[[先天性ミオパチー]]、[[運動ニューロン疾患]]、[[末梢神経障害]]などが挙げられる。さらに、筋ジストロフィーの中でも病型間の鑑別は重要であり、発症年齢、筋障害の分布、筋外症状、遺伝形式が手がかりとなる。たとえば、中枢神経症状が前景に出る場合にはデュシェンヌ型筋ジストロフィー関連認知障害や[[筋強直性ジストロフィー]]を考慮し、顔面・肩甲帯優位なら顔面肩甲上腕型筋ジストロフィー、近位筋優位なら肢帯型筋ジストロフィーを疑う<ref name=Birnkrant2018/><ref name=Harper2001/><ref name=Tawil2015/><ref name=Straub2018/><ref name=Udd2012/><ref name=日本神経学会/><ref name=Hendriksen2008/><ref name=Doorenweerd2017/>。 | |||
== 病態生理 == | |||
筋ジストロフィーの病態は病型により異なるが、多くは[[筋線維膜]](筋[[形質膜]])の安定化、[[細胞骨格]]と[[細胞外マトリックス]]の連結、[[核膜]]機能、[[糖鎖修飾]]、膜修復(筋線維膜の微小損傷を修復する機構)、[[RNA]]代謝、[[転写]]制御などの異常に起因する<ref name=Mercuri2013/><ref name=Emery2002/>。 | |||
さらに、多くの病型で骨格筋以外の臓器障害を伴う。心筋症や不整脈、呼吸障害、内分泌代謝異常、白内障、難聴、中枢神経症状などが代表的であり、病型特異性が高い<ref name=Mercuri2013/><ref name=Emery2002/><ref name=日本神経学会/>。脳科学の観点からは、デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーにおけるジストロフィン・アイソフォーム異常に関連して、発達、認知、行動面の変化、たとえば[[発達遅滞]]、[[学習障害]]、[[注意障害]]、[[自閉スペクトラム症]]特性などがみられることがある。さらに、筋強直性ジストロフィーにおける中枢神経症候、一部の先天性筋ジストロフィーや肢帯型筋ジストロフィーでみられる[[てんかん]]、[[知的機能]]低下、[[発達特性]]などが重要である。 | |||
=== ジストロフィン === | |||
デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーの原因分子である('''図1''')。筋線維膜においてジストロフィン糖タンパク質複合体を形成し、細胞骨格と[[細胞外マトリックス]]を連結する('''図2''')。デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーでは、この連結機構が障害されることで筋線維膜の脆弱性が増し、その結果、筋線維壊死と再生、慢性炎症、線維化、脂肪置換が進行し、筋力低下と筋萎縮を生じる。とくにデュシェンヌ型筋ジストロフィーでは、DMD遺伝子の欠失、重複、点変異、スプライシング異常によりmRNAの読み枠が崩れると、機能的タンパク質が産生されず重症化する。一方、読み枠が保たれる場合には短縮型ジストロフィン・タンパク質が産生され、比較的軽症のベッカー型筋ジストロフィーとなることが多い。こうした[[アウトオブフレーム変異]]と[[インフレーム変異]]の違い、および[[エクソン53スキッピング]]による読み枠回復の概念を'''図3'''に示す<ref name=Straub2022/><ref name=Komaki2020/><ref name=Anthony2014><pubmed>24217213</pubmed></ref>。 | |||
== 治療 == | |||
多くの筋ジストロフィーでは、現時点でも治療の基本は[[対症療法]]である。[[理学療法]]、拘縮予防、装具療法、呼吸管理、心機能管理、栄養管理、[[嚥下]]評価、生活支援は、ほぼすべての病型で重要である<ref name=Mercuri2013/><ref name=Emery2002/>。一部の病型では分子病態に基づく治療が導入されつつあり、遺伝学的診断は治療選択の観点からも重要性を増している。 | |||
デュシェンヌ型筋ジストロフィーなど一部の病型では、[[アンチセンス核酸]]、[[ウイルスベクター]]による[[遺伝子補充治療]]、[[ゲノム編集]]、[[RNA標的治療]]、細胞治療などの開発が進んでいる。たとえば、エクソン53スキッピング薬の[[ビルトラルセン]]([[ビルテプソ]]®)は、前駆体[[mRNA]]の[[スプライシング]]を操作して読み枠を回復し、短縮型ジストロフィン・タンパク質発現を促す治療である<ref name=Komaki2020/>。また、[[マイクロジストロフィン]]遺伝子を[[AAVベクター]]で導入する遺伝子治療薬の[[デランジストロゲン モキセパルボベク]]([[エレビジス]]®)は、デュシェンヌ型筋ジストロフィーに対する疾患修飾薬として臨床導入された<ref name=PMDA2025/>。一方で、適応となる病型や変異は限られており、長期的有効性と安全性の検討が続いている<ref name=Birnkrant2018/><ref name=Straub2022/><ref name=Aartsma-Rus2017><pubmed>27929755</pubmed></ref><ref name=Long2016><pubmed>26721683</pubmed></ref><ref name=PMDA2025/>。 | |||
== 疫学 == | |||
筋ジストロフィー全体の頻度は病型ごとに大きく異なる。デュシェンヌ型筋ジストロフィーは小児期発症の筋ジストロフィーとして最も頻度が高く、筋強直性ジストロフィー1型は成人発症筋ジストロフィーの中で最も頻度が高い病型である<ref name=Udd2012/><ref name=日本神経学会/>。一方、肢帯型筋ジストロフィーや先天性筋ジストロフィーは、原因遺伝子や地域差によって頻度が大きく変動する<ref name=Harper2001/><ref name=Tawil2015/><ref name=Straub2018/>。 | |||
==関連項目== | |||
* [[デュシェンヌ型筋ジストロフィー]] | |||
* [[筋強直性ジストロフィー]] | |||
* [[ジストロフィン]] | |||
==参考文献== | |||
2026年4月17日 (金) 22:49時点における最新版
小野 洋也、青木 吉嗣
国立研究開発法人国立精神・神経医療研究センター 神経研究所遺伝子疾患治療研究部
DOI:10.14931/bsd.11580 原稿受付日:2025年5月4日 原稿完成日:2026年4月15日
担当編集委員:石垣 診祐(滋賀医科大学 神経難病研究センター)
英:muscular dystrophy 独:Muskeldystrophie 仏:dystrophie musculaire
筋ジストロフィーは、遺伝的要因により慢性進行性の筋力低下と筋萎縮を生じる疾患群の総称である。単一の疾患ではなく、原因遺伝子、遺伝形式、発症年齢、障害される筋の分布、進行速度、筋外症状の異なる多数の病型を含む。代表的病型として、デュシェンヌ型筋ジストロフィー(Duchenne muscular dystrophy)、ベッカー型筋ジストロフィー(Becker muscular dystrophy)、筋強直性ジストロフィー(myotonic dystrophy)、顔面肩甲上腕型筋ジストロフィー(facioscapulohumeral muscular dystrophy)、肢帯型筋ジストロフィー(limb-girdle muscular dystrophy)などがある[1][2][3][4][5]。近年は遺伝学的検査が診断の中心となっている。また、一部の病型では変異に応じた分子病態に基づく治療や遺伝子治療が導入されている[6][7][8]。
筋ジストロフィーとは
骨格筋の進行性変性と筋力低下を主徴とする遺伝性筋疾患群である。従来は臨床症候に基づいて分類されてきたが、分子遺伝学の進歩により、それぞれ異なる原因遺伝子と病態機序をもつ疾患の集合体であることが明らかになった[1][9]。現在では50を超える病型・病型亜分類が知られており、臨床像、遺伝形式、病理所見、遺伝学的所見を統合して分類される。
代表的病型の分子基盤として、デュシェンヌ型筋ジストロフィー/ベッカー型筋ジストロフィーではDystrophin (DMD)遺伝子、筋強直性ジストロフィー1型ではDystrophia myotonica protein kinase (DMPK)遺伝子のCTGリピート伸長、筋強直性ジストロフィー2型ではCellular nucleic acid binding protein (CNBP)遺伝子のCCTGリピート伸長、顔面肩甲上腕型筋ジストロフィーではDouble homeobox 4 (DUX4)異常発現、肢帯型筋ジストロフィーではCalpain 3 (CAPN3)やDysferlin (DYSF)など複数遺伝子の異常が知られる[3][4][5][10][11]。
筋ジストロフィーは骨格筋のみの疾患ではない。デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーでは、脳内で発現するジストロフィン・アイソフォームの異常と関連して、発達、認知、行動面の変化がみられることがある。また、筋強直性ジストロフィーでは、認知機能障害、日中の過度の眠気、注意・遂行機能障害などの中枢神経症状がみられる[12][13][14][15]。代表的筋ジストロフィーの主な特徴と中枢神経系との対応を表1に示す。
| 病型 | 原因遺伝子・機序 | 主な筋症状 | 中枢神経症状 | 発症時期・特徴 |
|---|---|---|---|---|
| デュシェンヌ型筋ジストロフィー | Dystrophin (DMD) 遺伝子変異 | 小児期発症、近位筋優位の進行性筋力低下、歩行・呼吸・心筋障害 | 発達遅滞、学習障害、知的機能低下、注意障害、行動面の問題 | 幼児期発症、進行が比較的速い |
| ベッカー型筋ジストロフィー | DMD遺伝子変異 | 軽症で進行が緩徐、近位筋優位、心筋障害 | 認知・行動面の変化を示す例がある | 思春期以降発症が多い |
| 筋強直性ジストロフィー1型 | Dystrophia myotonica protein kinase (DMPK) 遺伝子のCTGリピート伸長 | 筋強直、遠位筋優位の筋力低下、顔面筋障害、白内障、心伝導障害 | 認知機能障害、日中の過度の眠気、注意・遂行機能障害 | 小児期〜成人期、成人で頻度が高い |
| 筋強直性ジストロフィー2型 | Cellular nucleic acid binding protein (CNBP) 遺伝子のCCTGリピート伸長 | 筋強直、近位筋優位の筋力低下、筋痛、白内障、不整脈 | 中枢神経症状を伴うことがある | 成人期発症、1型より緩徐 |
| 顔面肩甲上腕型筋ジストロフィー(1型および2型) | D4Z4リピート短縮やStructural maintenance of chromosomes flexible hinge domain containing 1 (SMCHD1) 異常などを背景としたDouble homeobox 4 (DUX4) 異常発現 | 顔面・肩甲帯優位の筋力低下、左右差を伴うことがある | 典型例では中枢神経症状は前景ではない、早期発症例では知的機能低下やてんかんを伴うことがある | 思春期〜成人期初期に発症することが多い |
| 肢帯型筋ジストロフィー | 複数の原因遺伝子 | 肩帯・骨盤帯筋優位の筋力低下 | 一部で知的機能低下などを伴う | 発症時期・進行速度とも多様 |
| 福山型先天性筋ジストロフィー | Fukutin (FKTN) 遺伝子変異 | 大脳皮質形成異常、てんかん、知的機能低下 | 乳児期発症、日本で比較的多い |
注:症状の頻度や重症度は病型および症例により異なる。

骨格筋、心筋、大脳、小脳などで発現する全長型ジストロフィン・タンパク質の主要ドメイン構造を示す。ジストロフィン・タンパク質は、アクチン結合ドメインを介してF-アクチンに、システインリッチドメインを介して筋線維膜貫通タンパク質であるβ-ジストログリカンに結合する(詳細は図2参照)。
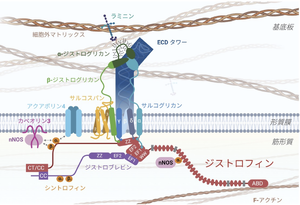
ジストロフィン糖タンパク質複合体を構成する主要分子と、その筋線維膜近傍での配置を示す。ECD( extracellular domain tower)タワー:膜外に突出した細胞外ドメイン群が形成する塔状構造。富成司博士作成図を改変。
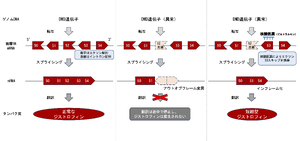
DMD遺伝子から前駆体mRNAが転写され、スプライシングを受けて成熟mRNAとなり、ジストロフィン・タンパク質が合成される。変異DMD遺伝子(例:エクソン52欠失)では、アンチセンス核酸であるビルトラルセンによりエクソン53スキップを誘導することで、アウトオブフレームがインフレーム化(mRNAの読み枠が回復)した成熟mRNAから短縮型ジストロフィン・タンパク質が産生される。
診断
筋ジストロフィーの診断は、病歴、家族歴、神経学的診察、血清クレアチンキナーゼ(creatine kinase: CK)測定、筋電図、筋画像、筋生検、遺伝子検査などを組み合わせて行う。進行性筋力低下の分布、発症年齢、筋強直の有無、心筋障害、呼吸障害、中枢神経症状などの筋外症状、および家族歴は、病型推定に有用である[1][9]。血清クレアチンキナーゼ値は多くの病型で上昇するが、上昇の程度は病型や病期によって異なる。近年は次世代シークエンスを含む遺伝学的検査が診断の中心であり、必要に応じて筋病理や画像所見を補助的に用いる[6]。とくにデュシェンヌ型筋ジストロフィー/ベッカー型筋ジストロフィーでは、欠失・重複、点変異、スプライシング異常の評価が重要である。
鑑別診断
炎症性筋疾患、代謝性ミオパチー、ミトコンドリア病、先天性ミオパチー、運動ニューロン疾患、末梢神経障害などが挙げられる。さらに、筋ジストロフィーの中でも病型間の鑑別は重要であり、発症年齢、筋障害の分布、筋外症状、遺伝形式が手がかりとなる。たとえば、中枢神経症状が前景に出る場合にはデュシェンヌ型筋ジストロフィー関連認知障害や筋強直性ジストロフィーを考慮し、顔面・肩甲帯優位なら顔面肩甲上腕型筋ジストロフィー、近位筋優位なら肢帯型筋ジストロフィーを疑う[2][3][4][5][12][13][14][15]。
病態生理
筋ジストロフィーの病態は病型により異なるが、多くは筋線維膜(筋形質膜)の安定化、細胞骨格と細胞外マトリックスの連結、核膜機能、糖鎖修飾、膜修復(筋線維膜の微小損傷を修復する機構)、RNA代謝、転写制御などの異常に起因する[1][9]。
さらに、多くの病型で骨格筋以外の臓器障害を伴う。心筋症や不整脈、呼吸障害、内分泌代謝異常、白内障、難聴、中枢神経症状などが代表的であり、病型特異性が高い[1][9][13]。脳科学の観点からは、デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーにおけるジストロフィン・アイソフォーム異常に関連して、発達、認知、行動面の変化、たとえば発達遅滞、学習障害、注意障害、自閉スペクトラム症特性などがみられることがある。さらに、筋強直性ジストロフィーにおける中枢神経症候、一部の先天性筋ジストロフィーや肢帯型筋ジストロフィーでみられるてんかん、知的機能低下、発達特性などが重要である。
ジストロフィン
デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーの原因分子である(図1)。筋線維膜においてジストロフィン糖タンパク質複合体を形成し、細胞骨格と細胞外マトリックスを連結する(図2)。デュシェンヌ型筋ジストロフィーおよびベッカー型筋ジストロフィーでは、この連結機構が障害されることで筋線維膜の脆弱性が増し、その結果、筋線維壊死と再生、慢性炎症、線維化、脂肪置換が進行し、筋力低下と筋萎縮を生じる。とくにデュシェンヌ型筋ジストロフィーでは、DMD遺伝子の欠失、重複、点変異、スプライシング異常によりmRNAの読み枠が崩れると、機能的タンパク質が産生されず重症化する。一方、読み枠が保たれる場合には短縮型ジストロフィン・タンパク質が産生され、比較的軽症のベッカー型筋ジストロフィーとなることが多い。こうしたアウトオブフレーム変異とインフレーム変異の違い、およびエクソン53スキッピングによる読み枠回復の概念を図3に示す[6][7][16]。
治療
多くの筋ジストロフィーでは、現時点でも治療の基本は対症療法である。理学療法、拘縮予防、装具療法、呼吸管理、心機能管理、栄養管理、嚥下評価、生活支援は、ほぼすべての病型で重要である[1][9]。一部の病型では分子病態に基づく治療が導入されつつあり、遺伝学的診断は治療選択の観点からも重要性を増している。
デュシェンヌ型筋ジストロフィーなど一部の病型では、アンチセンス核酸、ウイルスベクターによる遺伝子補充治療、ゲノム編集、RNA標的治療、細胞治療などの開発が進んでいる。たとえば、エクソン53スキッピング薬のビルトラルセン(ビルテプソ®)は、前駆体mRNAのスプライシングを操作して読み枠を回復し、短縮型ジストロフィン・タンパク質発現を促す治療である[7]。また、マイクロジストロフィン遺伝子をAAVベクターで導入する遺伝子治療薬のデランジストロゲン モキセパルボベク(エレビジス®)は、デュシェンヌ型筋ジストロフィーに対する疾患修飾薬として臨床導入された[8]。一方で、適応となる病型や変異は限られており、長期的有効性と安全性の検討が続いている[2][6][17][18][8]。
疫学
筋ジストロフィー全体の頻度は病型ごとに大きく異なる。デュシェンヌ型筋ジストロフィーは小児期発症の筋ジストロフィーとして最も頻度が高く、筋強直性ジストロフィー1型は成人発症筋ジストロフィーの中で最も頻度が高い病型である[12][13]。一方、肢帯型筋ジストロフィーや先天性筋ジストロフィーは、原因遺伝子や地域差によって頻度が大きく変動する[3][4][5]。
関連項目
参考文献
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5
Mercuri, E., & Muntoni, F. (2013).
Muscular dystrophies. Lancet (London, England), 381(9869), 845-60. [PubMed:23465426] [WorldCat] [DOI] - ↑ 2.0 2.1 2.2 Birnkrant DJ, Bushby K, Bann CM, et al. (2018)
Diagnosis and management of Duchenne muscular dystrophy, parts 1-3. Lancet Neurol. 17:251-267. - ↑ 3.0 3.1 3.2 3.3 Harper PS. (2001).
Myotonic Dystrophy. 3rd ed. London: WB Saunders - ↑ 4.0 4.1 4.2 4.3
Tawil, R., Kissel, J.T., Heatwole, C., Pandya, S., Gronseth, G., Benatar, M., ..., & Practice Issues Review Panel of the American Association of Neuromuscular & Electrodiagnostic Medicine (2015).
Evidence-based guideline summary: Evaluation, diagnosis, and management of facioscapulohumeral muscular dystrophy: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology and the Practice Issues Review Panel of the American Association of Neuromuscular & Electrodiagnostic Medicine. Neurology, 85(4), 357-64. [PubMed:26215877] [PMC] [WorldCat] [DOI] - ↑ 5.0 5.1 5.2 5.3
Straub, V., Murphy, A., Udd, B., & LGMD workshop study group (2018).
229th ENMC international workshop: Limb girdle muscular dystrophies - Nomenclature and reformed classification Naarden, the Netherlands, 17-19 March 2017. Neuromuscular disorders : NMD, 28(8), 702-710. [PubMed:30055862] [WorldCat] [DOI] - ↑ 6.0 6.1 6.2 6.3
Peng, Y., Xu, Y., Zhang, X., Deng, S., Yuan, Y., Luo, X., ..., & Jin, Z. (2021).
A novel protein AXIN1-295aa encoded by circAXIN1 activates the Wnt/β-catenin signaling pathway to promote gastric cancer progression. Molecular cancer, 20(1), 158. [PubMed:34863211] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1 7.2
Komaki, H., Takeshima, Y., Matsumura, T., Ozasa, S., Funato, M., Takeshita, E., ..., & Takeda, S. (2020).
Viltolarsen in Japanese Duchenne muscular dystrophy patients: A phase 1/2 study. Annals of clinical and translational neurology, 7(12), 2393-2408. [PubMed:33285037] [PMC] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2 Pharmaceuticals and Medical Devices Agency. Delandistrogene moxeparvovec (ELEVIDYS) for Duchenne muscular dystrophy: approval and safety information. 2025.
- ↑ 9.0 9.1 9.2 9.3 9.4
Emery, A.E. (2002).
The muscular dystrophies. Lancet (London, England), 359(9307), 687-95. [PubMed:11879882] [WorldCat] [DOI] - ↑
Richard, I., Broux, O., Allamand, V., Fougerousse, F., Chiannilkulchai, N., Bourg, N., ..., & Roudaut, C. (1995).
Mutations in the proteolytic enzyme calpain 3 cause limb-girdle muscular dystrophy type 2A. Cell, 81(1), 27-40. [PubMed:7720071] [WorldCat] [DOI] - ↑
Liu, J., Aoki, M., Illa, I., Wu, C., Fardeau, M., Angelini, C., ..., & Brown, R.H. (1998).
Dysferlin, a novel skeletal muscle gene, is mutated in Miyoshi myopathy and limb girdle muscular dystrophy. Nature genetics, 20(1), 31-6. [PubMed:9731526] [WorldCat] [DOI] - ↑ 12.0 12.1 12.2
Udd, B., & Krahe, R. (2012).
The myotonic dystrophies: molecular, clinical, and therapeutic challenges. The Lancet. Neurology, 11(10), 891-905. [PubMed:22995693] [WorldCat] [DOI] - ↑ 13.0 13.1 13.2 13.3 日本神経学会. 筋強直性ジストロフィー診療ガイドライン.
- ↑ 14.0 14.1
Hendriksen, J.G., & Vles, J.S. (2008).
Neuropsychiatric disorders in males with duchenne muscular dystrophy: frequency rate of attention-deficit hyperactivity disorder (ADHD), autism spectrum disorder, and obsessive--compulsive disorder. Journal of child neurology, 23(5), 477-81. [PubMed:18354150] [WorldCat] [DOI] - ↑ 15.0 15.1
Doorenweerd, N., Mahfouz, A., van Putten, M., Kaliyaperumal, R., T' Hoen, P.A.C., Hendriksen, J.G.M., ..., & Lelieveldt, B.P.F. (2017).
Timing and localization of human dystrophin isoform expression provide insights into the cognitive phenotype of Duchenne muscular dystrophy. Scientific reports, 7(1), 12575. [PubMed:28974727] [PMC] [WorldCat] [DOI] - ↑
Anthony, K., Arechavala-Gomeza, V., Ricotti, V., Torelli, S., Feng, L., Janghra, N., ..., & Muntoni, F. (2014).
Biochemical characterization of patients with in-frame or out-of-frame DMD deletions pertinent to exon 44 or 45 skipping. JAMA neurology, 71(1), 32-40. [PubMed:24217213] [WorldCat] [DOI] - ↑
Aartsma-Rus, A., & Krieg, A.M. (2017).
FDA Approves Eteplirsen for Duchenne Muscular Dystrophy: The Next Chapter in the Eteplirsen Saga. Nucleic acid therapeutics, 27(1), 1-3. [PubMed:27929755] [PMC] [WorldCat] [DOI] - ↑
Long, C., Amoasii, L., Mireault, A.A., McAnally, J.R., Li, H., Sanchez-Ortiz, E., ..., & Olson, E.N. (2016).
Postnatal genome editing partially restores dystrophin expression in a mouse model of muscular dystrophy. Science (New York, N.Y.), 351(6271), 400-3. [PubMed:26721683] [PMC] [WorldCat] [DOI]