「Ras関連核タンパク質」の版間の差分
細編集の要約なし |
細 →機能 |
||
| 22行目: | 22行目: | ||
最も重要な機能としては、細胞質-核質間のタンパク質輸送の制御があげられるが、他にも分裂期における紡錘体集合、微小管構築、核膜形成の制御などにも関与していることが知られている<ref name=Joseph2006 />。[[核膜孔複合体]]を介した核-細胞質間輸送では、[[カリオフェリン]]ファミリーのタンパク質(インポーチンやエクスポーチン)をはじめとする[[輸送担体]]が、輸送されるタンパク質(カーゴ)と結合して核膜孔の通過を助けている。Ranは、輸送単体とカーゴの結合と解離を制御している<ref name=Gorlich1999><pubmed>10611974</pubmed></ref><ref name=Weis2003><pubmed>12600309</pubmed></ref>。RanのGTP型とGDP型では細胞内局在に大きな違いが見られる。Ran-GEFである[[RCC1]]は[[クロマチン]]に結合しているため、間期核では核内のGTP型Ran濃度が細胞質に比べて高い。一方、細胞質ではRanGAPが局在しているため、GDP型が主要となる。このように、核膜を隔てたGTP型Ran-GDPの濃度勾配が、カリオフェリンを介した能動輸送の間接的なエネルギー源となっていると考えられる('''図3''')。 | 最も重要な機能としては、細胞質-核質間のタンパク質輸送の制御があげられるが、他にも分裂期における紡錘体集合、微小管構築、核膜形成の制御などにも関与していることが知られている<ref name=Joseph2006 />。[[核膜孔複合体]]を介した核-細胞質間輸送では、[[カリオフェリン]]ファミリーのタンパク質(インポーチンやエクスポーチン)をはじめとする[[輸送担体]]が、輸送されるタンパク質(カーゴ)と結合して核膜孔の通過を助けている。Ranは、輸送単体とカーゴの結合と解離を制御している<ref name=Gorlich1999><pubmed>10611974</pubmed></ref><ref name=Weis2003><pubmed>12600309</pubmed></ref>。RanのGTP型とGDP型では細胞内局在に大きな違いが見られる。Ran-GEFである[[RCC1]]は[[クロマチン]]に結合しているため、間期核では核内のGTP型Ran濃度が細胞質に比べて高い。一方、細胞質ではRanGAPが局在しているため、GDP型が主要となる。このように、核膜を隔てたGTP型Ran-GDPの濃度勾配が、カリオフェリンを介した能動輸送の間接的なエネルギー源となっていると考えられる('''図3''')。 | ||
[[インポーチンβ]]はGTP型Ranに対して高い親和性を示し、GDP型には結合しない。インポーチン βとGTP型Ranとの相互作用は、インポーチンβと荷物(カーゴ)との結合と競合する。これによりインポーチンβ | [[インポーチンβ]]はGTP型Ranに対して高い親和性を示し、GDP型には結合しない。インポーチン βとGTP型Ranとの相互作用は、インポーチンβと荷物(カーゴ)との結合と競合する。これによりインポーチンβは、GTP型Ranの少ない細胞質で荷物と結合しやすく、GTP型Ranの多い核内で荷物を離しやすい('''図3A''')。一方、エクスポーチンは荷物との相互作用に関して、インポーチンと正反対の性質を持っており、GTP型Ranとの結合でカーゴへの親和性を獲得し、GDPへの加水分解とともに荷物を離す('''図3B''')。これにより、タンパク質を核内から細胞質へと輸送する。このように、カリオフェリンが核膜孔を通過するプロセス自体には方向性はなく、核膜を挟んだGTP型Ranの濃度差により、核膜のどちら側で荷物を離しやすいかが決まり、見かけ上の能動輸送が成立する<ref name=Gorlich1999><pubmed>10611974</pubmed></ref><ref name=Nachury1999><pubmed>10449743</pubmed></ref>。 | ||
分裂期では、染色体に結合しているRCC1により染色体上にGTP型Ranの蓄積が見られ、染色体から遠ざかるにしたがって濃度が減少する。これにより、染色体周辺では、上記と同じ原理により、インポーチンなどの輸送担体がGTP型Ranに結合し、カーゴから解離しやすい環境となっている。特に[[キネトコア]]周辺では、[[紡錘体]]形成に必要な因子群がインポーチンから解離することで機能的複合体を形成し、紡錘体の正常な伸長、結合、維持を触媒している<ref name=Ciciarello2007><pubmed>17483873</pubmed></ref><ref name=Clarke2008><pubmed>18478030</pubmed></ref>。 | 分裂期では、染色体に結合しているRCC1により染色体上にGTP型Ranの蓄積が見られ、染色体から遠ざかるにしたがって濃度が減少する。これにより、染色体周辺では、上記と同じ原理により、インポーチンなどの輸送担体がGTP型Ranに結合し、カーゴから解離しやすい環境となっている。特に[[キネトコア]]周辺では、[[紡錘体]]形成に必要な因子群がインポーチンから解離することで機能的複合体を形成し、紡錘体の正常な伸長、結合、維持を触媒している<ref name=Ciciarello2007><pubmed>17483873</pubmed></ref><ref name=Clarke2008><pubmed>18478030</pubmed></ref>。 | ||
2025年3月10日 (月) 08:57時点における版
吉村 成弘
京都大学 大学院生命科学研究科
DOI:10.14931/bsd.10658 原稿受付日:2025年2月26日 原稿完成日:2025年3月10日
担当編集委員:古屋敷 智之(神戸大学大学院医学研究科・医学部 薬理学分野)
Ras関連核タンパク質 (Ras-related nuclear protein, Ran)は低分子量Gタンパク質ファミリーのひとつで、細胞質と核の間の物質輸送で重要な役割を果たしている。がんをはじめ、多くの疾患への関与が報告されていて、細胞内の重要なシグナル制御タンパク質として古くから知られている。
Ras関連核タンパク質とは
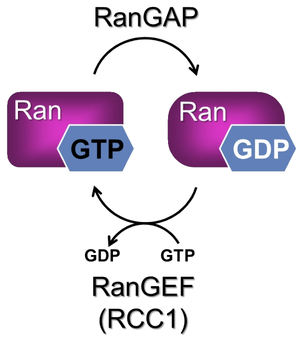
Ras関連核タンパク質 (Ras-related nuclear protein, Ran)は低分子量Gタンパク質ファミリーの一つであり、GTP結合型とGDP結合型との間の変換によって、さまざまな細胞内反応を制御するスイッチとして機能する。他の低分子量Gタンパク質と同様、グアニンヌクレオチドの変換サイクルは、特異的なグアニンヌクレオチド交換因子(guanine nucleotide exchange factor, GEF)とGTPase活性化因子 (GTPase activating protein, GAP)により行われる(図1)。最も重要な機能としては、細胞質-核質間のタンパク質輸送の制御があげられるが、他にも分裂期における紡錘体集合、微小管構築、核膜形成の制御などにも関与していることが知られている[1]。
構造
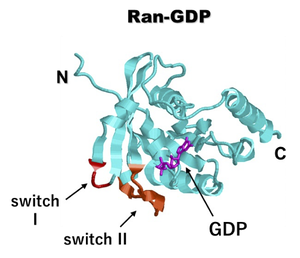
典型的な低分子Gタンパク質として1つのGTPaseドメインをもつ構造をとる。結晶構造はヌクレオチド結合型、非結合型で報告されており、様々なタンパク質との共結晶も数多く報告されている。低分子量Gタンパク質ファミリーに見られる保存されたループ領域がRanにも見られ、switch Iループとswitch IIループがGTPのγ位のリン酸を抱え込む構造になっている(図2)。GTP型とGDP型で最も顕著な構造の違いが見られるのもこれらのループ領域である[2]。この部位の構造変化により、相互作用対象の特異性が大きく変化し、分子スイッチとしての機能を発揮している。
サブファミリー
低分子量Gタンパク質ファミリーに属するが、サブファミリーはない。
発現
細胞機能に重要なタンパク質であるため、ほぼすべての組織で発現が認められる。脳においても、脳下垂体や脳梁以外のすべての領域で発現が確認される。間期細胞内では主に核内に存在するが、細胞質にも存在している。GTP結合型は核内に、GDP結合型は細胞質に多いと考えられている。
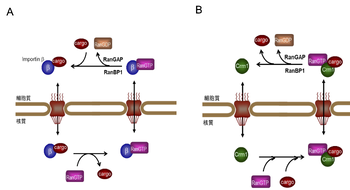
A. インポーチンによる核内輸送
B. エクスポーチンによる核外輸送
機能
最も重要な機能としては、細胞質-核質間のタンパク質輸送の制御があげられるが、他にも分裂期における紡錘体集合、微小管構築、核膜形成の制御などにも関与していることが知られている[1]。核膜孔複合体を介した核-細胞質間輸送では、カリオフェリンファミリーのタンパク質(インポーチンやエクスポーチン)をはじめとする輸送担体が、輸送されるタンパク質(カーゴ)と結合して核膜孔の通過を助けている。Ranは、輸送単体とカーゴの結合と解離を制御している[3][4]。RanのGTP型とGDP型では細胞内局在に大きな違いが見られる。Ran-GEFであるRCC1はクロマチンに結合しているため、間期核では核内のGTP型Ran濃度が細胞質に比べて高い。一方、細胞質ではRanGAPが局在しているため、GDP型が主要となる。このように、核膜を隔てたGTP型Ran-GDPの濃度勾配が、カリオフェリンを介した能動輸送の間接的なエネルギー源となっていると考えられる(図3)。
インポーチンβはGTP型Ranに対して高い親和性を示し、GDP型には結合しない。インポーチン βとGTP型Ranとの相互作用は、インポーチンβと荷物(カーゴ)との結合と競合する。これによりインポーチンβは、GTP型Ranの少ない細胞質で荷物と結合しやすく、GTP型Ranの多い核内で荷物を離しやすい(図3A)。一方、エクスポーチンは荷物との相互作用に関して、インポーチンと正反対の性質を持っており、GTP型Ranとの結合でカーゴへの親和性を獲得し、GDPへの加水分解とともに荷物を離す(図3B)。これにより、タンパク質を核内から細胞質へと輸送する。このように、カリオフェリンが核膜孔を通過するプロセス自体には方向性はなく、核膜を挟んだGTP型Ranの濃度差により、核膜のどちら側で荷物を離しやすいかが決まり、見かけ上の能動輸送が成立する[3][5]。
分裂期では、染色体に結合しているRCC1により染色体上にGTP型Ranの蓄積が見られ、染色体から遠ざかるにしたがって濃度が減少する。これにより、染色体周辺では、上記と同じ原理により、インポーチンなどの輸送担体がGTP型Ranに結合し、カーゴから解離しやすい環境となっている。特にキネトコア周辺では、紡錘体形成に必要な因子群がインポーチンから解離することで機能的複合体を形成し、紡錘体の正常な伸長、結合、維持を触媒している[6][7]。
Ranに結合するタンパク質は極めて多く、Ran結合タンパク質(Ran-binding protein, RanBP)と総称されている。カリオフェリンファミリーの一部(RanBP5 (インポーチン 5), RanBP6, RanBP17 (エクスポーチン7))や、核膜孔を構成するサブユニットの一部(RanBP2 (Nup358))も、RanBPとして同定された。Nup358は核膜孔複合体の細胞質側のfibrilを構成するサブユニットで、これを介してRanが核膜孔複合体に結合している。
また、分裂期染色体表面のGTP型Ranは、分裂期後半における核膜形成にも重要な役割を果たしている。GTP型Ranだけを結合させたビーズに分裂期細胞の抽出液を混ぜると、ビーズ表面に滑らかな核膜が形成されたことから、クロマチンではなくGTP型Ranが核膜再構成に必須であることが示された[8]。 その分子メカニズムはまだ不明な点が多いが、インポーチンβとインポーチンαの複合体が様々なタンパク質を染色体表面に呼び寄せることが重要であると考えられている。
疾患との関わり
他のRasファミリータンパク質と同様、がんとの関係性が多数報告されている[9]。特に、乳がん、大腸がん、肺がんなどとの関係性が強い。また、アルツハイマー病、パーキンソン病、ハンチントン病、前頭側頭葉変性症 (FTD)などの神経変性疾患との関係性も報告されている[10][11][12]。これらのケースでは、Ranの機能異常により核輸送が変化し、これが病気の原因タンパク質の細胞内局在に影響を及ぼすことで発症を促進していることが多い。FTDは、RNA/DNA結合タンパク質であるTDP-43の細胞内局在の異常により引き起こされる。TDP-43の核内輸送はRanに依存しており、Ranの機能異常によりFTDの発症が促進されると考えられている[10]。また、アルツハイマー病では、Ranの機能異常によるDNAメチル化酵素等の細胞内局在異常との関係性が報告されている[11]。
Ranを含め、低分子量Gタンパク質が神経変性疾患にどのように関与しているかはまだ不明な点が多く、これからの研究成果が期待される分野である。
関連語
参考文献
- ↑ 1.0 1.1
Joseph, J. (2006).
Ran at a glance. Journal of cell science, 119(Pt 17), 3481-4. [PubMed:16931595] [WorldCat] [DOI] - ↑
Paduch, M., Jeleń, F., & Otlewski, J. (2001).
Structure of small G proteins and their regulators. Acta biochimica Polonica, 48(4), 829-50. [PubMed:11995995] [WorldCat] - ↑ 3.0 3.1
Görlich, D., & Kutay, U. (1999).
Transport between the cell nucleus and the cytoplasm. Annual review of cell and developmental biology, 15, 607-60. [PubMed:10611974] [WorldCat] [DOI] - ↑
Weis, K. (2003).
Regulating access to the genome: nucleocytoplasmic transport throughout the cell cycle. Cell, 112(4), 441-51. [PubMed:12600309] [WorldCat] [DOI] - ↑
Nachury, M.V., & Weis, K. (1999).
The direction of transport through the nuclear pore can be inverted. Proceedings of the National Academy of Sciences of the United States of America, 96(17), 9622-7. [PubMed:10449743] [PMC] [WorldCat] [DOI] - ↑
Ciciarello, M., Mangiacasale, R., & Lavia, P. (2007).
Spatial control of mitosis by the GTPase Ran. Cellular and molecular life sciences : CMLS, 64(15), 1891-914. [PubMed:17483873] [PMC] [WorldCat] [DOI] - ↑
Clarke, P.R., & Zhang, C. (2008).
Spatial and temporal coordination of mitosis by Ran GTPase. Nature reviews. Molecular cell biology, 9(6), 464-77. [PubMed:18478030] [WorldCat] [DOI] - ↑
Zhang, C., & Clarke, P.R. (2000).
Chromatin-independent nuclear envelope assembly induced by Ran GTPase in Xenopus egg extracts. Science (New York, N.Y.), 288(5470), 1429-32. [PubMed:10827954] [WorldCat] [DOI] - ↑
Boudhraa, Z., Carmona, E., Provencher, D., & Mes-Masson, A.M. (2020).
Ran GTPase: A Key Player in Tumor Progression and Metastasis. Frontiers in cell and developmental biology, 8, 345. [PubMed:32528950] [PMC] [WorldCat] [DOI] - ↑ 10.0 10.1
Ward, M.E., Taubes, A., Chen, R., Miller, B.L., Sephton, C.F., Gelfand, J.M., ..., & Gan, L. (2014).
Early retinal neurodegeneration and impaired Ran-mediated nuclear import of TDP-43 in progranulin-deficient FTLD. The Journal of experimental medicine, 211(10), 1937-45. [PubMed:25155018] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Mastroeni, D., Chouliaras, L., Grover, A., Liang, W.S., Hauns, K., Rogers, J., & Coleman, P.D. (2013).
Reduced RAN expression and disrupted transport between cytoplasm and nucleus; a key event in Alzheimer's disease pathophysiology. PloS one, 8(1), e53349. [PubMed:23308199] [PMC] [WorldCat] [DOI] - ↑
Qu, L., Pan, C., He, S.M., Lang, B., Gao, G.D., Wang, X.L., & Wang, Y. (2019).
The Ras Superfamily of Small GTPases in Non-neoplastic Cerebral Diseases. Frontiers in molecular neuroscience, 12, 121. [PubMed:31213978] [PMC] [WorldCat] [DOI]