Eph受容体
膜貫通型の受容体型チロシンキナーゼの1種であり、エフリン (ephrin) と呼ばれる細胞膜に存在するリガンドと結合することによって細胞内にシグナルを伝達する。Eph受容体-エフリンのシグナルは細胞増殖、細胞移動、神経軸索ガイダンス、シナプス可塑性といった様々な現象に関与しており、脊椎動物および無脊椎動物の中枢神経系の発生と発達過程において重要な役割を果たしている。
| Ephrin receptor ligand binding domain | |||||||||
|---|---|---|---|---|---|---|---|---|---|
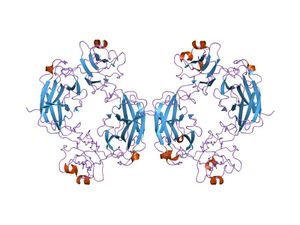 Crystal Structure of the EphB2-ephrinB2 complex base on 1kgy | |||||||||
| Identifiers | |||||||||
| Symbol | Ephrin_lbd | ||||||||
| Pfam | PF01404 | ||||||||
| InterPro | IPR001090 | ||||||||
| SCOP | 1nuk | ||||||||
| SUPERFAMILY | 1nuk | ||||||||
| CDD | cd10319 | ||||||||
| |||||||||
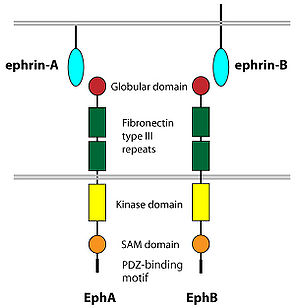
Eph受容体とephrinリガンドの構造
名称の由来
Ephは、Erythropoietin-producing hepatocellular carcinoma に発現する受容体型チロシンキナーゼをスクリーニングする過程で同定されたタンパク質である[1]。当初、それぞれのEph受容体は同定された生物種によって別々の名称で呼ばれていたが、Eph nomenclature committee により名称が統一された[2]。
構造とサブファミリー
Eph受容体は、そのアミノ酸配列及びとリガンドとの親和性の違いにより、EphAとEphBの2つのサブクラスに分類されている。脊椎動物において、EphAサブクラスは現在10種類 (EphA1-10)、EphBサブクラスは6種類同定されている (EphB1-6)。EphA、EphBはそれぞれエフリンAとエフリンBと呼ばれる細胞膜上のリガンドとほぼ選択的に結合するが、近年EphA4およびEphB2がそれぞれephrin-B3、ephrin-A5と結合することも報告されている[3]。EphA、EphBサブクラスともに共通して、細胞外領域にグロビュラードメイン、フィブロネクチンタイプIIIリピート、細胞内領域にチロシンキナーゼドメイン、SAMドメイン、 PDZ結合モチーフを有している。
細胞内シグナル
Eph受容体が細胞内にシグナルを伝達するためには、エフリンリガンドとの結合に加えて細胞膜上で受容体同士がお互いに結合すること (clustering) が必要である。リガンドの結合により、膜貫通領域の近傍に位置するチロシンとセリンがリン酸化され、チロシンキナーゼドメインが活性化されることで、下流分子にシグナルを伝達する。Eph受容体は様々な細胞内シグナル系を制御しているが、特にRas/Rhoファミリーの低分子量Gタンパク質を介したシグナルは、アクチンフィラメントの構築を制御し、細胞の形態変化や接着性の低下、あるいは亢進を誘導する。 こうしたEph受容体を介した細胞特性の変化は、細胞の移動や突起の伸張、また細胞選別といった基本的な発生現象において極めて重要な役割を担っている。Eph受容体を介して、受容体を発現する細胞に伝達されるシグナルを正方向性シグナル (forward signal)、またエフリンリガンドを介してリガンド発現細胞に伝達されるシグナルを逆方向性シグナル (reverse signal) と呼んでいる[3][4][5]。
中枢神経系における機能
中枢神経系の発生・発達過程において、Eph受容体を介したシグナルは特に、初期中枢神経系の領域化における組織境界の形成、神経前駆細胞の増殖と細胞死、神経軸索ガイダンスといった現象に深く関与している。また生後・成体脳では、シナプス形成の制御や神経幹細胞の増殖と分化にも重要な役割を果たしている。
- 中枢神経系の領域化における組織境界の形成
発生中の後脳胞では、Eph受容体とエフリンリガンドがロンボメアと呼ばれる後脳胞の分節構造に特異的に発現しており、ロンボメアを構成する組織境界の確立に機能している。また各ロンボメアに由来する神経堤細胞の移動にもEph受容体とエフリンシグナルが関与している[6]。
- 胎生期神経前駆細胞の増殖および細胞死の制御
Eph受容体とエフリンリガンドは胎生期の神経上皮細胞(神経前駆細胞)に発現しており、特にEphA4とephrin-B1を介したシグナルは神経前駆細胞の増殖を正に制御している[7]。また胎生期の大脳皮質原基において、EphA7とephrin-A5を介したシグナルは細胞死を亢進させる[8]。
- 神経細胞移動と軸索ガイダンス制御
Eph受容体とエフリンリガンドを介したシグナルは、視神経や聴神経、前交連、脳梁、中脳被蓋から線条体への線維投射、視床皮質路、皮質脊髄路といった様々な神経軸索の伸張と経路選択、標的領域への投射を制御している。軸索ガイダンスにおいては、Eph受容体を発現する軸索がエフリンリガンドを発現する標的に到達した際、軸索が反発する、いわゆる接触依存性の反発因子として機能する場合が多い。軸索を伸張させる組織と標的組織において受容体とリガンドの発現量に勾配がある場合、Eph受容体を介したシグナルは位置特異的な神経投射(トポグラフィックマップ)の形成に重要な役割を果たしている[9]。
- シナプス形成と可塑性制御
樹状突起の発達過程において、EphB2受容体が樹状突起に集積し、突起進展と維持に必須の役割を果たしている。またエフリンリガンドも樹状突起に局在しており、特にephrin-B1、ephirin-B3を介したシグナルが海馬神経細胞のスパインの成熟や後シナプス構造の形成を制御し、シナプス可塑性の維持に重要な役割を果たしている[10][11]。
- 成体神経幹細胞の増殖・分化制御
Eph受容体とエフリンリガンドは成体脳に存在する神経幹細胞とニッチ細胞にも発現している。成体側脳室壁では、EphA7受容体が上衣細胞に発現し、神経幹細胞および前駆細胞に発現しているephrin-A2リガンドを介した逆方向性シグナルにより細胞増殖を負に制御している[12]。またアストロサイトおよび移動中のニューロブラストに発現しているEphB受容体およびephrin-Bが、神経幹細胞の増殖とニューロブラストの移動様式を制御している[13] 。さらに成体海馬歯状回においては、神経前駆細胞に発現するEphB1およびEphB2が、前駆細胞の増殖と移動、突起進展を制御していることが報告されている[14]。
関連項目
参考文献
- ↑
Hirai, H., Maru, Y., Hagiwara, K., Nishida, J., & Takaku, F. (1987).
A novel putative tyrosine kinase receptor encoded by the eph gene. Science (New York, N.Y.), 238(4834), 1717-20. [PubMed:2825356] [WorldCat] [DOI] - ↑
(1997).
Unified nomenclature for Eph family receptors and their ligands, the ephrins. Eph Nomenclature Committee. Cell, 90(3), 403-4. [PubMed:9267020] [WorldCat] [DOI] - ↑ 3.0 3.1
Murai, K.K., & Pasquale, E.B. (2003).
'Eph'ective signaling: forward, reverse and crosstalk. Journal of cell science, 116(Pt 14), 2823-32. [PubMed:12808016] [WorldCat] [DOI] - ↑
Holland, S.J., Gale, N.W., Gish, G.D., Roth, R.A., Songyang, Z., Cantley, L.C., ..., & Pawson, T. (1997).
Juxtamembrane tyrosine residues couple the Eph family receptor EphB2/Nuk to specific SH2 domain proteins in neuronal cells. The EMBO journal, 16(13), 3877-88. [PubMed:9233798] [PMC] [WorldCat] [DOI] - ↑
Frisén, J., Holmberg, J., & Barbacid, M. (1999).
Ephrins and their Eph receptors: multitalented directors of embryonic development. The EMBO journal, 18(19), 5159-65. [PubMed:10508149] [PMC] [WorldCat] [DOI] - ↑
Cooke, J.E., & Moens, C.B. (2002).
Boundary formation in the hindbrain: Eph only it were simple... Trends in neurosciences, 25(5), 260-7. [PubMed:11972963] [WorldCat] [DOI] - ↑
North, H.A., Zhao, X., Kolk, S.M., Clifford, M.A., Ziskind, D.M., & Donoghue, M.J. (2009).
Promotion of proliferation in the developing cerebral cortex by EphA4 forward signaling. Development (Cambridge, England), 136(14), 2467-76. [PubMed:19542359] [PMC] [WorldCat] [DOI] - ↑
Depaepe, V., Suarez-Gonzalez, N., Dufour, A., Passante, L., Gorski, J.A., Jones, K.R., ..., & Vanderhaeghen, P. (2005).
Ephrin signalling controls brain size by regulating apoptosis of neural progenitors. Nature, 435(7046), 1244-50. [PubMed:15902206] [WorldCat] [DOI] - ↑
Frisén, J., & Barbacid, M. (1997).
Genetic analysis of the role of Eph receptors in the development of the mammalian nervous system. Cell and tissue research, 290(2), 209-15. [PubMed:9321682] [WorldCat] [DOI] - ↑
Henkemeyer, M., Itkis, O.S., Ngo, M., Hickmott, P.W., & Ethell, I.M. (2003).
Multiple EphB receptor tyrosine kinases shape dendritic spines in the hippocampus. The Journal of cell biology, 163(6), 1313-26. [PubMed:14691139] [PMC] [WorldCat] [DOI] - ↑
Henkemeyer, M., & Frisén, J. (2001).
Eph receptors tingle the spine. Neuron, 31(6), 876-7. [PubMed:11580887] [WorldCat] [DOI] - ↑
Holmberg, J., Armulik, A., Senti, K.A., Edoff, K., Spalding, K., Momma, S., ..., & Frisén, J. (2005).
Ephrin-A2 reverse signaling negatively regulates neural progenitor proliferation and neurogenesis. Genes & development, 19(4), 462-71. [PubMed:15713841] [PMC] [WorldCat] [DOI] - ↑
Conover, J.C., Doetsch, F., Garcia-Verdugo, J.M., Gale, N.W., Yancopoulos, G.D., & Alvarez-Buylla, A. (2000).
Disruption of Eph/ephrin signaling affects migration and proliferation in the adult subventricular zone. Nature neuroscience, 3(11), 1091-7. [PubMed:11036265] [WorldCat] [DOI] - ↑
Chumley, M.J., Catchpole, T., Silvany, R.E., Kernie, S.G., & Henkemeyer, M. (2007).
EphB receptors regulate stem/progenitor cell proliferation, migration, and polarity during hippocampal neurogenesis. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(49), 13481-90. [PubMed:18057206] [PMC] [WorldCat] [DOI]
(執筆担当者:野村 真 編集担当者:大隅典子)