プリオン
鈴木 元治郎、田中 元雅
独立行政法人理化学研究所 脳科学総合研究センター
DOI XXXX/XXXX 原稿受付日:2012年9月6日 原稿完成日:2013年月日
担当編集委員:漆谷 真(京都大学 大学院医学研究科)
英:prion 独:Prion 仏:prion
| Human Prion Protein. | |||||||||
|---|---|---|---|---|---|---|---|---|---|
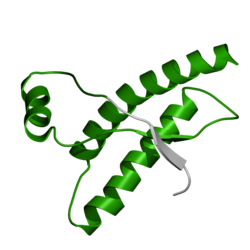 Crystal structure of human prion protein. From Zahn et al.[1] | |||||||||
| Identifiers | |||||||||
| Symbol | ? | ||||||||
| Pfam | PF00377 | ||||||||
| PROSITE | PDOC00263 | ||||||||
| SCOP | 2prp | ||||||||
| SUPERFAMILY | 2prp | ||||||||
| |||||||||
歴史
18世紀にイギリスでヒツジやヤギのスクレイピーが記録された。ヒトでは1920年と1921年にCreutzfeldtとJakobによってクロイツフェルト・ヤコブ病(Creutzfeldt-Jakob disease: CJD)が報告された。1936 年には、プリオン病であると考えられているゲルストマン・ストロイスラー・シャインカー症候群(Gerstmann-Straussler-Scheinker syndrome: GSS)が報告された。1947年には伝達性ミンク脳症の発生が報告された。1957年には、Gajdusekらによってパプア・ニューギニアにおけるクール―が報告され、1959年にはクール―とCJDとの類似性が指摘されている。1976年、Gajdusekがノーベル生理学・医学賞を受賞した。1982年、Prusinerがスクレイピー感染脳を用いた実験からproteinaceous infectious particlesの概念を提唱し、この感染性因子をプリオンと命名した(プリオン仮説の提唱)[3]。1986年、ウシ海綿状脳症(BSE)の発生がイギリスで報告され、1987年には人由来乾燥硬膜移植による医源性CJDが発生し、1996年にはBSE由来とされる変異型CJD (vCJD)が報告された。1997年にはPrusinerがノーベル医学・生理学賞を受賞した。2003年アメリカにおいてBSEの発生が確認され日本への米国産牛肉の輸入が禁止された。2005年、日本においてvCJDの患者が報告された。
プリオンタンパク質
哺乳類においてプリオンとしてふるまい、狂牛病などのプリオン病の原因となるのはPrPと呼ばれる。PrPは、ヒトでは253個、マウスでは254個のアミノ酸からなるタンパク質であり、そのアミノ酸配列は高度に保存されている[4]。 PrPは健康なヒトや動物でも発現しているタンパク質であり、脳、心臓、肝臓など多くの組織、臓器において発現が認められているが、特に脳、神経細胞において高い発現をしている。 同一のアミノ酸配列でありながら、正常プリオンタンパク質と異常プリオンタンパク質の二つの異なる高次構造をとることが知られており、異常プリオンタンパク質がプリオン病に特異的に検出される。 PrP遺伝子はヒトにおいては第20番染色体上に存在しており、2つのエクソンからなる。
正常プリオンタンパク質
正常プリオンタンパク質(cellular PrP, PrPC) は、前駆体タンパク質として翻訳される。N末端の22個のアミノ酸は小胞体への移行シグナルであり、小胞体移行後にシグナルペプチターゼによって切断される。C末端の23個のアミノ酸はグリコシルホスファチジルイノシトール(GPI)アンカーシグナルとして機能し、ゴルジ体での230番目のセリンへのGPIアンカー付加後に除去される。179番目と214番目のシステイン残基間にはジスルフィド結合が形成され、181番目と197番目のアスパラギンには糖鎖修飾がおこる。このような修飾ののち、主に細胞膜上のラフトと呼ばれるコレステロールやスフィンゴ脂質に富む領域に発現する[4]。細胞膜上に発現したPrPCは、エンドサイトーシスによって細胞内に取り込まれ、一部は分解されることなくリサイクルされ、一部はリソソームのタンパク質分解酵素によって分解される。
PrPCの機能についてはわかっていないことが多く、今後明らかにされると思われる。最初に報告されたプリオン遺伝子(PRNP)欠損(PrP-/-)マウスは何ら行動異常や神経異常を示さないことが報告されたが[5]、その後作成された欠損マウスでは老齢期の行動異常や小脳プルキンエ細胞の変性死などの異常が報告されている[6]。PrPはN末端に繰り返し配列を持っており、この配列を介して銅イオンと結合し、抗酸化作用に関係しているとの報告がある。また、アポトーシスや長期増強への関与なども報告されている。
異常プリオンタンパク質
異常プリオンタンパク質(scrapie PrP:PrPSc) は、PrPCが構造変化を起こしたものであり、プリオン病に特異的に検出される。PrPScは、PrPCと比べてβシート構造に富んだ構造をとっていることが明らかになってきている。また、PrPCが界面活性剤に可溶性を示し、プロテアーゼKなどのタンパク質分解酵素によって容易に分解されるのに対し、PrPScは、界面活性剤に難溶性であり、タンパク質分解酵素にも抵抗性を示す。 PrPScの凝集体はアミロイド線維とよばれる構造をとっており、PrPのアミロイド線維はPrP単量体が結合する鋳型として働くことができ、PrPの単量体がPrPのアミロイド線維にとりこまれることによってPrPのアミロイドは伸長することができる。また、毒性・感染力の強いPrPScはアミロイドよりもむしろオリゴマーであるという主張もある[7]。 ミスフォールドしたPrPが健康な個体に感染すると、健康な個体に存在していた正常な構造のPrPがミスフォールドしたPrPへの構造変換が起きる。つまりミスフォールドしたPrPは他のPrPの構造変換を引き起こす鋳型としてふるまい、可溶性の正常型タンパク質がアミロイドに重合していくことによって、構造変化がおこり異常型タンパク質の構造へと変化すると考えられている。 アミロイドは物理的にも化学的にも非常に安定な構造であり、このことがプリオン病の封じ込めを困難にしていると考えられる。
プリオン病
プリオン病とは、ヒトおよび動物において伝達性(感染性)のある異常プリオンタンパク質(PrPSc)が脳に蓄積し、脳が海綿状に変化することによって起きる疾患の総称である。現在までに知られているプリオン病は、有効な治療法が確立しておらず致死性である。
プリオン病に分類される疾患
動物では、ヒツジやヤギにみられるスクレイピー(scrapie)、ミンクでみられる伝達性ミンク脳症(transmissible mink encephalopathy: TME)、シカでみられる慢性消耗性疾患(chronic wasting disease: CWD)、ウシ海綿状脳症(bovine spongiform encephalopathy: BSE)、ネコ海綿状脳症(feline spongiform encephalopathy: FSE)などが知られている。ヒトでは、クロイツフェルト・ヤコブ病(Creutzfeldt-Jakob disease: CJD)、ゲルストマン・ストロイスラー・シャインカー症候群(Gerstmann-Straussler-Scheinker syndrome: GSS)などが知られており、その原因により特発性・遺伝性・感染性と大きく三つに分類される。
ヒトのプリオン病のうちもっとも頻度の高いものは特発性であり、原因が不明である孤発性CJD (sporadic CJD)であり、ヒトプリオン病の約80-85%を占めている。
遺伝性のプリオン病には家族性CJD (familial CJD)、GSS、致死性家族性不眠症(fatal familial insomnia: FFI)が知られており、プリオン遺伝子に変異を有している。
感染性のプリオン病には、狂牛病から感染することによって起こると考えられる変異型CJD (variant CJD)やCJD汚染成長ホルモン投与や汚染脳硬膜移植などによって起こる医原性CJD (iatrogenic CJD)などが知られている。また、クールーはパプア・ニューギニアのフォレ族の子供と女性にみられる疾患であり、食人習慣による経口感染が原因と考えられる。
臨床症状
ヒト、CJDの臨床症状としては、急速に進行する認知症、全身性ミオクローヌスなどが特徴である。しかし、生前診断ではCJDと診断されず、剖検によって初めてCJDと診断される症例が多く存在する(確定診断には、死後、剖検を行い、脳の病理学的な検索が必要)。CJDの早期診断は非常に困難なことが多いが、髄液中の14-3-3タンパク質、tauタンパク質、neuron specific enolase (NSE)による診断、脳波での周期性同期性放電、MRIにおける大脳基底核や大脳皮質での高信号などによる診断が有効であることが知られてきた。また、プリオン遺伝子の遺伝子検査も家族性、孤発性を問わず診断には重要である。
病理所見
病理所見としては、PrPScの沈着、灰白質における空砲の形成や海綿状変性、クールー斑の形成、グリオーシスなどが挙げられる。CJDでは海綿状変性が、GSSではクールー斑の出現が、それぞれ特徴的に観察される。PrPScの沈着はシナプス型、プラーク型の染色パターンがあり、プリオン病の指標となる。プリオン病の組織病理はプリオンタンパクの変異の種類や「プリオン株」の種類によって非常に多彩となり、プリオン病の大部分を占めるCJDにおいてもその病理所見は多彩である。
疫学
ヒトでのプリオン病の発症は人口100万人当たり1人程度とされており、非常にまれな疾患である。わが国では第五類感染症に指定されている。
プリオン仮説
これまでに発見されたウイルスなどの感染性因子は、遺伝情報としてDNAやRNAなどの核酸を保持している。しかし、プリオン病の病原体であるプリオンには、DNAやRNAは検出されていない。また、核酸分解酵素による処理や紫外線などの核酸障害処理に対してプリオンは耐性を示す。しかし、フェノール、グアニジン塩酸塩、尿素などのタンパク質変性剤に対しプリオンは感受性を示す。このことはプリオンが核酸に依存しない、タンパク質からなる感染因子であることを示している。Prusinerらは、スクレイピーに感染した脳から、プリオンを高純度に含む分画を精製することに成功し、この分画に特異的に認められるタンパク質としてPrPScを同定した。さらにPrPScがプリオンの感染価と一致した挙動を示すことを見出し、PrPScがプリオンであるとするプリオン仮説を提唱した。プリオン仮説によれば、PrPScがPrPCをPrPScに変換させることによってPrPScが新たに産生され、プリオンは複製し伝播すると考えられている。
プリオン仮説を支持する実験結果にプリオン遺伝子(PRNP)欠損(PrP-/-)マウスを利用した実験がある。PrP-/-マウスではPrPCもPrPScも存在しない。そのためプリオン仮説が正しければPrP-/-マウスは病原性のプリオンに感染せずプリオン病を発病しないはずである。感染実験の結果、野生型マウスでは感染しプリオン病を発病する条件においても、PrP-/-マウスではプリオンに感染せずプリオン病は発病せず、プリオンの感染・伝播にはPrPCが必要であることを示している[8]。さらに、PrPCからPrPScへの変換が試験管内で起きることや[9]、大腸菌から精製したPrPをPrPSc様の構造に試験管内で変換することによって感染性のあるPrPを作成できることが知られており[10]、これらの結果はプリオン仮説を強く支持している。一方でプリオン病は未知のスローウイルスが原因であるとの主張もある。
哺乳類のプリオン病は経口摂取により感染すると考えられているが、その詳細な感染過程については不明である。プリオンの不活性化には、熱、放射線、ホルマリンなどの処理では不十分であり、強酸、高温、高圧の処理が必要である。このことがプリオン病の封じ込めが難しい一つの要因となっている。
株
プリオンの特徴の一つにウイルスなどと同様に性質が異なる「株(strain)」が存在することがしられている。異なるプリオン株は病理変化、潜伏期間などで異なる性質を示す。プリオンにおける「株」の違いは原因となるPrPScの構造の違いによって引き起こされると考えられている[11]。
種の壁
また、プリオン感染には「種の壁(species barrier)」と呼ばれる現象が知られている。動物におけるプリオン病はすべてPrPScによって引き起こされると考えられているが、動物種を超えての感染はほとんど認められず、感染しても長い潜伏期間が必要となることが多い。しかし、ウシの狂牛病がヒトに感染し変異型CJDを引き起こすことが報告され、ウシのプリオンはウシとヒトとの種の壁を乗り越えることが明らかとなった。一方、ヒツジのスクレイピーはヒトには感染しないとされている。
他の生物におけるプリオン
哺乳類以外にも菌類やアメフラシでもプリオンが存在することが知られている[12][13]。ここでいうプリオンとは、タンパク質からなる細胞質性の遺伝因子という意味である。つまり、あるタンパク質が可溶性の正常型構造と不溶性のアミロイド構造をとることによって異なる機能となることであり、タンパク質の構造が伝播することによって遺伝因子となることである。哺乳類以外のプリオンは疾病というよりむしろ、何らかの細胞機能を担っているのではないかと考えられている。
菌類におけるプリオン
タンパク質のみからなる感染性因子(遺伝因子)としてのプリオンは、酵母やカビなどの菌類においても見出されており、精力的に研究が行われている。菌類におけるプリオンの発見は1994年にWicknerが出芽酵母(Saccharomyces cerevisiae)の[URE3]や[PSI+]といった細胞質性の遺伝因子がプリオンの要素を満たしており、それぞれUre2、Sup35タンパク質が構造変化を起こしたものが原因となっていることを発見した[14]。その後、出芽酵母ではRnq1、Swi1、Cyc8などいくつかのプリオンとなるタンパク質(プリオン化タンパク質)が同定されている[12]。また、分裂酵母のCinやタマホコリカビの[ Het-s ]などもプリオンであると考えられている。出芽酵母において発見されたプリオンタンパク質の特徴の一つとして、グルタミンとアスパラギンに富んだドメインを有しており、このドメインが構造変化に大きく寄与していると考えられている。また、出芽酵母では100を超えるタンパク質がそのようなドメインを有し、プリオン化する可能性が高いと考えられている。一方、動物のPrPタンパク質や[Het-s]の原因タンパク質であるHET-sはそのようなドメインを有していない。また、出芽酵母においてもそのようなドメインを有さないプリオン化タンパク質としてMod5が同定され、さらに多くのタンパク質がプリオン化する可能性があると考えられている[15]。
出芽酵母は、モデル生物として広く利用されている生物であり、プリオン研究においても有用なモデル生物として利用されてきた。特に大腸菌から精製したプリオン化タンパク質を酵母内に導入することで酵母をプリオン化させる、タンパク質の凝集体の性質の違いによってプリオン株の違いが引き起こされる、などプリオン仮説を強く支持するような研究結果が出芽酵母において報告されている[16]。
プリオン病を引き起こす動物のプリオンと違い、酵母プリオンは宿主細胞に対して毒性を示すことは少ない。むしろ酵母プリオンは宿主細胞に対して有益であることがあるのではないかという考え方が広がっている。実際、いくつかの酵母プリオンはストレス環境下への応答などに関与していることが示唆されている。また、自然界に存在する野生株酵母においてSup35などいくつかのタンパク質がプリオン化していることが発見され、酵母プリオンが宿主細胞に対して有益であるとの主張を支持している[17]。一方で酵母プリオンも動物プリオンと同様に病気の状態であるという主張も存在している。
長期記憶におけるプリオン
ショウジョウバエやアメフラシの神経細胞におけるcytoplasmic polyadenylation element binding protein (CPEB)はプリオンのように振る舞うことによって、長期記憶の形成と維持に関わっていることがわかってきている。アメフラシ(Aplysia)は神経細胞が大きいため神経細胞研究のモデル生物として利用されている。アメフラシのCPEB(ApCPEB)はシナプスの活性に依存してプリオン化状態に類似したオリゴマーを形成することがわかっており、オリゴマー形成が長期記憶の維持に重要であることがわかっている[18]。ショウジョウバエにおけるCPEBの一つであるOrb2も同様のオリゴマーを形成し、オリゴマー形成が長期記憶の維持に重要であることがわかっている[19]。これらのことから、神経細胞におけるCPEBのプリオン化状態に類似したオリゴマー形成が長期記憶の形成・維持に重要であることがわかり、プリオンが長期記憶の形成・維持という細胞機能の制御に重要であることを示している。
関連項目
参考文献
- ↑
Zahn, R., Liu, A., Lührs, T., Riek, R., von Schroetter, C., López García, F., ..., & Wüthrich, K. (2000).
NMR solution structure of the human prion protein. Proceedings of the National Academy of Sciences of the United States of America, 97(1), 145-50. [PubMed:10618385] [PMC] [WorldCat] [DOI] - ↑
Prusiner, S.B. (1998).
Prions. Proceedings of the National Academy of Sciences of the United States of America, 95(23), 13363-83. [PubMed:9811807] [PMC] [WorldCat] [DOI] - ↑
Prusiner, S.B. (1982).
Novel proteinaceous infectious particles cause scrapie. Science (New York, N.Y.), 216(4542), 136-44. [PubMed:6801762] [WorldCat] [DOI] - ↑ 4.0 4.1
Prusiner, S.B. (1991).
Molecular biology of prion diseases. Science (New York, N.Y.), 252(5012), 1515-22. [PubMed:1675487] [WorldCat] [DOI] - ↑
Büeler, H., Fischer, M., Lang, Y., Bluethmann, H., Lipp, H.P., DeArmond, S.J., ..., & Weissmann, C. (1992).
Normal development and behaviour of mice lacking the neuronal cell-surface PrP protein. Nature, 356(6370), 577-82. [PubMed:1373228] [WorldCat] [DOI] - ↑
Sakaguchi, S., Katamine, S., Nishida, N., Moriuchi, R., Shigematsu, K., Sugimoto, T., ..., & Noda, T. (1996).
Loss of cerebellar Purkinje cells in aged mice homozygous for a disrupted PrP gene. Nature, 380(6574), 528-31. [PubMed:8606772] [WorldCat] [DOI] - ↑
Silveira, J.R., Raymond, G.J., Hughson, A.G., Race, R.E., Sim, V.L., Hayes, S.F., & Caughey, B. (2005).
The most infectious prion protein particles. Nature, 437(7056), 257-61. [PubMed:16148934] [PMC] [WorldCat] [DOI] - ↑
Büeler, H., Aguzzi, A., Sailer, A., Greiner, R.A., Autenried, P., Aguet, M., & Weissmann, C. (1993).
Mice devoid of PrP are resistant to scrapie. Cell, 73(7), 1339-47. [PubMed:8100741] [WorldCat] [DOI] - ↑
Kocisko, D.A., Come, J.H., Priola, S.A., Chesebro, B., Raymond, G.J., Lansbury, P.T., & Caughey, B. (1994).
Cell-free formation of protease-resistant prion protein. Nature, 370(6489), 471-4. [PubMed:7913989] [WorldCat] [DOI] - ↑
Legname, G., Baskakov, I.V., Nguyen, H.O., Riesner, D., Cohen, F.E., DeArmond, S.J., & Prusiner, S.B. (2004).
Synthetic mammalian prions. Science (New York, N.Y.), 305(5684), 673-6. [PubMed:15286374] [WorldCat] [DOI] - ↑
Colby, D.W., & Prusiner, S.B. (2011).
De novo generation of prion strains. Nature reviews. Microbiology, 9(11), 771-7. [PubMed:21947062] [PMC] [WorldCat] [DOI] - ↑ 12.0 12.1
Liebman, S.W., & Chernoff, Y.O. (2012).
Prions in yeast. Genetics, 191(4), 1041-72. [PubMed:22879407] [PMC] [WorldCat] [DOI] - ↑
Si, K., Lindquist, S., & Kandel, E.R. (2003).
A neuronal isoform of the aplysia CPEB has prion-like properties. Cell, 115(7), 879-91. [PubMed:14697205] [WorldCat] [DOI] - ↑
Wickner, R.B. (1994).
[URE3] as an altered URE2 protein: evidence for a prion analog in Saccharomyces cerevisiae. Science (New York, N.Y.), 264(5158), 566-9. [PubMed:7909170] [WorldCat] [DOI] - ↑
Suzuki, G., Shimazu, N., & Tanaka, M. (2012).
A yeast prion, Mod5, promotes acquired drug resistance and cell survival under environmental stress. Science (New York, N.Y.), 336(6079), 355-9. [PubMed:22517861] [WorldCat] [DOI] - ↑
Tanaka, M., Chien, P., Naber, N., Cooke, R., & Weissman, J.S. (2004).
Conformational variations in an infectious protein determine prion strain differences. Nature, 428(6980), 323-8. [PubMed:15029196] [WorldCat] [DOI] - ↑
Halfmann, R., Jarosz, D.F., Jones, S.K., Chang, A., Lancaster, A.K., & Lindquist, S. (2012).
Prions are a common mechanism for phenotypic inheritance in wild yeasts. Nature, 482(7385), 363-8. [PubMed:22337056] [PMC] [WorldCat] [DOI] - ↑
Si, K., Choi, Y.B., White-Grindley, E., Majumdar, A., & Kandel, E.R. (2010).
Aplysia CPEB can form prion-like multimers in sensory neurons that contribute to long-term facilitation. Cell, 140(3), 421-35. [PubMed:20144764] [WorldCat] [DOI] - ↑
Majumdar, A., Cesario, W.C., White-Grindley, E., Jiang, H., Ren, F., Khan, M.R., ..., & Si, K. (2012).
Critical role of amyloid-like oligomers of Drosophila Orb2 in the persistence of memory. Cell, 148(3), 515-29. [PubMed:22284910] [WorldCat] [DOI]