POU転写因子
英語名:POU transcription factors
ホメオドメインタンパク質ファミリーのうち、POUドメインと呼ばれる、線虫からヒトに至るまで動物界で進化上高度に保存されたDNA結合ドメインを持った転写因子ファミリーの総称。POUは、いずれも1988年にその遺伝子クローニングが発表された最初のファミリーメンバーである、哺乳類のPit1、Oct1およびOct2と線虫のUnc86遺伝子産物の頭文字を取って命名された[1]。
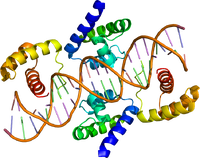
| Pouドメインの立体構造 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifiers | |||||||||
| Symbol | Pou | ||||||||
| Pfam | PF00157 | ||||||||
| InterPro | IPR000327 | ||||||||
| PROSITE | PDOC00035 | ||||||||
| SCOP | 1oct | ||||||||
| SUPERFAMILY | 1oct | ||||||||
| |||||||||
構造
POUドメインは、保存されていない15-56アミノ酸からなるリンカー配列によって2つのサブドメインに分かれており、N末端側の75アミノ酸からなるドメインはPOU特異的ドメイン(POUS: POU specific domain)、C末端側の60アミノ酸からなるドメインは、ホメオドメインタンパク質ファミリーに共通したDNA結合部位であるホメオドメインと相同性が高く、POUホメオドメイン(POUH: POU homeodomain)と名付けられている[3]。両者のサブドメインは、DNA結合モチーフの一種であるhelix-turn-helix構造をとり、オクタマー配列と呼ばれるDNA配列ATGCAAATに特異的に結合する[3]。また、親和性は低いが、それぞれのドメイン単独でDNAに結合することが可能であり、POUSは5’側のATGC、POUHは3’側のA/Tリッチな配列を認識する[4]。さらに、POUドメインは標的遺伝子の転写調節において、結合配列上でのホモ二量体やあるいは他ファミリーメンバーとのヘテロ二量体形成や、共役する他因子との結合にも必要とされる場合がある[5][6]。リンカー配列は、2つのドメインの局所的濃度を高め二量体形成やDNA結合能を高めるだけでなく、その長さの違いが両ドメインの相対的な空間配置の自由度の違いを生出し、実際の認識配列の多様性を決定しているとの報告がある[6][7]。なお、転写制御ドメインは、ファミリーメンバーによってPOUドメイン外のN末端側かC末端側、あるいはその両方に存在している[8]。
ファミリーメンバー
POU転写因子は、それぞれのPOUドメインにおけるアミノ酸配列の相同性に基づいてⅠ~Ⅵの6つのクラスに分類される。例として以下にヒトの遺伝子ホモログを列記する。
| Class | |
| I | POU1F1 |
| II | POU2F1; POU2F2; POU2F3 |
| III | POU3F1; POU3F2; POU3F3; POU3F4 |
| IV | POU4F1; POU4F2; POU4F3 |
| V | POU5F1; POU5F1P1; POU5F1P3; POU5F1P4; POU5F2 |
| VI | POU6F2 |
機能
POU転写因子ファミリーの様々なメンバーの生物学的機能は多岐にわたるが、その多くが個体発生における細胞増殖・分化・移動・生存等や神経内分泌を含めた内分泌系において、そこで必要とされる機能遺伝子の発現制御を行っている[8][9]。なお、標的遺伝子の発現制御においては、共役因子の違いや発現制御領域の構造によって転写活性化因子としても抑制因子としても働きうる[8]。
関連項目
参考文献
- ↑
Herr, W., Sturm, R.A., Clerc, R.G., Corcoran, L.M., Baltimore, D., Sharp, P.A., ..., & Ruvkun, G. (1988).
The POU domain: a large conserved region in the mammalian pit-1, oct-1, oct-2, and Caenorhabditis elegans unc-86 gene products. Genes & development, 2(12A), 1513-6. [PubMed:3215510] [WorldCat] [DOI] - ↑
Reményi, A., Tomilin, A., Pohl, E., Lins, K., Philippsen, A., Reinbold, R., ..., & Wilmanns, M. (2001).
Differential dimer activities of the transcription factor Oct-1 by DNA-induced interface swapping. Molecular cell, 8(3), 569-80. [PubMed:11583619] [WorldCat] [DOI] - ↑ 3.0 3.1
Herr, W., & Cleary, M.A. (1995).
The POU domain: versatility in transcriptional regulation by a flexible two-in-one DNA-binding domain. Genes & development, 9(14), 1679-93. [PubMed:7622033] [WorldCat] [DOI] - ↑
Klemm, J.D., Rould, M.A., Aurora, R., Herr, W., & Pabo, C.O. (1994).
Crystal structure of the Oct-1 POU domain bound to an octamer site: DNA recognition with tethered DNA-binding modules. Cell, 77(1), 21-32. [PubMed:8156594] [WorldCat] [DOI] - ↑
Malik, K.F., Jaffe, H., Brady, J., & Young, W.S. (1997).
The class III POU factor Brn-4 interacts with other class III POU factors and the heterogeneous nuclear ribonucleoprotein U. Brain research. Molecular brain research, 45(1), 99-107. [PubMed:9105675] [WorldCat] [DOI] - ↑ 6.0 6.1
Phillips, K., & Luisi, B. (2000).
The virtuoso of versatility: POU proteins that flex to fit. Journal of molecular biology, 302(5), 1023-39. [PubMed:11183772] [WorldCat] [DOI] - ↑
Reményi, A., Tomilin, A., Schöler, H.R., & Wilmanns, M. (2002).
Differential activity by DNA-induced quarternary structures of POU transcription factors. Biochemical pharmacology, 64(5-6), 979-84. [PubMed:12213595] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2
Andersen, B., & Rosenfeld, M.G. (2001).
POU domain factors in the neuroendocrine system: lessons from developmental biology provide insights into human disease. Endocrine reviews, 22(1), 2-35. [PubMed:11159814] [WorldCat] [DOI] - ↑
Ryan, A.K., & Rosenfeld, M.G. (1997).
POU domain family values: flexibility, partnerships, and developmental codes. Genes & development, 11(10), 1207-25. [PubMed:9171367] [WorldCat] [DOI]