「サイクリン依存性タンパク質キナーゼ5」の版間の差分
細編集の要約なし |
Toshioohshima (トーク | 投稿記録) 細 (→サイクリン依存性キナーゼとは) |
||
| (3人の利用者による、間の23版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0136206/?lang=japanese 大島 登志男]</font><br> | <font size="+1">[http://researchmap.jp/read0136206/?lang=japanese 大島 登志男]</font><br> | ||
''早稲田大学先進理工学部生命医科学科 早稲田大学先端生命医科学センター''<br> | ''早稲田大学先進理工学部生命医科学科 早稲田大学先端生命医科学センター''<br> | ||
[http://researchmap.jp/read0136206/ Toshio Ohshima]<br> | |||
''Department of Life Science and Medical Bio-Science, Waseda University''<br> | |||
DOI [[XXXX]]/XXXX BSD 2013-XXXX 原稿受付日:2013年5月20日 原稿完成日:2013年5月XX日 | |||
</div> | </div> | ||
英:cyclin-dependent kinase 5 英略語:Cdk5 | |||
{{box | {{box | ||
|text= | |text=抄録をお願い致します。 | ||
}} | }} | ||
== | ==サイクリン依存性キナーゼ5とは== | ||
{{PBB|geneid=1020}} | {{PBB|geneid=1020}} | ||
サイクリン依存性キナーゼは[[細胞周期]]を制御するタンパク質キナーゼファミリーとして発見された<ref name=ref1><pubmed>9442875</pubmed></ref>。真核細胞に共通した機能として、進化的に保存されている構造を有し、活性化に必要なサイクリンが結合する部位であるサイクリン結合ドメインとキナーゼドメインからなる、分子量34-40 kDaの比較的小さなタンパク質である。サイクリンと結合することで活性型となるが、Cdkのリン酸化状態により活性が制御される。各細胞周期の進行において細胞はサイクリン及びCdkの組み合わせを変えて使い分けており、サイクリンE/Cdk2はG1/S期に働き、[[G1期]]になるとサイクリンEの発現量が増加して細胞周期の進行に関与し、[[S期]]になるとユビキチン-[[プロテアソーム]]系により分解される。サイクリンBはCdk1と結合して[[M期]]の開始を制御し、M期からG1期に移行するためには、ユビキチンシステムによるサイクリンBの分解が不可欠である。このように細胞周期に依存してサイクリの発現量が変化するが、Cdkの発現量は変化しない。 | |||
サイクリン依存性キナーゼ5(Cdk5)はサイクリンDとの結合と高いアミノ酸配列の相同性からCdkの名前が付けられたが、その後、神経細胞に発現しているp35(Cdk5R1)およびp39(Cdk5R2)とヘテロダイマーを形成して活性型のキナーゼとなること判明した。 | |||
==構造== | ==構造== | ||
==ファミリー== | ==ファミリー== | ||
==発現== | ==発現== | ||
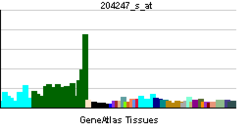
Cdk5は神経細胞以外の細胞にも発現しているが、神経細胞で高いレベルの発現がある。(組織分布、細胞内分布をお願い致します) | |||
==機能== | ==機能== | ||
===活性調節=== | ===活性調節=== | ||
Cdk5はサイクリンD,Eと結合するが活性化されず、最終分裂を終えた神経細胞に発現しているp35(CdkR1)またはp39(Cdk5R2)と結合することで活性型となる<ref name=ref2>Cdk5 book</ref>。活性化サブユニットp35 タンパク質は、Cdk5とヘテロダイマー形成後リン酸化され、プロテアソーム系で分解される事により、量的に調整されている<ref name=ref3><pubmed>9727024</pubmed></ref>。神経細胞の障害などによる細胞内へのCaイオンの流入により活性化したカルパインによりp25に限定分解される<ref name=ref4><pubmed>10604467</pubmed></ref>。p25はCdk5への結合と活性化に必要なドメインを含んでいる。しかし、リン酸化によりプロテアソーム系への分解へとは進まずCdk5/p25は安定した活性型のキナーゼとなる。さらにp35はN末端のミリストリル化により[[細胞膜]]にアンカーしているのに対し、N末を欠くp25は細胞膜にアンカリングせず、細胞質さらには核へ局在を変え、結果的に細胞質や核でのCdk5活性の上昇を来たす。 | |||
===基質=== | ===基質=== | ||
サイクリン依存性キナーゼはプロリン指向性セリン・スレオニンキナーゼで基質のリン酸化部位は[S/T]PX[K/R]のコンセンサスモチーフを持つ(S/Tはリン酸化されるセリン・スレオニン、 Pはプロリン、Xは不特定のアミノ酸、KはリジンRはアルギニン)。Cdk5は様々な神経細胞特異的な数多くのタンパク質がリン酸化基質として同定されており、それぞれリン酸化による機能制御が報告されている(表1)。 | |||
{| class="wikitable" | {| class="wikitable" | ||
|+ | |+表1.Cdk5の主な基質 | ||
|- | |- | ||
| style="background-color:#d3d3d3; text-align:center" | Cdk5 基質 | | style="background-color:#d3d3d3; text-align:center" | Cdk5 基質 | ||
| 66行目: | 47行目: | ||
| p35 | | p35 | ||
| Ser8, Thr138 | | Ser8, Thr138 | ||
| | | Patrick et al. (1998), Kamei et al. (2007) | ||
|- | |- | ||
| p39 | | p39 | ||
| | | | ||
| | | Tang et al. (1995) | ||
|- | |- | ||
| style="text-align:center" colspan="3" | '''[[細胞骨格]]制御''' | | style="text-align:center" colspan="3" | '''[[細胞骨格]]制御''' | ||
|- | |- | ||
| | | APP | ||
| Thr 668 | | Thr 668 | ||
| | | Smith (2003), Maccioni et al. (2001) | ||
|- | |- | ||
| | | Pak1 | ||
| T212 | | T212 | ||
| | | Nikolic et al. (1998), Rashid et al. (2001) | ||
|- | |- | ||
| | | Nudel | ||
| | | | ||
| | | Niethammer et al. (2000), Sasaki et al. (2000) | ||
|- | |- | ||
| | | Tau | ||
| S202, T205, T212, T217, S235, S396, S404 | | S202, T205, T212, T217, S235, S396, S404 | ||
| <ref name=ref4 /> | | Patrick et al. (1999)<ref name=ref4 /> | ||
|- | |- | ||
| | | Neurofilaments | ||
| Lys-Ser-Pro repeats in the tail region on the NFs | | Lys-Ser-Pro repeats in the tail region on the NFs | ||
| | | Sharma et al. (1999), Grant et al. (2001), Li et al. (2000) | ||
|- | |- | ||
| | | Cables | ||
| Tyr 15 | | Tyr 15 | ||
| | | Smith and Tsai (2002) | ||
|- | |- | ||
| | | MAP1b | ||
| | | | ||
| | | Paglini et al (1998), Pigino et al. (1997) | ||
|- | |- | ||
| | | WAVE1 | ||
| | | | ||
| | | Kim et al. (2006) | ||
|- | |- | ||
| | | CRMP2 | ||
| S522 | | S522 | ||
| | | Cole et al. (2004), Uchida et a. (2005) | ||
|- | |- | ||
| style="text-align:center" colspan="3" | '''神経細胞死制御、シナプス伝達、シナプス可塑性、シグナル伝達''' | | style="text-align:center" colspan="3" | '''神経細胞死制御、シナプス伝達、シナプス可塑性、シグナル伝達''' | ||
|- | |- | ||
| | | Rb | ||
| S87, 249,780, T252, 373, 821, 826 | | S87, 249,780, T252, 373, 821, 826 | ||
| | | Lee et al. (2007) | ||
|- | |- | ||
| [[MEF2]] | | [[MEF2]] | ||
| | | | ||
| | | Gong et al. (2003) | ||
|- | |- | ||
| | | Bcl-2 | ||
| | | | ||
| <ref name=ref7 | | Cheung et al. (2008)<ref name=ref7 /> | ||
|- | |- | ||
| | | β-Catenin | ||
| Tyr 654 | | Tyr 654 | ||
| | | Smith et al. (2001) | ||
|- | |- | ||
| | | Src | ||
| | | | ||
| | | Smith and Tsai (2002) | ||
|- | |- | ||
| | | NMDA receptor NR2A | ||
| Ser 1232 | | Ser 1232 | ||
| | | Li et al. (2001) | ||
|- | |- | ||
| | | TrkB | ||
| | | | ||
| | | Cheung et al. (2007) | ||
|- | |- | ||
| [[STAT3]] | | [[STAT3]] | ||
| | | | ||
| | | Fu et al. (2004) | ||
|- | |- | ||
| P/ | | P/Q type Ca channels | ||
| | | Intracellular loop domains II, III | ||
| | | Tomizawa et al. (2002) | ||
|- | |- | ||
| | | DARPP32 | ||
| Thr75 | | Thr75 | ||
| | | Bibb et al. (2003) | ||
|- | |- | ||
| | | Synapsin-1 | ||
| S551, S553 | | S551, S553 | ||
| | | Fischer et al. (1997) | ||
|- | |- | ||
| | | Munc-18 | ||
| T547, S158 | | T547, S158 | ||
| | | Shuang et al. (1998), Fletcher et al. (1999) | ||
|- | |- | ||
| [[PSD-95 | | [[PSD]]-95 | ||
| | | | ||
| | | Morabito et al. (2004) | ||
|- | |- | ||
| | | Amphyphysin-1 | ||
| S272, 276, 285 | | S272, 276, 285 | ||
| | | Floyd et al. (2001), Tan et al. (2003), Tomizawa et al (2003) | ||
|- | |- | ||
| | | ErbB | ||
| | | | ||
| | | Fu et al. (2001) | ||
|- | |- | ||
| | | Ephexin-1 | ||
| | | | ||
| | | Fu et al. (2007) | ||
|- | |- | ||
| | | α-chimerin | ||
| | | | ||
| | | Qi et al. (2004) | ||
|- | |- | ||
| | | MEK1 | ||
| | | | ||
| | | Sharma et al. (2002) | ||
|- | |- | ||
| | | Doublecortin | ||
| S297 | | S297 | ||
| | | Tanaka et al (2004) | ||
|- | |- | ||
| | | JUNK3 | ||
| | | | ||
| | | Li et al. (2002) | ||
|- | |- | ||
| | | Presinilin 1 | ||
| T354 | | T354 | ||
| | | Cruz et al. (2004) | ||
|- | |- | ||
| | | PPARγ | ||
| S723 | | S723 | ||
| <ref name=ref10 | | Choi et al. (2010)<ref name=ref10 /> | ||
|- | |- | ||
| style="text-align:center" colspan="3" | '''神経変性疾患関連''' | | style="text-align:center" colspan="3" | '''神経変性疾患関連''' | ||
|- | |- | ||
| | | Parkin | ||
| S131 | | S131 | ||
| | | Avraham et al. (2007) | ||
|- | |- | ||
| | | Prx2 | ||
| T89 | | T89 | ||
| | | Qu et al. (2007) | ||
|- | |- | ||
| [[Huntingtin]] | | [[Huntingtin]] | ||
| S434, S1181, S1201 | | S434, S1181, S1201 | ||
| <ref name=ref6 | | Luo et al. (2005)<ref name=ref6 />, Anne et al. (2007) | ||
|- | |- | ||
|} | |} | ||
== | ==神経系における機能== | ||
また、Cdk5はキナーゼとしての機能以外に、[[グルタミン酸]]受容体のNR2Bとタンパク質分解酵素カルパインと複合体を形成し、カルパインによるNR2Bの分解を調整しており、Cdk5のタンパク質量の低下はNR2Bのポストシナプスでの量的増加を来す<ref name=ref9><pubmed>17529984</pubmed></ref>。さらに近年、神経細胞以外の細胞での機能が推定されている。オリゴデンドロサイトの分化での機能やCdk5によるPPARγのリン酸化がインスリン抵抗性の発生機序にかかわっている可能性が示唆されている<ref name=ref10><pubmed>20651683</pubmed></ref>。 | |||
===アルツハイマー病=== | ===アルツハイマー病=== | ||
[[アルツハイマー病]]患者脳でのp25の増加とCdk5活性の上昇が報告され、p25産生がタウタンパク質の過剰リン酸化と神経細胞死をもたらすという説が提唱されている<ref name=ref4 />。しかし、アルツハイマー病では逆にp25量は低下しており、Cdk5活性も必ずしも上昇していないとの反論もある。 | [[アルツハイマー病]]患者脳でのp25の増加とCdk5活性の上昇が報告され、p25産生がタウタンパク質の過剰リン酸化と神経細胞死をもたらすという説が提唱されている<ref name=ref4 />。しかし、アルツハイマー病では逆にp25量は低下しており、Cdk5活性も必ずしも上昇していないとの反論もある。 | ||
| 230行目: | 206行目: | ||
===パーキンソン病、ハンチントン病=== | ===パーキンソン病、ハンチントン病=== | ||
その他パーキンソン病<ref name=ref5><pubmed>14595022</pubmed></ref>やハンチントン病<ref name=ref6><pubmed>15911879</pubmed></ref>などの神経変性疾患の病態に関与している可能性が示唆されている。これら病態でもパーキンやハッチンチンがCdk5の基質であり、Cdk5活性の上昇によりリン酸化型が増加することが病態と関連づけられるが、Cdk5が神経細胞死に対して保護的に働き、Cdk5活性が低下する細胞死を引き起こしやすくなるという報告がある<ref name=ref7><pubmed>18463240</pubmed></ref>。このように、Cdk5活性は神経細胞の生存において厳格に制御される必要があるが、神経機能においても同様であり、結合により活性を示さないサイクリンEとの結合もその活性制御に必要であることが示された<ref name=ref8><pubmed>21944720</pubmed></ref>。すなわち、サイクリンE量の低下はCdk5活性の上昇を来し、シナプス数やシナプス可塑性に影響を与えることが示された。 | |||
==関連項目== | ==関連項目== | ||
(特に関連性の強い項目があれば御指摘下さい) | |||
== 参考文献 == | == 参考文献 == | ||
<references /> | <references /> | ||
(執筆者:大島登志男 担当編集委員:尾藤 晴彦) | |||
2013年5月28日 (火) 12:51時点における版
大島 登志男
早稲田大学先進理工学部生命医科学科 早稲田大学先端生命医科学センター
Toshio Ohshima
Department of Life Science and Medical Bio-Science, Waseda University
DOI XXXX/XXXX BSD 2013-XXXX 原稿受付日:2013年5月20日 原稿完成日:2013年5月XX日
英:cyclin-dependent kinase 5 英略語:Cdk5
抄録をお願い致します。
サイクリン依存性キナーゼ5とは
サイクリン依存性キナーゼは細胞周期を制御するタンパク質キナーゼファミリーとして発見された[1]。真核細胞に共通した機能として、進化的に保存されている構造を有し、活性化に必要なサイクリンが結合する部位であるサイクリン結合ドメインとキナーゼドメインからなる、分子量34-40 kDaの比較的小さなタンパク質である。サイクリンと結合することで活性型となるが、Cdkのリン酸化状態により活性が制御される。各細胞周期の進行において細胞はサイクリン及びCdkの組み合わせを変えて使い分けており、サイクリンE/Cdk2はG1/S期に働き、G1期になるとサイクリンEの発現量が増加して細胞周期の進行に関与し、S期になるとユビキチン-プロテアソーム系により分解される。サイクリンBはCdk1と結合してM期の開始を制御し、M期からG1期に移行するためには、ユビキチンシステムによるサイクリンBの分解が不可欠である。このように細胞周期に依存してサイクリの発現量が変化するが、Cdkの発現量は変化しない。
サイクリン依存性キナーゼ5(Cdk5)はサイクリンDとの結合と高いアミノ酸配列の相同性からCdkの名前が付けられたが、その後、神経細胞に発現しているp35(Cdk5R1)およびp39(Cdk5R2)とヘテロダイマーを形成して活性型のキナーゼとなること判明した。
構造
ファミリー
発現
Cdk5は神経細胞以外の細胞にも発現しているが、神経細胞で高いレベルの発現がある。(組織分布、細胞内分布をお願い致します)
機能
活性調節
Cdk5はサイクリンD,Eと結合するが活性化されず、最終分裂を終えた神経細胞に発現しているp35(CdkR1)またはp39(Cdk5R2)と結合することで活性型となる[2]。活性化サブユニットp35 タンパク質は、Cdk5とヘテロダイマー形成後リン酸化され、プロテアソーム系で分解される事により、量的に調整されている[3]。神経細胞の障害などによる細胞内へのCaイオンの流入により活性化したカルパインによりp25に限定分解される[4]。p25はCdk5への結合と活性化に必要なドメインを含んでいる。しかし、リン酸化によりプロテアソーム系への分解へとは進まずCdk5/p25は安定した活性型のキナーゼとなる。さらにp35はN末端のミリストリル化により細胞膜にアンカーしているのに対し、N末を欠くp25は細胞膜にアンカリングせず、細胞質さらには核へ局在を変え、結果的に細胞質や核でのCdk5活性の上昇を来たす。
基質
サイクリン依存性キナーゼはプロリン指向性セリン・スレオニンキナーゼで基質のリン酸化部位は[S/T]PX[K/R]のコンセンサスモチーフを持つ(S/Tはリン酸化されるセリン・スレオニン、 Pはプロリン、Xは不特定のアミノ酸、KはリジンRはアルギニン)。Cdk5は様々な神経細胞特異的な数多くのタンパク質がリン酸化基質として同定されており、それぞれリン酸化による機能制御が報告されている(表1)。
| Cdk5 基質 | リン酸化部位 | 文献 |
| Cdk5 活性化サブユニット | ||
| p35 | Ser8, Thr138 | Patrick et al. (1998), Kamei et al. (2007) |
| p39 | Tang et al. (1995) | |
| 細胞骨格制御 | ||
| APP | Thr 668 | Smith (2003), Maccioni et al. (2001) |
| Pak1 | T212 | Nikolic et al. (1998), Rashid et al. (2001) |
| Nudel | Niethammer et al. (2000), Sasaki et al. (2000) | |
| Tau | S202, T205, T212, T217, S235, S396, S404 | Patrick et al. (1999)[4] |
| Neurofilaments | Lys-Ser-Pro repeats in the tail region on the NFs | Sharma et al. (1999), Grant et al. (2001), Li et al. (2000) |
| Cables | Tyr 15 | Smith and Tsai (2002) |
| MAP1b | Paglini et al (1998), Pigino et al. (1997) | |
| WAVE1 | Kim et al. (2006) | |
| CRMP2 | S522 | Cole et al. (2004), Uchida et a. (2005) |
| 神経細胞死制御、シナプス伝達、シナプス可塑性、シグナル伝達 | ||
| Rb | S87, 249,780, T252, 373, 821, 826 | Lee et al. (2007) |
| MEF2 | Gong et al. (2003) | |
| Bcl-2 | Cheung et al. (2008)[5] | |
| β-Catenin | Tyr 654 | Smith et al. (2001) |
| Src | Smith and Tsai (2002) | |
| NMDA receptor NR2A | Ser 1232 | Li et al. (2001) |
| TrkB | Cheung et al. (2007) | |
| STAT3 | Fu et al. (2004) | |
| P/Q type Ca channels | Intracellular loop domains II, III | Tomizawa et al. (2002) |
| DARPP32 | Thr75 | Bibb et al. (2003) |
| Synapsin-1 | S551, S553 | Fischer et al. (1997) |
| Munc-18 | T547, S158 | Shuang et al. (1998), Fletcher et al. (1999) |
| PSD-95 | Morabito et al. (2004) | |
| Amphyphysin-1 | S272, 276, 285 | Floyd et al. (2001), Tan et al. (2003), Tomizawa et al (2003) |
| ErbB | Fu et al. (2001) | |
| Ephexin-1 | Fu et al. (2007) | |
| α-chimerin | Qi et al. (2004) | |
| MEK1 | Sharma et al. (2002) | |
| Doublecortin | S297 | Tanaka et al (2004) |
| JUNK3 | Li et al. (2002) | |
| Presinilin 1 | T354 | Cruz et al. (2004) |
| PPARγ | S723 | Choi et al. (2010)[6] |
| 神経変性疾患関連 | ||
| Parkin | S131 | Avraham et al. (2007) |
| Prx2 | T89 | Qu et al. (2007) |
| Huntingtin | S434, S1181, S1201 | Luo et al. (2005)[7], Anne et al. (2007) |
神経系における機能
また、Cdk5はキナーゼとしての機能以外に、グルタミン酸受容体のNR2Bとタンパク質分解酵素カルパインと複合体を形成し、カルパインによるNR2Bの分解を調整しており、Cdk5のタンパク質量の低下はNR2Bのポストシナプスでの量的増加を来す[8]。さらに近年、神経細胞以外の細胞での機能が推定されている。オリゴデンドロサイトの分化での機能やCdk5によるPPARγのリン酸化がインスリン抵抗性の発生機序にかかわっている可能性が示唆されている[6]。
アルツハイマー病
アルツハイマー病患者脳でのp25の増加とCdk5活性の上昇が報告され、p25産生がタウタンパク質の過剰リン酸化と神経細胞死をもたらすという説が提唱されている[4]。しかし、アルツハイマー病では逆にp25量は低下しており、Cdk5活性も必ずしも上昇していないとの反論もある。
パーキンソン病、ハンチントン病
その他パーキンソン病[9]やハンチントン病[7]などの神経変性疾患の病態に関与している可能性が示唆されている。これら病態でもパーキンやハッチンチンがCdk5の基質であり、Cdk5活性の上昇によりリン酸化型が増加することが病態と関連づけられるが、Cdk5が神経細胞死に対して保護的に働き、Cdk5活性が低下する細胞死を引き起こしやすくなるという報告がある[5]。このように、Cdk5活性は神経細胞の生存において厳格に制御される必要があるが、神経機能においても同様であり、結合により活性を示さないサイクリンEとの結合もその活性制御に必要であることが示された[10]。すなわち、サイクリンE量の低下はCdk5活性の上昇を来し、シナプス数やシナプス可塑性に影響を与えることが示された。
関連項目
(特に関連性の強い項目があれば御指摘下さい)
参考文献
- ↑
Morgan, D.O. (1997).
Cyclin-dependent kinases: engines, clocks, and microprocessors. Annual review of cell and developmental biology, 13, 261-91. [PubMed:9442875] [WorldCat] [DOI] - ↑ Cdk5 book
- ↑
Patrick, G.N., Zhou, P., Kwon, Y.T., Howley, P.M., & Tsai, L.H. (1998).
p35, the neuronal-specific activator of cyclin-dependent kinase 5 (Cdk5) is degraded by the ubiquitin-proteasome pathway. The Journal of biological chemistry, 273(37), 24057-64. [PubMed:9727024] [WorldCat] [DOI] - ↑ 4.0 4.1 4.2
Patrick, G.N., Zukerberg, L., Nikolic, M., de la Monte, S., Dikkes, P., & Tsai, L.H. (1999).
Conversion of p35 to p25 deregulates Cdk5 activity and promotes neurodegeneration. Nature, 402(6762), 615-22. [PubMed:10604467] [WorldCat] [DOI] - ↑ 5.0 5.1
Cheung, Z.H., Gong, K., & Ip, N.Y. (2008).
Cyclin-dependent kinase 5 supports neuronal survival through phosphorylation of Bcl-2. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(19), 4872-7. [PubMed:18463240] [PMC] [WorldCat] [DOI] - ↑ 6.0 6.1
Choi, J.H., Banks, A.S., Estall, J.L., Kajimura, S., Boström, P., Laznik, D., ..., & Spiegelman, B.M. (2010).
Anti-diabetic drugs inhibit obesity-linked phosphorylation of PPARgamma by Cdk5. Nature, 466(7305), 451-6. [PubMed:20651683] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1
Luo, S., Vacher, C., Davies, J.E., & Rubinsztein, D.C. (2005).
Cdk5 phosphorylation of huntingtin reduces its cleavage by caspases: implications for mutant huntingtin toxicity. The Journal of cell biology, 169(4), 647-56. [PubMed:15911879] [PMC] [WorldCat] [DOI] - ↑
Hawasli, A.H., Benavides, D.R., Nguyen, C., Kansy, J.W., Hayashi, K., Chambon, P., ..., & Bibb, J.A. (2007).
Cyclin-dependent kinase 5 governs learning and synaptic plasticity via control of NMDAR degradation. Nature neuroscience, 10(7), 880-886. [PubMed:17529984] [PMC] [WorldCat] [DOI] - ↑
Smith, P.D., Crocker, S.J., Jackson-Lewis, V., Jordan-Sciutto, K.L., Hayley, S., Mount, M.P., ..., & Park, D.S. (2003).
Cyclin-dependent kinase 5 is a mediator of dopaminergic neuron loss in a mouse model of Parkinson's disease. Proceedings of the National Academy of Sciences of the United States of America, 100(23), 13650-5. [PubMed:14595022] [PMC] [WorldCat] [DOI] - ↑
Odajima, J., Wills, Z.P., Ndassa, Y.M., Terunuma, M., Kretschmannova, K., Deeb, T.Z., ..., & Sicinski, P. (2011).
Cyclin E constrains Cdk5 activity to regulate synaptic plasticity and memory formation. Developmental cell, 21(4), 655-68. [PubMed:21944720] [PMC] [WorldCat] [DOI]
(執筆者:大島登志男 担当編集委員:尾藤 晴彦)