「パッチ・マトリクス構造」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| (2人の利用者による、間の11版が非表示) | |||
| 1行目: | 1行目: | ||
<div align="right"> | <div align="right"> | ||
<font size="+1">[http://researchmap.jp/ | <font size="+1">[http://researchmap.jp/fuminofujiyama 藤山 文乃]</font>、執筆協力:[http://researchmap.jp/toshi-aka 赤沢年一]<br> | ||
''同志社大学 脳科学研究科''<br> | ''同志社大学 脳科学研究科''<br> | ||
DOI:<selfdoi /> 原稿受付日:2012年8月15日 原稿完成日:2015年4月22日<br> | |||
担当編集委員:[http:// | 担当編集委員:[http://researchmap.jp/noritakaichinohe 一戸 紀孝](国立精神・神経医療研究センター 神経研究所)<br> | ||
</div> | </div> | ||
| 16行目: | 16行目: | ||
== 定義 == | == 定義 == | ||
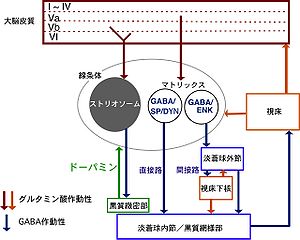
[[Image:striosome-matrix-compartments.jpg|thumb|300px|'''図1.パッチ・マトリックス構造の概念図'''<br>文献<ref name="ref3" />より改変して転載。SP:サブスタンスP、DYN:ダイノルフィン、ENK:エンケファリン]] | [[Image:striosome-matrix-compartments.jpg|thumb|300px|'''図1.パッチ・マトリックス構造の概念図'''<br>文献<ref name="ref3" />より改変して転載。SP:サブスタンスP、DYN:ダイノルフィン、ENK:エンケファリン.]] | ||
[[大脳基底核]]は[[小脳]]とともに[[錐体路]]の[[運動系]]を修飾し運動をスムーズに遂行するための大脳核であり、線条体はその大脳基底核の入力部位である。この線条体のニューロンは[[大脳皮質]]や小脳と違って、層構造をなしているわけではない。一見ランダムに存在しているのであるが、実は発生学的に異なるパッチ([[wikipedia:ja:齧歯類|齧歯類]]ではストリオソームと呼ばれることが多い)とマトリックスという名の二つのコンパートメントの中に散在している。パッチは発生学的に早く生まれ、[[ドーパミン]]入力を受けながら出現してくるのでドーパミンアイランドとも呼ばれるが、マトリックスはその後に発生し結果的に線条体全体の85%程度を占めるようになる。 | |||
== 分子マーカー == | == 分子マーカー == | ||
| 32行目: | 32行目: | ||
== 入力パターン == | == 入力パターン == | ||
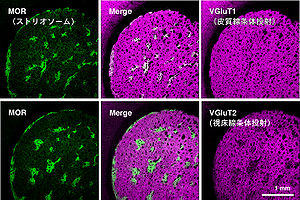
[[Image:striosome-matrix-inputs.jpg|thumb|300px|'''図2.線条体パッチ・マトリックス領域と興奮性入力(ラット)'''<br>文献<ref name="ref7" />より改変して転載。MOR:μオピオイド受容体、VGluT1:シナプス小胞型グルタミン酸トランスポーター1型、VGluT2: | [[Image:striosome-matrix-inputs.jpg|thumb|300px|'''図2.線条体パッチ・マトリックス領域と興奮性入力(ラット)'''<br>文献<ref name="ref7" />より改変して転載。MOR:μオピオイド受容体、VGluT1:シナプス小胞型グルタミン酸トランスポーター1型、VGluT2:同2型。]] | ||
入力に関しては大脳皮質からパッチへの入力は主として[[眼窩前頭皮質]]や[[島]]などの辺縁系大脳皮質に由来するのに対し、マトリックスへの入力は[[運動系皮質]]・[[体性感覚野]]・[[頭頂葉]]など広範囲な大脳[[新皮質]]に由来すると言われている。もっと明確な違いは大脳皮質の層構造であり、[[wikipedia:ja:ラット|ラット]]では大脳皮質のⅢ層とⅤa層はマトリックスに、Ⅴb層とⅥ層はパッチに投射していることが報告されている<ref name="ref5"><pubmed> 8910736 </pubmed></ref>。 | 入力に関しては大脳皮質からパッチへの入力は主として[[眼窩前頭皮質]]や[[島]]などの辺縁系大脳皮質に由来するのに対し、マトリックスへの入力は[[運動系皮質]]・[[体性感覚野]]・[[頭頂葉]]など広範囲な大脳[[新皮質]]に由来すると言われている。もっと明確な違いは大脳皮質の層構造であり、[[wikipedia:ja:ラット|ラット]]では大脳皮質のⅢ層とⅤa層はマトリックスに、Ⅴb層とⅥ層はパッチに投射していることが報告されている<ref name="ref5"><pubmed> 8910736 </pubmed></ref>。 | ||
[[視床]]からの入力に関しては[[束傍核]] | [[視床]]からの入力に関しては[[正中中心核]]・[[束傍核]](サル)または束傍核(げっ歯類)からの入力は主にマトリックスに終止するという報告が[[wikipedia:ja:サル|サル]]やラットでなされている。一方、パッチに特異的に投射する視床核はネコでは[[中心線核]]が報告されているものの<ref name="ref6"><pubmed> 1719043 </pubmed></ref>他の動物種では明らかにされていない。筆者らは視床から線条体への興奮性入力はマトリックスに比べるとパッチへの入力は3分の1程度であること(図2)やシナプス構造が違うことなどから<ref name="ref7"><pubmed> 17156206 </pubmed></ref><ref>'''藤山文乃、日置寛之、金子武嗣'''<br>中枢神経ネットワークにおけるシナプス小胞性グルタミン酸トランスポーター.<br>''脳21'': 2005, 8(4); 37-42, ''金芳堂''</ref><ref>'''藤山文乃、金子武嗣'''<br>大脳基底核の解剖.<br>''Clinical Neuroscience'': 2007, 25(1); 22〜24, ''中外医学社''</ref>、大脳皮質のみならず視床線条体入力においてもパッチとマトリックス各々に特徴的なネットワークがあると考え単一ニューロントレースで解析中である。一方、ドーパミンニューロンはシングルニューロンレベルでもパッチおよびマトリックス領域の両方に投射していることを証明した | ||
<ref name="ref10"><pubmed> 19144844 </pubmed></ref>。 | <ref name="ref10"><pubmed> 19144844 </pubmed></ref>。 | ||
| 50行目: | 50行目: | ||
== 機能 == | == 機能 == | ||
[[強化学習アルゴリズム]]の中でパッチのニューロンがstate valueを、マトリックスのニューロンがaction | [[強化学習アルゴリズム]]の中でパッチのニューロンがstate valueを、マトリックスのニューロンがaction valueを担っているという説がある | ||
<ref name="ref14"><pubmed> 12371507 </pubmed></ref>。 | <ref name="ref14"><pubmed> 12371507 </pubmed></ref>。 | ||
行動の動機づけの側面に深く関係するドーパミンニューロンが、辺縁系大脳皮質と強い神経連絡を持つパッチのニューロンの神経支配を受けているというのは極めて興味深く、学習と運動の両面において、今後さらなる機能的な解析が期待される。 | 行動の動機づけの側面に深く関係するドーパミンニューロンが、辺縁系大脳皮質と強い神経連絡を持つパッチのニューロンの神経支配を受けているというのは極めて興味深く、学習と運動の両面において、今後さらなる機能的な解析が期待される。 | ||
2015年4月22日 (水) 16:56時点における最新版
藤山 文乃、執筆協力:赤沢年一
同志社大学 脳科学研究科
DOI:10.14931/bsd.2321 原稿受付日:2012年8月15日 原稿完成日:2015年4月22日
担当編集委員:一戸 紀孝(国立精神・神経医療研究センター 神経研究所)
英:patch and matrix compartments
同義語:ストリオソーム・マトリックス構造
定義
大脳基底核は小脳とともに錐体路の運動系を修飾し運動をスムーズに遂行するための大脳核であり、線条体はその大脳基底核の入力部位である。この線条体のニューロンは大脳皮質や小脳と違って、層構造をなしているわけではない。一見ランダムに存在しているのであるが、実は発生学的に異なるパッチ(齧歯類ではストリオソームと呼ばれることが多い)とマトリックスという名の二つのコンパートメントの中に散在している。パッチは発生学的に早く生まれ、ドーパミン入力を受けながら出現してくるのでドーパミンアイランドとも呼ばれるが、マトリックスはその後に発生し結果的に線条体全体の85%程度を占めるようになる。
分子マーカー
線条体にはパッチとマトリックスという発現する分子を異にするコンパートメント構造が存在する [2] [3](図1)。 マトリックス領域はアセチルコリンエステラーゼにより濃染され、カルビンディンやソマトスタチンの発現が相対的に高い。パッチ領域にはμ-オピオイド受容体が濃密に存在する。
また著者らは間接路に多く発現しているエンケファリンの前駆体であるプレプロエンケファリン (preproenkephalin, PPE) の発現量がパッチ領域に少ないことも報告しており [1][4]、同じ線条体の構造でありながら別個に論じられてきた直接路・間接路とパッチ・マトリックスというコンセプトが分子マーカーを媒体として統一されたスキームで語られる日も近いのではないかと考えている。
入力パターン
入力に関しては大脳皮質からパッチへの入力は主として眼窩前頭皮質や島などの辺縁系大脳皮質に由来するのに対し、マトリックスへの入力は運動系皮質・体性感覚野・頭頂葉など広範囲な大脳新皮質に由来すると言われている。もっと明確な違いは大脳皮質の層構造であり、ラットでは大脳皮質のⅢ層とⅤa層はマトリックスに、Ⅴb層とⅥ層はパッチに投射していることが報告されている[6]。
視床からの入力に関しては正中中心核・束傍核(サル)または束傍核(げっ歯類)からの入力は主にマトリックスに終止するという報告がサルやラットでなされている。一方、パッチに特異的に投射する視床核はネコでは中心線核が報告されているものの[7]他の動物種では明らかにされていない。筆者らは視床から線条体への興奮性入力はマトリックスに比べるとパッチへの入力は3分の1程度であること(図2)やシナプス構造が違うことなどから[5][8][9]、大脳皮質のみならず視床線条体入力においてもパッチとマトリックス各々に特徴的なネットワークがあると考え単一ニューロントレースで解析中である。一方、ドーパミンニューロンはシングルニューロンレベルでもパッチおよびマトリックス領域の両方に投射していることを証明した [10]。
出力パターン
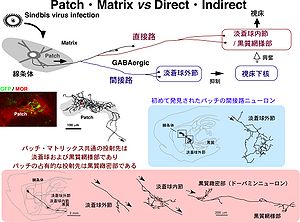
従来線条体の出力パターンはこのコンパートメント構造により違いがあると言われて来た。直接路の投射ニューロンはパッチのものはドーパミンニューロンに直接投射していると言われているが、マトリックスの直接路の投射ニューロンは淡蒼球内節と黒質網様部のGABAニューロンに投射していると言われていた [12] [13]。著者らはシングルニューロントレースを用いてマトリックスの直接路の投射ニューロンはGABAニューロンが存在する淡蒼球内節と黒質網様部に投射しており、パッチの直接路の投射ニューロンはこれに加えて黒質ドーパミンニューロンが存在する黒質緻密部に直接投射していることを明らかにした [11](図3)。
機能
強化学習アルゴリズムの中でパッチのニューロンがstate valueを、マトリックスのニューロンがaction valueを担っているという説がある [14]。 行動の動機づけの側面に深く関係するドーパミンニューロンが、辺縁系大脳皮質と強い神経連絡を持つパッチのニューロンの神経支配を受けているというのは極めて興味深く、学習と運動の両面において、今後さらなる機能的な解析が期待される。
関連項目
参考文献
- ↑ 1.0 1.1 藤山文乃
基底核ニューロンの分子マーカー.
Clinical Neuroscience: 2010,vol28.No12, 中外医学社 - ↑
Johnston, J.G., Gerfen, C.R., Haber, S.N., & van der Kooy, D. (1990).
Mechanisms of striatal pattern formation: conservation of mammalian compartmentalization. Brain research. Developmental brain research, 57(1), 93-102. [PubMed:1965303] [WorldCat] [DOI] - ↑
Nakamura, K.C., Fujiyama, F., Furuta, T., Hioki, H., & Kaneko, T. (2009).
Afferent islands are larger than mu-opioid receptor patch in striatum of rat pups. Neuroreport, 20(6), 584-8. [PubMed:19287319] [WorldCat] [DOI] - ↑
Koshimizu, Y., Wu, S.X., Unzai, T., Hioki, H., Sonomura, T., Nakamura, K.C., ..., & Kaneko, T. (2008).
Paucity of enkephalin production in neostriatal striosomal neurons: analysis with preproenkephalin-green fluorescent protein transgenic mice. The European journal of neuroscience, 28(10), 2053-64. [PubMed:19046386] [WorldCat] [DOI] - ↑ 5.0 5.1
Fujiyama, F., Unzai, T., Nakamura, K., Nomura, S., & Kaneko, T. (2006).
Difference in organization of corticostriatal and thalamostriatal synapses between patch and matrix compartments of rat neostriatum. The European journal of neuroscience, 24(10), 2813-24. [PubMed:17156206] [WorldCat] [DOI] - ↑
Kincaid, A.E., & Wilson, C.J. (1996).
Corticostriatal innervation of the patch and matrix in the rat neostriatum. The Journal of comparative neurology, 374(4), 578-92. [PubMed:8910736] [WorldCat] [DOI] - ↑
Ragsdale, C.W., & Graybiel, A.M. (1991).
Compartmental organization of the thalamostriatal connection in the cat. The Journal of comparative neurology, 311(1), 134-67. [PubMed:1719043] [WorldCat] [DOI] - ↑ 藤山文乃、日置寛之、金子武嗣
中枢神経ネットワークにおけるシナプス小胞性グルタミン酸トランスポーター.
脳21: 2005, 8(4); 37-42, 金芳堂 - ↑ 藤山文乃、金子武嗣
大脳基底核の解剖.
Clinical Neuroscience: 2007, 25(1); 22〜24, 中外医学社 - ↑
Matsuda, W., Furuta, T., Nakamura, K.C., Hioki, H., Fujiyama, F., Arai, R., & Kaneko, T. (2009).
Single nigrostriatal dopaminergic neurons form widely spread and highly dense axonal arborizations in the neostriatum. The Journal of neuroscience : the official journal of the Society for Neuroscience, 29(2), 444-53. [PubMed:19144844] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Fujiyama, F., Sohn, J., Nakano, T., Furuta, T., Nakamura, K.C., Matsuda, W., & Kaneko, T. (2011).
Exclusive and common targets of neostriatofugal projections of rat striosome neurons: a single neuron-tracing study using a viral vector. The European journal of neuroscience, 33(4), 668-77. [PubMed:21314848] [WorldCat] [DOI] - ↑
Graybiel, A.M. (1990).
Neurotransmitters and neuromodulators in the basal ganglia. Trends in neurosciences, 13(7), 244-54. [PubMed:1695398] [WorldCat] [DOI] - ↑ 藤山文乃
大脳基底核の構造(細胞構築と神経回路)
Brain and Nerve: 2009, 61(4); 341-349, 医学書院 - ↑
Doya, K. (2002).
Metalearning and neuromodulation. Neural networks : the official journal of the International Neural Network Society, 15(4-6), 495-506. [PubMed:12371507] [WorldCat]