「Notch」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| 9行目: | 9行目: | ||
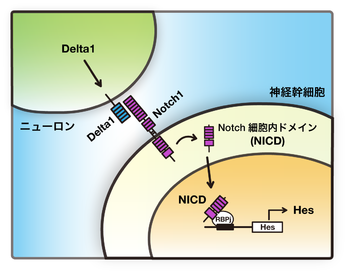
[[image:Notch_fig1.png|350px|thumb|'''図1.Notchシグナル伝達'''<br>Notchシグナルは隣接細胞間における膜タンパク質NotchとDeltaによる相互作用によって伝達されるシグナル伝達経路である。隣接細胞(神経発生過程においてはニューロン)が細胞膜上に発現するDeltaが、神経幹細胞の膜上に発現するNotchと相互作用することによってシグナルが伝達される。Deltaにより活性化されたNotchは膜から切り出され、細胞内ドメイン(NICD)が核内へと輸送され、標的遺伝子(ここではHes遺伝子)の発現を誘導する。]] | [[image:Notch_fig1.png|350px|thumb|'''図1.Notchシグナル伝達'''<br>Notchシグナルは隣接細胞間における膜タンパク質NotchとDeltaによる相互作用によって伝達されるシグナル伝達経路である。隣接細胞(神経発生過程においてはニューロン)が細胞膜上に発現するDeltaが、神経幹細胞の膜上に発現するNotchと相互作用することによってシグナルが伝達される。Deltaにより活性化されたNotchは膜から切り出され、細胞内ドメイン(NICD)が核内へと輸送され、標的遺伝子(ここではHes遺伝子)の発現を誘導する。]] | ||
Notchシグナルは、[[ショウジョウバエ]]から[[哺乳動物]]にまで広く保存されたシグナル伝達経路の一つである。このシグナル伝達の特徴は、細胞間の物理的な接触を必要とする近距離間でのシグナル伝達経路である。細胞表面上で起こるNotchリガンド(DeltaやJagged)とNotchとの相互作用によって、Notchタンパク質は[[細胞膜]]から切り出され、Notchの細胞内ドメイン(Notch intra-cellular domain; NICD)は、核内へと輸送される。核内へと運ばれたNICDはRBPj/CSLなどの[[DNA]] | Notchシグナルは、[[ショウジョウバエ]]から[[哺乳動物]]にまで広く保存されたシグナル伝達経路の一つである。このシグナル伝達の特徴は、細胞間の物理的な接触を必要とする近距離間でのシグナル伝達経路である。細胞表面上で起こるNotchリガンド(DeltaやJagged)とNotchとの相互作用によって、Notchタンパク質は[[細胞膜]]から切り出され、Notchの細胞内ドメイン(Notch intra-cellular domain; NICD)は、核内へと輸送される。核内へと運ばれたNICDはRBPj/CSLなどの[[DNA]]結合タンパク質と複合体を作り下流の標的遺伝子の発現を誘導する。この一連のシグナル伝達経路を「カノニカル(canonical)」信号伝達と呼ぶ(図1)<ref name=ref3><pubmed></pubmed></ref> <ref name=ref11><pubmed></pubmed></ref> <ref name=ref13><pubmed></pubmed></ref>。 | ||
==構造== | ==構造== | ||
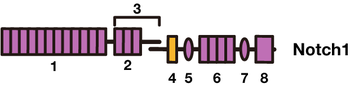
[[image:Notch_fig2.png|350px|thumb|'''図2.哺乳動物Notch1タンパク分子の構造'''<br>Notch1は、細胞外領域から順番に、(1)EGFリピート、(2)LNR (Lin12-Notch repeat)、(3)NRR(negative regulatory region)、(4)膜貫通ドメイン、(5)RAMドメイン、(6)アンキリンリピート、(7)核移行ドメイン、(8)PESTドメインにより構成される大きな分子である。]] | [[image:Notch_fig2.png|350px|thumb|'''図2.哺乳動物Notch1タンパク分子の構造'''<br>Notch1は、細胞外領域から順番に、(1)EGFリピート、(2)LNR (Lin12-Notch repeat)、(3)NRR(negative regulatory region)、(4)膜貫通ドメイン、(5)RAMドメイン、(6)アンキリンリピート、(7)核移行ドメイン、(8)PESTドメインにより構成される大きな分子である。]] | ||
巨大な分子構造を持つNotchタンパク質には生物種間で保存された幾つかのモチーフがある。細胞外領域(N末端側)から列記する(図2)<ref name=ref3 /> <ref name=ref13 />。 | |||
#'''[[EGF]]リピート : [[epidermal growth factor]] (EGF)-like repeats'''<br>Notchレセプターの細胞外ドメインには、29〜36個のタンデムにつながったEGFリピートがあり、この領域でリガンドと相互作用する。隣接細胞間とのシグナル伝達(trans-interactions)は、11番目と12番目のEGFリピートによってなされる。また、同一細胞内におけるリガンド分子との相互作用(cis-inhibition)においては、24〜29番目のEGFリピートを介して起こる。EGFリピートの多くは[[カルシウムイオン]]と結合することが知られているが、これらの[[カルシウム]][[イオン]] | #'''[[EGF]]リピート : [[epidermal growth factor]] (EGF)-like repeats'''<br>Notchレセプターの細胞外ドメインには、29〜36個のタンデムにつながったEGFリピートがあり、この領域でリガンドと相互作用する。隣接細胞間とのシグナル伝達(trans-interactions)は、11番目と12番目のEGFリピートによってなされる。また、同一細胞内におけるリガンド分子との相互作用(cis-inhibition)においては、24〜29番目のEGFリピートを介して起こる。EGFリピートの多くは[[カルシウムイオン]]と結合することが知られているが、これらの[[カルシウム]][[イオン]]はNotchレセプターの構造やリガンド分子との親和性を制御することによって、シグナル伝達効率を制御していると考えられている<ref name=ref5><pubmed></pubmed></ref> <ref name=ref17><pubmed></pubmed></ref>。 | ||
#'''LNR(Lin12-Notch repeat)'''<br>EGFリピートの後に続くリピート配列。NRRに含まれる。 | #'''LNR(Lin12-Notch repeat)'''<br>EGFリピートの後に続くリピート配列。NRRに含まれる。 | ||
#'''NRR: negative regulatory region'''<br>LNR(Lin12-Notch repeat)およびHDドメイン(heterodimerization domain)より成る。リガンドがない状態でレセプターが活性化するのを抑制している。 | #'''NRR: negative regulatory region'''<br>LNR(Lin12-Notch repeat)およびHDドメイン(heterodimerization domain)より成る。リガンドがない状態でレセプターが活性化するのを抑制している。 | ||
| 29行目: | 29行目: | ||
==機能== | ==機能== | ||
===Notchレセプターのプロセシング:成熟過程=== | ===Notchレセプターのプロセシング:成熟過程=== | ||
Notchレセプターの活性化にはタンパク質分解過程が連続的に起こることが重要である<ref name=ref3 /> <ref name=ref11><pubmed></pubmed></ref>。 | |||
#'''S1 cleavage: Furin cleavage'''<br>Notchレセプタータンパク質が[[翻訳]]され細胞膜へと輸送される間に、Notchタンパク質は[[ゴルジ装置]]へと運ばれ、Furinによって最初の切断をうける。この過程によってNotchレセプターはS1(site1)部分で半分に切断される。切り出された二つの領域は、HDドメインにて非共有結合によって結合したヘテロ二量体を形成する。ヘテロ二量体となったNotchレセプターは細胞表面へと輸送され、細胞外ドメインを外に出してリガンド分子との相互作用に備える。 | #'''S1 cleavage: Furin cleavage'''<br>Notchレセプタータンパク質が[[翻訳]]され細胞膜へと輸送される間に、Notchタンパク質は[[ゴルジ装置]]へと運ばれ、Furinによって最初の切断をうける。この過程によってNotchレセプターはS1(site1)部分で半分に切断される。切り出された二つの領域は、HDドメインにて非共有結合によって結合したヘテロ二量体を形成する。ヘテロ二量体となったNotchレセプターは細胞表面へと輸送され、細胞外ドメインを外に出してリガンド分子との相互作用に備える。 | ||
#'''S2 cleavage: [[ADAM]] cleavage'''<br>Notchレセプターと隣接細胞上のリガンドとの相互作用は、ADAM(a disintegrin and metaloprotease)タンパク質分解酵素による切断を誘導する。ADAMタンパク質分解酵素による切断は、S2領域で起こる。この領域はNRRドメインによって普段は奥まった場所に位置しており保護されている。この切断のプロセスはNotchシグナル伝達において重要なステップである。 | #'''S2 cleavage: [[ADAM]] cleavage'''<br>Notchレセプターと隣接細胞上のリガンドとの相互作用は、ADAM(a disintegrin and metaloprotease)タンパク質分解酵素による切断を誘導する。ADAMタンパク質分解酵素による切断は、S2領域で起こる。この領域はNRRドメインによって普段は奥まった場所に位置しており保護されている。この切断のプロセスはNotchシグナル伝達において重要なステップである。 | ||
#'''S3/S4 cleavage: γ-secretase cleavage'''<br>ADAMタンパク質分解酵素によるNotchレセプターの細胞外領域における切断(これによって生じた膜に繋がれたNotchの細胞内ドメインは、Notch extracellular | #'''S3/S4 cleavage: γ-secretase cleavage'''<br>ADAMタンパク質分解酵素によるNotchレセプターの細胞外領域における切断(これによって生じた膜に繋がれたNotchの細胞内ドメインは、Notch extracellular truncation(NEXT)と呼ばれる)は、次にγセクレターゼによる分解を誘導する。γセクレターゼは膜内タンパク質分解酵素であり<ref name=ref22><pubmed></pubmed></ref>、NEXTを膜貫通ドメイン(TMD)のS3およびS4の領域で切断する。γセクレターゼの切断が起こらないと、NICDの核内への輸送は起こらない。NICDは核内へと運ばれた後、RBPj/CSLと結合し、コアクチベーターと複合体を形成して、[[転写因子]]群の転写を活性化する。 | ||
===Notchシグナルの標的遺伝子=== | ===Notchシグナルの標的遺伝子=== | ||
哺乳動物の神経系におけるNotchシグナルの標的遺伝子は、[[bHLH]]型[[抑制性]]転写因子をコードする[[HESファミリー|Hesファミリー]]遺伝子([[Hes1]], [[Hes5]] | 哺乳動物の神経系におけるNotchシグナルの標的遺伝子は、[[bHLH]]型[[抑制性]]転写因子をコードする[[HESファミリー|Hesファミリー]]遺伝子([[Hes1]], [[Hes5]])<ref name=ref15><pubmed></pubmed></ref>および[[Hes]]-related遺伝子(Hey1, Hey2)<ref name=ref19><pubmed></pubmed></ref>が報告されている。[[Hesファミリー]]遺伝子は神経[[分化]]を誘導するプロニューラル遺伝子(Ascl1やNeurogenin)の発現や機能を抑制することによって、幹細胞がニューロンへと分化しないように機能している。また、[[BLBP]]([[brain lipid-binding protein]])もNotchシグナルによって直接制御されていることが報告されている<ref name=ref1><pubmed></pubmed></ref>。 | ||
===神経発生におけるNotchシグナル伝達の役割=== | ===神経発生におけるNotchシグナル伝達の役割=== | ||
哺乳動物の神経発生においてNotchシグナルは、[[神経幹細胞]]の維持に重要な機能を果たしている。また発生過程の網膜において[[ミュラーグリア]]への運命決定に寄与するなど、[[グリア細胞]]の運命決定にもNotchが寄与している。さらに中枢神経系において、Zli、Isthmus、Floor plate、[[Roof plate]] | 哺乳動物の神経発生においてNotchシグナルは、[[神経幹細胞]]の維持に重要な機能を果たしている。また発生過程の網膜において[[ミュラーグリア]]への運命決定に寄与するなど、[[グリア細胞]]の運命決定にもNotchが寄与している。さらに中枢神経系において、Zli、Isthmus、Floor plate、[[Roof plate]]といった領域の境界を形成する構造の形成にも機能していることが報告されている<ref name=ref2><pubmed></pubmed></ref> <ref name=ref4><pubmed></pubmed></ref>。 | ||
====神経幹細胞維持のためのNotchシグナル==== | ====神経幹細胞維持のためのNotchシグナル==== | ||
隣接細胞が発現するDeltaによって活性化されたNotchレセプターは、細胞膜上でレセプターのタンパク質が切り出され、細胞内ドメイン(NICD: Notch intracellular | 隣接細胞が発現するDeltaによって活性化されたNotchレセプターは、細胞膜上でレセプターのタンパク質が切り出され、細胞内ドメイン(NICD: Notch intracellular domain)が核内へと移行しNotchシグナルが活性化される。NICDの過剰発現により神経幹細胞からのニューロン分化は抑制される。また、Notchシグナルが活性化された細胞においては、bHLH型抑制性転写因子Hes1、Hes5が発現し、これらの因子がプロニューラル遺伝子の発現や機能を抑制することによって、幹細胞の未分化性を維持している<ref name=ref10><pubmed></pubmed></ref> <ref name=ref16><pubmed></pubmed></ref> <ref name=ref19><pubmed></pubmed></ref>。 | ||
====グリア細胞分化のためのNotchシグナル==== | ====グリア細胞分化のためのNotchシグナル==== | ||
神経幹細胞から神経細胞が分化した後、Notchシグナルは[[グリア]]細胞の分化に寄与していることが報告されている。発生過程の網膜においてHes1の過剰発現によりミュラーグリアの産生が亢進されるのに対して、Hes1の[[ドミナントネガティブ]] | 神経幹細胞から神経細胞が分化した後、Notchシグナルは[[グリア]]細胞の分化に寄与していることが報告されている。発生過程の網膜においてHes1の過剰発現によりミュラーグリアの産生が亢進されるのに対して、Hes1の[[ドミナントネガティブ]]による機能阻害によって、産生されるグリアの数が減少する<ref name=ref6><pubmed></pubmed></ref>。またHes5の過剰発現、欠損による実験においても同様の結果が報告されている<ref name=ref9><pubmed></pubmed></ref>。 | ||
==Notchシグナル関連疾患== | ==Notchシグナル関連疾患== | ||
| 49行目: | 49行目: | ||
発生過程における疾患<ref name=ref7><pubmed></pubmed></ref> <ref name=ref8><pubmed></pubmed></ref> | |||
*Alagille synorome | *Alagille synorome | ||
*Tetralogy of Fallot | *Tetralogy of Fallot | ||
| 57行目: | 57行目: | ||
成体における疾患<ref name=ref12><pubmed></pubmed></ref> | |||
*CADASIL | *CADASIL | ||
*Cerebral autosomal dominant arteriopathy | *Cerebral autosomal dominant arteriopathy | ||
| 63行目: | 63行目: | ||
癌<ref name=ref14><pubmed></pubmed></ref> <ref name=ref18><pubmed></pubmed></ref> <ref name=ref20><pubmed></pubmed></ref> <ref name=ref21><pubmed></pubmed></ref> | |||
*T cell acute lymphoblastic leukemia | *T cell acute lymphoblastic leukemia | ||
*Colon cancer | *Colon cancer | ||
2016年5月6日 (金) 18:42時点における版
下條 博美、影山 龍一郎
京都大学
DOI:10.14931/bsd.7111 原稿受付日:2016年5月6日 原稿完成日:2016年月日
担当編集委員:村上 富士夫(大阪大学 大学院生命機能研究科)
Notchシグナル伝達(概要)
Notchシグナルは、ショウジョウバエから哺乳動物にまで広く保存されたシグナル伝達経路の一つである。このシグナル伝達の特徴は、細胞間の物理的な接触を必要とする近距離間でのシグナル伝達経路である。細胞表面上で起こるNotchリガンド(DeltaやJagged)とNotchとの相互作用によって、Notchタンパク質は細胞膜から切り出され、Notchの細胞内ドメイン(Notch intra-cellular domain; NICD)は、核内へと輸送される。核内へと運ばれたNICDはRBPj/CSLなどのDNA結合タンパク質と複合体を作り下流の標的遺伝子の発現を誘導する。この一連のシグナル伝達経路を「カノニカル(canonical)」信号伝達と呼ぶ(図1)[1] [2] [3]。
構造
巨大な分子構造を持つNotchタンパク質には生物種間で保存された幾つかのモチーフがある。細胞外領域(N末端側)から列記する(図2)[1] [3]。
- EGFリピート : epidermal growth factor (EGF)-like repeats
Notchレセプターの細胞外ドメインには、29〜36個のタンデムにつながったEGFリピートがあり、この領域でリガンドと相互作用する。隣接細胞間とのシグナル伝達(trans-interactions)は、11番目と12番目のEGFリピートによってなされる。また、同一細胞内におけるリガンド分子との相互作用(cis-inhibition)においては、24〜29番目のEGFリピートを介して起こる。EGFリピートの多くはカルシウムイオンと結合することが知られているが、これらのカルシウムイオンはNotchレセプターの構造やリガンド分子との親和性を制御することによって、シグナル伝達効率を制御していると考えられている[4] [5]。 - LNR(Lin12-Notch repeat)
EGFリピートの後に続くリピート配列。NRRに含まれる。 - NRR: negative regulatory region
LNR(Lin12-Notch repeat)およびHDドメイン(heterodimerization domain)より成る。リガンドがない状態でレセプターが活性化するのを抑制している。 - 膜貫通ドメイン:transmembrane domain(TMD)
- RAMドメイン:RBPjκ association module domain
核内へ運ばれた後、DNA結合タンパク質であるCSL(CBF1/RBPjκ/Su(H)/Lag-1)に強く結合する領域。 - アンキリンリピート:ankyrin repeats(ANK domain)
7つのアンキリン配列が連なった領域。CSLと結合しコアクチベーターであるMastermind/Lag-3をリクルートする。 - 核移行配列:nuclear localization sequences(NLS)
- PEST配列:proline/glutamic acid/serine/threonine-rich motifes(PEST)
分解促進配列。NICDの安定性を制御する。
Notchレセプターの種類
Notchレセプターは1回膜貫通型タンパク質である。ショウジョウバエ(Drosophila melanogaster)では1種類のNotchレセプター(Notch)があるのに対し、線虫(Caenorhabditis elegans)では2種類のNotchレセプター(LIN12, GLP1)、哺乳動物では4種類のNotchパラログ(Notch1-4)が報告されている。
機能
Notchレセプターのプロセシング:成熟過程
Notchレセプターの活性化にはタンパク質分解過程が連続的に起こることが重要である[1] [2]。
- S1 cleavage: Furin cleavage
Notchレセプタータンパク質が翻訳され細胞膜へと輸送される間に、Notchタンパク質はゴルジ装置へと運ばれ、Furinによって最初の切断をうける。この過程によってNotchレセプターはS1(site1)部分で半分に切断される。切り出された二つの領域は、HDドメインにて非共有結合によって結合したヘテロ二量体を形成する。ヘテロ二量体となったNotchレセプターは細胞表面へと輸送され、細胞外ドメインを外に出してリガンド分子との相互作用に備える。 - S2 cleavage: ADAM cleavage
Notchレセプターと隣接細胞上のリガンドとの相互作用は、ADAM(a disintegrin and metaloprotease)タンパク質分解酵素による切断を誘導する。ADAMタンパク質分解酵素による切断は、S2領域で起こる。この領域はNRRドメインによって普段は奥まった場所に位置しており保護されている。この切断のプロセスはNotchシグナル伝達において重要なステップである。 - S3/S4 cleavage: γ-secretase cleavage
ADAMタンパク質分解酵素によるNotchレセプターの細胞外領域における切断(これによって生じた膜に繋がれたNotchの細胞内ドメインは、Notch extracellular truncation(NEXT)と呼ばれる)は、次にγセクレターゼによる分解を誘導する。γセクレターゼは膜内タンパク質分解酵素であり[6]、NEXTを膜貫通ドメイン(TMD)のS3およびS4の領域で切断する。γセクレターゼの切断が起こらないと、NICDの核内への輸送は起こらない。NICDは核内へと運ばれた後、RBPj/CSLと結合し、コアクチベーターと複合体を形成して、転写因子群の転写を活性化する。
Notchシグナルの標的遺伝子
哺乳動物の神経系におけるNotchシグナルの標的遺伝子は、bHLH型抑制性転写因子をコードするHesファミリー遺伝子(Hes1, Hes5)[7]およびHes-related遺伝子(Hey1, Hey2)[8]が報告されている。Hesファミリー遺伝子は神経分化を誘導するプロニューラル遺伝子(Ascl1やNeurogenin)の発現や機能を抑制することによって、幹細胞がニューロンへと分化しないように機能している。また、BLBP(brain lipid-binding protein)もNotchシグナルによって直接制御されていることが報告されている[9]。
神経発生におけるNotchシグナル伝達の役割
哺乳動物の神経発生においてNotchシグナルは、神経幹細胞の維持に重要な機能を果たしている。また発生過程の網膜においてミュラーグリアへの運命決定に寄与するなど、グリア細胞の運命決定にもNotchが寄与している。さらに中枢神経系において、Zli、Isthmus、Floor plate、Roof plateといった領域の境界を形成する構造の形成にも機能していることが報告されている[10] [11]。
神経幹細胞維持のためのNotchシグナル
隣接細胞が発現するDeltaによって活性化されたNotchレセプターは、細胞膜上でレセプターのタンパク質が切り出され、細胞内ドメイン(NICD: Notch intracellular domain)が核内へと移行しNotchシグナルが活性化される。NICDの過剰発現により神経幹細胞からのニューロン分化は抑制される。また、Notchシグナルが活性化された細胞においては、bHLH型抑制性転写因子Hes1、Hes5が発現し、これらの因子がプロニューラル遺伝子の発現や機能を抑制することによって、幹細胞の未分化性を維持している[12] [13] [8]。
グリア細胞分化のためのNotchシグナル
神経幹細胞から神経細胞が分化した後、Notchシグナルはグリア細胞の分化に寄与していることが報告されている。発生過程の網膜においてHes1の過剰発現によりミュラーグリアの産生が亢進されるのに対して、Hes1のドミナントネガティブによる機能阻害によって、産生されるグリアの数が減少する[14]。またHes5の過剰発現、欠損による実験においても同様の結果が報告されている[15]。
Notchシグナル関連疾患
Notchシグナル伝達は発生過程および成体の幹細胞維持において重要な機能を果たしているため、このシグナル伝達における欠陥は様々な疾患を引き起こすことが知られている。
- Alagille synorome
- Tetralogy of Fallot
- Syndactyly
- Spondylocostal dysostosis
- Familial aortic valve disease
成体における疾患[18]
- CADASIL
- Cerebral autosomal dominant arteriopathy
- With subcortical infarcts and leukoencephalopathy
- T cell acute lymphoblastic leukemia
- Colon cancer
- Curb tumor angiogenesis
参考文献
- ↑ 1.0 1.1 1.2 Resource not found in PubMed.
- ↑ 2.0 2.1 Resource not found in PubMed.
- ↑ 3.0 3.1 Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ 8.0 8.1 Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.