細胞時計
鳥居 雅樹、深田 吉孝
東京大学 大学院理学系研究科 生物化学専攻
DOI:10.14931/bsd.3520 原稿受付日:2013年3月25日 原稿完成日:2020年1月31日
担当編集委員:河西 春郎(東京大学 大学院医学系研究科)
英語名:cellular clock
同義語: 末梢時計(peripheral clock)
一日サイクルで変化する生命現象は多いが、この日内変動が一定の環境条件においても継続する時、その生命現象は生体内の計時機構によって支配されていることが分かる。このような計時機構は「概ね一日」を刻む時計という意味で概日時計(circadian clock)と呼ばれ、この時計が制御している変動を概日リズム (circadian rhythm)と呼ぶ。動物の概日リズムを生み出す概日時計システムは、脳に存在する中枢時計と、末梢組織に存在する末梢時計とが階層構造をなして構成されている。
回路メカニズム
動物の概日リズムを生み出す概日時計システムは、脳に存在する中枢時計と、末梢組織に存在する末梢時計とが階層構造をなして構成されている。哺乳類においては、個体の行動リズム形成には視床下部の視交叉上核(suprachiasmatic nucleus; SCN)が重要な役割を果たしている。例えば、SCNを破壊したり、SCNと他の脳部位との神経連絡を切断すると、行動の概日リズムが消失する。SCNのように、個体の概日リズム形成に決定的な役割を果たす振動体を主時計(master clock)もしくは中枢時計(central clock)という。
哺乳類の中枢時計が存在するSCNは、視交叉の直上に存在する左右一対の神経核である。SCNに存在する左右合わせて約20,000個のニューロンは、個々の細胞内に強力な振動体を有しており、実際、個体から単離して分散培養したSCNニューロンは、神経発火の頻度リズムや時計遺伝子の発現リズムが何十日間にもわたって観察される。
一方、哺乳類の多くの組織の細胞は、生体から取り出して培養しても時計遺伝子の発現リズムが自由継続する。したがって、SCN以外の全身の多くの細胞にも自律発振する時計が存在している事になる。このような末梢組織の概日時計は、SCNの中枢時計と対比させて末梢時計(peripheral clock)または細胞時計と呼ばれ、各組織において固有の位相の概日リズムを生み出す。
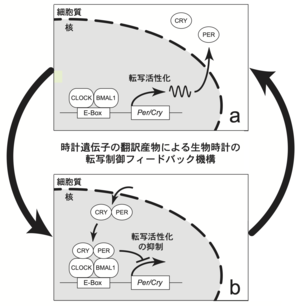
分子機構
bHLH-PAS型の転写因子CLOCKとBMAL1はヘテロ二量体を形成してDNA上に数千ヶ所も存在するE-box配列(CACGTGとそのバリエーション)に結合する。その結果、E-box配列の近傍の多くの遺伝子の転写が活性化される。
このようにE-box依存的に転写活性化される遺伝子には、時計遺伝子であるPer(ヒトやマウスではPer1, Per2, Per3)やCryが含まれる(ヒトやマウスではCry1とCry2)。Per・Cry遺伝子のmRNAは細胞質中で翻訳され、PER・CRYタンパク質(いずれも転写抑制因子)が昼の時間帯に細胞質にゆっくり時間をかけて蓄積する(図a)。このようにして転写・翻訳されたPER・CRYタンパク質は夜の時間帯に徐々に核に移行してCLOCK-BMAL1複合体に結合し、その結果、Per・Cry遺伝子の転写活性化を自ら抑制する(図b)。これと同時に、Per・Cry遺伝子のmRNAとPER・CRYタンパク質はゆっくりと分解を受けて減少するので自らの転写阻害が解除され、再びE-box依存的な転写活性化が活性化される(図a)。
このフィードバックサイクルが約24時間の周期で繰り返すことにより、Per・Cry遺伝子の転写・翻訳の一日サイクルの増減リズムが生み出される。これが、中枢時計と末梢時計に共通した概日リズムの発生メカニズムであると考えられている[1]
関連項目
参考文献
- ↑ 金尚宏、深田吉孝(2019)
生物時計と体のリズム、特集「生活時間と健康」学術の動向、8: 8-19. 日本学術会議