「中心体」の版間の差分
細編集の要約なし |
Hirokiumeshima (トーク | 投稿記録) 細編集の要約なし |
||
| (3人の利用者による、間の30版が非表示) | |||
| 1行目: | 1行目: | ||
英:centrosome | |||
重要な関連語:中心小体、中心子、微小管形成中心、一次繊毛、基底小体 | |||
動物細胞に存在する[[wikipedia:jp:細胞小器官|細胞内小器官]]の1つであり、主要な'''[[微小管]]形成中心(microtubule organizing center: MTOC)'''として機能する。[[wikipedia:jp:細胞分裂|細胞分裂]]の際に[[wikipedia:jp:紡錘体|紡錘体]]極に存在し紡錘体の形成に関与する他、[[神経細胞]]を含む多くの細胞において[[細胞極性化|細胞極性]]の形成・維持に関与すると考えられている。また、ある種の細胞においては'''基底小体(basal body)'''として'''一次[[wikipedia:jp:繊毛|繊毛]](primary cilia)'''の基部に存在しその形成に重要な役割を担う。 | |||
== 構造および性質 == | == 構造および性質 == | ||
[[image:Centrosome-sheme.jpg|300px|thumb|''' | [[image:Centrosome-sheme.jpg|300px|thumb|'''図1 中心体の構造'''<br>母中心小体はdistal appendageおよびsubdistal appendageと呼ばれる特徴的な構造を持つ。また、母中心小体と娘中心小体はC-Nap1、rootletinなどのリンカー蛋白質によって連結されている。<br>mother centriole:母中心小体、daugher centriole:娘中心小体、pericentriolar material:中心小体周辺物質、γ-TuRC: γ-tubulin ring complex、microtubule:微小管]][[image:Centrosome-sheme2.jpg|300px|thumb|'''図2 中心小体の構造'''<br>中心小体の長軸に対して水平方向(左)および垂直方向(右)の断面を示した模式図。中心小体は3本の連結した微小管が9つ円周上に並びシリンダー構造を形成している。シリンダー内腔(lumen)にはCentrinなど多数の蛋白質が局在している。]] | ||
中心体は、一対の'''中心小体(または中心子;centriole)'''と'''中心小体周辺物質(pericentriolar material: PCM)'''によって構成される(図1)。中心小体は9つの三連微小管が円周上に並んだ直径0.2μm、長さ0.5μm程度のシリンダー構造を有しており(図2)、その周囲を多数の繊維状[[wikipedia:jp:蛋白質|蛋白質]]によって構成される不定形のPCMが覆っている。PCMに局在する'''γ-[[チュブリン|tubulin]] ring complex (γ-TuRC)'''は微小管の重合核として機能しそこから微小管が伸長する。 | |||
中心体は染色体と同様に細胞周期の制御下で複製され、娘細胞に分配されることが知られている。まず、G1期からS期にかけて各々の中心小体の側部にSas6などの新たな中心小体の鋳型となる分子が集積する。S期からG2期には鋳型を基に中心小体を構成する微小管が伸長し、二対の中心小体が形成される。M期に入ると元の中心小体を連結していたリンカーが解離し、新たに形成された2つの中心体は分離して紡錘体の両端にそれぞれ局在し、紡錘体の形成に関与する。それらの中心体は細胞分裂によって[[wikipedia:jp:娘細胞|娘細胞]]に一つずつ分配される。分配された一対の中心小体は次のG1期においてリンカー蛋白質によって再び連結される<ref><pubmed>22321829</pubmed></ref>。 | |||
中心体内に存在する2つの中心小体は同質ではなく、”より古い”方の中心小体('''母中心小体: mother centriole''')は'''distal appendage'''や'''subdistal appendage'''と呼ばれる構造を持つ。distal appendageは一次繊毛形成時に中心体を[[wikipedia:jp:細胞膜|形質膜]]へと移動させるのに必要であると考えられている。subdistal appendageにはNineinなどの蛋白質が局在しており微小管を中心小体に繋ぎ留める機能を持つ。このような中心小体の非対称性は[[神経幹細胞]]の非対称分裂機構に寄与している可能性が示唆されている(下記参照)。 | |||
一般に間期の細胞では、中心体は細胞体の中心部に位置し周縁部に向かって微小管を放射状に伸ばしている(ただし、中心体で重合した微小管は必ずしも常に中心体に繋ぎ止められているわけではなく、細胞によっては速やかに微小管から放出される場合もある)。また、中心体の近傍にはゴルジ体が配置しており、微小管に沿った輸送システムにより膜小胞を細胞周縁部に供給している。極性化した細胞では中心体の位置が中心からずれることにより、不均等な微小管の配置や局所的な膜成分および蛋白質の供給を促すと考えられている。 | |||
== 神経発生における役割 == | == 神経発生における役割 == | ||
[[image:Centrosome-sheme3.jpg|300px|thumb|'''図3 移動中の小脳顆粒細胞の免疫染色像'''<br>核周辺の微小管は必ずしも中心体に収束していない。<br>青:DAPI(細胞核)、黄色:γ-tubulin(中心体)、マゼンダ:アセチル化チューブリン(安定な微小管)、緑:チロシン化チューブリン(動的な微小管)]] | |||
=== 神経幹細胞の非対称分裂 === | === 神経幹細胞の非対称分裂 === | ||
[[大脳皮質]]の神経幹細胞は、発生初期においては対称分裂により自らと同じ性質をもつ娘細胞を2つ産生し神経幹細胞の数を増大させる。その後、'''非対称分裂'''により1つの神経幹細胞と1つの神経細胞を産生し、神経幹細胞の数を維持しながら神経細胞の数を増大させる。中心体は神経幹細胞の分裂の制御にも重要であると考えられている。Cdk5rap2などの中心体関連蛋白質を欠失させると神経幹細胞を維持できなくなり、大脳皮質の神経細胞数が著しく減少する('''小頭症''')<ref><pubmed>21632253</pubmed></ref>。また、非対称分裂の際には”より古い”中心小体を含む中心体が神経幹細胞側の娘細胞に継承されること、subdistal appendageに局在するNineinが神経幹細胞の維持に必要であることが報告されている<ref><pubmed>19829375</pubmed></ref>。 | |||
=== | === 軸索形成 === | ||
[[海馬]]や[[大脳皮質]]の錐体ニューロンはまず複数の未分化な神経突起を形成した後、そのうちの1本を急速に伸長させ[[軸索]]へと分化させる。その際、中心体は軸索へと分化する神経突起の根元に局在することが報告されており、中心体が神経細胞における軸索決定に関与することが示唆されている<ref><pubmed>16079847</pubmed></ref><ref><pubmed>20685982</pubmed></ref>。中心体が主要な微小管重合開始点であることに加えて、[[ゴルジ体]]が中心体近傍に局在することから、中心体の局在により特定の神経突起に対して選択的に微小管や膜成分を供給している可能性が考えられる。しかし、他のニューロンにおいては軸索決定と中心体の位置に相関は見られないという報告もあり、軸索決定における中心体の局在は特定の神経細胞において必要なのか、神経細胞の極性化に付随して起こる現象にすぎないのかはいまだ明らかではない<ref><pubmed>21722732</pubmed></ref>。また、レーザー照射による中心体破壊実験の結果から、決定した後の軸索の伸長には中心体が必要ないことも報告されている<ref><pubmed>20056854</pubmed></ref>。分化した神経細胞では中心体の微小管重合能は低下しており、主な微小管重合は軸索および[[樹状突起]]内に広く分布した非中心体性のγ-tubulinによって担われると考えられている。 | |||
=== 神経細胞移動 === | === 神経細胞移動 === | ||
神経細胞は脳室帯等の細胞分裂層で産生された後、自らが機能する部位へと移動する([[神経細胞移動]])。神経細胞移動の不全は皮質の層構造形成に異常を引き起こすことが知られており、層構造異常の原因遺伝子として同定されたLis1, Doublecortin等の中心体および微小管関連遺伝子が神経細胞移動に関与することが示されている。神経細胞は移動に際して先導突起と呼ばれる神経突起を進行方向へと伸ばし、細胞核およびその他の細胞内小器官を先導突起内へと移入させる。これまでに、中心体が移動中の神経細胞において細胞核の前方(先導突起側)に局在しており細胞核に先行して先導突起内に移動すること、移動時の細胞核が'''microtubule cage'''と呼ばれる微小管の籠状構造に覆われていることが報告されており<ref><pubmed>15173193</pubmed></ref><ref><pubmed>15475953</pubmed></ref>、このことから中心体は自身から伸長する微小管によって先導突起と細胞核を連結し、細胞核を先導突起内へ牽引するというモデルが提唱されている。しかし、移動中の神経細胞内では細胞核周辺の微小管が必ずしも中心体に収束しておらず(図3)細胞核と中心体は独立に移動するという、上記の核牽引モデルと矛盾する報告もある<ref><pubmed>17913873</pubmed></ref>。中心体は細胞の極性形成および維持に関与することから、細胞核を牽引するのではなく移動方向を決定することで間接的に細胞核移動に関与しているのかもしれない。また、細胞核移動を駆動する力は微小管モーター蛋白質[[ダイニン]]が担うと考えられているが、ダイニンが細胞内のどこで作用しているのか(先導突起内、中心体、細胞核表面等)は明らかではない。加えてアクチンモーターである[[ミオシン]]が細胞核移動に作用するという報告もある<ref><pubmed>15958735</pubmed></ref><ref><pubmed>16174753</pubmed></ref>。中心体自身の移動もダイニンとミオシンの連動により制御されると考えられているがその詳細は不明である<ref><pubmed>17618279</pubmed></ref><ref><pubmed>19607793</pubmed></ref>。 | |||
=== 繊毛の形成 === | |||
神経幹細胞を含む多くの細胞は一次繊毛と呼ばれる微小管束によって膜が突出したアンテナ状構造を持つ。一次繊毛は[[wikipedia:jp:ソニック・ヘッジホッグ|hedgehog]][[シグナル伝達|シグナル]]やPDGFシグナルなどの細胞外シグナルに対するセンサーとして働く。[[wikipedia:jp:細胞周期|間期]]の細胞において中心体は基底小体として一次繊毛の基部に存在しその形成に関与する。繊毛の形成不全は脳の発生過程や機能において様々な障害を引き起こすことが知られている<ref><pubmed></pubmed>21435552</ref>。小脳顆粒細胞や海馬歯状回顆粒細胞の前駆細胞はSonic Hedgehogシグナル依存的な細胞増殖を行うことが知られており、一次繊毛の形成不全を示すIFT88やKif3a欠損マウスにおいてはこれらの細胞数が減少する。また、嗅覚受容神経細胞や上衣細胞は一次繊毛から派生した二次繊毛を持つ。一次繊毛が1つの細胞にⅠ本なのに対して二次繊毛は1つの細胞に複数存在し得る。嗅覚受容神経細胞は嗅覚受容体を局在させた二次繊毛を嗅上皮に露出させることでにおい物質を感知する。繊毛の形成不全に起因する疾患において嗅覚障害が伴うことが知られている。上衣細胞は脳室壁に存在しており複数の二次繊毛を脳室に向かって伸ばしている。上衣細胞の繊毛は単細胞生物の繊毛や鞭毛のように運動を行い、脳室内の脳脊髄液を循環させる。 | |||
== 中心体関連遺伝子と神経疾患 == | |||
これまで脳の形成不全を伴う神経疾患の原因遺伝子として多くの中心体関連分子が同定されている。小頭症に関してはその原因遺伝子として7つの中心体関連遺伝子(''MCPH1~7'')が同定されている。小頭症では大脳皮質の神経細胞数が著しく減少していることから、細胞分裂または対称・非対称分裂の制御に異常があることが示唆される。ただし、中心体関連遺伝子の多くはDNA損傷応答にも関与しており、DNA損傷に伴う細胞死が関与している可能性もある。小頭症では皮質の層構造には異常が見られないことから神経細胞移動の関与は少ないと考えられる。一方、'''Ⅰ型滑脳症'''においては神経細胞移動の障害に起因する皮質の層構造異常が見られる。Ⅰ型滑脳症の原因遺伝子としてLis1、Doublecortinなどが同定されているがこれらの分子もまた中心体や微小管に局在することが報告されている。また、一次繊毛の形成および機能に関連する遺伝子の変異は'''Joubert症候群'''や'''Bardet – Biedl症候群'''等の'''ciliopathy'''と呼ばれる疾患を引き起こすことが知られている<ref><pubmed>21386674</pubmed></ref>。 | |||
==関連項目== | ==関連項目== | ||
| 62行目: | 51行目: | ||
*[[神経細胞移動]] | *[[神経細胞移動]] | ||
*[[細胞極性化]] | *[[細胞極性化]] | ||
==参考文献== | ==参考文献== | ||
<references /> | <references /> | ||
(執筆者:梅嶋 宏樹、見学 美根子 担当編集委員:村上 冨士夫) | |||
2012年6月18日 (月) 00:33時点における版
英:centrosome
重要な関連語:中心小体、中心子、微小管形成中心、一次繊毛、基底小体
動物細胞に存在する細胞内小器官の1つであり、主要な微小管形成中心(microtubule organizing center: MTOC)として機能する。細胞分裂の際に紡錘体極に存在し紡錘体の形成に関与する他、神経細胞を含む多くの細胞において細胞極性の形成・維持に関与すると考えられている。また、ある種の細胞においては基底小体(basal body)として一次繊毛(primary cilia)の基部に存在しその形成に重要な役割を担う。
構造および性質
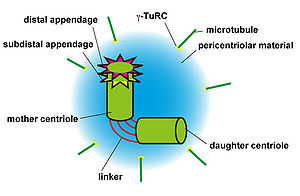
母中心小体はdistal appendageおよびsubdistal appendageと呼ばれる特徴的な構造を持つ。また、母中心小体と娘中心小体はC-Nap1、rootletinなどのリンカー蛋白質によって連結されている。
mother centriole:母中心小体、daugher centriole:娘中心小体、pericentriolar material:中心小体周辺物質、γ-TuRC: γ-tubulin ring complex、microtubule:微小管
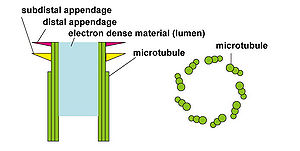
中心小体の長軸に対して水平方向(左)および垂直方向(右)の断面を示した模式図。中心小体は3本の連結した微小管が9つ円周上に並びシリンダー構造を形成している。シリンダー内腔(lumen)にはCentrinなど多数の蛋白質が局在している。
中心体は、一対の中心小体(または中心子;centriole)と中心小体周辺物質(pericentriolar material: PCM)によって構成される(図1)。中心小体は9つの三連微小管が円周上に並んだ直径0.2μm、長さ0.5μm程度のシリンダー構造を有しており(図2)、その周囲を多数の繊維状蛋白質によって構成される不定形のPCMが覆っている。PCMに局在するγ-tubulin ring complex (γ-TuRC)は微小管の重合核として機能しそこから微小管が伸長する。
中心体は染色体と同様に細胞周期の制御下で複製され、娘細胞に分配されることが知られている。まず、G1期からS期にかけて各々の中心小体の側部にSas6などの新たな中心小体の鋳型となる分子が集積する。S期からG2期には鋳型を基に中心小体を構成する微小管が伸長し、二対の中心小体が形成される。M期に入ると元の中心小体を連結していたリンカーが解離し、新たに形成された2つの中心体は分離して紡錘体の両端にそれぞれ局在し、紡錘体の形成に関与する。それらの中心体は細胞分裂によって娘細胞に一つずつ分配される。分配された一対の中心小体は次のG1期においてリンカー蛋白質によって再び連結される[1]。
中心体内に存在する2つの中心小体は同質ではなく、”より古い”方の中心小体(母中心小体: mother centriole)はdistal appendageやsubdistal appendageと呼ばれる構造を持つ。distal appendageは一次繊毛形成時に中心体を形質膜へと移動させるのに必要であると考えられている。subdistal appendageにはNineinなどの蛋白質が局在しており微小管を中心小体に繋ぎ留める機能を持つ。このような中心小体の非対称性は神経幹細胞の非対称分裂機構に寄与している可能性が示唆されている(下記参照)。
一般に間期の細胞では、中心体は細胞体の中心部に位置し周縁部に向かって微小管を放射状に伸ばしている(ただし、中心体で重合した微小管は必ずしも常に中心体に繋ぎ止められているわけではなく、細胞によっては速やかに微小管から放出される場合もある)。また、中心体の近傍にはゴルジ体が配置しており、微小管に沿った輸送システムにより膜小胞を細胞周縁部に供給している。極性化した細胞では中心体の位置が中心からずれることにより、不均等な微小管の配置や局所的な膜成分および蛋白質の供給を促すと考えられている。
神経発生における役割
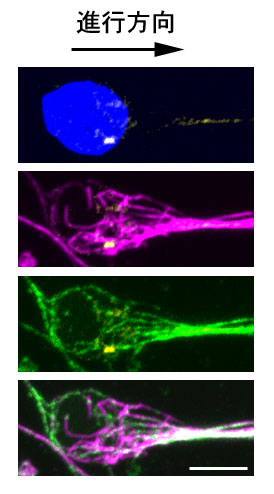
核周辺の微小管は必ずしも中心体に収束していない。
青:DAPI(細胞核)、黄色:γ-tubulin(中心体)、マゼンダ:アセチル化チューブリン(安定な微小管)、緑:チロシン化チューブリン(動的な微小管)
神経幹細胞の非対称分裂
大脳皮質の神経幹細胞は、発生初期においては対称分裂により自らと同じ性質をもつ娘細胞を2つ産生し神経幹細胞の数を増大させる。その後、非対称分裂により1つの神経幹細胞と1つの神経細胞を産生し、神経幹細胞の数を維持しながら神経細胞の数を増大させる。中心体は神経幹細胞の分裂の制御にも重要であると考えられている。Cdk5rap2などの中心体関連蛋白質を欠失させると神経幹細胞を維持できなくなり、大脳皮質の神経細胞数が著しく減少する(小頭症)[2]。また、非対称分裂の際には”より古い”中心小体を含む中心体が神経幹細胞側の娘細胞に継承されること、subdistal appendageに局在するNineinが神経幹細胞の維持に必要であることが報告されている[3]。
軸索形成
海馬や大脳皮質の錐体ニューロンはまず複数の未分化な神経突起を形成した後、そのうちの1本を急速に伸長させ軸索へと分化させる。その際、中心体は軸索へと分化する神経突起の根元に局在することが報告されており、中心体が神経細胞における軸索決定に関与することが示唆されている[4][5]。中心体が主要な微小管重合開始点であることに加えて、ゴルジ体が中心体近傍に局在することから、中心体の局在により特定の神経突起に対して選択的に微小管や膜成分を供給している可能性が考えられる。しかし、他のニューロンにおいては軸索決定と中心体の位置に相関は見られないという報告もあり、軸索決定における中心体の局在は特定の神経細胞において必要なのか、神経細胞の極性化に付随して起こる現象にすぎないのかはいまだ明らかではない[6]。また、レーザー照射による中心体破壊実験の結果から、決定した後の軸索の伸長には中心体が必要ないことも報告されている[7]。分化した神経細胞では中心体の微小管重合能は低下しており、主な微小管重合は軸索および樹状突起内に広く分布した非中心体性のγ-tubulinによって担われると考えられている。
神経細胞移動
神経細胞は脳室帯等の細胞分裂層で産生された後、自らが機能する部位へと移動する(神経細胞移動)。神経細胞移動の不全は皮質の層構造形成に異常を引き起こすことが知られており、層構造異常の原因遺伝子として同定されたLis1, Doublecortin等の中心体および微小管関連遺伝子が神経細胞移動に関与することが示されている。神経細胞は移動に際して先導突起と呼ばれる神経突起を進行方向へと伸ばし、細胞核およびその他の細胞内小器官を先導突起内へと移入させる。これまでに、中心体が移動中の神経細胞において細胞核の前方(先導突起側)に局在しており細胞核に先行して先導突起内に移動すること、移動時の細胞核がmicrotubule cageと呼ばれる微小管の籠状構造に覆われていることが報告されており[8][9]、このことから中心体は自身から伸長する微小管によって先導突起と細胞核を連結し、細胞核を先導突起内へ牽引するというモデルが提唱されている。しかし、移動中の神経細胞内では細胞核周辺の微小管が必ずしも中心体に収束しておらず(図3)細胞核と中心体は独立に移動するという、上記の核牽引モデルと矛盾する報告もある[10]。中心体は細胞の極性形成および維持に関与することから、細胞核を牽引するのではなく移動方向を決定することで間接的に細胞核移動に関与しているのかもしれない。また、細胞核移動を駆動する力は微小管モーター蛋白質ダイニンが担うと考えられているが、ダイニンが細胞内のどこで作用しているのか(先導突起内、中心体、細胞核表面等)は明らかではない。加えてアクチンモーターであるミオシンが細胞核移動に作用するという報告もある[11][12]。中心体自身の移動もダイニンとミオシンの連動により制御されると考えられているがその詳細は不明である[13][14]。
繊毛の形成
神経幹細胞を含む多くの細胞は一次繊毛と呼ばれる微小管束によって膜が突出したアンテナ状構造を持つ。一次繊毛はhedgehogシグナルやPDGFシグナルなどの細胞外シグナルに対するセンサーとして働く。間期の細胞において中心体は基底小体として一次繊毛の基部に存在しその形成に関与する。繊毛の形成不全は脳の発生過程や機能において様々な障害を引き起こすことが知られている[15]。小脳顆粒細胞や海馬歯状回顆粒細胞の前駆細胞はSonic Hedgehogシグナル依存的な細胞増殖を行うことが知られており、一次繊毛の形成不全を示すIFT88やKif3a欠損マウスにおいてはこれらの細胞数が減少する。また、嗅覚受容神経細胞や上衣細胞は一次繊毛から派生した二次繊毛を持つ。一次繊毛が1つの細胞にⅠ本なのに対して二次繊毛は1つの細胞に複数存在し得る。嗅覚受容神経細胞は嗅覚受容体を局在させた二次繊毛を嗅上皮に露出させることでにおい物質を感知する。繊毛の形成不全に起因する疾患において嗅覚障害が伴うことが知られている。上衣細胞は脳室壁に存在しており複数の二次繊毛を脳室に向かって伸ばしている。上衣細胞の繊毛は単細胞生物の繊毛や鞭毛のように運動を行い、脳室内の脳脊髄液を循環させる。
中心体関連遺伝子と神経疾患
これまで脳の形成不全を伴う神経疾患の原因遺伝子として多くの中心体関連分子が同定されている。小頭症に関してはその原因遺伝子として7つの中心体関連遺伝子(MCPH1~7)が同定されている。小頭症では大脳皮質の神経細胞数が著しく減少していることから、細胞分裂または対称・非対称分裂の制御に異常があることが示唆される。ただし、中心体関連遺伝子の多くはDNA損傷応答にも関与しており、DNA損傷に伴う細胞死が関与している可能性もある。小頭症では皮質の層構造には異常が見られないことから神経細胞移動の関与は少ないと考えられる。一方、Ⅰ型滑脳症においては神経細胞移動の障害に起因する皮質の層構造異常が見られる。Ⅰ型滑脳症の原因遺伝子としてLis1、Doublecortinなどが同定されているがこれらの分子もまた中心体や微小管に局在することが報告されている。また、一次繊毛の形成および機能に関連する遺伝子の変異はJoubert症候群やBardet – Biedl症候群等のciliopathyと呼ばれる疾患を引き起こすことが知られている[16]。
関連項目
参考文献
- ↑
Brito, D.A., Gouveia, S.M., & Bettencourt-Dias, M. (2012).
Deconstructing the centriole: structure and number control. Current opinion in cell biology, 24(1), 4-13. [PubMed:22321829] [WorldCat] [DOI] - ↑
Megraw, T.L., Sharkey, J.T., & Nowakowski, R.S. (2011).
Cdk5rap2 exposes the centrosomal root of microcephaly syndromes. Trends in cell biology, 21(8), 470-80. [PubMed:21632253] [PMC] [WorldCat] [DOI] - ↑
Wang, X., Tsai, J.W., Imai, J.H., Lian, W.N., Vallee, R.B., & Shi, S.H. (2009).
Asymmetric centrosome inheritance maintains neural progenitors in the neocortex. Nature, 461(7266), 947-55. [PubMed:19829375] [PMC] [WorldCat] [DOI] - ↑
de Anda, F.C., Pollarolo, G., Da Silva, J.S., Camoletto, P.G., Feiguin, F., & Dotti, C.G. (2005).
Centrosome localization determines neuronal polarity. Nature, 436(7051), 704-8. [PubMed:16079847] [WorldCat] [DOI] - ↑
de Anda, F.C., Meletis, K., Ge, X., Rei, D., & Tsai, L.H. (2010).
Centrosome motility is essential for initial axon formation in the neocortex. The Journal of neuroscience : the official journal of the Society for Neuroscience, 30(31), 10391-406. [PubMed:20685982] [PMC] [WorldCat] [DOI] - ↑
Kuijpers, M., & Hoogenraad, C.C. (2011).
Centrosomes, microtubules and neuronal development. Molecular and cellular neurosciences, 48(4), 349-58. [PubMed:21722732] [WorldCat] [DOI] - ↑
Stiess, M., Maghelli, N., Kapitein, L.C., Gomis-Rüth, S., Wilsch-Bräuninger, M., Hoogenraad, C.C., ..., & Bradke, F. (2010).
Axon extension occurs independently of centrosomal microtubule nucleation. Science (New York, N.Y.), 327(5966), 704-7. [PubMed:20056854] [WorldCat] [DOI] - ↑
Tanaka, T., Serneo, F.F., Higgins, C., Gambello, M.J., Wynshaw-Boris, A., & Gleeson, J.G. (2004).
Lis1 and doublecortin function with dynein to mediate coupling of the nucleus to the centrosome in neuronal migration. The Journal of cell biology, 165(5), 709-21. [PubMed:15173193] [PMC] [WorldCat] [DOI] - ↑
Solecki, D.J., Model, L., Gaetz, J., Kapoor, T.M., & Hatten, M.E. (2004).
Par6alpha signaling controls glial-guided neuronal migration. Nature neuroscience, 7(11), 1195-203. [PubMed:15475953] [WorldCat] [DOI] - ↑
Umeshima, H., Hirano, T., & Kengaku, M. (2007).
Microtubule-based nuclear movement occurs independently of centrosome positioning in migrating neurons. Proceedings of the National Academy of Sciences of the United States of America, 104(41), 16182-7. [PubMed:17913873] [PMC] [WorldCat] [DOI] - ↑
Bellion, A., Baudoin, J.P., Alvarez, C., Bornens, M., & Métin, C. (2005).
Nucleokinesis in tangentially migrating neurons comprises two alternating phases: forward migration of the Golgi/centrosome associated with centrosome splitting and myosin contraction at the rear. The Journal of neuroscience : the official journal of the Society for Neuroscience, 25(24), 5691-9. [PubMed:15958735] [PMC] [WorldCat] [DOI] - ↑
Schaar, B.T., & McConnell, S.K. (2005).
Cytoskeletal coordination during neuronal migration. Proceedings of the National Academy of Sciences of the United States of America, 102(38), 13652-7. [PubMed:16174753] [PMC] [WorldCat] [DOI] - ↑
Tsai, J.W., Bremner, K.H., & Vallee, R.B. (2007).
Dual subcellular roles for LIS1 and dynein in radial neuronal migration in live brain tissue. Nature neuroscience, 10(8), 970-9. [PubMed:17618279] [WorldCat] [DOI] - ↑
Solecki, D.J., Trivedi, N., Govek, E.E., Kerekes, R.A., Gleason, S.S., & Hatten, M.E. (2009).
Myosin II motors and F-actin dynamics drive the coordinated movement of the centrosome and soma during CNS glial-guided neuronal migration. Neuron, 63(1), 63-80. [PubMed:19607793] [PMC] [WorldCat] [DOI] - ↑ Resource not found in PubMed.21435552
- ↑
Lee, J.E., & Gleeson, J.G. (2011).
Cilia in the nervous system: linking cilia function and neurodevelopmental disorders. Current opinion in neurology, 24(2), 98-105. [PubMed:21386674] [PMC] [WorldCat] [DOI]
(執筆者:梅嶋 宏樹、見学 美根子 担当編集委員:村上 冨士夫)