「小胞GABAトランスポーター」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| (同じ利用者による、間の1版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0148418 高森 茂雄]</font><br> | <font size="+1">[http://researchmap.jp/read0148418 高森 茂雄]</font><br> | ||
''同志社大学 脳科学研究科''<br> | ''同志社大学 脳科学研究科''<br> | ||
DOI [[XXXX]]/XXXX 原稿受付日:2014年4月29日 原稿完成日:2014年月日<br> | |||
担当編集委員:[http://researchmap.jp/haruokasai 河西 春郎](東京大学 大学院医学系研究科)<br> | 担当編集委員:[http://researchmap.jp/haruokasai 河西 春郎](東京大学 大学院医学系研究科)<br> | ||
</div> | </div> | ||
| 29行目: | 29行目: | ||
== GABA輸送機構 == | == GABA輸送機構 == | ||
[[image:小胞GABAトランスポーター1.jpg|thumb|350px|'''図1.抑制性シナプス終末におけるシナプス小胞GABA再充填機構'''<br>抑制性神経伝達物質であるGABAは、シナプス終末の細胞質に存在するグルタミン酸脱炭酸酵素(GAD)の働きにより興奮性神経伝達物質であるグルタミン酸から作られる。VGATによるGABA輸送は、液胞型プロトンATPaseが形成するプロトン電気化学勾配によって駆動されるが、輸送メカニズムの詳細は不明である。現在、GABA/プロトンの対向輸送モデルと、GABA/ | [[image:小胞GABAトランスポーター1.jpg|thumb|350px|'''図1.抑制性シナプス終末におけるシナプス小胞GABA再充填機構'''<br>抑制性神経伝達物質であるGABAは、シナプス終末の細胞質に存在するグルタミン酸脱炭酸酵素(GAD)の働きにより興奮性神経伝達物質であるグルタミン酸から作られる。VGATによるGABA輸送は、液胞型プロトンATPaseが形成するプロトン電気化学勾配によって駆動されるが、輸送メカニズムの詳細は不明である。現在、GABA/プロトンの対向輸送モデルと、GABA/Cl–の共輸送モデルが提唱されている。]] | ||
GABAおよびグリシンのシナプス小胞内への輸送は、プロトンの電気化学勾配を駆動力とする[[二次輸送]]である<ref name=ref15><pubmed>1678614</pubmed></ref> <ref name=ref16><pubmed>2903047</pubmed></ref> <ref name=ref17><pubmed>2566998</pubmed></ref>。プロトン勾配は、液胞型プロトンATPaseが細胞質から小胞内腔にプロトンを運ぶことにより、[[膜電位]]勾配(小胞内が+)とpH勾配(小胞内が酸性)が形成される。[[グルタミン酸]]の輸送は、主に膜電位勾配、[[アセチルコリン]]や[[モノアミン]]類の輸送は主にpH勾配によって駆動されることが知られているが、GABAおよびグリシンの輸送は丁度その中間に位置しているとされている<ref name=ref18><pubmed>9843673</pubmed></ref>。基質とプロトンとの共役を含めVGAT/VIAATの詳細な輸送メカニズムは不明であるが、最近、VGAT/VIAATの再構成実験の結果から、VGAT/VIAATは膜電位勾配を駆動力として使い、GABAとCl<sup>–</sup>を1:2で輸送する共輸送体であるとする新しい仮説が提唱された<ref name=ref19><pubmed>19843525</pubmed></ref>(図1)。 | GABAおよびグリシンのシナプス小胞内への輸送は、プロトンの電気化学勾配を駆動力とする[[二次輸送]]である<ref name=ref15><pubmed>1678614</pubmed></ref> <ref name=ref16><pubmed>2903047</pubmed></ref> <ref name=ref17><pubmed>2566998</pubmed></ref>。プロトン勾配は、液胞型プロトンATPaseが細胞質から小胞内腔にプロトンを運ぶことにより、[[膜電位]]勾配(小胞内が+)とpH勾配(小胞内が酸性)が形成される。[[グルタミン酸]]の輸送は、主に膜電位勾配、[[アセチルコリン]]や[[モノアミン]]類の輸送は主にpH勾配によって駆動されることが知られているが、GABAおよびグリシンの輸送は丁度その中間に位置しているとされている<ref name=ref18><pubmed>9843673</pubmed></ref>。基質とプロトンとの共役を含めVGAT/VIAATの詳細な輸送メカニズムは不明であるが、最近、VGAT/VIAATの再構成実験の結果から、VGAT/VIAATは膜電位勾配を駆動力として使い、GABAとCl<sup>–</sup>を1:2で輸送する共輸送体であるとする新しい仮説が提唱された<ref name=ref19><pubmed>19843525</pubmed></ref>(図1)。 | ||
2015年1月16日 (金) 13:14時点における版
英語名:vesicular GABA transporter, vesicular inhibitory amino acid transporter
英語略語名:VGAT, VIAAT
同義語:小胞型抑制性神経伝達物質トランスポーター
哺乳類中枢神経系における抑制性神経伝達物質はγ—酪酸(GABA)である。GABAをシナプス小胞内腔に輸送するトランスポーターは、線虫のGABA神経伝達を司る遺伝子の1つであるunc-47の相同遺伝子として1998年にクローニングされ、VGAT(vesicular GABA transporter)と名付けられた。VGATは脳幹・脊髄系の抑制性伝達物質であるグリシンも基質とするため、VIAAT(vesicular inhibitory amino acid transporter)とも呼ばれる。VGATは、液胞型プロトンATPaseによって形成されるプロトン(H+)電気化学勾配を駆動力として、GABAやグリシンを小胞内に濃縮する。VGATノックアウトマウスは胎生致死であり、臍帯ヘルニアや口蓋裂などGAD67(GABA合成酵素)ノックアウトマウスと類似した所見を呈することから、GABAシグナリングの発生過程での重要性が明らかになった。
分子クローニングと構造
運動失調(uncordinate)を呈する幾つかの線虫の変異体のうち、unc-47はGABAニューロンのシナプス終末における機能破綻が示唆されていた[1] [2]。1998年にUNC-47遺伝子の哺乳類相同遺伝子がクローニングされ、遺伝子産物が抑制性シナプス終末に存在しシナプス小胞へのGABA充填に関わることが示され、小胞GABAトランスポーターと名付けられた[3]。また、UNC-47遺伝子は脳幹・脊髄の主な抑制性神経伝達物質であるグリシンも輸送することから、小胞型抑制性神経伝達物質トランスポーター(VIAAT)とも呼ばれる[4]。
SLC32ファミリーに属し、SCL32A1と呼ばれるが、現在までに同じファミリーに属する相同遺伝子が同定されていない[5]。また、C末端側の配列が異なるスプライシング変異体の存在が知られている[6]。
タンパク質の一次構造から、VGAT/VIAATは約500個余りのアミノ酸からなり、N末端が細胞質側、C末端が小胞内腔にある9回膜貫通型タンパク質であることが示唆されている[7]。脳のサンプルのウェスタンブロットでは、55KDaと45KDa付近に二本の主要なバンドとして観察されるが、これらはリン酸化による修飾の違いである[8]。リン酸化部位の特定はされていない。スプライシング変異体やリン酸化の違いによる機能の差異は不明である。
発現分布
中枢神経系のGABAニューロンとグリシンニューロンの神経終末に局在する[9]。GABA合成酵素であるグルタミン酸脱炭酸酵素(glutamic acid decarboxylase, GAD)よりも神経終末に局在するので、抑制性シナプス終末の分子マーカーとして免疫組織化学的な同定によく用いられている。また、VGATのC末端側が小胞内腔にあることを利用して、C末端を認識する抗体を培養細胞や生体脳に暴露させることで、GABAシナプス終末を特異的に蛍光標識する技術も開発されている[7]。更に、神経系以外でも下垂体分泌細胞、松果体や膵臓のグルカゴン分泌細胞などでもVGAT/VIAATの発現が確認されているが、生理機能は明らかではない[10] [11] [12] [13] [14]。
GABA輸送機構
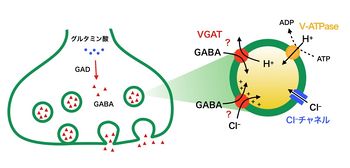
抑制性神経伝達物質であるGABAは、シナプス終末の細胞質に存在するグルタミン酸脱炭酸酵素(GAD)の働きにより興奮性神経伝達物質であるグルタミン酸から作られる。VGATによるGABA輸送は、液胞型プロトンATPaseが形成するプロトン電気化学勾配によって駆動されるが、輸送メカニズムの詳細は不明である。現在、GABA/プロトンの対向輸送モデルと、GABA/Cl–の共輸送モデルが提唱されている。
GABAおよびグリシンのシナプス小胞内への輸送は、プロトンの電気化学勾配を駆動力とする二次輸送である[15] [16] [17]。プロトン勾配は、液胞型プロトンATPaseが細胞質から小胞内腔にプロトンを運ぶことにより、膜電位勾配(小胞内が+)とpH勾配(小胞内が酸性)が形成される。グルタミン酸の輸送は、主に膜電位勾配、アセチルコリンやモノアミン類の輸送は主にpH勾配によって駆動されることが知られているが、GABAおよびグリシンの輸送は丁度その中間に位置しているとされている[18]。基質とプロトンとの共役を含めVGAT/VIAATの詳細な輸送メカニズムは不明であるが、最近、VGAT/VIAATの再構成実験の結果から、VGAT/VIAATは膜電位勾配を駆動力として使い、GABAとCl–を1:2で輸送する共輸送体であるとする新しい仮説が提唱された[19](図1)。
遺伝子改変マウスと生理機能
VGAT/VIAATノックアウトマウスは胎生致死であり、胎生期18日目以降にGAD67ノックアウトマウスと類似した臍帯ヘルニアと口蓋裂の所見が認められる[20] [21]。このことからGABAあるいはグリシンが司るシグナル伝達は胎生期の発達に不可欠であることが示された。VGAT/VIAATノックアウトマウスでは、IPSCが顕著に減弱しているが、微小IPSCは振幅・頻度が野生型に比べて激減するものの、若干検出される[21]。このIPSCがVGAT/VIAAT以外の未知の小胞型GABAトランスポーターによるものなのか、あるいはVGAT/VIAATに依存しないGABA再充填メカニズムや非小胞型GABA放出によるものなのかは不明である。
参考文献
- ↑
McIntire, S.L., Jorgensen, E., & Horvitz, H.R. (1993).
Genes required for GABA function in Caenorhabditis elegans. Nature, 364(6435), 334-7. [PubMed:8332190] [WorldCat] [DOI] - ↑
McIntire, S.L., Jorgensen, E., Kaplan, J., & Horvitz, H.R. (1993).
The GABAergic nervous system of Caenorhabditis elegans. Nature, 364(6435), 337-41. [PubMed:8332191] [WorldCat] [DOI] - ↑
McIntire, S.L., Reimer, R.J., Schuske, K., Edwards, R.H., & Jorgensen, E.M. (1997).
Identification and characterization of the vesicular GABA transporter. Nature, 389(6653), 870-6. [PubMed:9349821] [WorldCat] [DOI] - ↑
Sagné, C., El Mestikawy, S., Isambert, M.F., Hamon, M., Henry, J.P., Giros, B., & Gasnier, B. (1997).
Cloning of a functional vesicular GABA and glycine transporter by screening of genome databases. FEBS letters, 417(2), 177-83. [PubMed:9395291] [WorldCat] [DOI] - ↑
Gasnier, B. (2004).
The SLC32 transporter, a key protein for the synaptic release of inhibitory amino acids. Pflugers Archiv : European journal of physiology, 447(5), 756-9. [PubMed:12750892] [WorldCat] [DOI] - ↑
Ebihara, S., Obata, K., & Yanagawa, Y. (2003).
Mouse vesicular GABA transporter gene: genomic organization, transcriptional regulation and chromosomal localization. Brain research. Molecular brain research, 110(1), 126-39. [PubMed:12573541] [WorldCat] [DOI] - ↑ 7.0 7.1
Martens, H., Weston, M.C., Boulland, J.L., Grønborg, M., Grosche, J., Kacza, J., ..., & Härtig, W. (2008).
Unique luminal localization of VGAT-C terminus allows for selective labeling of active cortical GABAergic synapses. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(49), 13125-31. [PubMed:19052203] [PMC] [WorldCat] [DOI] - ↑
Bedet, C., Isambert, M.F., Henry, J.P., & Gasnier, B. (2000).
Constitutive phosphorylation of the vesicular inhibitory amino acid transporter in rat central nervous system. Journal of neurochemistry, 75(4), 1654-63. [PubMed:10987847] [WorldCat] [DOI] - ↑
Chaudhry, F.A., Reimer, R.J., Bellocchio, E.E., Danbolt, N.C., Osen, K.K., Edwards, R.H., & Storm-Mathisen, J. (1998).
The vesicular GABA transporter, VGAT, localizes to synaptic vesicles in sets of glycinergic as well as GABAergic neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 18(23), 9733-50. [PubMed:9822734] [PMC] [WorldCat] - ↑
End, K., Gamel-Didelon, K., Jung, H., Tolnay, M., Lüdecke, D., Gratzl, M., & Mayerhofer, A. (2005).
Receptors and sites of synthesis and storage of gamma-aminobutyric acid in human pituitary glands and in growth hormone adenomas. American journal of clinical pathology, 124(4), 550-8. [PubMed:16146821] [WorldCat] [DOI] - ↑
Geigerseder, C., Doepner, R., Thalhammer, A., Frungieri, M.B., Gamel-Didelon, K., Calandra, R.S., ..., & Mayerhofer, A. (2003).
Evidence for a GABAergic system in rodent and human testis: local GABA production and GABA receptors. Neuroendocrinology, 77(5), 314-23. [PubMed:12806177] [WorldCat] [DOI] - ↑
Gammelsaeter, R., Frøyland, M., Aragón, C., Danbolt, N.C., Fortin, D., Storm-Mathisen, J., ..., & Gundersen, V. (2004).
Glycine, GABA and their transporters in pancreatic islets of Langerhans: evidence for a paracrine transmitter interplay. Journal of cell science, 117(Pt 17), 3749-58. [PubMed:15252115] [WorldCat] [DOI] - ↑
Echigo, N., & Moriyama, Y. (2004).
Vesicular inhibitory amino acid transporter is expressed in gamma-aminobutyric acid (GABA)-containing astrocytes in rat pineal glands. Neuroscience letters, 367(1), 79-84. [PubMed:15308302] [WorldCat] [DOI] - ↑
Hayashi, M., Otsuka, M., Morimoto, R., Muroyama, A., Uehara, S., Yamamoto, A., & Moriyama, Y. (2003).
Vesicular inhibitory amino acid transporter is present in glucagon-containing secretory granules in alphaTC6 cells, mouse clonal alpha-cells, and alpha-cells of islets of Langerhans. Diabetes, 52(8), 2066-74. [PubMed:12882924] [WorldCat] [DOI] - ↑
Burger, P.M., Hell, J., Mehl, E., Krasel, C., Lottspeich, F., & Jahn, R. (1991).
GABA and glycine in synaptic vesicles: storage and transport characteristics. Neuron, 7(2), 287-93. [PubMed:1678614] [WorldCat] [DOI] - ↑
Hell, J.W., Maycox, P.R., Stadler, H., & Jahn, R. (1988).
Uptake of GABA by rat brain synaptic vesicles isolated by a new procedure. The EMBO journal, 7(10), 3023-9. [PubMed:2903047] [PMC] [WorldCat] - ↑
Kish, P.E., Fischer-Bovenkerk, C., & Ueda, T. (1989).
Active transport of gamma-aminobutyric acid and glycine into synaptic vesicles. Proceedings of the National Academy of Sciences of the United States of America, 86(10), 3877-81. [PubMed:2566998] [PMC] [WorldCat] [DOI] - ↑
Edwards, R.H. (1998).
Neurotransmitter release: variations on a theme. Current biology : CB, 8(24), R883-5. [PubMed:9843673] [WorldCat] [DOI] - ↑
Juge, N., Muroyama, A., Hiasa, M., Omote, H., & Moriyama, Y. (2009).
Vesicular inhibitory amino acid transporter is a Cl-/gamma-aminobutyrate Co-transporter. The Journal of biological chemistry, 284(50), 35073-8. [PubMed:19843525] [PMC] [WorldCat] [DOI] - ↑
Saito, K., Kakizaki, T., Hayashi, R., Nishimaru, H., Furukawa, T., Nakazato, Y., ..., & Yanagawa, Y. (2010).
The physiological roles of vesicular GABA transporter during embryonic development: a study using knockout mice. Molecular brain, 3, 40. [PubMed:21190592] [PMC] [WorldCat] [DOI] - ↑ 21.0 21.1
Wojcik, S.M., Katsurabayashi, S., Guillemin, I., Friauf, E., Rosenmund, C., Brose, N., & Rhee, J.S. (2006).
A shared vesicular carrier allows synaptic corelease of GABA and glycine. Neuron, 50(4), 575-87. [PubMed:16701208] [WorldCat] [DOI]