鈴木 秀典
日本医科大学大学院医学研究科 薬理学分野
DOI:10.14931/bsd.6219 原稿受付日:2015年8月4日 原稿完成日:2015年月日
担当編集委員:
サブスタンスP substance P(SP)は、ウマの脳および腸管に存在し、血圧を下降させ、平滑筋を収縮させる物質として、1931年にvon EulerとGaddumによって見出され、1971年に単離された神経ペプチドである。類似の構造を持つペプチドと共に、タキキニンtachykininsと総称される。SPに高親和性を持つNK1受容体を介して、様々な細胞内情報伝達系を活性化し、複数のイオンチャネルを修飾する。SPおよびNK1受容体は、神経細胞だけでなく、末梢の非神経細胞にも発現している。従って痛覚、神経原性炎症、情動、報酬系等、広範囲な生理機能と疾患病態に関与している。
| サブスタンスP | |
|---|---|
| |
| Identifiers | |
| 33507-63-0 | |
| ChEMBL | ChEMBL235363 |
| ChemSpider | 33558 |
| |
| 2098 | |
| MeSH | Substance+P |
| PubChem | 36511 |
| UNII | 675VGV5J1D |
| Properties | |
| Molar mass | 1347.63 g/mol |
| 特記なき場合、データは常温(25 °C)・常圧(100 kPa)におけるものである。 | |
| タキキニン前駆体1 | |
|---|---|
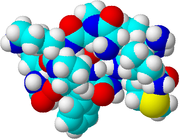 サブスタンスPの空間充填モデル | |
| Identifiers | |
| Symbol | TAC1 |
| Alt. symbols | TAC2, NKNA |
| Entrez | 6863 |
| HUGO | 11517 |
| OMIM | 162320 |
| RefSeq | NM_003182 |
| UniProt | P20366 |
| Other data | |
| Locus | Chr. 7 q21-q22 |
サブスタンスPとは
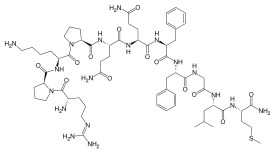
11個のアミノ酸からなる神経ペプチドである。SPは一次求心性ニューロンの一部に含まれ、脊髄後角で刺激に応じて神経終末のシナプス小胞から放出され、脊髄ニューロンで時間経過の遅い脱分極をひきおこし、neprilysin (EC 3.4.24.11: enkephalinase)、aminopeptidase N (EC 3.4.11.2)やpeptidyl dipeptidase A (EC 3.4.15.1: angiotensin converting enzyme)など複数の酵素で分解されて不活性化される1), 2)。
SPはタキキニンファミリーに属している。同じファミリーには、ニューロキニンA neurokinin A (NKA)、ニューロキニンB neurokinin B (NKB)、ヘモキニン-1 hemokinin-1 (HK-1)が含まれ、そのC末端に共通のアミノ酸配列、-Phe-X-Gly-Leu-Met-NH2を持っている。SP、NKA、NKBは哺乳類でアミノ酸全配列が共通であるが、HK-1はヒトとマウス/ラット間で配列に違いがある。(表1)。ヒトでは、Tac 1遺伝子から選択的スプライシングによって、α, β, γ, δ Tac1 mRNAスプライスバリアントが生成され、それぞれのmRNAからSPが翻訳される。NKAもTac 1遺伝子に由来するが、β, γ Tac1 mRNAから翻訳される。NKBはTac3遺伝子、HK-1、endokinin AおよびBは Tac4遺伝子にコードされている3)。(表1)
SP、NKA、NKBのC末端のそれぞれ6、7、8個以上のアミノ酸を含むペプチドは、受容体に対し、原ペプチドとほぼ同等の活性を示すが、N末端フラグメントやC末端のアミド基を除いたSP free acidは活性がない1)。
| タキキニン | 配列 | 遺伝子 | mRNAスプライスバリアント |
| Substance P | Arg-Pro-Lys-Pro-Gln-Gln-Phe-Phe-Gly-Leu-Met-NH2 | Tac1 | α, β, g, δ Tac1 |
| Neurokinin A | His-Lys-Thr-Asp-Ser-Phe-Val-Gly-Leu-Met-NH2 | Tac1 | β, g Tac1 |
| Neurokinin B | Asp-Met-His-Asp-Phe-Phe-Val-Gly-Leu-Met-NH2 | Tac3 | α, β Tac3 |
| マウスhemokinin-1 | Arg-Ser-Arg-Thr-Arg-Gln-Phe-Tyr-Gly-Leu-Met-NH2 | Tac4 | Tac4 |
| ヒトhemokinin-1 | Thr-Gly-Lys-Ala-Ser-Gln-Phe-Phe- Gly-Leu-Met-NH2 | Tac4 | α Tac4 |
| ヒトEndokinin A and B | –Gly-Lys-Ala-Ser-Gln-Phe-Phe- Gly-Leu-Met-NH2 | Tac4 | α Tac4 (Endokinin A) |
| β, g, δ Tac4 (Endokinin B) |
注)ヒトEndokinin AとBはそれぞれ全長47、41アミノ酸の内、C末端の10アミノ酸のみ示している。赤字は共通配列。
受容体
哺乳類のタキキニン受容体はG蛋白質共役型受容体で、NK1, NK2, NK3の3種類があり、それぞれSP、NKA、NKBが高い親和性を持っている4)。NK1受容体の細胞内情報伝達経路は当初考えられていた以上に多岐に亘っている3)。Protein kinase C、protein kinase A、phospholipase A2の活性化だけでなく、Rho-ROCK経路を介したmyosin light chain kinaseのリン酸化やepidermal growth factor receptor (EGFR)のトランス活性化を介したmitogen-activated protein kinaseの活性化も報告されている5)。HK-1はSPと同様にNK1受容体に対して親和性が高く、SPとほぼ同等のKiを示している6)。HK-1に固有の高親和性受容体は見いだされていない。
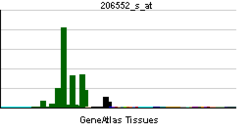
発現
タキキニンの神経系における発現分布に関しては、SPとNKAは中枢神経系および末梢神経系の神経細胞に、NKBは脊髄および大脳を含む中枢神経系細胞に発現している。タキキニンは従来神経細胞由来と考えられてきたが、現在は神経細胞だけでなく、末梢の非神経細胞にも発現していることが分かっている。例えば、SPは血管内皮細胞や種々の免疫細胞、線維芽細胞、NKBは胎盤組織3)、HK-1は心、肺、骨格筋、皮膚などの末梢組織に主に分布している6), 7)。HK-1はマウスpre-B細胞の成熟に対し自己分泌分子として働く他、T細胞の成熟や女性生殖器機能にも関与している8)。
タキキニン受容体の組織分布に関しては、NK1受容体は中枢神経系(視床下部、嗅球、線条体、脊髄など)と末梢組織(膀胱、唾液腺、腸管など)、NK2受容体は末梢組織(膀胱、輸精管、腸管など)、NK3受容体は中枢神経系(視床下部、大脳皮質、脊髄など)に分布している9, 10)。
機能
ニューロンにおいて、様々なチャネルの修飾機構が報告されている。前脳基底野細胞では、Gq/11およびPLCβ-1を細胞内情報伝達系として、SPは内向き整流性K+チャネルを抑制し、脱分極をおこす11)。ラット上頸神経節細胞では、SPが電位非依存性にN型Ca2+チャネルを抑制するが12)、チャネルを構成するCaVβサブユニットの種類によっては、SPがN電流を増強する報告もある13)。ラット舌下運動神経およびラット延髄pre-Bőtzinger complex吸気ニューロンでは、SP はtwo-pore domainカリウムチャネル1つであるTASK-1を抑制する14), 15), 16)。TASK-1を介したリーク電流は、これらのニューロンにおいて静止膜電位の形成やリズムの制御に関わっている。Von EulerとGaddumが見出したSPによる血圧下降作用は、血管内皮細胞のNK1受容体刺激を介して産生された一酸化窒素によって、細動脈平滑筋が弛緩したと考えられている17)。
疾患との関連
疼痛
SPは侵害刺激を伝える一次求心性ニューロンの一部に含まれ、SP陽性細胞は後根神経細胞の約30%を占める18)。SP陽性細胞の約80%にTRPV1受容体が発現している19)。神経成長因子(NGF)を過剰発現させたトランスジェニックマウスでは脊髄後角でSPの発現が増加し、痛覚過敏hyperalgesiaを示す20)。NK1とNK2受容体は一次求心性ニューロンと脊髄後角ニューロンに発現している。従って、神経刺激等によって一次求心性神経末端で放出されたSPは、後角ニューロンに作用するだけでなく、自己あるいは傍分泌様式で、一次求心性ニューロンにNK1受容体と共発現しているTRPV1を活性化させ、痛覚過敏に関与する21)。NK1受容体遺伝子ホモ欠失マウスでは、通常の痛覚反応はあるが、強い侵害刺激に対する反応が減弱している22)。神経障害によって、通常では触覚を伝達するAβ線維においてSPが発現してくることから23)、この変化も神経障害性疼痛の発症機序の一部に関与していると考えられる。脊髄後角のNK1発現ニューロンは高次脳部位へ投射し、脳幹の下行性経路を介して脊髄の興奮性を制御する24)。一方、青斑核を起始とする下行性ノルアドレナリン含有神経は痛覚抑制系として作用しているが、青斑核細胞はNK1受容体を発現しており、SPの青斑核への局所投与は一過性の鎮痛をおこす25)。現在のところ、鎮痛薬として臨床応用されているタキキニン受容体拮抗薬はない。
神経原性炎症
SPおよびNKAは三叉神経節、後根神経節や迷走神経節状神経節などの一次知覚ニューロンの一部に含まれており、これらのニューロンの末梢側および中枢側神経終末から放出される。一次求心性神経における活動電位の逆行性伝導や末梢側終末に発現するTRPV1の活性化などに伴って、末梢側神経終末から放出されたSPやNKAは、細動脈の拡張、血漿成分の血管外漏出、顆粒球の浸潤などを含む、神経原性炎症を惹起すると考えられている3), 26)。Tac-1欠損マウスでは、神経原性炎症が抑制される27)。好中球、マクロファージ、樹状細胞およびTリンパ球では、SPおよびNK1受容体に発現していることが報告されており、SP刺激によってサイトカイン、ケモカインなどの炎症を促進する物質が放出され、炎症反応が起きると考えられている。
化学療法誘発性嘔気・嘔吐
脳幹部にある孤束核は迷走神経の求心性入力および他の脳部位からの入力を受けて情報を統合し、嘔吐反射の遠心路に関連する部位に出力している。NK1受容体は孤束核に分布しており、SPは孤束核ニューロンの自発発火を増強するが、この効果はNK1受容体拮抗薬で抑制される28)。孤束核は、制吐薬としてのNK1受容体拮抗薬の主な標的と考えられている29)。中枢作用に加えて、腸管の迷走神経終末に分布する末梢のNK1受容体も治療効果に関与していると考えられている29)。Cisplatin等の抗がん薬による治療において、嘔気嘔吐を抑制するために、セロトニン5-HT3受容体拮抗薬とステロイドを組み合わせた治療法に比べ、非ペプチド性経口NK1受容体拮抗薬aprepitantを加えた3薬併用療法の優位性が認められ30)、現在臨床応用されている。
精神疾患
上位中枢神経系において情動や不安恐怖反応に関与すると考えられている中隔野、海馬、扁桃体、視床下部、あるいは中脳中心灰白質にNK1とNK3受容体が豊富に存在している9), 10)。ラットに拘束ストレスをかけたり、高架台に乗せると、扁桃体内側核のSP放出が上昇し、同部位へNK1受容体拮抗薬を微量投与すると、不安関連行動が減弱する31)。新生仔に母仔分離ストレスを与えると扁桃体前部基底外側核においてNK1受容体の細胞内取り込み(internalization)がおきることから、内因性SP放出の増加が示唆されている32)。一方、抗不安薬をラットに投与すると海馬と中脳中心灰白質においてSPの合成が減少する33)。NK1受容体遺伝子ホモ欠失マウスでは、高架式十字迷路試験において、不安関連行動および血清コルチゾール上昇の減少が観察され、伴って背側縫線核セロトニンニューロンの発火頻度が増加する34)。居住者-侵入者試験では攻撃性が減少する22)。不安及びうつ症状に対するNK1拮抗薬の臨床応用に関しては、まだ上市されている薬物はない。
SP-NK1神経系は薬物依存や報酬系にも関わっている。オピオイドの報酬効果に関しては、条件付け場所嗜好性試験において、NK1受容体遺伝子ホモ欠失マウスではmorphineによる場所嗜好性の獲得が抑制され、離脱症状の一部も減少する35)。Cocaineや食物の嗜好性は影響を受けないという35)。ラットにおけるheroinの自己投与や消費の動機付けがNK1受容体拮抗薬で抑制される36)。またheroinの投与で前頭前野と側坐核でNK1が増加が見られている36)。アルコールに関しては、NK1受容体遺伝子ホモ欠失マウスでは自発的アルコール摂取の増加が抑制され、アルコール依存症患者ではNK1受容体拮抗薬の投与でアルコールに対する欲求が改善している37)。健常者を対象にした機能的磁気共鳴撮像法による研究では、報酬予測時の側坐核の脳活動(BOLD信号)が、NK1受容体拮抗薬の単回投与によりプラセボと比較して有意に減少することが報告されている38)。
性腺機能不全症
NKBおよびNK3の遺伝子変異(機能欠損)による家族性低ゴナドトロピン性性腺機能不全症が報告されている39)。漏斗・弓状核細胞にあるkisspeptin含有ニューロンは、正中隆起のGnRH含有ニューロンを直接神経支配し、GnRHのパルス状の放出に関与している。このkisspeptinを含有する漏斗・弓状核細胞の一群では、NKBおよびダイノルフィンを含有し、NK3受容体も発現している。NKBは自己あるいは傍分泌によってkisspeptin分泌を刺激しているので、NKBあるいはNK3の機能欠損によって、kisspeptin含有ニューロンの機能不全とそれに起因する正中隆起細胞からのGnRH分泌障害が起きると考えられている40)。
参考文献
1. Otsuka M, Yoshioka K: Neurotransmitter functions of mammalian tachykinins. Physiol Rev 1993; 73: 229-308. 2. Suzuki H, Yoshioka K, Yanagisawa M, Urayama O, Kurihara T, Hosoki R, Saito K, Otsuka M: Involvement of enzymatic degradation in the inactivation of tachykinin neurotransmitters in neonatal rat spinal cord. Br J Pharmacol 1994; 113: 310-316. 3. Steinhoff MS, von Mentzer B, Geppetti P, Pothoulakis C, Bunnett NW: Tachykinins and their receptors: contributions to physiological control and the mechanisms of disease. Physiol Rev 2014; 94: 265–301. 4. Nakanishi S: Mammalian tachykinin receptors. Annu Rev Neurosci 1991; 14: 123-136. 5. Castagliuolo I, Valenick L, Liu J, Pothoulakis C: Epidermal growth factor receptor transactivation mediates substance P-induced mitogenic responses in U-373 MG cells. J Biol Chem 2000; 276: 26545-26550. 6. Kurtz MM, Wang R, Clements MK, Cascieri MA, Austin CP, Cunningham BR, Chicchi GG, Liu Q: Identification, localization and receptor characterization of novel mammalian substance P-like peptides. Gene 2002; 296: 205-212. 7. Page NM, Bell NJ, Gardiner SM, Manyonda IT, Brayley KJ, Strange PG, Lowry PJ: Characterization of the endokinins: human tachykinins with cardiovascular activity. Proc Natl Acad Sci USA 2003; 100: 6245-6250. 8. Patacchini R, Lecci A, Holzer P, Maggi CA: Newly discovered tachykinins raise new questions about their peripheral roles and the tachykinin nomenclature. Trends Pharmacol Sci 2004; 25: 1-3. 9. Nakaya Y, Kaneko T, Shigemoto R, Nakanishi S, Mizuno N: Immunohistochemical localization of substance P receptor in the central nervous system of the adult rat. J Comp Neurol 1994; 347: 249-274. 10. Ding Y-Q, Shigemoto R, Takada M, Ohishi H, Nakanishi S, Mizuno N: Localization of the neuromedin K receptor (NK3) in the central nervous system of the rat. J Comp Neurol 1996; 364: 290-310. 11. Takano K, Yasufuku-Takano J, Kozasa T, Singer WD, Nakajima S, Nakajima Y: Gq/11 and PLC-β1 mediate the substance P-induced inhibition of an inward rectifier K+ channel in brain neurons. J Neurophysiol 1996; 76: 2131-2136. 12. Mitra-Ganguli T, Vitko I, Perez-Reyes E, Rittenhouse AR: Orientation of palmitoylated CaVβ2a relative to CaV2.2 is critical for slow pathway modulation of N-type Ca2+ current by tachykinin receptor activation. J Gen Physiol 2009; 134: 5385–5396. 13. Shapiro MS, Hille B: Substance P and somatostatin inhibit calcium channels in rat sympathetic neurons via different G protein pathways. Neuron 1993; 10: 11-20. 14. Talley EM, Lei Q, Sirois JE, Bayliss DA: TASK-1, a two–pore domain K+ channel is modulated by multiple neurotransmitters in motoneurons. Neuron 2000; 25: 399-410. 15. Koizumi H, Smerin SE, Yamanishi T, Moorjani BR, Zhang R, Smith JC: TASK channels contribute to the K+-dominated leak current regulating respiratory rhythm generation in vitro. J Neurosci 2010; 30: 4273-4284. 16. Ptak K, Yamanishi T, Aungst J, Milescu LS, Zhang R, Richerson GB, Smith JC: Raphé neurons stimulate respiratory circuit activity by multiple mechanisms via endogenously released serotonin and substance P. J Neurosci 2009; 29: 3720-3737. 17. Whittle BJR, Lopez-Belmonte J, Rees DD: Modulation of the vasodepressor actions of acetylcholine, bradykinin, substance P and endothelin in the rat by a specific inhibitor of nitric oxide formation. Br J Pharmacol 1989; 98: 646-652. 18. Snider WD, McMahon SB: Tackling pain at the source: new ideas about nociceptors. Neuron 1998; 20: 629-632. 19. Guo A, Vulchanova L, Wang J, Li X, Elde R: Immunocytochemical localization of the vanilloid receptor 1 (VR1): relationship to neuropeptides, the P2X3 purinoceptor and IB4 binding sites. Eur J Neurosci 1999; 11: 946-958. 20. McLeod AL, Ritchie J, Cuello AC, Julien J-P, Ribeiro-da-Silva A, Henry JL: Transgenic mice over-expressing substance P exhibit allodynia and hyperalgesia which are reversed by substance P and N-methyl-D-aspartate receptor antagonists. Neuroscience 1999; 89: 891-899. 21. Zhang Z, Cang C-L, Kawasaki Y, Liang L-L, Zhang Y-Q, Ji R-R, ZhaoZ-Q: Neurokinin-1 receptor enhances TRPV1 activity in primary sensory neurons via PKCε: a novel pathway for heat hyperalgesia. J Neurosci 2007; 27: 12067-12077. 22. De Felipe C, Herrero JF, O'Brien JA, Palmer JA, Doyle CA, Smith AJH, Laird JMA, Belmonte C, Cervero F, Hunt SP: Altered nociception, analgesia and aggression in mice lacking the receptor for substance P. Nature 1998; 392: 394-397. 23. Nitzan-Luques A , Devor M, Tal M: Genotype-selective phenotypic switch in primary afferent neurons contributes to neuropathic pain. Pain 2011; 152: 2413-2426. 24. Suzuki1 R, Morcuende S, Webber M, Hunt SP, Dickenson AH: Superficial NK1-expressing neurons control spinal excitability through activation of descending pathways. Nature Neurosci. 2002; 5: 1319-1326. 25. Muto Y, Sakai A, Sakamoto A, Suzuki H: Activation of NK1 receptors in the locus coeruleus induces analgesia through noradrenergic-mediated descending inhibition in a rat model of neuropathic pain. Br J Pharmacol 2012; 166: 1047-1057. 26. Chiu IM, von Hehn CA, Woolf CJ: Neurogenic inflammation and the peripheral nervous system in host defense and immunopathology. Nature Neurosci 2012; 15: 1063-1067. 27. Cao YQ, Mantyh PW, Carlson EJ, Gillespie AM, Epstein CJ, Basbaum AI: Primary afferent tachykinins are required to experience moderate to intense pain. Nature 1998; 392: 390-394. 28. Saito R, Suehiro Y, Ariumi H, Migita K, Hori N, Hashiguchi T, Sakai M, Saeki M, Takano Y, Kamiya H: Anti-emetic effects of a novel NK-1 receptor antagonist HSP-117 in ferrets. Neurosci Lett 1998; 254: 169-172. 29. Diemunsch P, Joshi GP, Brichant JF: Neurokinin-1 receptor antagonists in the prevention of postoperative nausea and vomiting. Br J Anaesthesia 2009; 103: 7-13. 30. de Wit R, Herrstedt J, Rapoport B, Carides AD, Guoguang-Ma J, Elmer M, Schmidt C, Evans JK, Horgan KJ: The oral NK1 antagonist, aprepitant, given with standard antiemetics provides protection against nausea and vomiting over multiple cycles of cisplatin-based chemotherapy: a combined analysis of two randomised, placebo-controlled phase III clinical trials. Eur J Cancer 2004; 40: 403-410. 31. Ebner K, Rupniak NM, Saria A, Singewald N: Substance P in the medial amygdala: emotional stress-sensitive release and modulation of anxiety-related behavior in rats. Proc Natl Acad Sci USA 2004; 101: 4280-4285. 32. Kramer MS, Cutler N, Feighner J, Shrivastava R, Carman J, et al. : Distinct mechanism for antidepressant activity by blockade of central substance P receptors. Science 1998; 281: 1640-1645. 33. Brodin E, Rosén A, Schött E, Brodin K: Effects of sequential removal of rats from a group cage, and of individual housing of rats, on substance P, cholecystokinin and somatostatin levels in the periaqueductal grey and limbic regions. Neuropeptides 1994; 26: 253-260. 34. Santarelli L, Gobbi G, Debs PC, Sibille ET, Blier P, Hen R, Heath MJ: Genetic and pharmacological disruption of neurokinin 1 receptor function decreases anxiety-related behaviors and increases serotonergic function. Proc Natl Acad Sci USA 2001; 98: 1912-1917. 35. Murtra P, Sheasby AM, Hunt SP, De Felipe C: Rewarding effects of opiates are absent in mice lacking the receptor for substance P. Nature 2000; 405: 180-183. 36. Barbier E, Vendruscolo LF, Schlosburg JE, Edwards S, Juergens N, Park PE, Misra KK, Cheng K, Rice KC, Schank J, Schulteis G, Koob GF, Heilig M: The NK1 receptor antagonist L822429 reduces heroin reinforcement. Neuropsychopharmacology. 2013; 38: 976-984. 37. George DT, Gilman J, Hersh J, Thorsell A, Herion D, Geyer C, Peng X, Kielbasa W, Rawlings R, Brandt JE, Gehlert DR, Tauscher JT, Hunt SP, Hommer D, Heilig M: Neurokinin 1 receptor antagonism as a possible therapy for alcoholism. Science 2008; 319: 1536-1539. 38. Saji K, Ikeda Y, Kim W, Shingai Y, Tateno A, Takahashi H, Okubo Y, Fukayama H, Suzuki H: Acute NK₁ receptor antagonist administration affects reward incentive anticipation processing in healthy volunteers. Int J Neuropsychopharmacol 2013; 16: 1461-1471. 39. Topaloglu AK, Reimann F, Guclu M, Yalin AS, Kotan LD, Porter KM, Serin A, Mungan NO, Cook JR, Ozbek MN, Imamoglu S, Akalin NS, Yuksel B, O'Rahilly S, Semple RK: TAC3 and TACR3 mutations in familial hypogonadotropic hypogonadism reveal a key role for Neurokinin B in the central control of reproduction. Nature Genet 2009; 41: 354-358. 40. Skorupskaite K, George JT, Anderson RA: The kisspeptin-GnRH pathway in human reproductive health and disease. Human Reproduction Update 2014; 20: 485-500.