「L1」の版間の差分
細編集の要約なし |
細編集の要約なし |
||
| (同じ利用者による、間の3版が非表示) | |||
| 10行目: | 10行目: | ||
英語名:L1 | 英語名:L1 | ||
同義語:L1CAM | 同義語:L1CAM | ||
== 分子構造 == | == 分子構造 == | ||
L1は、6個の[[ | L1は、6個の[[wikipedia:JA:免疫グロブリン|免疫グロブリン]]様ドメインと5個の[[wikipedia:JA:フィブロネクチン|フィブロネクチン]]III型様ドメインからなる細胞外領域、1回膜貫通領域および細胞内領域から構成される分子量200-220 kDaの[[細胞接着分子]]である<ref><pubmed> 3412448 </pubmed></ref>。L1遺伝子を構成する28個の[[wikipedia:JA:エクソン|エクソン]]のうち、2番目と27番目のエクソンが[[wikipedia:JA:選択的スプライシング|選択的スプライシング]]を受ける。主として、神経細胞には全長型L1が発現し、非神経細胞には両エクソン配列を含まないL1が発現する。2番目のエクソンがコードするアミノ酸配列YEGHHVはL1細胞外領域に存在し、L1同士の結合(ホモフィリック結合)および他種の接着分子との結合(ヘテロフィリック結合)を増強する<ref><pubmed> 11435440 </pubmed></ref>。27番目のエクソンがコードするアミノ酸配列RSLEはL1細胞内領域に存在し、クラスリン[[アダプタータンパク質複合体|アダプター]]AP2と結合してL1の[[エンドサイト−シス]]を引き起こす<ref><pubmed> 9651214 </pubmed></ref>。L1の[[wikipedia:JA:相同#.E9.81.BA.E4.BC.9D.E5.AD.90.E3.81.AE.E7.9B.B8.E5.90.8C.E6.80.A7|ホモログ]]として、[[wikipedia:JA:ニワトリ|ニワトリ]]のNgCAM、[[wikipedia:JA:ゼブラフィッシュ|ゼブラフィッシュ]]のL1.2、[[wikipedia:JA:ショウジョウバエ|ショウジョウバエ]]のニューログリアン、[[線虫]]のLAD-1/SAX-7などが知られている。 | ||
== 発現様式 == | == 発現様式 == | ||
| 23行目: | 21行目: | ||
== 結合タンパク質 == | == 結合タンパク質 == | ||
L1細胞外領域は、隣接する細胞表面のL1細胞外領域と結合して細胞間接着を媒介する(ホモフィリック結合)。また、[[インテグリン]]、[[TAG1]]/ | L1細胞外領域は、隣接する細胞表面のL1細胞外領域と結合して細胞間接着を媒介する(ホモフィリック結合)。また、[[インテグリン]]、[[TAG1]]/アキソニン-1、F3/F11/[[コンタクティン]]などの接着分子とのヘテロフィリック結合も報告されている <ref><pubmed> 12957823 </pubmed></ref>。軸索ガイダンス分子[[セマフォリン]]の受容体である[[ニューロピリン]]-1と同一形質膜上でヘテロ2量体を形成する。L1細胞内領域と細胞骨格を連結するタンパク質として、[[アンキリン]]、[[ERM]](エズリン/ラディキシン/モエシン)、[[ダブルコルティン]]などが同定されている<ref><pubmed> 17189949 </pubmed></ref>。L1細胞内領域は、[[非受容体型チロシンキナーゼ]]Src、[[カゼインキナーゼ]]II、[[extracellular signal-regulated kinase]] 2 (Erk2)、[[p90rsk]]などの[[タンパク質リン酸化酵素]]と結合して[[リン酸化]]修飾を受ける。 | ||
== 生理機能 == | == 生理機能 == | ||
ホモフィリック結合とヘテロフィリック結合により細胞間接着を媒介する。またL1の接着性および[[細胞骨格]]との連結は時空間的に制御されるため、L1は単なる静的な細胞間接着だけでなく、動的な細胞間相互作用(細胞移動など)にも関与する。神経系での具体的なL1の機能として、[[神経細胞移動]]の促進、軸索伸長の促進、軸索束形成の促進、[[ミエリン]]形成の促進、[[シナプス可塑性]]の制御などが報告されている<ref><pubmed> 17189949 </pubmed></ref>。また、L1とニューロピリン-1のヘテロ2量体はセマフォリン3A受容体として機能し、軸索の反発性ガイダンスを媒介する<ref><pubmed> 12456642 </pubmed></ref>。 | ホモフィリック結合とヘテロフィリック結合により細胞間接着を媒介する。またL1の接着性および[[細胞骨格]]との連結は時空間的に制御されるため、L1は単なる静的な細胞間接着だけでなく、動的な細胞間相互作用(細胞移動など)にも関与する。神経系での具体的なL1の機能として、[[神経細胞移動]]の促進、軸索伸長の促進、軸索束形成の促進、[[ミエリン]]形成の促進、[[シナプス可塑性]]の制御などが報告されている<ref><pubmed> 17189949 </pubmed></ref>。また、L1とニューロピリン-1のヘテロ2量体はセマフォリン3A受容体として機能し、軸索の反発性ガイダンスを媒介する<ref><pubmed> 12456642 </pubmed></ref>。 L1の機能は、細胞内領域のリン酸化/脱リン酸化、エンドサイト−シス/[[エキソサイトーシス]]、細胞骨格との連結、[[プロテオリシス]]などによって制御されている。27番目のエクソンがコードするアミノ酸配列RSLEとそれに隣接するチロシン残基は、クラスリンアダプターAP2の認識配列YRSLを構成する。このチロシンがリン酸化された状態ではAP2に認識されないが、チロシンが脱リン酸化されたL1はAP2に認識されてクラスリン依存性エンドサイト−シス経路により細胞内へ取り込まれる<ref><pubmed> 12082080 </pubmed></ref>。取り込まれたL1は細胞内小胞輸送を経てエキソサイトーシスされる。L1のエンドサイト−シスとエキソサイトーシスは、細胞接着を空間的に制御して細胞移動に重要な役割を担う。L1は、アンキリンやERMなどの分子を介して[[アクチン]]骨格と結合し、神経突起が伸長するための駆動力を伝達する。タンパク質分解酵素[[ADAM]](a disintegrin and metalloprotease)はL1細胞外領域を細胞膜近傍で切断し、遊離したL1細胞外領域は隣接細胞あるいは同一細胞のインテグリンに結合して細胞移動を促進する。また、ADAMによるプロテオリシスに続き、[[γ-セクレターゼ]]が膜貫通領域を切断し、遊離したL1細胞内領域は[[wikipedia:JA:核|核]]内に移行して遺伝子の[[wikipedia:JA:転写|転写]]を制御する<ref><pubmed> 20237819 </pubmed></ref>。 | ||
== 遺伝子変異 == | |||
ヒトL1遺伝子はXq28に存在する。L1の遺伝子変異は、[[伴性劣性遺伝性水頭症]]と[[MASA症候群]]([[精神発達遅滞]]、[[失語症]]、[[痙性歩行]]、母指の内転屈曲)の原因となることが報告されているが、これらの疾患は連続したスペクトラムであり、[[L1症候群]]と総称される<ref><pubmed> 9530493 </pubmed></ref>。病理学的には、[[脳梁低形成]]、[[錐体路低形成]]、[[小脳虫部]]低形成を示し、特発性[[水頭症]]と比較して脳室腹腔シャント術後の予後は不良である。L1ノックアウトマウスも類似の神経発生異常を示し、L1症候群の発症機序の研究に利用されている。 | |||
== 参考文献 == | == 参考文献 == | ||
<references /> | <references /> | ||
2015年9月2日 (水) 11:17時点における版
上口 裕之
独立行政法人理化学研究所 脳科学総合研究センター
DOI:10.14931/bsd.743 原稿受付日:2012年3月5日 原稿完成日:2012年4月28日
担当編集委員:村上 富士夫(大阪大学 大学院生命機能研究科)
英語名:L1 同義語:L1CAM
分子構造
L1は、6個の免疫グロブリン様ドメインと5個のフィブロネクチンIII型様ドメインからなる細胞外領域、1回膜貫通領域および細胞内領域から構成される分子量200-220 kDaの細胞接着分子である[1]。L1遺伝子を構成する28個のエクソンのうち、2番目と27番目のエクソンが選択的スプライシングを受ける。主として、神経細胞には全長型L1が発現し、非神経細胞には両エクソン配列を含まないL1が発現する。2番目のエクソンがコードするアミノ酸配列YEGHHVはL1細胞外領域に存在し、L1同士の結合(ホモフィリック結合)および他種の接着分子との結合(ヘテロフィリック結合)を増強する[2]。27番目のエクソンがコードするアミノ酸配列RSLEはL1細胞内領域に存在し、クラスリンアダプターAP2と結合してL1のエンドサイト−シスを引き起こす[3]。L1のホモログとして、ニワトリのNgCAM、ゼブラフィッシュのL1.2、ショウジョウバエのニューログリアン、線虫のLAD-1/SAX-7などが知られている。
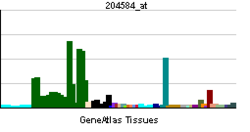
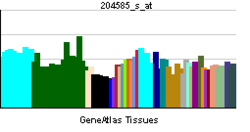
発現様式
L1は発生段階の神経組織に強く発現し、成体になると発現量は減少する。さまざまな種類の神経細胞、シュワン細胞とオリゴデンドロサイトがL1を発現する。脊髄後根神経節神経細胞では細胞体から神経突起先端部まで比較的均一に存在するが、海馬神経細胞のように極性化した細胞では、軸索遠位部から成長円錐に集積し、細胞体と樹状突起での発現は低い。したがって、神経細胞の極性化の解析において、 L1は軸索マーカーとして利用される。
結合タンパク質
L1細胞外領域は、隣接する細胞表面のL1細胞外領域と結合して細胞間接着を媒介する(ホモフィリック結合)。また、インテグリン、TAG1/アキソニン-1、F3/F11/コンタクティンなどの接着分子とのヘテロフィリック結合も報告されている [4]。軸索ガイダンス分子セマフォリンの受容体であるニューロピリン-1と同一形質膜上でヘテロ2量体を形成する。L1細胞内領域と細胞骨格を連結するタンパク質として、アンキリン、ERM(エズリン/ラディキシン/モエシン)、ダブルコルティンなどが同定されている[5]。L1細胞内領域は、非受容体型チロシンキナーゼSrc、カゼインキナーゼII、extracellular signal-regulated kinase 2 (Erk2)、p90rskなどのタンパク質リン酸化酵素と結合してリン酸化修飾を受ける。
生理機能
ホモフィリック結合とヘテロフィリック結合により細胞間接着を媒介する。またL1の接着性および細胞骨格との連結は時空間的に制御されるため、L1は単なる静的な細胞間接着だけでなく、動的な細胞間相互作用(細胞移動など)にも関与する。神経系での具体的なL1の機能として、神経細胞移動の促進、軸索伸長の促進、軸索束形成の促進、ミエリン形成の促進、シナプス可塑性の制御などが報告されている[6]。また、L1とニューロピリン-1のヘテロ2量体はセマフォリン3A受容体として機能し、軸索の反発性ガイダンスを媒介する[7]。 L1の機能は、細胞内領域のリン酸化/脱リン酸化、エンドサイト−シス/エキソサイトーシス、細胞骨格との連結、プロテオリシスなどによって制御されている。27番目のエクソンがコードするアミノ酸配列RSLEとそれに隣接するチロシン残基は、クラスリンアダプターAP2の認識配列YRSLを構成する。このチロシンがリン酸化された状態ではAP2に認識されないが、チロシンが脱リン酸化されたL1はAP2に認識されてクラスリン依存性エンドサイト−シス経路により細胞内へ取り込まれる[8]。取り込まれたL1は細胞内小胞輸送を経てエキソサイトーシスされる。L1のエンドサイト−シスとエキソサイトーシスは、細胞接着を空間的に制御して細胞移動に重要な役割を担う。L1は、アンキリンやERMなどの分子を介してアクチン骨格と結合し、神経突起が伸長するための駆動力を伝達する。タンパク質分解酵素ADAM(a disintegrin and metalloprotease)はL1細胞外領域を細胞膜近傍で切断し、遊離したL1細胞外領域は隣接細胞あるいは同一細胞のインテグリンに結合して細胞移動を促進する。また、ADAMによるプロテオリシスに続き、γ-セクレターゼが膜貫通領域を切断し、遊離したL1細胞内領域は核内に移行して遺伝子の転写を制御する[9]。
遺伝子変異
ヒトL1遺伝子はXq28に存在する。L1の遺伝子変異は、伴性劣性遺伝性水頭症とMASA症候群(精神発達遅滞、失語症、痙性歩行、母指の内転屈曲)の原因となることが報告されているが、これらの疾患は連続したスペクトラムであり、L1症候群と総称される[10]。病理学的には、脳梁低形成、錐体路低形成、小脳虫部低形成を示し、特発性水頭症と比較して脳室腹腔シャント術後の予後は不良である。L1ノックアウトマウスも類似の神経発生異常を示し、L1症候群の発症機序の研究に利用されている。
参考文献
- ↑
Moos, M., Tacke, R., Scherer, H., Teplow, D., Früh, K., & Schachner, M. (1988).
Neural adhesion molecule L1 as a member of the immunoglobulin superfamily with binding domains similar to fibronectin. Nature, 334(6184), 701-3. [PubMed:3412448] [WorldCat] [DOI] - ↑
De Angelis, E., Brummendorf, T., Cheng, L., Lemmon, V., & Kenwrick, S. (2001).
Alternative use of a mini exon of the L1 gene affects L1 binding to neural ligands. The Journal of biological chemistry, 276(35), 32738-42. [PubMed:11435440] [WorldCat] [DOI] - ↑
Kamiguchi, H., Long, K.E., Pendergast, M., Schaefer, A.W., Rapoport, I., Kirchhausen, T., & Lemmon, V. (1998).
The neural cell adhesion molecule L1 interacts with the AP-2 adaptor and is endocytosed via the clathrin-mediated pathway. The Journal of neuroscience : the official journal of the Society for Neuroscience, 18(14), 5311-21. [PubMed:9651214] [PMC] [WorldCat] - ↑
Haspel, J., & Grumet, M. (2003).
The L1CAM extracellular region: a multi-domain protein with modular and cooperative binding modes. Frontiers in bioscience : a journal and virtual library, 8, s1210-25. [PubMed:12957823] [WorldCat] [DOI] - ↑
Maness, P.F., & Schachner, M. (2007).
Neural recognition molecules of the immunoglobulin superfamily: signaling transducers of axon guidance and neuronal migration. Nature neuroscience, 10(1), 19-26. [PubMed:17189949] [WorldCat] [DOI] - ↑
Maness, P.F., & Schachner, M. (2007).
Neural recognition molecules of the immunoglobulin superfamily: signaling transducers of axon guidance and neuronal migration. Nature neuroscience, 10(1), 19-26. [PubMed:17189949] [WorldCat] [DOI] - ↑
Castellani, V., De Angelis, E., Kenwrick, S., & Rougon, G. (2002).
Cis and trans interactions of L1 with neuropilin-1 control axonal responses to semaphorin 3A. The EMBO journal, 21(23), 6348-57. [PubMed:12456642] [PMC] [WorldCat] [DOI] - ↑
Schaefer, A.W., Kamei, Y., Kamiguchi, H., Wong, E.V., Rapoport, I., Kirchhausen, T., ..., & Lemmon, V. (2002).
L1 endocytosis is controlled by a phosphorylation-dephosphorylation cycle stimulated by outside-in signaling by L1. The Journal of cell biology, 157(7), 1223-32. [PubMed:12082080] [PMC] [WorldCat] [DOI] - ↑
Schäfer, M.K., & Altevogt, P. (2010).
L1CAM malfunction in the nervous system and human carcinomas. Cellular and molecular life sciences : CMLS, 67(14), 2425-37. [PubMed:20237819] [WorldCat] [DOI] - ↑
Kamiguchi, H., Hlavin, M.L., Yamasaki, M., & Lemmon, V. (1998).
Adhesion molecules and inherited diseases of the human nervous system. Annual review of neuroscience, 21, 97-125. [PubMed:9530493] [WorldCat] [DOI]