シナプス前終末
英語名;presynaptic terminal
神経細胞の軸索の先端は、他の細胞と接触してシナプスを形成する。軸索終末のシナプス結合部はやや膨大しており、これをシナプス前終末 (presynaptic terminal)と呼ぶ。シナプス前終末には神経伝達物質を貯蔵しているシナプス小胞、伝達物質の放出にかかわるSNAREタンパク質、電位依存性のカルシウムチャネル、神経伝達物質を回収するためのトランスポーター等が存在する。こうした分子の働きにより、シナプス前終末に活動電位が到達すると、神経伝達物質が放出される。
概要
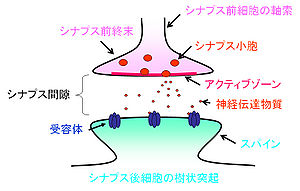
神経細胞はシナプスという構造を介して情報の伝達を行っている[1]。神経細胞は情報を受容する細胞体と樹状突起、情報を出力する軸索から成る。軸索のシナプス結合部はやや膨大しており、シナプス前終末(presynaptic terminal)と呼ばれる。グルタミン酸を神経伝達物質とする興奮性シナプスでは、シナプス前終末からシナプス後細胞の樹状突起上のスパインへ情報が伝えられる(図1)。一方、GABAを伝達物質とする抑制性シナプス前終末は、樹状突起の幹および細胞体に接合する。シナプス前細胞と後細胞の間にはシナプス間隙(20nm)があり、情報伝達の場を形成している。その中には数百のシナプス小胞(50nm)が存在する。シナプス小胞がシナプス前終末の細胞膜と融合し、その中の神経伝達物質を開口放出(エクソサイトーシス;exocytosis)する領域はアクティブゾーンと呼ばれる。アクティブゾーンは5-20μm2の広さで、膜が肥厚しているように見え、5-10個のシナプス小胞が結合している。
伝達物質放出とその制御
シナプス小胞は、小胞膜上のトランスポーターのはたらきで神経伝達物質を内部に取り込む。まず液胞型プロトンポンプが小胞内を酸性にし、膜を介した電気化学的な勾配を作る。これが伝達物質取り込みのためのエネルギー源となり、選択的トランスポーターにより伝達物質は内部に取り込まれる。そして、神経伝達物質が詰め込まれた小胞はアクティブゾーンに移動し、細胞膜に結合した状態になる(docking)。次に、結合したシナプス小胞は、カルシウム依存的に細胞膜と融合できる状態になる(priming)。そして、シナプス前細胞の細胞体からシナプス前終末へ活動電位が到達すると、膜電位が脱分極して電位依存性カルシウムチャネルが開き、シナプス前終末内へカルシウムイオンが流入し、それが引き金となってシナプス小胞内の神経伝達物質が開口放出される。シナプス前終末には複数種の電位依存性カルシウムチャネルが集積している。P/Q(Cav2.1)、N(Cav2.2)、R(Cav2.3)タイプのカルシウムチャネルがシナプス伝達に寄与すると考えられている[2]。しかし、シナプスによって各カルシウムチャネルのシナプス伝達への寄与率は異なり、また発生に伴って変化する[3]。シナプス前終末内に流入したカルシウムイオンは、シナプス小胞膜上のカルシウム作動性タンパク質であるシナプトタグミンに結合する。そしてシナプトタグミンの構造変化が、アクティブゾーンに接しているシナプス小胞の膜融合を促し、シナプス小胞内の神経伝達物質がシナプス間隙へ開口放出されると考えられている。その後、神経伝達物質は拡散によりシナプス後部にある受容体に到達して結合し、情報が伝達される。開口放出により細胞膜へ移行したシナプ
ス小胞膜は、その後エンドサイトーシスによりシナプス前終末に取り込まれ、シナプス小胞として再利用される。また、シナプス間隙に残存する神経伝達物質は、高親和性の細胞膜トランスポーターによりシナプス前終末へ再取り込みされる。そして、シナプス前終末に取り込まれた神経伝達物質は、低親和性の小胞型トランスポーターによりシナプス小胞に充填される。グルタミン酸およびGABAの小胞型トランスポーターであるvglut、vgatが各々のシナプス小胞膜に局在している。神経伝達物質のシナプス小胞内への輸送は、小胞膜上のプロトンATPase (V-ATPase)によって形成されるプロトン電気化学勾配によって駆動される[4]。また、アクティブゾーン特異的蛋白質として、RIM1(Rab3-interacting molecules 1), Munc13等が知られている。Munc13はシナプス小胞のprimingに関与し、カルシウムイオンとRIM1によって制御を受ける。RIM1は、アクティブゾーンに存在する他の多くのタンパク質とも直接あるいは間接的に結合し、アクティブゾーンの形成や機能において重要な役割を担っている[5]。
なおシナプス伝達は、シナプス前終末に存在する種々の受容体によって制御を受ける。シナプス前終末にある受容体は他のシナプスからの入力によって制御を受ける。また、シナプス後細胞から放出されるエンドカンナビノイド等の逆行性伝達物質によっても制御される[6]。
SNARE仮説
N-ethylmaleimide-sensitive fusion protein (NSF)とsoluble NSF attachment protein (SNAP)は、ゴルジ体膜間の小胞輸送に必須な細胞質タンパク質である。これらのタンパク質は、2つの対峙した生体膜上に存在する受容体であるSNARE(SNAP receptor)タンパク質と相互作用することで、膜の融合を促すと考えられた。SNAREタンパク質は、融合する双方の膜表面に分かれた形で存在し、複合体を形成することによって膜間の距離を縮め、その結果として膜融合が引き起こされるというのがSNARE仮説である。一方を小胞、他方を細胞膜と想定し、それらの膜に存在するSNAREタンパク質は、各々v-SNARE、t-SNAREと名づけられた。シナプス前終末においては、シナプス小胞上のシナプトブレビン(VAMP; vesicle-associated membrane protein)がv-SNAREであり、アクティブゾーン細胞膜にあるシンタキシンとSNAP-25(synaptosomal associated protein-25)がt-SNAREに相当する[7]。SNARE複合体が、シナプスでの開口放出に中心的かつ必須な役割を果たすが、個々のSNAREタンパク質やSNARE複合体に相互作用するさまざまなタンパク質群が、いかに開口放出の時間的空間的制御に関わっているのかはまだよくわからない。前述したシナプス小胞上のシナプトタグミンは、エキソサイトーシスのカルシウムセンサーとしてはたらいて開口放出を制御するが、そのメカニズムは明確ではない[8]。
- ↑ D Purves, GJ Augustine, D Fitzpatrick, WC Hall, AS LaMantia, JO McNamara, and LE White
Neuroscience Fourth Edition
Sinauer:2011 - ↑
Catterall, W.A., & Few, A.P. (2008).
Calcium channel regulation and presynaptic plasticity. Neuron, 59(6), 882-901. [PubMed:18817729] [WorldCat] [DOI] - ↑
Iwasaki, S., Momiyama, A., Uchitel, O.D., & Takahashi, T. (2000).
Developmental changes in calcium channel types mediating central synaptic transmission. The Journal of neuroscience : the official journal of the Society for Neuroscience, 20(1), 59-65. [PubMed:10627581] [PMC] [WorldCat] - ↑
Omote, H., Miyaji, T., Juge, N., & Moriyama, Y. (2011).
Vesicular neurotransmitter transporter: bioenergetics and regulation of glutamate transport. Biochemistry, 50(25), 5558-65. [PubMed:21612282] [WorldCat] [DOI] - ↑
Südhof, T.C., & Rizo, J. (2011).
Synaptic vesicle exocytosis. Cold Spring Harbor perspectives in biology, 3(12). [PubMed:22026965] [PMC] [WorldCat] [DOI] - ↑
Regehr, W.G., Carey, M.R., & Best, A.R. (2009).
Activity-dependent regulation of synapses by retrograde messengers. Neuron, 63(2), 154-70. [PubMed:19640475] [PMC] [WorldCat] [DOI] - ↑
Lin, R.C., & Scheller, R.H. (2000).
Mechanisms of synaptic vesicle exocytosis. Annual review of cell and developmental biology, 16, 19-49. [PubMed:11031229] [WorldCat] [DOI] - ↑
Kochubey, O., Lou, X., & Schneggenburger, R. (2011).
Regulation of transmitter release by Ca(2+) and synaptotagmin: insights from a large CNS synapse. Trends in neurosciences, 34(5), 237-46. [PubMed:21439657] [WorldCat] [DOI]