SNARE複合体
英語名:soluble NSF attachment protein receptor complex, SNARE complex
細胞内小胞輸送や開口分泌が起こるためには、輸送小胞膜やシナプス小胞膜と標的となる生体膜との融合が起こることが不可欠である。SNAREタンパク質は、これらの膜融合を誘発する役割を担うタンパク質で、小胞膜にあるv-SNAREと標的膜にあるt-SNAREとが、分子内にあるSNAREモチーフを介して会合しSNARE複合体を形成することで膜融合が引き起こされる。シナプス小胞に貯蔵される神経伝達物質の放出にもSNAREタンパク質が関与しているが、神経終末への活動電位の到達後数ミリ秒以内に素早く放出するため、シナプスでのSNARE複合体形成は様々なタンパク質によって巧みに制御されている。シナプス前膜に融合したシナプス小胞膜はエンドサイトーシスによって回収され再びシナプス小胞が作られ、そのためにはSNARE複合体を解離させる必要がある。吸エルゴン反応であるSNARE複合体の解離に必要な自由エネルギーはNSFと呼ばれるATPaseがATPを加水分解することで供給される。SNAREタンパク質は4つの主サブファミリーから構成されるファミリータンパク質で、異なる組み合わせのSNAREタンパク質が様々な細胞内小胞輸送系に関わっている。さらにSNAREタンパク質は開口放出による細胞膜タンパク質の細胞膜への組み込みや、細胞膜の伸長などにも関与している。
イントロダクション
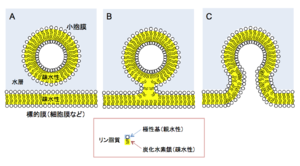
A. 標的膜への小胞膜の接近。2つの脂質膜のリン脂質の混ざり合いは起こっていない。
B. へミフュージョン。小胞膜の外側のリン脂質が標的膜のリン脂質と融合し、小胞膜と標的膜の疎水性部位(黄色で表示)が、水層を超えて連絡している。
C. フュージョン。2つの脂質膜が完全に融合している。
[1]より改変
神経伝達物質や水溶性ホルモンの分泌は、シナプス小胞膜や分泌小胞膜が細胞膜と融合する開口放出機構によって営まれている。さらに小胞体からゴルジ体を含むさまざまな細胞内小器官への膜タンパク質輸送は、送り手の膜から出芽した輸送小胞が標的の生体膜に融合する細胞内小胞輸送機構によって営まれている。これらの過程では小胞膜が標的の生体膜と融合するステップが必須である。
細胞膜や細胞内膜は脂質二重層からできており、表面は親水性であるリン脂質の極性部分が被い、膜の内部には疎水性の炭化水素の尾の部分が並んでいる(図1)。小胞膜と標的の生体膜が融合するためには、二つの膜の疎水性部分が水層を超えて連絡するヘミフュージョン状態をとる必要があり、そのためには2つの膜が非常に接近する必要がある。しかしリン脂質の親水性の頭部には水分子が水和しており、2つの脂質膜は2.5Å以内に接近することは通常では困難である。このため脂質膜の融合が起こるためには、タンパク質の助けが必要となるが、その役割を担うタンパク質がSNAREタンパク質と呼ばれる一群のタンパク質である。
Chinese Hamster Ovary(CHO)細胞を用いた研究から、細胞内小胞輸送に必須なタンパク質としてN-ethylmaleimide-sensitive factor(NSF)とSoluble NSF Attachment Protein(SNAP)が特定された[2]。脳からNSF/αSNAP複合体に結合するタンパク質としてシンタキシン1(syntaxin 1)、SNAP-25およびシナプトブレビン2(VAMP-2とも呼ばれる)が同定され、SNAP REceptor(SNARE)と総称された[3]。リコンビナントタンパク質や脳から調整された内在性のタンパク質を用いた免疫沈降法などで、シンタキシン1、 SNAP-25およびシナプトブレビン2が複合体を形成することが示された[4] [5]。X線解析やNMR解析の結果、SNAREタンパク質はSNAREモチーフを持つ4本のへリックスからなるコイルドコイル複合体を形成することが示された[6]。
シンタキシン1 、SNAP-25、シナプトブレビン2のノックアウトマウスでは開口放出による同期した神経伝達物質放出が見られないことや[7] [8] [9]、タイプ特異的にSNAREタンパク質を切断する破傷風毒素やボツリヌス毒素を作用させると、神経伝達物質放出が抑制されること[10]、リポソームにSNAREタンパク質を組み込むとリポソーム同士の融合が引き起こされることなどから[11] [12]、SNARE複合体の形成が脂質膜の融合を引き起こすと考えられるようになった[13] [14] [15]。
SNAREタンパク質は多くのメンバーを持つファミリータンパク質で、細胞膜での開口放出のみならず、様々な細胞内小胞輸送に関わっている[5] [16]。更に細胞膜へのタンパク質の組み込みや[17]、細胞の大きさや形態変化に伴う細胞膜の伸展などにもSNAREタンパク質が関わっていることも明らかにされている[18]。
特徴
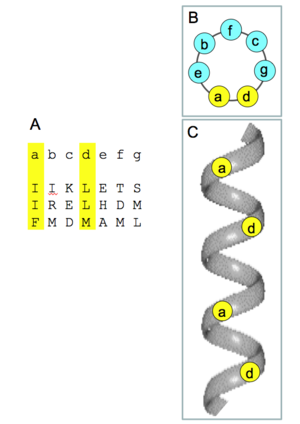
A. Heptad repeatモチーフを持つポリペプチド鎖のアミノ酸配列を、7残基ごとに改行してアミノ酸の1文字表記で表したもの。7アミノ酸をa~gとした場合、a位とd位に疎水性のアミノ酸が配置されている。
B. Heptad repeatモチーフを持つポリペプチド鎖が3.5アミノ酸残基で一回転するへリックス構造をとった場合のa~gアミノ酸の位置をへリックスの上から見たもの。
C. 同じく横から見たもの。疎水性のa位とd位のアミノ酸(黄色で示してある)が、へリックスの片面に集まって配置される。
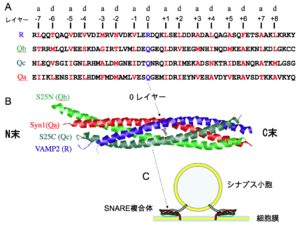
A. シナプトブレビン(R)、シンタキシン1A(Qa)SNAP-25のN末側(Qb)およびSNAP-25のC末側(Qc)のSNAREモチーフのアミノ酸の一次配列。N末端を左にして、アミノ酸の1文字表記で示してある。Heptad repeatのa位およびd位のアミノ酸を赤字で示してある。SNAREモチーフの中央付近にはd位のアミノ酸に親水性のアルギニン(R)あるいはグルタミン(Q)が配置された箇所があり、これらのアミノ酸側鎖が作るレイヤーを0レイヤーと呼んでいる。0レイヤーを中心に、各レイヤーには-7~-1および+1~+8の番号が振られている。
B. X線結晶解析で明らかにされたSNARE複合体の構造。シンタキシン1(赤, Syn1)、SNAP-25(緑, S25NおよびS25C)、シナプトブレビン2(青, VAMP2)のSNAREモチーフを含む領域を、N末端が左手に来るようにカートゥーンモデルで示し、0レイヤーのアミノ酸側鎖のみを球棒モデルで示してある。
C. SNARE複合体が形成されたシナプス小胞と細胞膜の模式図。
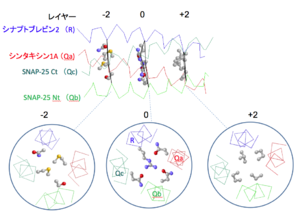
A. シナプスのSNARE複合体の0レイヤー、-2レイヤー、+2レイヤーのレイヤー面のアミノ酸側鎖を棒球モデルで示してある。上図はSNARE複合体を側面から、下図は真横から見たもので、ポリペプチド主鎖はバックボーンモデルで示してある。棒球モデルの赤色、青色、黄色および灰色の球は、それぞれ酸素、窒素、硫黄、および炭素原子を表している。
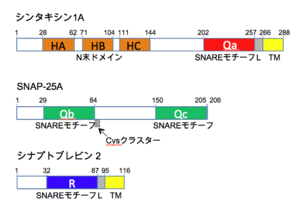
シナプス小胞の開口放出に関わるSNAREタンパク質であるシンタキシン1A, SNAP-25およびシナプトブレビン2の分子構造。N末端が左側に来るように表示してある。シンタキシン1AのN末端側には、HA、HB、HCの3つのへリックスからなるN末ドメインが、C末端側にはSNAREモチーフが存在する。カルボキシ末端には20残基以上の疎水性アミノ酸が連なる膜貫通領域(TM)が存在し、リンカ―(L)によってSNAREモチーフと結ばれている。SNAP-25にはN末側とC末側の2か所にSNAREモチーフが存在する。SNAP-25は膜貫通領域を持たないが、分子の中央付近にあるパルミトイル化されたシステイン残基のクラスターを介して細胞膜に係留されている。シナプトブレビン2にはSNAREモチーフが1か所存在し、カルボキシ末端にある膜貫通領域とリンカ―で結ばれている。
SNAREタンパク質は概してアミノ酸100~300位からなる小さなタンパク質で、分子内に約60アミノ酸からなるSNAREモチーフを持っている。SNAREモチーフにはheptad repeatと呼ばれる7アミノ酸の繰り返し構造がある(図2)。Heptad repeatを構成する7つのアミノ酸残基をa~gとした時、aとdの位置にはロイシン、イソロイシン、バリンなどの疎水性アミノ酸が、他の部位には主に親水性アミノ酸が配置されている。Heptad repeatを持つポリペプチド鎖がヘリックス構造を取ると、へリックスの片側に疎水性残基が帯状に連なるため、heptad repeatを持つ他のへリックスと疎水性面を介して会合しコイルドコイル複合体を作る。
シナプス膜での開口放出に関わるSNAREタンパク質であるシンタキシン1はイソロイシン202 –チロシン257、シナプトブレビン2はロイシン32 –リシン87、SNAP-25はトレオニン29 –フェニルアラニン84およびロイシン150 –セリン205の2か所にSNAREモチーフが存在し、それぞれheptad repeat が8回繰り返されている。SNAREタンパク質はSNAREモチーフを介して会合し、4本のへリックスからなるヘテロ複合体であるSNARE複合体を形成する[6](図3)。
SNAREモチーフではaおよびdの位置にくるアミノ酸側鎖は複合体の内側に向いており、疎水性結合で結ばれたレイヤー面を構成する(図4)。SNAREモチーフではaとdの位置にロイシン、イソロイシン、バリン以外の残基も見られ、フェニルアラニンのようにかさばる残基がくる場合には、同じレイヤー面の他のへリックスではアラニンになる。SNAREモチーフではモチーフの中央付近にある4つ目のheptad repeatのd位は正電荷をもつアルギニンか親水性のグルタミンであるという顕著な特徴を持っており、これらの残基を含む面を0レイヤーと呼んでいる。0レイヤーにアルギニン(R)を供出するSNAREをR-SNAREと呼び、グルタミン(Q)を供出するSNAREをQ-SNAREと呼んでいる。シナプス膜ではシナプトブレビン2がR-SNAREで、シンタキシン1とSNAP-25の二つのSNAREモチーフがQ-SNAREである。SNARE複合体ではSNAREモチーフを持つ4つのへリックスのN末端が同じ方向に向くように配置されている(図3)。
シナプトブレビン2とシンタキシン1を含む多くのSNAREタンパク質はC末に膜貫通へリックスを持ち脂質膜に組み込まれている。それに対してSNAP-25は膜貫通部位を持たないが、分子の中央付近にパルミトイル化されたシステイン残基クラスターを持ち、細胞膜に係留されている[19](図5)。
SNAREタンパク質の種類
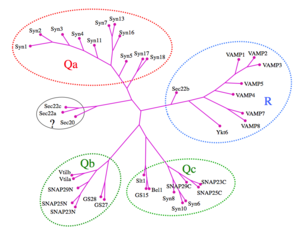
ヒトのSNAREタンパク質をSNAREモチーフのアミノ酸配列の近縁性を基に作成した。Qa、Qb、Qc、Rの主要なグループに分類され、SNARE複合体の形成に際しては、各グループから一つずつSNAREモチーフが供出される。
[5]より改変
小胞体で作られた膜タンパク質は、細胞内小胞輸送機構で細胞膜やゴルジ体をはじめとする様々な細胞内小器官に輸送されていく。これらのタンパク質輸送には送り手の膜から出芽した輸送小胞が標的の膜に融合する細胞内小胞輸送機構によって営まれており、全ての膜融合にSNAREタンパク質が関わっている。小胞膜のSNAREをv-SNARE、融合する標的膜のSNAREをt-SNAREと呼ぶが、シナプスではシナプス小胞にあるシナプトブレビン2がv-SNAREとして、シナプス前膜にあるシンタキシン1とSNAP-25がt-SNAREとして機能している。
哺乳類ではこれまでに40種類近いSNAREタンパク質が見出されており、SNAREモチーフのアミノ酸配列の類似性を基に系統樹が作られている[5](図6)。様々な生体膜間での小胞輸送には、それぞれ特有のSNAREタンパク質の組み合わせが関与している[5] [16]。
小胞輸送の素過程
標的の脂質膜に接近した輸送小胞が、標的膜に接触してから膜融合を起こすまでにはいくつかの素過程を経由する。接近してきた小胞膜が標的の膜にゆるく結合する状態をtethering(係留)、強固に結合した状態をdocking(結合)、膜融合が可能になった状態をpriming(プライミング)、2つの脂質膜が融合する過程をfusionと呼んでいる。それぞれのステップにSNAREタンパク質の関与が示唆されているが、どのように寄与しているかは必ずしも明確にはされていない。
SNARE複合体形成の制御
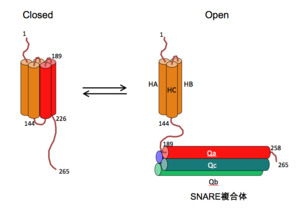
シンタキシン1の細胞内領域には、HA、HBおよびHCへリックスから構成されるN末側のN末ドメインとC末側のSNAREモチーフが存在する。シンタキシン1はN末ドメインにSNAREモチーフの一部が結合したclosed conformationとN末ドメインと、SNAREモチーフが解離したopen conformationをとり得る。Open conformationのシンタキシン1は、SNAP-25やシナプトブレビン2と会合しSNARE複合体を形成できるが、closed conformationのシンタキシン1はSNARE複合体を形成できない。Munc18はclosed conformationのシンタキシン1に結合し安定化させることによりSNARE複合体形成を抑制する。Munc13には二つのコンフォメーションの平衡をopen conformation側にずらす作用があり、SNARE複合体形成を促進させるプライミング因子である。
[20]より改変
細胞膜に存在するシンタキシン1の細胞質部分は、HA、HBおよびHCの3つのへリックス構造をとり得るN末ドメイン(27-146)と、C末側のSNAREモチーフを持つH3ドメインから構成されている(図5)。HA、HB、HCの3つのへリックスは交互に折りたたまれたHabc 3-helical bundleを形成し、SNARE複合体形成制御に関わっている[21]。
シンタキシン1はHabc 3-helical bundle にシンタキシン1のSNAREモチーフが結合したclosed conformation と、Habc 3-helical bundle とSNAREモチーフが解離したopen conformation とをとる[20] [22] [23](図7)。Open conformationにあるSNAREモチーフは、SNAP-25およびシナプトブレビン2のSNAREモチーフと結合しSNARE複合体を形成できるが、closed conformationをとるシンタキシン1は、N末ドメインがSNAREモチーフを持つH3に結合してシナプトブレビン2との結合を抑制するためSNARE複合体を形成することができない。
Munc18は68 kDaのタンパク質でclosed conformationにあるシンタキシン1に結合し安定化させることで、SNARE複合体形成に抑制的な制御因子として働いている[20] [24]。Munc18には、このような抑制的な機能の他に、SNARE複合体の会合解離サイクルの全体でSNARE複合体に常に結合し、開口放出に必須な役割も果たしているが、その詳細は明らかにはなっていない[25] [26] [27]。
SNARE複合体形成とクランプ
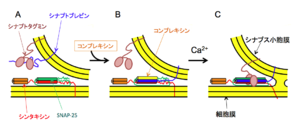
シンタキシン/SNAP-25複合体にコンプレキシンが作用すると(A)、シナプトブレビン2との複合体形成が促進されるが、N末端側から始まるSNARE複合体形成は0-レイヤー付近で停止ししている(B, クランプ状態)。Ca2+濃度が上昇するとシナプトタグミンがコンプレキシンに代わってSNARE複合体に結合してクランプが外れ、SNARE複合体形成が最後まで進行して小胞膜と細胞膜の融合が引き起こされる。このような機構を用いることにより、Ca2+濃度上昇後数ミリ秒以内での膜融合が可能になると考えられる。
[28]より改変
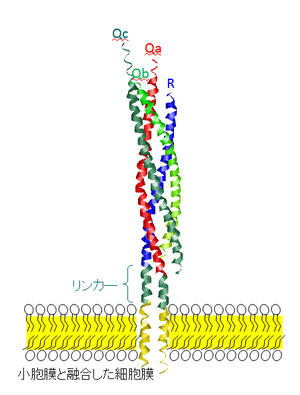
小胞膜と細胞膜が融合する前のSNARE複合体は、v-SNAREとt-SNAREは別々の生体膜に存在するtrans型であるが、融合後は同一の膜上に存在するcis型となる。細胞膜貫通領域を含めたcis-SNARE複合体では、シンタキシン1やシナプトブレビン2のSNAREモチーフのへリックス構造はリンカ―や細胞膜貫通部位にまでつながっている。このためリンカ―や細胞膜貫通部位でも、シンタキシン1のシナプトブレビン2のへリックスは側鎖を介して会合し複合体を形成し、小胞膜と細胞膜を著しく接近させることで膜融合が起こると考えられる。
[29]より改変
v-SNAREを組み込んだリポソームの平面膜への融合速度は遅く、結合してから10-100 ms後でないと起らないが、神経伝達物質放出は非常に素早く起こり、Ca2+流入後1 ms以内には完了する。このような素早い放出を可能にするためには、律速段階であるSNARE複合体形成は予めある段階まで進行させておき、Ca2+の流入に即応して素早く複合体形成が完了できる状態にしておく必要があると考えられる[22] [28] [30] [31]。
SNARE複合体形成はN末端側から始まり、ジッパーを締めるようにC末方向に進行していく。
コンプレキシン(Complexin)は134アミノ酸からなる小型のタンパク質で、分子の中央部のへリックス部位がSNARE複合体のN末側に結合しSNARE複合体形成の開始を促進する[32]。しかしコンプレキシンのN末側のへリックスはシナプトブレビン2のSNAREモチーフのC末側と拮抗しSNARE複合体形成の完了を阻害する。このためコンプレキシン存在下ではSNARE複合体形成は0レイヤー付近で停止した「クランプ」状態に止まることになり膜融合は引き起こされない[33] [34] [35]。
Ca2+濃度が高まるとシナプトタグミン(Synaptotagmin)がコンプレキシンにとって代わって結合してクランプ状態を解除し、その結果SNARE複合体形成が完了して膜融合が速やかに引き起こされる[14] [36](図8)。シナプトタグミンはCa2+依存的にリン脂質に結合するが、リポソームにシナプトタグミンを加えると、チューブ状の構造ができることから、結合した脂質2重膜の曲率を変化させる作用があると考えられる。これらのことからシナプトタグミンにはクランプ状態を解除させる機能に加え、細胞膜の曲率を局所的に変えることにより、膜融合の速度をさらに加速する機能もあると考えられる[37] [38] [39]。
膜融合
膜融合が完全に進行し、小胞膜が細胞膜に完全に組み込まれると、SNARE複合体はv-SNAREとt-SNAREが異なる膜に存在するtrans型から、同一の膜に存在するcis型に移行する(図9)。v-SNAREであるシナプトブレビン2とt-SNAREであるシンタキシンはC末端に細胞膜貫通するへリックス構造を持つが、SNAREモチーフとの間にはリンカー部分が存在する(図5)。細胞膜貫通部位を含むcis-SNARE複合体の構造がNMR構造解析で明らかにされたが、へリックス構造はSNAREモチーフのみならず、リンカー部分や膜貫通部位にまで及んでいる[29](図8)。このためt-SNAREとv-SNAREの複合体形成はSNARE複合体を超えて細胞膜貫通部位にまで及び、その結果2つの脂質膜は非常に接近させられ膜融合へと移行すると考えられる。
SNARE複合体形成は発エルゴン反応であるが、SNARE複合体形成により放出される自由エネルギーは膜融合を起こすのに十分な大きさであることが示されている[5]。膜融合が完全に進行する以前に小胞膜と細胞膜が連結すると、フュージョンポアが形成され、小胞の内容物の放出が始まる。フュージョンポアが形成されるにはSNARE複合体が完全に形成されることが必要で、フュージョンポアの形成にはシナプトブレビン2やシンタキシン1の膜貫通領域が間接的に寄与している[40] [41]。
SNARE複合体の解離
エンドサイトーシスで小胞膜タンパク質が再回収されるためには、cis-SNARE複合体が解離し、v-SNAREとt-SNAREに分離される必要がある。この変化は吸エルゴン反応であり、進行するためには自由エネルギーの供給が必要である。N-ethylmaleimide-sensitive factor(NSF)はATPase活性を持ち、ATPの加水分解エネルギーを利用してcis-SNARE複合体を解離させる。cis-SNARE複合体へのNSFの結合にはsoluble N-ethylmaleimide-sensitive factor attachment protein(αSNAP)と呼ばれるタンパク質が必要である。cis-SNARE複合体に結合した3分子の αSNAPが6量体のNSFと結合し20S複合体を形成した後、ATP加水分解に伴いcis-SNARE複合体の解離が引き起こされる[2] [5] [13] [42]。
SNAREサイクルの制御タンパク質
Munc18やコンプレキシン、シナプトタグミン以外にもSNAREサイクルの制御に関わるタンパク質が知られている。Munc13はシンタキシン/Munc18-1複合体に結合し、シンタキシンのclosed conformationをopen conformationに変化させることによりSNARE複合体形成を促進するプライミング因子である[43]。シンタキシン1とSNAP-25を組み込んだリポソームはシナプトタグミンが存在すればシナプトブレビン2を組み込んだリポソームと効率的に融合する。それに対して、シンタキシンとMunc18を組み込んだリポソームがシナプトブレビン2を組み込んだリポソームと融合するにはSNAP-25とシナプトタグミン以外にMunc13が必要であることが明らかにされている[44]。シンタキシン1/SNAP-25複合体はNSF/αSNAPの作用で解離させられるが、Munc18とMunc13が存在するとNSF/αSNAPの作用を受けなくなり、SNARE複合体形成とそれに続く膜融合が効率的に進行すると考えられる。
198アミノ酸からなるタンパク質であるcysteine string protein(csp)はシャペロンタンパク質であるHsc70のコシャペロンで、DnaJファミリーに属し分子内にJドメインを有している。Cspα/Hsc70/SGT複合体はSNAP-25のミスフォールディングを抑える働きがあり、cspを欠失させるとSNAP-25のミスフォールディングが増加し、SNARE複合体量が減少する[45]。
関連語
参考文献
- ↑
Hughson, F.M. (1995).
Structural characterization of viral fusion proteins. Current biology : CB, 5(3), 265-74. [PubMed:7780737] [WorldCat] [DOI] - ↑ 2.0 2.1
Rothman, J.E. (1996).
The protein machinery of vesicle budding and fusion. Protein science : a publication of the Protein Society, 5(2), 185-94. [PubMed:8745395] [PMC] [WorldCat] [DOI] - ↑
Söllner, T., Whiteheart, S.W., Brunner, M., Erdjument-Bromage, H., Geromanos, S., Tempst, P., & Rothman, J.E. (1993).
SNAP receptors implicated in vesicle targeting and fusion. Nature, 362(6418), 318-24. [PubMed:8455717] [WorldCat] [DOI] - ↑
Jahn, R., & Scheller, R.H. (2006).
SNAREs--engines for membrane fusion. Nature reviews. Molecular cell biology, 7(9), 631-43. [PubMed:16912714] [WorldCat] [DOI] - ↑ 5.0 5.1 5.2 5.3 5.4 5.5 5.6
Hong, W. (2005).
SNAREs and traffic. Biochimica et biophysica acta, 1744(3), 493-517. [PubMed:16038056] [WorldCat] - ↑ 6.0 6.1
Sutton, R.B., Fasshauer, D., Jahn, R., & Brunger, A.T. (1998).
Crystal structure of a SNARE complex involved in synaptic exocytosis at 2.4 A resolution. Nature, 395(6700), 347-53. [PubMed:9759724] [WorldCat] [DOI] - ↑
Washbourne, P., Thompson, P.M., Carta, M., Costa, E.T., Mathews, J.R., Lopez-Benditó, G., ..., & Wilson, M.C. (2002).
Genetic ablation of the t-SNARE SNAP-25 distinguishes mechanisms of neuroexocytosis. Nature neuroscience, 5(1), 19-26. [PubMed:11753414] [WorldCat] [DOI] - ↑
Schoch, S., Deák, F., Königstorfer, A., Mozhayeva, M., Sara, Y., Südhof, T.C., & Kavalali, E.T. (2001).
SNARE function analyzed in synaptobrevin/VAMP knockout mice. Science (New York, N.Y.), 294(5544), 1117-22. [PubMed:11691998] [WorldCat] [DOI] - ↑
Mishima, T., Fujiwara, T., Sanada, M., Kofuji, T., Kanai-Azuma, M., & Akagawa, K. (2014).
Syntaxin 1B, but not syntaxin 1A, is necessary for the regulation of synaptic vesicle exocytosis and of the readily releasable pool at central synapses. PloS one, 9(2), e90004. [PubMed:24587181] [PMC] [WorldCat] [DOI] - ↑
Xu, T., Binz, T., Niemann, H., & Neher, E. (1998).
Multiple kinetic components of exocytosis distinguished by neurotoxin sensitivity. Nature neuroscience, 1(3), 192-200. [PubMed:10195143] [WorldCat] [DOI] - ↑
Weber, T., Zemelman, B.V., McNew, J.A., Westermann, B., Gmachl, M., Parlati, F., ..., & Rothman, J.E. (1998).
SNAREpins: minimal machinery for membrane fusion. Cell, 92(6), 759-72. [PubMed:9529252] [WorldCat] [DOI] - ↑
Kiessling, V., Liang, B., & Tamm, L.K. (2015).
Reconstituting SNARE-mediated membrane fusion at the single liposome level. Methods in cell biology, 128, 339-63. [PubMed:25997356] [PMC] [WorldCat] [DOI] - ↑ 13.0 13.1
Südhof, T.C., & Rothman, J.E. (2009).
Membrane fusion: grappling with SNARE and SM proteins. Science (New York, N.Y.), 323(5913), 474-7. [PubMed:19164740] [PMC] [WorldCat] [DOI] - ↑ 14.0 14.1
Südhof, T.C. (2013).
Neurotransmitter release: the last millisecond in the life of a synaptic vesicle. Neuron, 80(3), 675-90. [PubMed:24183019] [PMC] [WorldCat] [DOI] - ↑
Jahn, R., & Fasshauer, D. (2012).
Molecular machines governing exocytosis of synaptic vesicles. Nature, 490(7419), 201-7. [PubMed:23060190] [PMC] [WorldCat] [DOI] - ↑ 16.0 16.1
Fukuda, R., McNew, J.A., Weber, T., Parlati, F., Engel, T., Nickel, W., ..., & Söllner, T.H. (2000).
Functional architecture of an intracellular membrane t-SNARE. Nature, 407(6801), 198-202. [PubMed:11001059] [WorldCat] [DOI] - ↑
Jurado, S. (2014).
The dendritic SNARE fusion machinery involved in AMPARs insertion during long-term potentiation. Frontiers in cellular neuroscience, 8, 407. [PubMed:25565955] [PMC] [WorldCat] [DOI] - ↑
Nozumi, M., Togano, T., Takahashi-Niki, K., Lu, J., Honda, A., Taoka, M., ..., & Igarashi, M. (2009).
Identification of functional marker proteins in the mammalian growth cone. Proceedings of the National Academy of Sciences of the United States of America, 106(40), 17211-6. [PubMed:19805073] [PMC] [WorldCat] [DOI] - ↑
Veit, M., Söllner, T.H., & Rothman, J.E. (1996).
Multiple palmitoylation of synaptotagmin and the t-SNARE SNAP-25. FEBS letters, 385(1-2), 119-23. [PubMed:8641455] [WorldCat] [DOI] - ↑ 20.0 20.1 20.2
Dulubova, I., Sugita, S., Hill, S., Hosaka, M., Fernandez, I., Südhof, T.C., & Rizo, J. (1999).
A conformational switch in syntaxin during exocytosis: role of munc18. The EMBO journal, 18(16), 4372-82. [PubMed:10449403] [PMC] [WorldCat] [DOI] - ↑
Fernandez, I., Ubach, J., Dulubova, I., Zhang, X., Südhof, T.C., & Rizo, J. (1998).
Three-dimensional structure of an evolutionarily conserved N-terminal domain of syntaxin 1A. Cell, 94(6), 841-9. [PubMed:9753330] [WorldCat] [DOI] - ↑ 22.0 22.1
Fiebig, K.M., Rice, L.M., Pollock, E., & Brunger, A.T. (1999).
Folding intermediates of SNARE complex assembly. Nature structural biology, 6(2), 117-23. [PubMed:10048921] [WorldCat] [DOI] - ↑
Munson, M., Chen, X., Cocina, A.E., Schultz, S.M., & Hughson, F.M. (2000).
Interactions within the yeast t-SNARE Sso1p that control SNARE complex assembly. Nature structural biology, 7(10), 894-902. [PubMed:11017200] [WorldCat] [DOI] - ↑
Hata, Y., Slaughter, C.A., & Südhof, T.C. (1993).
Synaptic vesicle fusion complex contains unc-18 homologue bound to syntaxin. Nature, 366(6453), 347-51. [PubMed:8247129] [WorldCat] [DOI] - ↑
Deák, F., Xu, Y., Chang, W.P., Dulubova, I., Khvotchev, M., Liu, X., ..., & Rizo, J. (2009).
Munc18-1 binding to the neuronal SNARE complex controls synaptic vesicle priming. The Journal of cell biology, 184(5), 751-64. [PubMed:19255244] [PMC] [WorldCat] [DOI] - ↑
Shen, J., Tareste, D.C., Paumet, F., Rothman, J.E., & Melia, T.J. (2007).
Selective activation of cognate SNAREpins by Sec1/Munc18 proteins. Cell, 128(1), 183-95. [PubMed:17218264] [WorldCat] [DOI] - ↑
Gerber, S.H., Rah, J.C., Min, S.W., Liu, X., de Wit, H., Dulubova, I., ..., & Südhof, T.C. (2008).
Conformational switch of syntaxin-1 controls synaptic vesicle fusion. Science (New York, N.Y.), 321(5895), 1507-10. [PubMed:18703708] [PMC] [WorldCat] [DOI] - ↑ 28.0 28.1
Sørensen, J.B., Wiederhold, K., Müller, E.M., Milosevic, I., Nagy, G., de Groot, B.L., ..., & Fasshauer, D. (2006).
Sequential N- to C-terminal SNARE complex assembly drives priming and fusion of secretory vesicles. The EMBO journal, 25(5), 955-66. [PubMed:16498411] [PMC] [WorldCat] [DOI] - ↑ 29.0 29.1
Stein, A., Weber, G., Wahl, M.C., & Jahn, R. (2009).
Helical extension of the neuronal SNARE complex into the membrane. Nature, 460(7254), 525-8. [PubMed:19571812] [PMC] [WorldCat] [DOI] - ↑
Pobbati, A.V., Stein, A., & Fasshauer, D. (2006).
N- to C-terminal SNARE complex assembly promotes rapid membrane fusion. Science (New York, N.Y.), 313(5787), 673-6. [PubMed:16888141] [WorldCat] [DOI] - ↑
Walter, A.M., Wiederhold, K., Bruns, D., Fasshauer, D., & Sørensen, J.B. (2010).
Synaptobrevin N-terminally bound to syntaxin-SNAP-25 defines the primed vesicle state in regulated exocytosis. The Journal of cell biology, 188(3), 401-13. [PubMed:20142423] [PMC] [WorldCat] [DOI] - ↑
Chen, X., Tomchick, D.R., Kovrigin, E., Araç, D., Machius, M., Südhof, T.C., & Rizo, J. (2002).
Three-dimensional structure of the complexin/SNARE complex. Neuron, 33(3), 397-409. [PubMed:11832227] [WorldCat] [DOI] - ↑
Giraudo, C.G., Garcia-Diaz, A., Eng, W.S., Yamamoto, A., Melia, T.J., & Rothman, J.E. (2008).
Distinct domains of complexins bind SNARE complexes and clamp fusion in vitro. The Journal of biological chemistry, 283(30), 21211-9. [PubMed:18499660] [PMC] [WorldCat] [DOI] - ↑
Kümmel, D., Krishnakumar, S.S., Radoff, D.T., Li, F., Giraudo, C.G., Pincet, F., ..., & Reinisch, K.M. (2011).
Complexin cross-links prefusion SNAREs into a zigzag array. Nature structural & molecular biology, 18(8), 927-33. [PubMed:21785414] [PMC] [WorldCat] [DOI] - ↑
Maximov, A., Tang, J., Yang, X., Pang, Z.P., & Südhof, T.C. (2009).
Complexin controls the force transfer from SNARE complexes to membranes in fusion. Science (New York, N.Y.), 323(5913), 516-21. [PubMed:19164751] [PMC] [WorldCat] [DOI] - ↑
Krishnakumar, S.S., Radoff, D.T., Kümmel, D., Giraudo, C.G., Li, F., Khandan, L., ..., & Rothman, J.E. (2011).
A conformational switch in complexin is required for synaptotagmin to trigger synaptic fusion. Nature structural & molecular biology, 18(8), 934-40. [PubMed:21785412] [PMC] [WorldCat] [DOI] - ↑
Martens, S., Kozlov, M.M., & McMahon, H.T. (2007).
How synaptotagmin promotes membrane fusion. Science (New York, N.Y.), 316(5828), 1205-8. [PubMed:17478680] [WorldCat] [DOI] - ↑
McMahon, H.T., Kozlov, M.M., & Martens, S. (2010).
Membrane curvature in synaptic vesicle fusion and beyond. Cell, 140(5), 601-5. [PubMed:20211126] [WorldCat] [DOI] - ↑
Hui, E., Johnson, C.P., Yao, J., Dunning, F.M., & Chapman, E.R. (2009).
Synaptotagmin-mediated bending of the target membrane is a critical step in Ca(2+)-regulated fusion. Cell, 138(4), 709-21. [PubMed:19703397] [PMC] [WorldCat] [DOI] - ↑
Fang, Q., & Lindau, M. (2014).
How could SNARE proteins open a fusion pore? Physiology (Bethesda, Md.), 29(4), 278-85. [PubMed:24985331] [PMC] [WorldCat] [DOI] - ↑
Han, X., Wang, C.T., Bai, J., Chapman, E.R., & Jackson, M.B. (2004).
Transmembrane segments of syntaxin line the fusion pore of Ca2+-triggered exocytosis. Science (New York, N.Y.), 304(5668), 289-92. [PubMed:15016962] [WorldCat] [DOI] - ↑
Zhao, M., Wu, S., Zhou, Q., Vivona, S., Cipriano, D.J., Cheng, Y., & Brunger, A.T. (2015).
Mechanistic insights into the recycling machine of the SNARE complex. Nature, 518(7537), 61-7. [PubMed:25581794] [PMC] [WorldCat] [DOI] - ↑
Ma, C., Li, W., Xu, Y., & Rizo, J. (2011).
Munc13 mediates the transition from the closed syntaxin-Munc18 complex to the SNARE complex. Nature structural & molecular biology, 18(5), 542-9. [PubMed:21499244] [PMC] [WorldCat] [DOI] - ↑
Ma, C., Su, L., Seven, A.B., Xu, Y., & Rizo, J. (2013).
Reconstitution of the vital functions of Munc18 and Munc13 in neurotransmitter release. Science (New York, N.Y.), 339(6118), 421-5. [PubMed:23258414] [PMC] [WorldCat] [DOI] - ↑
Sharma, M., Burré, J., & Südhof, T.C. (2011).
CSPα promotes SNARE-complex assembly by chaperoning SNAP-25 during synaptic activity. Nature cell biology, 13(1), 30-9. [PubMed:21151134] [WorldCat] [DOI]