抑制性シナプス
中畑 義久、稲田 浩之、加藤 剛、鍋倉 淳一
自然科学研究機構生理学研究所
DOI:10.14931/bsd.3012 原稿受付日:2012年12月20日 原稿完成日:2015年4月13日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
英:inhibitory synapse 独:hemmende Synapse 仏:synapse inhibitrice
抑制性シナプスとは、シナプス伝達によってシナプス後細胞を過分極させ、活動電位の発生を抑制するシナプス結合のことである。抑制性シナプスを形成するシナプス前細胞は、抑制性神経細胞と呼ばれる。抑制性の化学シナプスにおいては、GABAやグリシンなどの神経伝達物質を放出する抑制性神経細胞の軸索終末とシナプス後細胞が抑制性シナプスを構成する。主な抑制性シナプスは、GABA作動性シナプスとグリシン作動性シナプスであり、複数の神経伝達物質を共放出するシナプスも存在する。
基本構造
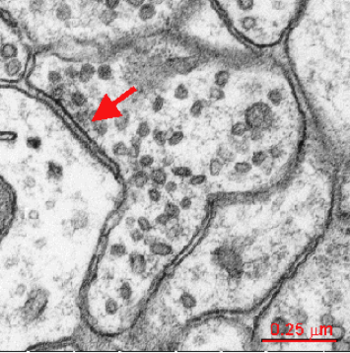
矢印はシナプス前終末側から抑制性シナプスを示している。Synapsewebより Kristen Harris博士の許可を得て転載
多くの抑制性シナプスは、形態学的分類におけるGray Ⅱ型シナプス(対称性シナプス)に相当する(図1)。抑制性シナプス前終末およびシナプス後膜を捉えた電子顕微鏡像によると、Gray I型シナプス(対称性シナプス)とは異なり顕著な電子高密度構造は認められない[1]。また、Gray I型シナプスに比べてシナプス間隙(synaptic cleft)が狭く、シナプス小胞が楕円形(扁平)である[2]。Gray II型シナプスは、主に樹状突起シャフト部や細胞体に形成されるが、棘突起(スパイン)を標的とするGABAを含んだシナプス前終末も存在する[3] [4]。
抑制性シナプスにおいても、シナプス前膜とシナプス後膜を繋ぐ接着分子が存在する。シナプス前膜にはニューレキシン(neurexin:NRXもしくはNRXN)が局在し、シナプス後膜にはニューロリギン(neuroligin:NLもしくはNLGN)が局在することが知られており、これらの接着分子の結合によってシナプスの安定化に寄与していると考えられる[5] [6]。
シナプス前部
GABA作動性シナプス
GABA作動性ニューロンには、グルタミン酸からGABAを合成するグルタミン酸脱炭酸酵素(glutamic acid decarboxylase: GAD)が存在する。GADには、GAD65とGAD67の二つのアイソフォームがあり、GABA作動性ニューロン特異的に発現している[7]。GAD65は神経終末部に限局している一方、GAD67は細胞体などにも存在し、GABA合成において主要な役割を担っている[8]。また、GAD67はパルブアルブミン陽性の介在ニューロンに強い発現がみられる[9]。合成されたGABAは、液胞型ATPアーゼ(vacuolar-type H+‐ATPase: V-ATPase)によってできるH+濃度勾配および電位勾配に従い、小胞抑制性アミノ酸輸送体(vesicular inhibitory amino acid transporter: VIAAT)注1によって、シナプス小胞に充填される[10] [11]。そして、シナプス間隙に開口放出されたGABAは、ニューロンおよびグリア細胞の細胞膜に存在するGABA輸送体(GABA transporter: GAT)によって回収される[12]。また、Gタンパク質共役型受容体であるGABAB受容体は、K+チャネルを開口させて神経終末を過分極させると共に、Ca2+チャネルを閉口させて伝達物質の放出を抑制する(以下詳述)。
グリシン作動性シナプス
グリシンはセリンヒドロキシメチルトランスフェラーゼ(serine hydroxymethyltransferase: SHMT)によってセリンから可逆的に変換される。GABA同様にグリシンも小胞抑制性アミノ酸輸送体によってシナプス小胞に充填されるが、充填効率はGABAに比べて低い[13] [14]。
シナプスに放出されたグリシンは、ニューロンとアストロサイトの細胞膜上に発現するグリシン輸送体(glycine transporter: GlyT)によって回収される[15]。グリシン輸送体の働きはNa+(ナトリウムイオン: sodium ion)とCl-(塩化物イオン: chloride ion)に依存しており、2つのアイソフォームが知られている。アストロサイト特異的に発現するGlyT1は、グリシンを細胞内外の両方向へ輸送する。一方、グリシン作動性シナプス前終末において特異的に認められる GlyT2は、細胞内外のNa+濃度勾配によって細胞外から細胞内へ一方向性の輸送を行い、シナプス小胞へのグリシン充填に不可欠である[16] [17]。
シナプス後部

(GABA:γアミノ酪酸、GAD67:グルタミン酸脱炭酸酵素67、GAD65:グルタミン酸脱炭酸酵素65、VIAAT(VGAT):小胞抑制性アミノ酸輸送体(小胞GABA輸送体)、SHMT:セリンヒドロキシメチルトランスフェラーゼ)
シナプス前終末から開口放出されたGABAやグリシンなどの神経伝達物質は、シナプス後膜に存在するGABAA受容体およびグリシン受容体に結合する(図2)。いずれも塩化物イオンチャネルに共役したイオンチャネル型受容体であり、活性化に伴って塩化物イオンの透過性(コンダクタンス)注2を上昇させる。これらは各々複数のサブタイプを持っている[18] [19]。
これらの受容体は細胞内の粗面小胞体(rER)で合成され、ゴルジ体にて分泌小胞に包まれて細胞質へ移行する[20]。そして、GABAA受容体はGABARAP(GABAA receptor-associated protein)、グリシン受容体は足場タンパク質であるゲフィリン(gephyrin)を介して順行性モータータンパク質であるキネシンスーパーファミリータンパク質(kinesin superfamily protein: KIF)に結合し、微小管(microtubule)に沿って輸送される[21] [22]。その後、受容体はエキソサイトーシス(exocytosis)によって細胞膜へ移行して側方拡散(lateral diffusion)し、ゲフィリンを介してシナプスへ集積すると考えられている[23] [24]注3。また、シナプスでは受容体の凝集するサブドメイン(ナノドメイン)を形成していることが示唆されている[25] [26]。しかし、細胞膜上の受容体は側方拡散によってシナプス内外を移動すると共に、クラスリン(clathrin)やダイナミン(dynamin)依存的なエンドサイトーシス(endocytosis)によってエンドソームに取り込まれ、細胞内へ移行する。微小管に沿った逆行性輸送はダイニン(dynein)によって行われ、リソソームでの分解、もしくは再度エキソサイトーシスされて再利用されると考えられる[20]。
また、シナプス後膜にはGタンパク質共役型受容体であるGABAB受容体も存在している。
生理機能
イオンチャネル型受容体を介した抑制機構
GABAA受容体/グリシン受容体を介した抑制
神経終末から放出されたGABAやグリシンによって、それぞれに対応したイオンチャネル型受容体であるGABAA受容体およびグリシン受容体が活性化し、受容体内部のチャネルが開口する。これによって、塩化物イオンの透過性が上昇すると、負の電荷をもつ塩化物イオンが細胞内に流入し、膜電位の過分極作用をもたらす。通常、哺乳類の成体における細胞外塩化物イオン濃度はおよそ150 mMであるのに対し、細胞内はおよそ10 mM程度である[27] [28]。そのため、通常塩化物イオンの平衡電位は-70~-80 mV付近であり、静止膜電位よりも僅かにマイナス側にある。このように、膜電位が静止電位付近の場合には電位勾配が小さく、GABAA受容体やグリシン受容体の活性化によってチャネルの透過性が上昇しても、細胞内へ塩化物イオンの大量流入は生じない。その上、短絡効果(後述)も相まって、膜電位に与える影響は比較的小さい。しかし、興奮性入力によって膜が脱分極している状況では、塩化物イオンの電位勾配が大きくなり、より多くの塩化物イオンが細胞内へ流入することから、膜電位は静止電位付近へ引き戻される。その結果、興奮性の入力によって生じた脱分極が減弱し、活動電位の発生を抑制する。
発達期および傷害回復期におけるGABA・グリシンに対する応答変化
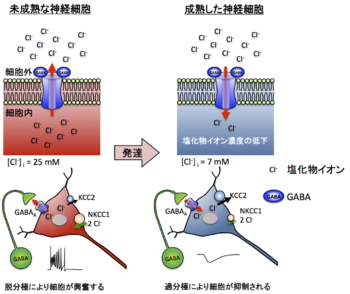
発達に伴ってNa+-K+-Cl-共輸送体1(NKCC1) による塩化物イオン(Cl-)の細胞内汲み入れが減少する一方、K+-Cl-共輸送体2(KCC2) による細胞外への汲み出しが増加する。そのため、GABAA受容体の活性化は、未成熟な神経細胞において細胞外へ塩化物イオンの流出をもたらし、脱分極応答となる。一方、成熟した神経細胞では細胞内への塩化物イオンの流入を引き起こし、過分極応答となる。([29]を改変)
GABAA受容体やグリシン受容体のチャネルを流れる塩化物イオンの向きと量は、細胞内外における塩化物イオンの濃度勾配と膜電位に依存している[30]。そのため、細胞内塩化物イオン濃度が高い状態である幼若期のニューロンでは、GABAA受容体(もしくはグリシン受容体)の活性化に伴って塩化物イオンの流出をもたらし、脱分極することも知られている[29](図3)。
こうした細胞内塩化物イオン濃度は、細胞膜上に発現するNa+-K+-Cl-共輸送体(NKCC) 、K+-Cl-共輸送体(KCC) およびCl-/HCO3-交換輸送体など、多数の塩化物イオン輸送体によって制御されている[31] [32]。NKCCは塩化物イオンを細胞内へ汲み入れ、KCCは塩化物イオンを細胞外へ汲み出す働きを担っており、これらのバランスによって細胞内の塩化物イオン濃度が決定される[33]。発達初期はKCC2に比べてNKCC1の機能発現が高く、細胞内塩化物イオン濃度が高い状態である。一方、成熟したニューロンではNKCC1に比べてKCC2の機能発現が上昇することから、細胞内塩化物イオン濃度が低い状態に保たれている[28] [29](図3)。しかし、成熟したニューロンにおいても、細胞ストレスや神経損傷を受けると、KCC2の機能が低下することから、GABAA受容体の活性化に伴って脱分極することが報告されている[34] [35] [36]。
つまり、GABAもしくはグリシン作動性入力が標的細胞に対して抑制性もしくは興奮性のいずれの作用をもたらすどうかは、標的細胞内の塩化物イオン濃度に依存している。そのため、GABAやグリシン作動性シナプスであっても、幼若期や傷害回復期においては、必ずしも抑制作用を持つシナプスではない。
短絡効果
シナプス後細胞の興奮性を抑えるメカニズムとして、短絡効果(シャント効果) も知られている[37]。抑制性入力によってGABAA受容体やグリシン受容体が活性化すると、それらのチャネルのコンダクタンスが大きくなり、膜抵抗が局所的に減少する。すると、オームの法則に従って電流の変化量に対する電位の変化量が低下する。その結果、(仮に塩化物イオンの平衡電位が静止膜電位付近のため、抑制性シナプス入力が過分極をもたらさない場合であっても、)近傍の興奮性シナプスでは興奮性シナプス後電位(EPSP)の振幅が減少し、結果としてシナプス後細胞の興奮性が抑えられる。
GABAB受容体を介した抑制機構
Gi/o共役型受容体であるGABAB受容体は、興奮性と抑制性を問わず、シナプス前終末、シナプス後膜、シナプス外領域のいずれの細胞膜にも存在しており、抑制性シナプスでは特にシナプス後膜に強い発現がみられる[38]。GABAB受容体はGタンパク質を介してK+チャネルを開口させることで、細胞膜を過分極させる。また、Gタンパク質を介して電位依存性Ca2+チャネルを閉口させる。そのため、神経終末では活動電位が到達しても伝達物質の放出が起こりにくくなり、GABA作動性神経終末においては、自ら放出したGABAによってその後の放出を抑制する自己受容体(autoreceptor)として働く。また、GABAB受容体を介した応答は、GABAA受容体やグリシン受容体などのイオンチャネル型受容体よりも遅く、長い時間スケールでの抑制作用を持つことが知られている[39]。
長期増強と長期抑圧
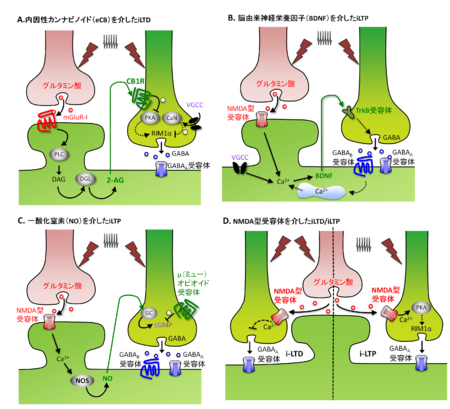
(A)内因性カンナビノイド(eCB)を介したiLTD, (B)脳由来神経栄養因子(BDNF)を介したiLTP, (C)一酸化窒素(NO)を介したiLTP, (D)前シナプスのNMDA型グルタミン酸受容体を介したiLTDおよびiLTP
(mGluR-I:グループ1代謝型グルタミン酸受容体、PLC:ホスホリパーゼC、DAG:ジアシルグリセロール、DGL:ジアシルグリセロールリパーゼ、2-AG:2-アラキドノイルグリセロール、CB1R:カンナビノイド受容体I型、VGCC:電位依存性カルシウムチャネル、PKA:プロテインキナーゼA、CaN:カルシニューリン、RIM1α:Rab3相互作用分子1α、TrkB受容体:脳由来神経栄養因子受容体、NOS:一酸化窒素合成酵素、GC:グアニル酸シクラーゼ、cGMP:環状グアノシン一リン酸)[40]を改変
長期増強(long-term potentiation:LTP)と長期抑圧(long-term depression:LTD)は、刺激の頻度とタイミングによって、その後のシナプス伝達効率の変化が長時間に渡って持続する現象である。前者は伝達効率が上昇する一方、後者は伝達効率が減少する。このLTPとLTDは興奮性シナプスにおいてよく知られているが、抑制性シナプスにおいても生じることが報告されている(iLTP/iLTD)[41] [42] [43] [44]。いずれの現象についても、前シナプスと後シナプスそれぞれにおける様々な機序によって生じることが報告されている[45]。前シナプスについては、内因性カンナビノイド(eCB)、脳由来神経栄養因子(BDNF)、一酸化窒素(NO)などの逆行性シグナルや神経前終末のNMDA型グルタミン酸受容体を介して、伝達物質の放出確率を調節するメカニズムが考えられている(図4)。
- 内因性カンナビノイドを介したiLTD(図4A)
シナプス後膜のグループI代謝型グルタミン酸受容体(mGluR-I)の活性化によって、内因性カンナビノイドである2-アラキドノイルグリセロール(2-AG)が産生、放出される。これにより抑制性シナプス前終末のカンナビノイド受容体I型(CB1R)が活性化すると、プロテインキナーゼA(PKA)活性が低下し、アクティブゾーンタンパク質であるRIM1α(Rab3相互作用分子1α)のリン酸化が減少する。同時に、細胞内カルシウム上昇によってカルシニューリン(CaN)が活性化すると、RIM1αの脱リン酸化が促進され、結果的にRIM1α依存的なGABAの放出が減弱する。
- 脳由来神経栄養因子を介したiLTP(図4B)
細胞内のカルシウムイオン濃度上昇によってシナプス後細胞から脳由来神経栄養因子が放出される。それによりシナプス前終末に発現するTrkB受容体が活性化することで、GABA放出が増加する。また、シナプス後細胞におけるGABAB受容体の活性化は、細胞内カルシウムストアからのカルシウムイオンの放出を誘導する。
- 一酸化窒素を介したiLTP(図4C)
細胞内のカルシウム濃度上昇によって一酸化窒素合成酵素(NOS)が活性化し、一酸化窒素が産生される。細胞膜を透過したNOは、シナプス前終末のグアニル酸シクラーゼ(GC)に作用して環状グアノシン一リン酸(cGMP)を増加させ、その結果GABA放出を増加させる。一方、NOによるcGMPの上昇は、μオピオイド受容体(μOR)の活性化によって阻害される。
- 前シナプスのNMDA型受容体を介したiLTDおよびiLTP(図4D)
抑制性神経前終末に発現したNMDA型グルタミン酸受容体の活性化は、細胞内カルシウム濃度を上昇させる。これによって、GABA放出の減弱(iLTD)、あるいはプロテインキナーゼA(PKA)の活性化とアクティブゾーンタンパク質であるRab3相互作用分子1α(RIM1α)のリン酸化を介してGABA放出の増強(iLTP)を誘導する。
一方、後シナプスについては、GABARAPなど受容体の輸送に関わる分子やGABAA受容体自体のリン酸化‐脱リン酸化によって、シナプスにおける受容体の数や局在、イオン透過性などの構造的・機能的修飾が生じることが報告されている[40]。また、この他にはKCC2やNKCC1などの細胞内塩化物イオン濃度調節機構への作用によって細胞内塩化物イオン濃度が変化し、その結果GABAやグリシンによる応答の振幅が変化することも示唆されている[46]。
シナプス外受容体による持続性抑制
GABAA受容体およびグリシン受容体は、シナプスに高密度で集積するだけでなく、シナプス外においても低密度で存在し、持続性抑制(tonic inhibition)に関わることが知られている[47]。こうしたシナプス外の受容体は、シナプス間隙から漏出(spillover)したリガンドや細胞外に低濃度で存在するリガンドによって活性化することで、細胞の興奮性を調節すると考えられている。そのため、脱感作しにくい特徴を持っており、δサブユニットを含むGABAA受容体など、受容体のサブユニット構成によって機能的特徴が異なると考えられる[20]。
GABAおよびグリシン作動性シナプスの相違点
GABA作動性シナプスは中枢神経系全般に広く分布し、大脳新皮質、海馬、視床、小脳などにおいて主要な抑制性伝達を担う[48]。一方、グリシン作動性シナプスは脳幹、脊髄における主要な抑制性伝達を担い、小脳や網膜においても機能している[49] [50]。また、脊髄や脳幹などでは、単一神経終末において、同一のシナプス小胞からGABAとグリシンの共放出が確認されている[51]。加えて、これらのシナプスでは未熟期においてGABA優位であった神経伝達が、発達に従ってグリシン優位に変化(スイッチング)することが知られているが[52] [53]、成熟後もGABAとグリシンの共放出が認められる[54]。
GABAA受容体およびグリシン受容体は、いずれも塩化物イオンを選択的に透過させる点で共通している。しかし、GABAA受容体を介した抑制性シナプス後電流(inhibitory post synaptic current: IPSC)は、グリシン受容体のそれに比べて減衰時間が長い[51]。また、先述の通り、GABA作動性シナプスではGABAB受容体が自己受容体として働くことも特徴的である。
電気シナプスによる抑制
上述の化学シナプスとは別に、電気シナプス(electric synapse / electrical synapse)を介した抑制も知られている。電気シナプスの場合、ギャップ結合(gap junction)を介して異なるニューロン同士の細胞質が直接連結しており、細胞間のイオンの移動が容易である。そのため、あるニューロンにおける過分極が、他のニューロンへ瞬時に伝播して過分極させる。
例えば、マウス小脳皮質に存在する抑制性ニューロンの一種であるゴルジ細胞は、互いにギャップ結合を形成して同期発火している。しかし、苔状線維から興奮性入力を受けると、直接入力を受けた細胞とその周囲の細胞の間で脱同期化が生じることが知られている[55]。これはギャップ結合を介して周囲のゴルジ細胞に後過分極(after-hyperpolarization)が伝播するためであり、ギャップ結合が抑制性の電気シナプスとして機能している例である[56]。
注釈
注1. 小胞GABA輸送体(VGAT)とも呼ばれる。
注2. チャネルの開閉に伴う細胞内外のイオンの出入りを考えるとき、しばしば「透過性(permeability)」と「コンダクタンス(conductance)」という語が使用される。前者はイオンの通りやすさを指しているのに対し、後者はイオンの電気的な伝導性を指している。
注3. ゲフィリンはグリシン受容体βサブユニットと結合し、足場タンパク質として働くことがよく知られている。しかし、GABAA受容体のサブタイプは、構成するサブユニットの種類によって非常に多様であり、ゲフィリンが足場タンパクとして働くものはそれらの一部であると考えられている[24]。
関連項目
外部リンク
- Synapseweb シナプスの電子顕微鏡解析の第一人者であるKristen Harrisのウェブページ。
参考文献
- ↑
GRAY, E.G. (1959).
Axo-somatic and axo-dendritic synapses of the cerebral cortex: an electron microscope study. Journal of anatomy, 93, 420-33. [PubMed:13829103] [PMC] [WorldCat] - ↑ E.R.Kandel, J.H.Schwartz, T.M.Jessell, S.A.Siegelbaum, & A.J.Hudspeth (Eds.)
Principles of Neural Science, Fifth Edition.
2012, McGraw-Hill Professional, New York, pp.211-4.
ISBN 978-0071390118 - ↑
Beaulieu, C., Kisvarday, Z., Somogyi, P., Cynader, M., & Cowey, A. (1992).
Quantitative distribution of GABA-immunopositive and -immunonegative neurons and synapses in the monkey striate cortex (area 17). Cerebral cortex (New York, N.Y. : 1991), 2(4), 295-309. [PubMed:1330121] [WorldCat] [DOI] - ↑
Kubota, Y., Hatada, S., Kondo, S., Karube, F., & Kawaguchi, Y. (2007).
Neocortical inhibitory terminals innervate dendritic spines targeted by thalamocortical afferents. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(5), 1139-50. [PubMed:17267569] [PMC] [WorldCat] [DOI] - ↑
Südhof, T.C. (2008).
Neuroligins and neurexins link synaptic function to cognitive disease. Nature, 455(7215), 903-11. [PubMed:18923512] [PMC] [WorldCat] [DOI] - ↑
Bang, M.L., & Owczarek, S. (2013).
A matter of balance: role of neurexin and neuroligin at the synapse. Neurochemical research, 38(6), 1174-89. [PubMed:23559421] [WorldCat] [DOI] - ↑
Dupuy, S.T., & Houser, C.R. (1996).
Prominent expression of two forms of glutamate decarboxylase in the embryonic and early postnatal rat hippocampal formation. The Journal of neuroscience : the official journal of the Society for Neuroscience, 16(21), 6919-32. [PubMed:8824330] [WorldCat] - ↑
Asada, H., Kawamura, Y., Maruyama, K., Kume, H., Ding, R.G., Kanbara, N., ..., & Obata, K. (1997).
Cleft palate and decreased brain gamma-aminobutyric acid in mice lacking the 67-kDa isoform of glutamic acid decarboxylase. Proceedings of the National Academy of Sciences of the United States of America, 94(12), 6496-9. [PubMed:9177246] [PMC] [WorldCat] [DOI] - ↑
Fukuda, T., Heizmann, C.W., & Kosaka, T. (1997).
Quantitative analysis of GAD65 and GAD67 immunoreactivities in somata of GABAergic neurons in the mouse hippocampus proper (CA1 and CA3 regions), with special reference to parvalbumin-containing neurons. Brain research, 764(1-2), 237-43. [PubMed:9295216] [WorldCat] [DOI] - ↑
Chaudhry, F.A., Reimer, R.J., Bellocchio, E.E., Danbolt, N.C., Osen, K.K., Edwards, R.H., & Storm-Mathisen, J. (1998).
The vesicular GABA transporter, VGAT, localizes to synaptic vesicles in sets of glycinergic as well as GABAergic neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 18(23), 9733-50. [PubMed:9822734] [PMC] [WorldCat] - ↑
Wojcik, S.M., Katsurabayashi, S., Guillemin, I., Friauf, E., Rosenmund, C., Brose, N., & Rhee, J.S. (2006).
A shared vesicular carrier allows synaptic corelease of GABA and glycine. Neuron, 50(4), 575-87. [PubMed:16701208] [WorldCat] [DOI] - ↑
Conti, F., Minelli, A., & Melone, M. (2004).
GABA transporters in the mammalian cerebral cortex: localization, development and pathological implications. Brain research. Brain research reviews, 45(3), 196-212. [PubMed:15210304] [DOI] - ↑
Christensen, H., Fykse, E.M., & Fonnum, F. (1991).
Inhibition of gamma-aminobutyrate and glycine uptake into synaptic vesicles. European journal of pharmacology, 207(1), 73-9. [PubMed:1915594] [WorldCat] [DOI] - ↑
McIntire, S.L., Reimer, R.J., Schuske, K., Edwards, R.H., & Jorgensen, E.M. (1997).
Identification and characterization of the vesicular GABA transporter. Nature, 389(6653), 870-6. [PubMed:9349821] [WorldCat] [DOI] - ↑
Zafra, F., & Giménez, C. (2008).
Glycine transporters and synaptic function. IUBMB life, 60(12), 810-7. [PubMed:18798526] [WorldCat] [DOI] - ↑
Gomeza, J., Ohno, K., Hülsmann, S., Armsen, W., Eulenburg, V., Richter, D.W., ..., & Betz, H. (2003).
Deletion of the mouse glycine transporter 2 results in a hyperekplexia phenotype and postnatal lethality. Neuron, 40(4), 797-806. [PubMed:14622583] [WorldCat] [DOI] - ↑
Rousseau, F., Aubrey, K.R., & Supplisson, S. (2008).
The glycine transporter GlyT2 controls the dynamics of synaptic vesicle refilling in inhibitory spinal cord neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(39), 9755-68. [PubMed:18815261] [PMC] [WorldCat] [DOI] - ↑
Macdonald, R.L., & Olsen, R.W. (1994).
GABAA receptor channels. Annual review of neuroscience, 17, 569-602. [PubMed:7516126] [WorldCat] [DOI] - ↑
Lynch, J.W. (2004).
Molecular structure and function of the glycine receptor chloride channel. Physiological reviews, 84(4), 1051-95. [PubMed:15383648] [WorldCat] [DOI] - ↑ 20.0 20.1 20.2
Jacob, T.C., Moss, S.J., & Jurd, R. (2008).
GABA(A) receptor trafficking and its role in the dynamic modulation of neuronal inhibition. Nature reviews. Neuroscience, 9(5), 331-43. [PubMed:18382465] [PMC] [WorldCat] [DOI] - ↑
Nakajima, K., Yin, X., Takei, Y., Seog, D.H., Homma, N., & Hirokawa, N. (2012).
Molecular motor KIF5A is essential for GABA(A) receptor transport, and KIF5A deletion causes epilepsy. Neuron, 76(5), 945-61. [PubMed:23217743] [WorldCat] [DOI] - ↑
Maas, C., Belgardt, D., Lee, H.K., Heisler, F.F., Lappe-Siefke, C., Magiera, M.M., ..., & Kneussel, M. (2009).
Synaptic activation modifies microtubules underlying transport of postsynaptic cargo. Proceedings of the National Academy of Sciences of the United States of America, 106(21), 8731-6. [PubMed:19439658] [PMC] [WorldCat] [DOI] - ↑
Renner, M., Specht, C.G., & Triller, A. (2008).
Molecular dynamics of postsynaptic receptors and scaffold proteins. Current opinion in neurobiology, 18(5), 532-40. [PubMed:18832033] [WorldCat] [DOI] - ↑ 24.0 24.1
Tyagarajan, S.K., & Fritschy, J.M. (2014).
Gephyrin: a master regulator of neuronal function? Nature reviews. Neuroscience, 15(3), 141-56. [PubMed:24552784] [WorldCat] [DOI] - ↑
Specht, C.G., Izeddin, I., Rodriguez, P.C., El Beheiry, M., Rostaing, P., Darzacq, X., ..., & Triller, A. (2013).
Quantitative nanoscopy of inhibitory synapses: counting gephyrin molecules and receptor binding sites. Neuron, 79(2), 308-21. [PubMed:23889935] [WorldCat] [DOI] - ↑
Choquet, D., & Triller, A. (2013).
The dynamic synapse. Neuron, 80(3), 691-703. [PubMed:24183020] [WorldCat] [DOI] - ↑
Rhee, J.S., Ebihara, S., & Akaike, N. (1994).
Gramicidin perforated patch-clamp technique reveals glycine-gated outward chloride current in dissociated nucleus solitarii neurons of the rat. Journal of neurophysiology, 72(3), 1103-8. [PubMed:7528790] [WorldCat] [DOI] - ↑ 28.0 28.1
Kakazu, Y., Akaike, N., Komiyama, S., & Nabekura, J. (1999).
Regulation of intracellular chloride by cotransporters in developing lateral superior olive neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 19(8), 2843-51. [PubMed:10191302] [PMC] [WorldCat] - ↑ 29.0 29.1 29.2
Ben-Ari, Y., Gaiarsa, J.L., Tyzio, R., & Khazipov, R. (2007).
GABA: a pioneer transmitter that excites immature neurons and generates primitive oscillations. Physiological reviews, 87(4), 1215-84. [PubMed:17928584] [WorldCat] [DOI] - ↑
Ueno, T., Okabe, A., Akaike, N., Fukuda, A., & Nabekura, J. (2002).
Diversity of neuron-specific K+-Cl- cotransporter expression and inhibitory postsynaptic potential depression in rat motoneurons. The Journal of biological chemistry, 277(7), 4945-50. [PubMed:11733521] [WorldCat] [DOI] - ↑
Price, T.J., Cervero, F., & de Koninck, Y. (2005).
Role of cation-chloride-cotransporters (CCC) in pain and hyperalgesia. Current topics in medicinal chemistry, 5(6), 547-55. [PubMed:16022677] [PMC] [WorldCat] [DOI] - ↑
Stauber, T., Weinert, S., & Jentsch, T.J. (2012).
Cell biology and physiology of CLC chloride channels and transporters. Comprehensive Physiology, 2(3), 1701-44. [PubMed:23723021] [WorldCat] [DOI] - ↑
Payne, J.A., Rivera, C., Voipio, J., & Kaila, K. (2003).
Cation-chloride co-transporters in neuronal communication, development and trauma. Trends in neurosciences, 26(4), 199-206. [PubMed:12689771] [WorldCat] [DOI] - ↑
Nabekura, J., Ueno, T., Okabe, A., Furuta, A., Iwaki, T., Shimizu-Okabe, C., ..., & Akaike, N. (2002).
Reduction of KCC2 expression and GABAA receptor-mediated excitation after in vivo axonal injury. The Journal of neuroscience : the official journal of the Society for Neuroscience, 22(11), 4412-7. [PubMed:12040048] [PMC] [WorldCat] [DOI] - ↑
Toyoda, H., Ohno, K., Yamada, J., Ikeda, M., Okabe, A., Sato, K., ..., & Fukuda, A. (2003).
Induction of NMDA and GABAA receptor-mediated Ca2+ oscillations with KCC2 mRNA downregulation in injured facial motoneurons. Journal of neurophysiology, 89(3), 1353-62. [PubMed:12612004] [WorldCat] [DOI] - ↑
Wake, H., Watanabe, M., Moorhouse, A.J., Kanematsu, T., Horibe, S., Matsukawa, N., ..., & Nabekura, J. (2007).
Early changes in KCC2 phosphorylation in response to neuronal stress result in functional downregulation. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(7), 1642-50. [PubMed:17301172] [PMC] [WorldCat] [DOI] - ↑
Staley, K.J., & Mody, I. (1992).
Shunting of excitatory input to dentate gyrus granule cells by a depolarizing GABAA receptor-mediated postsynaptic conductance. Journal of neurophysiology, 68(1), 197-212. [PubMed:1381418] [WorldCat] [DOI] - ↑
Gonchar, Y., Pang, L., Malitschek, B., Bettler, B., & Burkhalter, A. (2001).
Subcellular localization of GABA(B) receptor subunits in rat visual cortex. The Journal of comparative neurology, 431(2), 182-97. [PubMed:11169999] [WorldCat] [DOI] - ↑
Gassmann, M., & Bettler, B. (2012).
Regulation of neuronal GABA(B) receptor functions by subunit composition. Nature reviews. Neuroscience, 13(6), 380-94. [PubMed:22595784] [WorldCat] [DOI] - ↑ 40.0 40.1
Castillo, P.E., Chiu, C.Q., & Carroll, R.C. (2011).
Long-term plasticity at inhibitory synapses. Current opinion in neurobiology, 21(2), 328-38. [PubMed:21334194] [PMC] [WorldCat] [DOI] - ↑
Stelzer, A., Slater, N.T., & ten Bruggencate, G. (1987).
Activation of NMDA receptors blocks GABAergic inhibition in an in vitro model of epilepsy. Nature, 326(6114), 698-701. [PubMed:2882427] [WorldCat] [DOI] - ↑
Korn, H., Oda, Y., & Faber, D.S. (1992).
Long-term potentiation of inhibitory circuits and synapses in the central nervous system. Proceedings of the National Academy of Sciences of the United States of America, 89(1), 440-3. [PubMed:1729715] [PMC] [WorldCat] [DOI] - ↑
Kano, M., Rexhausen, U., Dreessen, J., & Konnerth, A. (1992).
Synaptic excitation produces a long-lasting rebound potentiation of inhibitory synaptic signals in cerebellar Purkinje cells. Nature, 356(6370), 601-4. [PubMed:1313949] [WorldCat] [DOI] - ↑
Komatsu, Y., & Iwakiri, M. (1993).
Long-term modification of inhibitory synaptic transmission in developing visual cortex. Neuroreport, 4(7), 907-10. [PubMed:8103683] [WorldCat] [DOI] - ↑
Gaiarsa, J.L., Caillard, O., & Ben-Ari, Y. (2002).
Long-term plasticity at GABAergic and glycinergic synapses: mechanisms and functional significance. Trends in neurosciences, 25(11), 564-70. [PubMed:12392931] [WorldCat] [DOI] - ↑
Wang, L., Kitai, S.T., & Xiang, Z. (2006).
Activity-dependent bidirectional modification of inhibitory synaptic transmission in rat subthalamic neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 26(28), 7321-7. [PubMed:16837578] [PMC] [WorldCat] [DOI] - ↑
Farrant, M., & Nusser, Z. (2005).
Variations on an inhibitory theme: phasic and tonic activation of GABA(A) receptors. Nature reviews. Neuroscience, 6(3), 215-29. [PubMed:15738957] [WorldCat] [DOI] - ↑
Pirker, S., Schwarzer, C., Wieselthaler, A., Sieghart, W., & Sperk, G. (2000).
GABA(A) receptors: immunocytochemical distribution of 13 subunits in the adult rat brain. Neuroscience, 101(4), 815-50. [PubMed:11113332] [WorldCat] [DOI] - ↑
Dieudonné, S. (1995).
Glycinergic synaptic currents in Golgi cells of the rat cerebellum. Proceedings of the National Academy of Sciences of the United States of America, 92(5), 1441-5. [PubMed:7877998] [PMC] [WorldCat] [DOI] - ↑
Kirsch, J. (2006).
Glycinergic transmission. Cell and tissue research, 326(2), 535-40. [PubMed:16807723] [WorldCat] [DOI] - ↑ 51.0 51.1
Jonas, P., Bischofberger, J., & Sandkühler, J. (1998).
Corelease of two fast neurotransmitters at a central synapse. Science (New York, N.Y.), 281(5375), 419-24. [PubMed:9665886] [WorldCat] [DOI] - ↑
Kotak, V.C., Korada, S., Schwartz, I.R., & Sanes, D.H. (1998).
A developmental shift from GABAergic to glycinergic transmission in the central auditory system. The Journal of neuroscience : the official journal of the Society for Neuroscience, 18(12), 4646-55. [PubMed:9614239] [PMC] [WorldCat] - ↑
Nabekura, J., Katsurabayashi, S., Kakazu, Y., Shibata, S., Matsubara, A., Jinno, S., ..., & Ishibashi, H. (2004).
Developmental switch from GABA to glycine release in single central synaptic terminals. Nature neuroscience, 7(1), 17-23. [PubMed:14699415] [WorldCat] [DOI] - ↑
Dufour, A., Tell, F., Kessler, J.P., & Baude, A. (2010).
Mixed GABA-glycine synapses delineate a specific topography in the nucleus tractus solitarii of adult rat. The Journal of physiology, 588(Pt 7), 1097-115. [PubMed:20156844] [PMC] [WorldCat] [DOI] - ↑
Vervaeke, K., Lorincz, A., Gleeson, P., Farinella, M., Nusser, Z., & Silver, R.A. (2010).
Rapid desynchronization of an electrically coupled interneuron network with sparse excitatory synaptic input. Neuron, 67(3), 435-51. [PubMed:20696381] [PMC] [WorldCat] [DOI] - ↑
Bennett, M.V., & Zukin, R.S. (2004).
Electrical coupling and neuronal synchronization in the Mammalian brain. Neuron, 41(4), 495-511. [PubMed:14980200] [WorldCat] [DOI]