「神経細胞リプログラミング」の版間の差分
細編集の要約なし |
|||
| (同じ利用者による、間の3版が非表示) | |||
| 1行目: | 1行目: | ||
<div align="right"> | <div align="right"> | ||
<font size="+1"> | <font size="+1">山下 徹</font><br> | ||
<font size="+1">[https://researchmap.jp/read0168070 阿部 康二]</font><br> | |||
''岡山大学大学院 医歯薬学総合研究科 脳神経内科学''<br> | ''岡山大学大学院 医歯薬学総合研究科 脳神経内科学''<br> | ||
DOI:<selfdoi /> | DOI:<selfdoi /> 原稿受付日:2020年6月29日 原稿完成日:2020年X月XX日<br> | ||
担当編集委員:[https://researchmap.jp/hiroshikawasaki 河崎 洋志](金沢大学 医学系 脳神経医学教室)<br> | 担当編集委員:[https://researchmap.jp/hiroshikawasaki 河崎 洋志](金沢大学 医学系 脳神経医学教室)<br> | ||
</div> | </div> | ||
| 10行目: | 11行目: | ||
{{box|text= 神経細胞へのリプログラミング(以下神経細胞リプログラミング)とは、本来、分化多能性を喪失している体細胞から多能性幹細胞を経ずに神経系細胞を直接誘導することを意味する。また本手法で誘導された細胞をinduced neuronal (iN)細胞と呼称する。比較的短期間で誘導可能かつ腫瘍形成リスクが低いため、ヒト疾患細胞モデルを利用した病態解明や薬剤スクリーニングならびに再生医療への応用が期待されている。}} | {{box|text= 神経細胞へのリプログラミング(以下神経細胞リプログラミング)とは、本来、分化多能性を喪失している体細胞から多能性幹細胞を経ずに神経系細胞を直接誘導することを意味する。また本手法で誘導された細胞をinduced neuronal (iN)細胞と呼称する。比較的短期間で誘導可能かつ腫瘍形成リスクが低いため、ヒト疾患細胞モデルを利用した病態解明や薬剤スクリーニングならびに再生医療への応用が期待されている。}} | ||
== | == 神経細胞リプログラミング発見の経緯 == | ||
[[ファイル:Yamashita Fig1.jpg|サムネイル|200px|'''図1. マウスiN細胞'''<br>[[樹状突起]]マーカー[[MAP2]]並びに[[カテコールアミン]]神経のマーカーである[[チロシン水酸化酵素]](TH)の染色。矢印がiN細胞の[[細胞体]]。]] | [[ファイル:Yamashita Fig1.jpg|サムネイル|200px|'''図1. マウスiN細胞'''<br>[[樹状突起]]マーカー[[MAP2]]並びに[[カテコールアミン]]神経のマーカーである[[チロシン水酸化酵素]](TH)の染色。矢印がiN細胞の[[細胞体]]。]] | ||
2006年の[[iPS細胞]]の発見により、いくつかの[[転写因子]]を強制発現することで、[[線維芽細胞]]などの[[体細胞]]から異なる細胞種を誘導できることが示された。[[ES細胞]]に強く発現し機能的に重要な[[Oct3]]/[[Oct4|4]]、[[Sox2]]、[[Klf4]]、[[c-Myc]]の4つの転写因子群を強制発現させるとES細胞に非常に類似した性質を持つiPS細胞が誘導できた事実から、神経細胞に強く発現している転写因子群を強制発現させると、直接神経細胞を誘導できるのではないかと多くの研究者達が予想したのである。 | 2006年の[[iPS細胞]]の発見により、いくつかの[[転写因子]]を強制発現することで、[[線維芽細胞]]などの[[体細胞]]から異なる細胞種を誘導できることが示された。[[ES細胞]]に強く発現し機能的に重要な[[Oct3]]/[[Oct4|4]]、[[Sox2]]、[[Klf4]]、[[c-Myc]]の4つの転写因子群を強制発現させるとES細胞に非常に類似した性質を持つiPS細胞が誘導できた事実から、神経細胞に強く発現している転写因子群を強制発現させると、直接神経細胞を誘導できるのではないかと多くの研究者達が予想したのである。 | ||
| 17行目: | 18行目: | ||
この発見を嚆矢として[[運動ニューロン]]<ref name=Son2011><pubmed>21852222</pubmed></ref> や[[ドパミン]]作動性ニューロン<ref name=Caiazzo2011><pubmed>21725324</pubmed></ref> 、[[ノルアドレナリン]]作動性ニューロン<ref name=Li2019><pubmed>31315047</pubmed></ref> 、[[神経幹細胞]]<ref name=Han2012><pubmed>22445517</pubmed></ref><ref name=Lujan2012><pubmed>22308465</pubmed></ref> など多様な神経系細胞が誘導できることがこれまでに報告されてきている'''(図1)'''。 | この発見を嚆矢として[[運動ニューロン]]<ref name=Son2011><pubmed>21852222</pubmed></ref> や[[ドパミン]]作動性ニューロン<ref name=Caiazzo2011><pubmed>21725324</pubmed></ref> 、[[ノルアドレナリン]]作動性ニューロン<ref name=Li2019><pubmed>31315047</pubmed></ref> 、[[神経幹細胞]]<ref name=Han2012><pubmed>22445517</pubmed></ref><ref name=Lujan2012><pubmed>22308465</pubmed></ref> など多様な神経系細胞が誘導できることがこれまでに報告されてきている'''(図1)'''。 | ||
== 特徴 == | == 特徴 == | ||
iN細胞は、iPS細胞の状態を介さずに直接目的である神経系細胞に分化誘導するため、①比較的短期間で誘導可能、②腫瘍化のリスクが低い点が利点である。一方、iN細胞を誘導した時点で原則[[細胞分裂]]が停止し増殖させることが出来ない点が欠点である。 | iN細胞は、iPS細胞の状態を介さずに直接目的である神経系細胞に分化誘導するため、①比較的短期間で誘導可能、②腫瘍化のリスクが低い点が利点である。一方、iN細胞を誘導した時点で原則[[細胞分裂]]が停止し増殖させることが出来ない点が欠点である。 | ||
2020年7月2日 (木) 00:39時点における版
山下 徹
阿部 康二
岡山大学大学院 医歯薬学総合研究科 脳神経内科学
DOI:10.14931/bsd.9081 原稿受付日:2020年6月29日 原稿完成日:2020年X月XX日
担当編集委員:河崎 洋志(金沢大学 医学系 脳神経医学教室)
英語名: direct reprogramming to neuronal cells
神経細胞へのリプログラミング(以下神経細胞リプログラミング)とは、本来、分化多能性を喪失している体細胞から多能性幹細胞を経ずに神経系細胞を直接誘導することを意味する。また本手法で誘導された細胞をinduced neuronal (iN)細胞と呼称する。比較的短期間で誘導可能かつ腫瘍形成リスクが低いため、ヒト疾患細胞モデルを利用した病態解明や薬剤スクリーニングならびに再生医療への応用が期待されている。
神経細胞リプログラミング発見の経緯
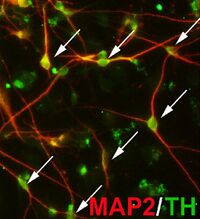
樹状突起マーカーMAP2並びにカテコールアミン神経のマーカーであるチロシン水酸化酵素(TH)の染色。矢印がiN細胞の細胞体。
2006年のiPS細胞の発見により、いくつかの転写因子を強制発現することで、線維芽細胞などの体細胞から異なる細胞種を誘導できることが示された。ES細胞に強く発現し機能的に重要なOct3/4、Sox2、Klf4、c-Mycの4つの転写因子群を強制発現させるとES細胞に非常に類似した性質を持つiPS細胞が誘導できた事実から、神経細胞に強く発現している転写因子群を強制発現させると、直接神経細胞を誘導できるのではないかと多くの研究者達が予想したのである。
そういった背景の中、2010年1月スタンフォード大学のWernig博士の研究グループはAscl1, Brn2, Myt1lという神経細胞に特異的に発現している3つの転写因子群をレトロウイルスベクターを用いてマウス皮膚線維芽細胞に強制発現し、グルタミン酸作動性ニューロン様の細胞を直接誘導できることを発見した[1] 。この誘導された神経細胞は神経細胞特有の活動電位や、シナプス形成能を持つことが示され、induced neuronal(iN)細胞と名づけられている。
この発見を嚆矢として運動ニューロン[2] やドパミン作動性ニューロン[3] 、ノルアドレナリン作動性ニューロン[4] 、神経幹細胞[5][6] など多様な神経系細胞が誘導できることがこれまでに報告されてきている(図1)。
特徴
iN細胞は、iPS細胞の状態を介さずに直接目的である神経系細胞に分化誘導するため、①比較的短期間で誘導可能、②腫瘍化のリスクが低い点が利点である。一方、iN細胞を誘導した時点で原則細胞分裂が停止し増殖させることが出来ない点が欠点である。
誘導因子と阻害因子
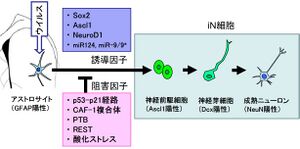
[7] より改変転載
神経細胞リプログラミングを誘導する最も重要な転写因子はAscl1であると現時点で考えられている。2013年Wapinskiらが、線維芽細胞ではAscl1の標的遺伝子座のクロマチンは閉じているが、Ascl1が発現すると閉じたクロマチンの構造変化を起こすことで、ニューロン関連遺伝子の転写を活性化させることを報告している[8] 。
一方、Ascl1は線維芽細胞特異的遺伝子のプロモーター領域をメチル化してクロマチンを閉じさせ、線維芽細胞特異的遺伝子の発現を抑制することも明らかにされている[9] 。このようにAscl1はニューロン関連遺伝子の発現を上昇させるだけでなく、元の線維芽細胞関連遺伝子を抑制することで、神経細胞リプログラミングを行うと考えられている。
またAscl1の他にも様々な神経細胞特異的な転写因子群(Brn2、Mytl1、NeuroD1)やmicroRNA(miR-124, miR-9/9*)を線維芽細胞などに強制発現させることでiN細胞を誘導できることが報告されている[10] 。さらに転写因子などの強制発現を行わなくとも、cAMPの産生作用をもつフォルスコリンやGSK-3β阻害作用をもつCHIR99021などの低分子化合物を細胞培養の培地に加えることでiN細胞を誘導できることが可能になってきた[11][12] 。
一方、通常の体内では線維芽細胞がいきなり神経細胞に変わるようなことが起きないように様々な制御機構が働いていると考えられており、これまでにp53-p21経路[13] 、CAF-1複合体[14] 、RE1-silencing transcription factor (REST)[15]、そして過剰な酸化ストレスの存在[16] が神経細胞リプログラミングを阻害することが報告されてきている(図2)。
特筆すべきこととしてはmiR-124の標的遺伝子であるpyrimidine-tract-binding protein (PTB)というRNA結合タンパク質をshRNA等でノックダウンするだけでiN細胞が誘導できることが報告されている[17] 。miR-124はPTBならびにRESTの発現を抑制することから、これら誘導因子と阻害因子はお互いに相互作用があり、両者のバランスによって細胞の運命が最終決定されていると現在考えられている。
臨床応用の可能性
iN細胞は未分化な状態を経ずに誘導可能なことから、細胞DNAメチル化のパターンがiN細胞誘導後も保存されることが知られている[18] 。この特徴は、中高年に多い神経変性疾患の疾患モデルを作るうえで特に重要であり、実際、iN細胞を用いた様々な神経変性疾患(アルツハイマー病、筋萎縮性側索硬化症、脊髄性筋萎縮症など)の疾患モデルが報告されてきている。神経疾患患者由来のiN細胞を大量に作成し、ドラッグスクリーニングを行うなど創薬分野への応用も展開が今後可能になると期待されている。
さらに、iN細胞はiPS細胞などの未熟な状態を経ずに作成できるため、腫瘍形成のリスクが低いと考えられている。そこでアストロサイトなどのグリア細胞を脳内で直接目的の神経細胞に誘導するin vivoでの神経細胞リプログラミングが近年注目を集めてきている。脳梗塞や神経変性疾患患者の脳内ではニューロンは脱落しその数が減少している一方でアストロサイトやミクログリアなどのグリア細胞が多く存在していることから、iN細胞の有望な供給源と考えられる。2019年7月には著者らが脳梗塞マウス脳内グリア細胞からiN細胞を誘導できたことを報告した[19] 。2020年4、5月には複数の研究グループから、PTBノックダウンの手法でマウス脳内アストロサイトからドパミン作動性ニューロンを直接誘導し、パーキンソン症状を改善させる実験結果も報告されてきており[20][21] 、このin vivo神経細胞リプログラミング法は今後の脳梗塞やパーキンソン病の有望な治療戦略となる可能性がある。
| 誘導されたiN細胞 | 転写因子 | 主な内容 | 文献 |
|---|---|---|---|
| グルタミン酸作動性ニューロン | Ascl1, Brn2, Myt1l | 直接的に誘導されたグルタミン酸作動性ニューロンが電気生理学的にみて機能していることを示した。 | Vierbuchenら[1] |
| 運動ニューロン | Ascl1, Brn2, Myt1l, Lhx3, Hb9, Isl1, Ngn2 | 直接的に誘導された運動ニューロンが電気生理学的に機能し、かつ筋細胞と機能的シナプスを形成できることを示した。 | Sonら[2] |
| ドパミン作動性ニューロン | Ascl1, Brn2, Myt1l | 直接的に誘導されたドパミン作動性ニューロンは電気生理学的に機能し、かつドパミン産生能を持つことを示した。 | Caiazzoら[3] |
| ノルアドレナリン作動性ニューロン | Ascl1, Phox2b, AP-2α, Gata3, Hand2, Nurr1, Phox2a | 直接的に誘導されたノルアドレナリン作動性ニューロンは、電気生理学的に機能し、共培養した心筋細胞の拍動数を制御できた。 | Liら[4] |
| 神経幹細胞 | Sox2, Brn2, FoxG1 またはSox2, Brn4, Klf4, c-Myc |
直接的に誘導した神経幹細胞が自己複製能を持ち、かつニューロン、アストロサイト、オリゴデンドロサイトに分化できること示した。 | Lujanら[6] Hanら[5] |
| グルタミン酸作動性ニューロン | PTB1に対するshRNAの導入 | マウスの胎生線維芽細胞から電気生理学的にも機能しているグルタミン酸作動性ニューロンが誘導された。 | Xueら[17] |
| グルタミン酸作動性ニューロン | cAMP産生作用をもつフォルスコリンとGSK-3β阻害作用をもつCHIR99021などの低分子化合物を培地に添加 | マウス・ヒト線維芽細胞から電気生理学的にも機能しているグルタミン酸作動性ニューロンが誘導された。 | Liら[12] Huら[11] |
参考文献
- ↑ 1.0 1.1
Vierbuchen, T., Ostermeier, A., Pang, Z.P., Kokubu, Y., Südhof, T.C., & Wernig, M. (2010).
Direct conversion of fibroblasts to functional neurons by defined factors. Nature, 463(7284), 1035-41. [PubMed:20107439] [PMC] [WorldCat] [DOI] - ↑ 2.0 2.1
Son, E.Y., Ichida, J.K., Wainger, B.J., Toma, J.S., Rafuse, V.F., Woolf, C.J., & Eggan, K. (2011).
Conversion of mouse and human fibroblasts into functional spinal motor neurons. Cell stem cell, 9(3), 205-18. [PubMed:21852222] [PMC] [WorldCat] [DOI] - ↑ 3.0 3.1
Caiazzo, M., Dell'Anno, M.T., Dvoretskova, E., Lazarevic, D., Taverna, S., Leo, D., ..., & Broccoli, V. (2011).
Direct generation of functional dopaminergic neurons from mouse and human fibroblasts. Nature, 476(7359), 224-7. [PubMed:21725324] [WorldCat] [DOI] - ↑ 4.0 4.1
Li, S., Shi, Y., Yao, X., Wang, X., Shen, L., Rao, Z., ..., & Cheng, L. (2019).
Conversion of Astrocytes and Fibroblasts into Functional Noradrenergic Neurons. Cell reports, 28(3), 682-697.e7. [PubMed:31315047] [WorldCat] [DOI] - ↑ 5.0 5.1
Han, D.W., Tapia, N., Hermann, A., Hemmer, K., Höing, S., Araúzo-Bravo, M.J., ..., & Schöler, H.R. (2012).
Direct reprogramming of fibroblasts into neural stem cells by defined factors. Cell stem cell, 10(4), 465-72. [PubMed:22445517] [WorldCat] [DOI] - ↑ 6.0 6.1
Lujan, E., Chanda, S., Ahlenius, H., Südhof, T.C., & Wernig, M. (2012).
Direct conversion of mouse fibroblasts to self-renewing, tripotent neural precursor cells. Proceedings of the National Academy of Sciences of the United States of America, 109(7), 2527-32. [PubMed:22308465] [PMC] [WorldCat] [DOI] - ↑ 山下徹、阿部康二 (2018)
ダイレクトリプログラミングによる神経再生
Clinical Neuroscience 36, 370-372 - ↑
Wapinski, O.L., Vierbuchen, T., Qu, K., Lee, Q.Y., Chanda, S., Fuentes, D.R., ..., & Wernig, M. (2013).
Hierarchical mechanisms for direct reprogramming of fibroblasts to neurons. Cell, 155(3), 621-35. [PubMed:24243019] [PMC] [WorldCat] [DOI] - ↑
Luo, C., Lee, Q.Y., Wapinski, O., Castanon, R., Nery, J.R., Mall, M., ..., & Ecker, J.R. (2019).
Global DNA methylation remodeling during direct reprogramming of fibroblasts to neurons. eLife, 8. [PubMed:30644360] [PMC] [WorldCat] [DOI] - ↑
Yoo, A.S., Sun, A.X., Li, L., Shcheglovitov, A., Portmann, T., Li, Y., ..., & Crabtree, G.R. (2011).
MicroRNA-mediated conversion of human fibroblasts to neurons. Nature, 476(7359), 228-31. [PubMed:21753754] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Hu, W., Qiu, B., Guan, W., Wang, Q., Wang, M., Li, W., ..., & Pei, G. (2015).
Direct Conversion of Normal and Alzheimer's Disease Human Fibroblasts into Neuronal Cells by Small Molecules. Cell stem cell, 17(2), 204-12. [PubMed:26253202] [WorldCat] [DOI] - ↑ 12.0 12.1
Li, X., Zuo, X., Jing, J., Ma, Y., Wang, J., Liu, D., ..., & Deng, H. (2015).
Small-Molecule-Driven Direct Reprogramming of Mouse Fibroblasts into Functional Neurons. Cell stem cell, 17(2), 195-203. [PubMed:26253201] [WorldCat] [DOI] - ↑
Jiang, H., Xu, Z., Zhong, P., Ren, Y., Liang, G., Schilling, H.A., ..., & Feng, J. (2015).
Cell cycle and p53 gate the direct conversion of human fibroblasts to dopaminergic neurons. Nature communications, 6, 10100. [PubMed:26639555] [PMC] [WorldCat] [DOI] - ↑
Cheloufi, S., Elling, U., Hopfgartner, B., Jung, Y.L., Murn, J., Ninova, M., ..., & Hochedlinger, K. (2015).
The histone chaperone CAF-1 safeguards somatic cell identity. Nature, 528(7581), 218-24. [PubMed:26659182] [PMC] [WorldCat] [DOI] - ↑
Masserdotti, G., Gillotin, S., Sutor, B., Drechsel, D., Irmler, M., Jørgensen, H.F., ..., & Götz, M. (2015).
Transcriptional Mechanisms of Proneural Factors and REST in Regulating Neuronal Reprogramming of Astrocytes. Cell stem cell, 17(1), 74-88. [PubMed:26119235] [PMC] [WorldCat] [DOI] - ↑
Gascón, S., Murenu, E., Masserdotti, G., Ortega, F., Russo, G.L., Petrik, D., ..., & Götz, M. (2016).
Identification and Successful Negotiation of a Metabolic Checkpoint in Direct Neuronal Reprogramming. Cell stem cell, 18(3), 396-409. [PubMed:26748418] [WorldCat] [DOI] - ↑ 17.0 17.1
Xue, Y., Ouyang, K., Huang, J., Zhou, Y., Ouyang, H., Li, H., ..., & Fu, X.D. (2013).
Direct conversion of fibroblasts to neurons by reprogramming PTB-regulated microRNA circuits. Cell, 152(1-2), 82-96. [PubMed:23313552] [PMC] [WorldCat] [DOI] - ↑
Huh, C.J., Zhang, B., Victor, M.B., Dahiya, S., Batista, L.F., Horvath, S., & Yoo, A.S. (2016).
Maintenance of age in human neurons generated by microRNA-based neuronal conversion of fibroblasts. eLife, 5. [PubMed:27644593] [PMC] [WorldCat] [DOI] - ↑
Yamashita, T., Shang, J., Nakano, Y., Morihara, R., Sato, K., Takemoto, M., ..., & Abe, K. (2019).
In vivo direct reprogramming of glial linage to mature neurons after cerebral ischemia. Scientific reports, 9(1), 10956. [PubMed:31358888] [PMC] [WorldCat] [DOI] - ↑
Qian, H., Kang, X., Hu, J., Zhang, D., Liang, Z., Meng, F., ..., & Fu, X.D. (2020).
Reversing a model of Parkinson's disease with in situ converted nigral neurons. Nature, 582(7813), 550-556. [PubMed:32581380] [WorldCat] [DOI] - ↑
Zhou, H., Su, J., Hu, X., Zhou, C., Li, H., Chen, Z., ..., & Yang, H. (2020).
Glia-to-Neuron Conversion by CRISPR-CasRx Alleviates Symptoms of Neurological Disease in Mice. Cell, 181(3), 590-603.e16. [PubMed:32272060] [WorldCat] [DOI]