アダプタータンパク質複合体
松田 信爾
電気通信大学大学院 情報理工学研究科 基盤理工学専攻
DOI:10.14931/bsd.7734 原稿受付日:2018年6月12日 原稿完成日:2018年11月17日
担当編集委員:和田 圭司(国立研究開発法人国立精神・神経医療研究センター)
英語名:adaptor protein complex 独:Adaptorproteinkomplexe 仏:protéine adaptatrice
英略語:AP complex
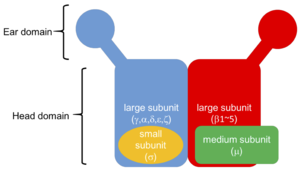
アダプタータンパク質複合体は4種類のポリペプチド鎖からなるヘテロ4量体で、2種類のlarge subunit, 1種類のmedium subunit, 1種類のsmall subunitから構成されている。このタンパク質複合体はファミリーを形成し、AP-1からAP-5の5つのメンバーが報告されている。AP-1からAP-5はいずれも、それぞれが積み荷となる膜貫通タンパク質を細胞内の特定の膜領域へと輸送する機能を持っている 。積荷タンパク質の認識はmedium subunitが積荷タンパク質の細胞内領域に存在するシグナル配列に結合することにより行われるのが一般的である。アダプタータンパク質複合体のメンバーは全て共通の高次構造をとっていると考えられている。2つのlarge subunitのC末領域は”Ear domain”を形成し、”Head domain”はlarge subunitのN末領域とmedium subunitとsmall subunitからなっている。
アダプタータンパク質複合体とは
[1]より引用。
真核細胞は細胞をつつむ細胞膜と共に、様々な細胞内膜系を有しており、それぞれの膜が特有の機能を果たしている。これらの膜機能は、細胞膜と細胞内膜系、あるいは細胞内膜系間での厳密に制御されたタンパク質輸送に大きく依存していることから、その輸送機構が盛んに研究されてきている。
これまでに膜タンパク質の輸送に中心的な役割を果たす分子として、AP-1からAP-5の5種類アダプタータンパク質複合体が報告されている(表)。これら5種類のアダプタータンパク質は、全て、2種類のlarge subunit, 1種類のmedium subunit, 1種類のsmall subunitからなるヘテロ4量体構造をとっており、図1に示すような共通の高次構造を持つと考えられている。2つのlarge subunitのC末領域は”Ear domain”を形成し、”Head domain”はlarge subunitのN末領域とmedium subunitとsmall subunitからなっている。
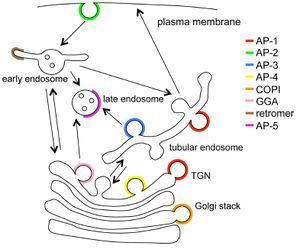
5種類のアダプタータンパク質はいずれも、それぞれが積み荷となる膜貫通タンパク質を細胞内の特定の膜領域から別の膜領域へと輸送する機能を持っている[2][3](図2)。
アダプタータンパク質が司る膜輸送にはクラスリン依存性のものと非依存性のものがあり、AP-1およびAP-2は主にβサブユニットを介してクラスリンに結合し、膜タンパク質のクラスリン依存的な輸送を司る。これに対して、AP-3, AP-4, AP-5はクラスリン非依存的に膜タンパク質の輸送を行うと考えられている。
いずれのアダプタータンパク質の場合も、積荷タンパク質の認識はmedium subunitが積荷タンパク質の細胞内領域に存在するシグナル配列に結合することにより行われるのが一般的である。
| 複合体 | Large subunit 1 | Large subunit 2 | Medium subunit | Small subunit |
|---|---|---|---|---|
| AP-1 | γ1,2 | β1 | μ1A,B | σ1A-C |
| AP-2 | α | β2 | μ2 | σ2 |
| AP-3 | δ | β3A,B | μ3A,B | σ3 |
| AP-4 | ε | β4 | μ4 | σ4 |
| AP-5 | ζ | β5 | μ5 | σ5 |
AP-1
機能
AP-1はエンドソームとトランスゴルジネットワークとの間で膜タンパク質の輸送を行うアダプタータンパク質複合体である[4] 。
神経細胞や上皮細胞といった極性をもつ細胞においては、ある種の膜タンパク質を樹状突起や側基底膜へと輸送することも知られている[5][6][7][8] 。
AP-1はクラスリンを細胞内膜上に集積させると共に積荷タンパク質を認識することで積荷タンパク質を含んだクラスリン被覆小胞を形成し、積荷タンパク質を輸送する。AP-1の細胞内膜への集積は低分子量Gタンパク質であるARFに依存している。ARFによってホスファチジルイノシトール4リン酸が細胞内膜上に合成されることによりAP-1がリクルートされると考えられている[9][10] 。また、AP-1がホスファチジルイノシトール4リン酸と結合することも報告されている[10] 。
こうして細胞内膜上にリクルートされたAP-1は積荷タンパク質のYXXΦ配列や[DE]XXXL[LI]配列、あるいはこれら以外の非典型的な配列を認識して結合する[11][12] 。同時にAP-1はクラスリンに対する結合能も有することから細胞内膜系に存在する積荷タンパク質をクラスリン被覆小胞へと運びこむことができる[13] 。
サブユニット構造
AP-1は2つのlarge subunit (β1とγ)、1つのmedium subunit (μ1)、1つのsmall subunit (σ1)からなる[3] 。
主なクラスリン結合部位はβ1サブユニットに存在する[14] が、γサブユニットもクラスリン結合に関与していることが報告されている[15] 。積荷タンパク質との結合は主にμサブユニットによって行われている。γサブユニットにはγ1とγ2の2つのisoformが、μ1サブユニットにはμ1Aとμ1Bの2つ、σ1サブユニットにはσ1A~σ1Cの3つのisoformが存在する[6][16][17] 。
発現パターンおよび欠損マウス
μ1Aはユビキタスに発現しているが、μ1Bの発現は上皮細胞特異的であることが報告されている[18] 。つまり、μ1Aを含むAP-1(AP-1A)はユビキタスに発現しており、μ1Bを含むAP-1(AP-1B)は上皮細胞特異的に発現している。
ゼブラフィッシュでは、μ1Bは受精直後の2細胞期には多く発現するものの、その後一時的に大きく減少し、受精後24時間から再び発現し始めることも報告されている[19] 。またσ1サブユニットはどれもユビキタスに発現しているが、σ1Aとσ1Bの発現は脳で最も強いことが知られている[20] 。
σ1Bの欠損マウスでは運動失調並びに空間記憶の異常が生じることも報告されている。μ1Aおよびγ1の欠損マウスは胎生致死である[21][22] 。μ1Bの欠損マウスでは一部の側基底膜に存在するサイトカイン受容体が頂端膜へと輸送されることで、上皮細胞の抗菌性タンパク質の発現の減少やIgAの分泌異常が引き起こされ、腸管免疫が異常をきたし、慢性大腸炎をしめす。[23]
疾患との関連
MEDNIK症候群
σ1Aの欠損によりMEDNIK (mental retardation, enteropathy, deafness, neuropathy, ichthyosis, and keratodermia) 症候群が引き起こされることが報告されている[24] 。健常者由来の繊維芽細胞では、銅イオンポンプATP7Aは基底状態ではゴルジ体に、高濃度の銅イオン存在下では細胞膜に輸送されるのに対し、患者由来の繊維芽細胞では基底状態でも細胞膜に多くATP7Aが検出されることが報告されている [25] 。その為、この疾患は銅ポンプであるATP7AおよびそのホモログであるATP7Bの細胞内輸送の異常のために引き起こされると考えられている。
Pettigrew症候群
σ1Bの欠損によりX連鎖精神遅滞であるPettigrew症候群[26] に関連しているといわれている。
汎発性膿疱性乾癬
σ1Cの欠損は汎発性膿疱性乾癬[16] に関連しているといわれている。
AP-2
機能
AP-2はクラスリン依存性エンドサイトーシスを司り、細胞膜からエンドソームへの膜タンパク質の輸送を行うアダプタータンパク質である[4] 。
AP-2はAP-1と同様にクラスリン結合部位を有しており、クラスリンを細胞膜上に集積させる。同時に、積荷タンパク質を認識することによって、AP-2は積荷タンパク質をクラスリン被覆小胞によってエンドサイトーシスさせる。
AP-2はホスファチジルイノシトール-4,5-2リン酸(PIP2)により細胞膜上にリクルートされる[27] 。細胞膜上にリクルートされたAP-2は、AP-1と同様に積荷タンパク質の輸送シグナルに結合する。
AP-2と積荷タンパク質の結合はリン酸化によって調節されることが知られている。例えばCTLA-4やL1といった膜タンパク質に含まれるYXXΦ配列のチロシン残基がリン酸化されるとAP-2と結合できなくなる[28][29] 。
さらにAMPA型グルタミン酸受容体(AMPA受容体)の副サブユニットであるTARP (Transmembane AMPA receptor Regulatory Protein)とAP-2との結合がリン酸化によって制御されていることも報告されている[30] 。TARPとAP-2とのリン酸化に依存した結合によりシナプス後部におけるAMPA受容体のエンドサイトーシスが調整されており、シナプス可塑性の1つである長期抑圧(LTD)の分子基盤となっていると考えられている。
シナプス前部におけるシナプス小胞のエンドサイトーシスにもAP-2は重要な役割を果たしている。シナプス小胞がシナプス前部の細胞膜と融合するエキソサイトーシスにより神経伝達物質は放出されるが、その後シナプス小胞上に存在するタンパク質はクラスリン依存性エンドサイトーシスによって再び細胞膜から回収される[31][32] 。
サブユニット構造
AP-2も2つのlarge subunit (β2とα)、1つのmedium subunit (μ2)、1つのsmall subunit (σ2)からなる[3] 。
YXXΦ配列とμ2サブユニットとの結合の構造的基盤が明らかにされており[33] 、それによるとμ2サブユニットの2つの疎水性ポケットの一方にチロシンが、もう一方にΦが結合することが示されている。YXXΦ配列はAP-1の輸送シグナル配列と同じであるが、XやΦの位置に存在するアミノ酸によってどちらのアダプタータンパク質に結合しやすいかが決まると考えられている[34] 。
発現パターンと欠損マウス
AP-2はユビキタスに発現しており、μ2サブユニットの欠損マウスは胎生致死であることが報告されている[35] 。
AP-3
機能
AP-3はエンドソームからリソソームヘの輸送を制御するアダプタータンパク質複合体である[4] 。
In vitroではクラスリンに結合することが報告されている[36] が、この結合と実際の小胞輸送との関連性は明らかではなく[37] 、むしろAP-3はVPS41とも結合し、これが小胞輸送に重要であるとの報告がなされている[38] 。
AP-3はホスファチジルイノシトール3リン酸に対する結合能を有しており[39] 、これによりエンドソームに集積すると考えられる。AP-3が認識する積荷タンパク質の輸送シグナルはAP-1およびAP-2の認識配列と同様のアミノ酸配列である[11] 。神経細胞のシナプス後部においては、AP-3はAP-2と同様にAMPA受容体の副サブユニットであるTARPとリン酸化依存的に結合しAMPA受容体-TARP複合体をリソソームヘと輸送することで、長期抑圧の誘導に必須の役割を果たしていると考えられている[30] 。
またシナプス前部において、シナプス小胞前駆体からのシナプス小胞の形成に寄与[40] すると共に、神経ペプチドの有芯小胞への輸送[41] 、さらに線虫では軸索へのタンパク質輸送も司っていることが報告されている[42] 。
サブユニット構造
AP-3も2つのlarge subunit (β3とδ)、1つのmedium subunit (μ3)、1つのsmall subunit (σ3)からなっている[3] 。βサブユニットとμサブユニットにはそれぞれ脳特異的なβ3Bとμ3Bサブユニットが存在する[2] 。
発現パターンと欠損マウス
β3Bとμ3Bを含むAP-3(AP-3B)は脳特異的に発現するが、これらを含まないAP-3Aはユビキタスに存在する。ユビキタスに発現するδサブユニットが欠損した変異マウス(mocha)は、眼や皮膚の色素が薄まり、血小板やリソソーム、内耳の異常と共に神経系の異常も見られ、後述の10型Hermansky-Pudlak症候群のモデルマウスと考えられている [43] 。脳特異的なβ3Bのノックアウトマウスでは、シナプスの形態やGABAの放出に異常が見られ、てんかん発作を起こすことが知られている [40] 。
疾患との関連
10型Hermansky-Pudlak症候群
δサブユニットの欠損により10型Hermansky-Pudlak症候群が引き起こされることが報告されている[44] 。この疾患では上述のmochaマウスと類似した様々な症状が現れるが、神経症状としては、重篤な神経発達遅延、小頭症、てんかん、聴覚異常、終脳萎縮がみられる。。
2型Hermansky-Pudlak症候群
β3Aサブユニットの欠損により2型Hermansky-Pudlak症候群が引き起こされる[45] 。この疾患での神経発達遅延は軽微である。
早期発症型てんかん性脳症
脳特異的なβ3Bの欠損では早期発症型てんかん性脳症(EOEE)が発症し、重篤な神経発達遅延、知的障害、てんかん、視神経萎縮症などの症状が現れる[46] 。
AP-4
機能
AP-4はクラスリン非依存的に積荷タンパク質をトランスゴルジネットワークから輸送するアダプタータンパク質である[2] 。
上皮細胞や神経細胞といった極性をもった細胞においてAP-4はこの極性に従った膜タンパク質の輸送に関与することが知られている。上皮細胞においては低密度リポタンパク質受容体(LDLR)やカチオン依存性マンノース6リン酸受容体を側基底膜へと輸送[47] し、神経細胞ではδ2グルタミン酸受容体(GluD2)やAMPA型グルタミン酸受容体―TARP複合体を樹状突起特異的に輸送することが報告されている[48] 。AP-4欠損マウスではAMPA受容体―TARP複合体は樹状突起だけでなく軸索にも輸送され、軸索ではオートファゴソーム様の構造体に取り込まれることが知られている。一方、同じ樹状突起特異的に存在するタンパク質であってもNMDA型グルタミン酸受容体、あるいは代謝型グルタミン酸受容体1はAP-4非依存的に樹状突起へと輸送されることも明らかになっている。
さらに、AP-4はアミロイド前駆体タンパク質(APP)の細胞質領域に結合し、トランスゴルジネットワークからエンドソームへと輸送すること[49] 、ATG9Aをトランスゴルジネットワークからエンドソームあるいはオートファゴソーム前駆構造へと輸送することも報告されている[50] 。
サブユニット構造
AP-4も2つのlarge subunit (β4とε)、1つのmedium subunit (μ4)、1つのsmall subunit (σ4)からなっている。βサブユニットとεサブユニットにはクラスリン結合モチーフが含まれておらず、また電子顕微鏡による解析からAP-4がクラスリンに覆われていない小胞上に存在することが示されており、これらのことからクラスリン非依存性の小胞輸送に関与すると考えられている[2][51] 。
発現パターンと欠損マウス
AP-4はユビキタスにみられるアダプタータンパク質であり[52] 、β4のノックアウトマウスには軽度の運動失調が見られることが報告されている[48]。
疾患との関連
AP-4欠損症候群
AP-4の4つのサブユニットのいずれが欠損しても神経発達障害が引き起こされ、AP-4欠損症候群と呼ばれ、常染色体劣性遺伝を示す[53][54][55][56] 。乳児期に筋緊張低下がおこり、その後四肢麻痺や筋緊張亢進、そして歩行不能となる。また重篤な知的障害が引き起こされ、言語発達障害あるいは顕著な遅れが見られる。さらにこれまで脳性麻痺と診断されてきた110名の患者のσ4遺伝子に変異があることが報告されている[57] 。
脳神経疾患以外の症状としてはAP-4ε遺伝子にナンセンス変異をもつ一卵性双生児がBCGワクチンの接種によりリンパ節炎を発症した[58] 。このことからAP-4は免疫系にも重要な役割を果たしている可能性が考えられる。
AP-5
機能
AP-5は最も新しく発見されたアダプタータンパク質複合体であり、後期エンドソームおよびリソソームに存在している[59] 。クラスリン非依存的に積荷タンパク質を輸送するアダプタータンパク質であり[2] 、カチオン非依存性マンノース6リン酸受容体(CI-MPR)、ゴルジタンパク質であるGOLIM4, GOLM1を後期エンドソームからゴルジ体へと輸送する機能を持つ[60] 。
サブユニット構造
AP-5も2つのlarge subunit (β5とζ)、1つのmedium subunit (μ5)、1つのsmall subunit (σ5)からなっている[1] 。AP-5はクラスリンには結合せず、その代わりにspatacsin (SPG11)とspastizin (SPG15)に結合することが知られている[61] 。
発現パターンと欠損マウス
AP-5は最も新しく発見されたアダプタータンパク質であり、詳しいサブユニットの発現部位および欠損マウスの表現型については報告されていない。
疾患との関連
AP-5ζサブユニットの欠損およびSPG11とSPG15の欠損の患者は脳梁が薄く、白質病変を有し、神経障害、パーキンソン症、認知障害を示すことが報告されている[62][63] 。
参考文献
- ↑ 1.0 1.1
Hirst, J., Barlow, L.D., Francisco, G.C., Sahlender, D.A., Seaman, M.N., Dacks, J.B., & Robinson, M.S. (2011).
The fifth adaptor protein complex. PLoS biology, 9(10), e1001170. [PubMed:22022230] [PMC] [WorldCat] [DOI] - ↑ 2.0 2.1 2.2 2.3 2.4
Guardia, C.M., De Pace, R., Mattera, R., & Bonifacino, J.S. (2018).
Neuronal functions of adaptor complexes involved in protein sorting. Current opinion in neurobiology, 51, 103-110. [PubMed:29558740] [PMC] [WorldCat] [DOI] - ↑ 3.0 3.1 3.2 3.3
Robinson, M.S., & Bonifacino, J.S. (2001).
Adaptor-related proteins. Current opinion in cell biology, 13(4), 444-53. [PubMed:11454451] [WorldCat] [DOI] - ↑ 4.0 4.1 4.2
Robinson, M.S. (2004).
Adaptable adaptors for coated vesicles. Trends in cell biology, 14(4), 167-74. [PubMed:15066634] [WorldCat] [DOI] - ↑
Dwyer, N.D., Adler, C.E., Crump, J.G., L'Etoile, N.D., & Bargmann, C.I. (2001).
Polarized dendritic transport and the AP-1 mu1 clathrin adaptor UNC-101 localize odorant receptors to olfactory cilia. Neuron, 31(2), 277-87. [PubMed:11502258] [WorldCat] [DOI] - ↑ 6.0 6.1
Fölsch, H., Ohno, H., Bonifacino, J.S., & Mellman, I. (1999).
A novel clathrin adaptor complex mediates basolateral targeting in polarized epithelial cells. Cell, 99(2), 189-98. [PubMed:10535737] [WorldCat] [DOI] - ↑
Fölsch, H., Pypaert, M., Schu, P., & Mellman, I. (2001).
Distribution and function of AP-1 clathrin adaptor complexes in polarized epithelial cells. The Journal of cell biology, 152(3), 595-606. [PubMed:11157985] [PMC] [WorldCat] [DOI] - ↑
Jain, S., Farías, G.G., & Bonifacino, J.S. (2015).
Polarized sorting of the copper transporter ATP7B in neurons mediated by recognition of a dileucine signal by AP-1. Molecular biology of the cell, 26(2), 218-28. [PubMed:25378584] [PMC] [WorldCat] [DOI] - ↑
Robinson, M.S., & Kreis, T.E. (1992).
Recruitment of coat proteins onto Golgi membranes in intact and permeabilized cells: effects of brefeldin A and G protein activators. Cell, 69(1), 129-38. [PubMed:1555237] [WorldCat] [DOI] - ↑ 10.0 10.1
Wang, Y.J., Wang, J., Sun, H.Q., Martinez, M., Sun, Y.X., Macia, E., ..., & Yin, H.L. (2003).
Phosphatidylinositol 4 phosphate regulates targeting of clathrin adaptor AP-1 complexes to the Golgi. Cell, 114(3), 299-310. [PubMed:12914695] [WorldCat] [DOI] - ↑ 11.0 11.1
Bonifacino, J.S., & Traub, L.M. (2003).
Signals for sorting of transmembrane proteins to endosomes and lysosomes. Annual review of biochemistry, 72, 395-447. [PubMed:12651740] [WorldCat] [DOI] - ↑
Ohno, H., Stewart, J., Fournier, M.C., Bosshart, H., Rhee, I., Miyatake, S., ..., & Bonifacino, J.S. (1995).
Interaction of tyrosine-based sorting signals with clathrin-associated proteins. Science (New York, N.Y.), 269(5232), 1872-5. [PubMed:7569928] [WorldCat] [DOI] - ↑
Keen, J.H. (1987).
Clathrin assembly proteins: affinity purification and a model for coat assembly. The Journal of cell biology, 105(5), 1989-98. [PubMed:2890644] [PMC] [WorldCat] [DOI] - ↑
Gallusser, A., & Kirchhausen, T. (1993).
The beta 1 and beta 2 subunits of the AP complexes are the clathrin coat assembly components. The EMBO journal, 12(13), 5237-44. [PubMed:8262066] [PMC] [WorldCat] - ↑
Doray, B., & Kornfeld, S. (2001).
Gamma subunit of the AP-1 adaptor complex binds clathrin: implications for cooperative binding in coated vesicle assembly. Molecular biology of the cell, 12(7), 1925-35. [PubMed:11451993] [PMC] [WorldCat] [DOI] - ↑ 16.0 16.1
Setta-Kaffetzi, N., Simpson, M.A., Navarini, A.A., Patel, V.M., Lu, H.C., Allen, M.H., ..., & Capon, F. (2014).
AP1S3 mutations are associated with pustular psoriasis and impaired Toll-like receptor 3 trafficking. American journal of human genetics, 94(5), 790-7. [PubMed:24791904] [PMC] [WorldCat] [DOI] - ↑
Takatsu, H., Sakurai, M., Shin, H.W., Murakami, K., & Nakayama, K. (1998).
Identification and characterization of novel clathrin adaptor-related proteins. The Journal of biological chemistry, 273(38), 24693-700. [PubMed:9733768] [WorldCat] [DOI] - ↑
Ohno, H., Tomemori, T., Nakatsu, F., Okazaki, Y., Aguilar, R.C., Foelsch, H., ..., & Bonifacino, J.S. (1999).
Mu1B, a novel adaptor medium chain expressed in polarized epithelial cells. FEBS letters, 449(2-3), 215-20. [PubMed:10338135] [WorldCat] [DOI] - ↑
Zizioli, D., Forlanelli, E., Guarienti, M., Nicoli, S., Fanzani, A., Bresciani, R., ..., & Schu, P. (2010).
Characterization of the AP-1 μ1A and μ1B adaptins in zebrafish (Danio rerio). Developmental dynamics : an official publication of the American Association of Anatomists, 239(9), 2404-12. [PubMed:20652956] [WorldCat] [DOI] - ↑
Glyvuk, N., Tsytsyura, Y., Geumann, C., D'Hooge, R., Hüve, J., Kratzke, M., ..., & Schu, P. (2010).
AP-1/sigma1B-adaptin mediates endosomal synaptic vesicle recycling, learning and memory. The EMBO journal, 29(8), 1318-30. [PubMed:20203623] [PMC] [WorldCat] [DOI] - ↑
Meyer, C., Zizioli, D., Lausmann, S., Eskelinen, E.L., Hamann, J., Saftig, P., ..., & Schu, P. (2000).
mu1A-adaptin-deficient mice: lethality, loss of AP-1 binding and rerouting of mannose 6-phosphate receptors. The EMBO journal, 19(10), 2193-203. [PubMed:10811610] [PMC] [WorldCat] [DOI] - ↑
Zizioli, D., Meyer, C., Guhde, G., Saftig, P., von Figura, K., & Schu, P. (1999).
Early embryonic death of mice deficient in gamma-adaptin. The Journal of biological chemistry, 274(9), 5385-90. [PubMed:10026148] [WorldCat] [DOI] - ↑
Takahashi, D., Hase, K., Kimura, S., Nakatsu, F., Ohmae, M., Mandai, Y., ..., & Ohno, H. (2011).
The epithelia-specific membrane trafficking factor AP-1B controls gut immune homeostasis in mice. Gastroenterology, 141(2), 621-32. [PubMed:21669204] [WorldCat] [DOI] - ↑
Montpetit, A., Côté, S., Brustein, E., Drouin, C.A., Lapointe, L., Boudreau, M., ..., & Cossette, P. (2008).
Disruption of AP1S1, causing a novel neurocutaneous syndrome, perturbs development of the skin and spinal cord. PLoS genetics, 4(12), e1000296. [PubMed:19057675] [PMC] [WorldCat] [DOI] - ↑
Martinelli, D., Travaglini, L., Drouin, C.A., Ceballos-Picot, I., Rizza, T., Bertini, E., ..., & Dionisi-Vici, C. (2013).
MEDNIK syndrome: a novel defect of copper metabolism treatable by zinc acetate therapy. Brain : a journal of neurology, 136(Pt 3), 872-81. [PubMed:23423674] [WorldCat] [DOI] - ↑
Tarpey, P.S., Stevens, C., Teague, J., Edkins, S., O'Meara, S., Avis, T., ..., & Raymond, F.L. (2006).
Mutations in the gene encoding the Sigma 2 subunit of the adaptor protein 1 complex, AP1S2, cause X-linked mental retardation. American journal of human genetics, 79(6), 1119-24. [PubMed:17186471] [PMC] [WorldCat] [DOI] - ↑
Rohde, G., Wenzel, D., & Haucke, V. (2002).
A phosphatidylinositol (4,5)-bisphosphate binding site within mu2-adaptin regulates clathrin-mediated endocytosis. The Journal of cell biology, 158(2), 209-14. [PubMed:12119359] [PMC] [WorldCat] [DOI] - ↑
Schaefer, A.W., Kamei, Y., Kamiguchi, H., Wong, E.V., Rapoport, I., Kirchhausen, T., ..., & Lemmon, V. (2002).
L1 endocytosis is controlled by a phosphorylation-dephosphorylation cycle stimulated by outside-in signaling by L1. The Journal of cell biology, 157(7), 1223-32. [PubMed:12082080] [PMC] [WorldCat] [DOI] - ↑
Shiratori, T., Miyatake, S., Ohno, H., Nakaseko, C., Isono, K., Bonifacino, J.S., & Saito, T. (1997).
Tyrosine phosphorylation controls internalization of CTLA-4 by regulating its interaction with clathrin-associated adaptor complex AP-2. Immunity, 6(5), 583-9. [PubMed:9175836] [WorldCat] [DOI] - ↑ 30.0 30.1
Matsuda, S., Kakegawa, W., Budisantoso, T., Nomura, T., Kohda, K., & Yuzaki, M. (2013).
Stargazin regulates AMPA receptor trafficking through adaptor protein complexes during long-term depression. Nature communications, 4, 2759. [PubMed:24217640] [WorldCat] [DOI] - ↑
Jockusch, W.J., Praefcke, G.J., McMahon, H.T., & Lagnado, L. (2005).
Clathrin-dependent and clathrin-independent retrieval of synaptic vesicles in retinal bipolar cells. Neuron, 46(6), 869-78. [PubMed:15953416] [WorldCat] [DOI] - ↑
Jung, N., Wienisch, M., Gu, M., Rand, J.B., Müller, S.L., Krause, G., ..., & Haucke, V. (2007).
Molecular basis of synaptic vesicle cargo recognition by the endocytic sorting adaptor stonin 2. The Journal of cell biology, 179(7), 1497-510. [PubMed:18166656] [PMC] [WorldCat] [DOI] - ↑
Owen, D.J., & Evans, P.R. (1998).
A structural explanation for the recognition of tyrosine-based endocytotic signals. Science (New York, N.Y.), 282(5392), 1327-32. [PubMed:9812899] [PMC] [WorldCat] [DOI] - ↑
Ohno, H., Aguilar, R.C., Yeh, D., Taura, D., Saito, T., & Bonifacino, J.S. (1998).
The medium subunits of adaptor complexes recognize distinct but overlapping sets of tyrosine-based sorting signals. The Journal of biological chemistry, 273(40), 25915-21. [PubMed:9748267] [WorldCat] [DOI] - ↑
Mitsunari, T., Nakatsu, F., Shioda, N., Love, P.E., Grinberg, A., Bonifacino, J.S., & Ohno, H. (2005).
Clathrin adaptor AP-2 is essential for early embryonal development. Molecular and cellular biology, 25(21), 9318-23. [PubMed:16227583] [PMC] [WorldCat] [DOI] - ↑
Dell'Angelica, E.C., Klumperman, J., Stoorvogel, W., & Bonifacino, J.S. (1998).
Association of the AP-3 adaptor complex with clathrin. Science (New York, N.Y.), 280(5362), 431-4. [PubMed:9545220] [WorldCat] [DOI] - ↑
Peden, A.A., Rudge, R.E., Lui, W.W., & Robinson, M.S. (2002).
Assembly and function of AP-3 complexes in cells expressing mutant subunits. The Journal of cell biology, 156(2), 327-36. [PubMed:11807095] [PMC] [WorldCat] [DOI] - ↑
Asensio, C.S., Sirkis, D.W., Maas, J.W., Egami, K., To, T.L., Brodsky, F.M., ..., & Edwards, R.H. (2013).
Self-assembly of VPS41 promotes sorting required for biogenesis of the regulated secretory pathway. Developmental cell, 27(4), 425-37. [PubMed:24210660] [PMC] [WorldCat] [DOI] - ↑
Baust, T., Anitei, M., Czupalla, C., Parshyna, I., Bourel, L., Thiele, C., ..., & Hoflack, B. (2008).
Protein networks supporting AP-3 function in targeting lysosomal membrane proteins. Molecular biology of the cell, 19(5), 1942-51. [PubMed:18287518] [PMC] [WorldCat] [DOI] - ↑ 40.0 40.1
Nakatsu, F., Okada, M., Mori, F., Kumazawa, N., Iwasa, H., Zhu, G., ..., & Ohno, H. (2004).
Defective function of GABA-containing synaptic vesicles in mice lacking the AP-3B clathrin adaptor. The Journal of cell biology, 167(2), 293-302. [PubMed:15492041] [PMC] [WorldCat] [DOI] - ↑
Asensio, C.S., Sirkis, D.W., & Edwards, R.H. (2010).
RNAi screen identifies a role for adaptor protein AP-3 in sorting to the regulated secretory pathway. The Journal of cell biology, 191(6), 1173-87. [PubMed:21149569] [PMC] [WorldCat] [DOI] - ↑
Li, P., Merrill, S.A., Jorgensen, E.M., & Shen, K. (2016).
Two Clathrin Adaptor Protein Complexes Instruct Axon-Dendrite Polarity. Neuron, 90(3), 564-80. [PubMed:27151641] [PMC] [WorldCat] [DOI] - ↑
Kantheti, P., Qiao, X., Diaz, M.E., Peden, A.A., Meyer, G.E., Carskadon, S.L., ..., & Burmeister, M. (1998).
Mutation in AP-3 delta in the mocha mouse links endosomal transport to storage deficiency in platelets, melanosomes, and synaptic vesicles. Neuron, 21(1), 111-22. [PubMed:9697856] [WorldCat] [DOI] - ↑
Ammann, S., Schulz, A., Krägeloh-Mann, I., Dieckmann, N.M., Niethammer, K., Fuchs, S., ..., & Ehl, S. (2016).
Mutations in AP3D1 associated with immunodeficiency and seizures define a new type of Hermansky-Pudlak syndrome. Blood, 127(8), 997-1006. [PubMed:26744459] [WorldCat] [DOI] - ↑
Dell'Angelica, E.C., Shotelersuk, V., Aguilar, R.C., Gahl, W.A., & Bonifacino, J.S. (1999).
Altered trafficking of lysosomal proteins in Hermansky-Pudlak syndrome due to mutations in the beta 3A subunit of the AP-3 adaptor. Molecular cell, 3(1), 11-21. [PubMed:10024875] [WorldCat] [DOI] - ↑
Assoum, M., Philippe, C., Isidor, B., Perrin, L., Makrythanasis, P., Sondheimer, N., ..., & Thevenon, J. (2016).
Autosomal-Recessive Mutations in AP3B2, Adaptor-Related Protein Complex 3 Beta 2 Subunit, Cause an Early-Onset Epileptic Encephalopathy with Optic Atrophy. American journal of human genetics, 99(6), 1368-1376. [PubMed:27889060] [PMC] [WorldCat] [DOI] - ↑
Simmen, T., Höning, S., Icking, A., Tikkanen, R., & Hunziker, W. (2002).
AP-4 binds basolateral signals and participates in basolateral sorting in epithelial MDCK cells. Nature cell biology, 4(2), 154-9. [PubMed:11802162] [WorldCat] [DOI] - ↑ 48.0 48.1
Matsuda, S., Miura, E., Matsuda, K., Kakegawa, W., Kohda, K., Watanabe, M., & Yuzaki, M. (2008).
Accumulation of AMPA receptors in autophagosomes in neuronal axons lacking adaptor protein AP-4. Neuron, 57(5), 730-45. [PubMed:18341993] [WorldCat] [DOI] - ↑
Burgos, P.V., Mardones, G.A., Rojas, A.L., daSilva, L.L., Prabhu, Y., Hurley, J.H., & Bonifacino, J.S. (2010).
Sorting of the Alzheimer's disease amyloid precursor protein mediated by the AP-4 complex. Developmental cell, 18(3), 425-36. [PubMed:20230749] [PMC] [WorldCat] [DOI] - ↑
Mattera, R., Park, S.Y., De Pace, R., Guardia, C.M., & Bonifacino, J.S. (2017).
AP-4 mediates export of ATG9A from the trans-Golgi network to promote autophagosome formation. Proceedings of the National Academy of Sciences of the United States of America, 114(50), E10697-E10706. [PubMed:29180427] [PMC] [WorldCat] [DOI] - ↑
Hirst, J., Bright, N.A., Rous, B., & Robinson, M.S. (1999).
Characterization of a fourth adaptor-related protein complex. Molecular biology of the cell, 10(8), 2787-802. [PubMed:10436028] [PMC] [WorldCat] [DOI] - ↑
Dell'Angelica, E.C., Mullins, C., & Bonifacino, J.S. (1999).
AP-4, a novel protein complex related to clathrin adaptors. The Journal of biological chemistry, 274(11), 7278-85. [PubMed:10066790] [WorldCat] [DOI] - ↑
Abou Jamra, R., Philippe, O., Raas-Rothschild, A., Eck, S.H., Graf, E., Buchert, R., ..., & Colleaux, L. (2011).
Adaptor protein complex 4 deficiency causes severe autosomal-recessive intellectual disability, progressive spastic paraplegia, shy character, and short stature. American journal of human genetics, 88(6), 788-795. [PubMed:21620353] [PMC] [WorldCat] [DOI] - ↑
Hardies, K., May, P., Djémié, T., Tarta-Arsene, O., Deconinck, T., Craiu, D., ..., & Hirst, J. (2015).
Recessive loss-of-function mutations in AP4S1 cause mild fever-sensitive seizures, developmental delay and spastic paraplegia through loss of AP-4 complex assembly. Human molecular genetics, 24(8), 2218-27. [PubMed:25552650] [PMC] [WorldCat] [DOI] - ↑
Moreno-De-Luca, A., Helmers, S.L., Mao, H., Burns, T.G., Melton, A.M., Schmidt, K.R., ..., & Martin, C.L. (2011).
Adaptor protein complex-4 (AP-4) deficiency causes a novel autosomal recessive cerebral palsy syndrome with microcephaly and intellectual disability. Journal of medical genetics, 48(2), 141-4. [PubMed:20972249] [PMC] [WorldCat] [DOI] - ↑
Verkerk, A.J., Schot, R., Dumee, B., Schellekens, K., Swagemakers, S., Bertoli-Avella, A.M., ..., & Mancini, G.M. (2009).
Mutation in the AP4M1 gene provides a model for neuroaxonal injury in cerebral palsy. American journal of human genetics, 85(1), 40-52. [PubMed:19559397] [PMC] [WorldCat] [DOI] - ↑
Tessa, A., Battini, R., Rubegni, A., Storti, E., Marini, C., Galatolo, D., ..., & Santorelli, F.M. (2016).
Identification of mutations in AP4S1/SPG52 through next generation sequencing in three families. European journal of neurology, 23(10), 1580-7. [PubMed:27444738] [WorldCat] [DOI] - ↑
Kong, X.F., Bousfiha, A., Rouissi, A., Itan, Y., Abhyankar, A., Bryant, V., ..., & Boisson-Dupuis, S. (2013).
A novel homozygous p.R1105X mutation of the AP4E1 gene in twins with hereditary spastic paraplegia and mycobacterial disease. PloS one, 8(3), e58286. [PubMed:23472171] [PMC] [WorldCat] [DOI] - ↑
Hirst, J., Irving, C., & Borner, G.H. (2013).
Adaptor protein complexes AP-4 and AP-5: new players in endosomal trafficking and progressive spastic paraplegia. Traffic (Copenhagen, Denmark), 14(2), 153-64. [PubMed:23167973] [WorldCat] [DOI] - ↑
Hirst, J., Itzhak, D.N., Antrobus, R., Borner, G.H.H., & Robinson, M.S. (2018).
Role of the AP-5 adaptor protein complex in late endosome-to-Golgi retrieval. PLoS biology, 16(1), e2004411. [PubMed:29381698] [PMC] [WorldCat] [DOI] - ↑
Hirst, J., Borner, G.H., Edgar, J., Hein, M.Y., Mann, M., Buchholz, F., ..., & Robinson, M.S. (2013).
Interaction between AP-5 and the hereditary spastic paraplegia proteins SPG11 and SPG15. Molecular biology of the cell, 24(16), 2558-69. [PubMed:23825025] [PMC] [WorldCat] [DOI] - ↑
Hirst, J., Edgar, J.R., Esteves, T., Darios, F., Madeo, M., Chang, J., ..., & Robinson, M.S. (2015).
Loss of AP-5 results in accumulation of aberrant endolysosomes: defining a new type of lysosomal storage disease. Human molecular genetics, 24(17), 4984-96. [PubMed:26085577] [PMC] [WorldCat] [DOI] - ↑
Renvoisé, B., Chang, J., Singh, R., Yonekawa, S., FitzGibbon, E.J., Mankodi, A., ..., & Pierson, T.M. (2014).
Lysosomal abnormalities in hereditary spastic paraplegia types SPG15 and SPG11. Annals of clinical and translational neurology, 1(6), 379-389. [PubMed:24999486] [PMC] [WorldCat] [DOI]