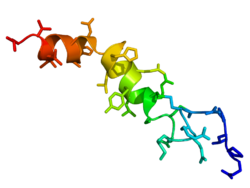
オレキシン
櫻井 武
金沢大学 医薬保健研究域 医学系 医薬保健研究域 医学系
DOI:10.14931/bsd.2302 原稿受付日:2013年2月28日 原稿完成日:2013年8月12日
担当編集委員:林 康紀(独立行政法人理化学研究所 脳科学総合研究センター)
英語名:orexin
同義語:ヒポクレチン (hypocretin)
オレキシンとは、神経ペプチドの一種である。摂食中枢として知られる視床下部外側野限局するニューロンに局在し、またラットやマウスに脳室内投与すると摂食量が上昇すること、絶食によって発現が亢進することなどから、当初、摂食行動の制御因子の一つとして注目を浴びた。その後、オレキシンやその受容体の変異動物モデルの解析、および臨床的研究によりオレキシン産生ニューロンの変性・脱落がナルコレプシーの原因であることが明らかになり、この物質が覚醒の維持にも重要な役割を担っていることが明らかになった。さらに、各種遺伝子改変マウスの解析によるオレキシン産生ニューロンの入出力系の解明により、大脳辺縁系、摂食行動の制御系、覚醒制御システムとの相互の関係が明らかになった。オレキシン系は睡眠・覚醒調節機構の重要な要素であるだけでなく、情動やエネルギーバランスに応じ、睡眠・覚醒や報酬系そして摂食行動を適切に制御する統合的な機能を担っている。
オレキシンとは
オレキシンはオーファンGタンパク質共役型受容体(GPCR)を用いた新規生理活性物質の探索により同定された[1]。オレキシンA (orexin A)とオレキシンB(orexin B)の二つのイソペプチドが存在する。同時期に、視床下部に特異的に発現するmRNAから推測されたペプチド前駆体より、二つの神経ペプチドが予測されヒポクレチン-1、ヒポクレチン-2として発表されているが、オレキシンAおよびBと同じものである(当初論文のヒポクレチンの構造の推測には間違いがあったが現在ではオレキシンと同義語として用いられている。)
オレキシンは摂食行動の制御系と睡眠・覚醒の制御系の両者と深い関係をもっている[1] [2]。オレキシンと報酬系との関連も示唆されており、情動や体内時計、エネルギー恒常性を統合した情報をもとに、適切な睡眠・覚醒状態をサポートする機能をもっていると考えられる[2]。
行動を制御するには覚醒の維持が必須であるが、オレキシンはさまざまな行動をサポートするために、覚醒を維持する機能をはたしている。一方、オレキシンの機能障害はナルコレプシーなどの過眠症に、機能亢進は不眠症などの病態に結び付くと予想される。
構造
オレキシンAは33アミノ酸からなり、分子内に2対のジスルフィド結合を有する。N末端はピログルタミン酸、C末端はアミド化されており、きわめて安定な構造をもっている。従って脳内での半減期も作用時間も神経ペプチドとしては例外的に長い。一方、オレキシンBは28アミノ酸残基の直線状のペプチドである。これら二つのペプチドは共通の前駆体(プレプロオレキシン:prepro-orexin)からプロホルモン変換酵素によって生成されると考えられる。これらは二つのGタンパク質共役型受容体、オレキシン1受容体(OX1R)およびオレキシン2受容体(OX2R)に作用する[1]。
サブファミリー
オレキシンA (orexin A)とオレキシンB(orexin B)の二つのイソペプチドが存在する。Orexin Aはhypocretin-1、orexin-Bはhypocretin-2に相当する。
| ||||||||
| 遺伝子名はAllen Brain Atlasのin situハイブリダイゼーションデーターへのリンク |
発現(組織分布、細胞内分布)
オレキシンAとオレキシンBは同一の前駆体から切り出されるため、同じ細胞によって発現される。オレキシン産生ニューロンは視床下部の「摂食中枢」とされる視床下部外側野(lateral hypothalamic area: LHA)を中心にその近傍の視床下部脳弓周囲野(perifornical area)、そして視床下部後部(posterior hypothalamus:PH)に存在する[3] [4]。
これらのニューロンは他のニューロンと混在しながら散在している。たとえばMCHを作るニューロンも似た領域に存在するが両者は別々の集団である。一方、ダイノルフィンやニューロテンシンはオレキシン産生ニューロンに共存している。またオレキシン産生ニューロンはグルタミン酸作動性ニューロンのマーカーであるvGluT2を発現しており、グルタミン酸作動性ニューロンでもあると考えられている。
オレキシン産生ニューロンの数はマウスで数千個、ヒトで70000個ほどといわれている。これらのニューロンから伸びる軸索は、数多く分枝しつつきわめて広範な領域に投射している[3]。
機能
オレキシンはMulti-takingなファクターであり、さまざまな機能を持っていると考えられている。摂食行動、自律神経系、内分泌、報酬系などその機能は多岐にわたる。ただし、オレキシンを脳室内投与した結果見られる摂食量の亢進、交感神経系の興奮、HPA軸の活性化、ドーパミンニューロンの興奮などは、すべて覚醒に応じて引き起こされる現象、あるいは覚醒が引き起こされた結果ととらえることも可能でもあり、オレキシンのもっとも中心的な役割は覚醒の維持にあると考えられている。
1999年、動物モデルからナルコレプシーとオレキシン欠損の関連が示唆され、オレキシンと覚醒の関連は強く支持されることになった。遺伝性のナルコレプシーのイヌでは複数の系統にOX2受容体の遺伝子に突然変異が見いだされた[5]。また、オレキシン遺伝子欠損マウス、OX2受容体遺伝子欠損マウス、そしてオレキシン産生ニューロンを特異的に欠損させたorexin-ataxin3トランスジェニックマウスは、ヒトのナルコレプシーと似た睡眠・覚醒の分断化とカタプレキシー様発作を示す[6] [7]。
さらにはヒトのナルコレプシー患者の髄液中のオレキシン濃度の顕著な低下が報告され[3]、また死後脳においてオレキシン産生ニューロンが消失していることがしめされた[4]。現在、患者の90%以上に髄液中のオレキシンA濃度の著しい低下がみられることが明らかになっており[8]、アメリカでは2005年より髄液中のオレキシンA濃度はナルコレプシーの診断基準にとり入れられている。このように、ナルコレプシーがオレキシンの欠損によって引き起こされることが明らかになったことから、オレキシンは種をこえて「睡眠・覚醒状態の安定化」に重要な働きをもっていることが明らかになっている。
受容体
オレキシンAとオレキシンBは二つのGタンパク質共役型受容体、オレキシン1受容体(OX1R)およびオレキシン2受容体(OX2R)に作用する[1]。一般にどちらの受容体を介する作用も受容体発現ニューロンに対して強力かつ持続的な興奮性作用を示す。
後で述べるオレキシン作動性ニューロンの投射領域に一致してOX1RおよびOX2Rも分布するが、脳内の組織分布はサブタイプにより異なる[9]。青斑核(locus coeruleus: LC、ノルアドレナリン作動性)ではOX1Rのみが発現しているのに対し、結節乳頭体核(tuberomamillary nucleus: TMN、ヒスタミン作動性)ではOX2Rのみが発現している。また、背側縫線核(dorsal raphe nucleus:DR、セロトニン作動性)や橋被蓋に局在するコリン作動性神経の起始核、外背側被蓋核(laterodorsal tegmental nucleus: LDT)や脚橋被蓋核(pedunculopontine tegmental nucleus: PPT)には両方の受容体が発現している。
DRではセロトニン作動性ニューロンに両方の受容体が発現しており、LDT/PPTでは、コリン作動性ニューロンにはOX1Rのみが発現しており、GABA作動性介在ニューロンには両方の受容体が発現している。これらのことは、2つのオレキシン受容体が明確に別々の役割をしていることを示唆している[10]。オレキシン受容体拮抗薬は理想的な睡眠導入薬として期待されており、2014年8月1日非選択性オレキシン受容体拮抗薬であるスボレキサント (suvorexant)が厚生労働省の薬事・食品衛生審議会医薬品第一部会の承認を受けた。
関連項目
参考文献
- ↑ 1.0 1.1 1.2 1.3
Sakurai, T., Amemiya, A., Ishii, M., Matsuzaki, I., Chemelli, R.M., Tanaka, H., ..., & Yanagisawa, M. (1998).
Orexins and orexin receptors: a family of hypothalamic neuropeptides and G protein-coupled receptors that regulate feeding behavior. Cell, 92(4), 573-85. [PubMed:9491897] [WorldCat] [DOI] - ↑ 2.0 2.1
Sakurai, T. (2007).
The neural circuit of orexin (hypocretin): maintaining sleep and wakefulness. Nature reviews. Neuroscience, 8(3), 171-81. [PubMed:17299454] [WorldCat] [DOI] - ↑ 3.0 3.1 3.2
Nishino, S., Ripley, B., Overeem, S., Lammers, G.J., & Mignot, E. (2000).
Hypocretin (orexin) deficiency in human narcolepsy. Lancet (London, England), 355(9197), 39-40. [PubMed:10615891] [WorldCat] [DOI] - ↑ 4.0 4.1
Peyron, C., Faraco, J., Rogers, W., Ripley, B., Overeem, S., Charnay, Y., ..., & Mignot, E. (2000).
A mutation in a case of early onset narcolepsy and a generalized absence of hypocretin peptides in human narcoleptic brains. Nature medicine, 6(9), 991-7. [PubMed:10973318] [WorldCat] [DOI] - ↑
Lin, L., Faraco, J., Li, R., Kadotani, H., Rogers, W., Lin, X., ..., & Mignot, E. (1999).
The sleep disorder canine narcolepsy is caused by a mutation in the hypocretin (orexin) receptor 2 gene. Cell, 98(3), 365-76. [PubMed:10458611] [WorldCat] [DOI] - ↑
Chemelli, R.M., Willie, J.T., Sinton, C.M., Elmquist, J.K., Scammell, T., Lee, C., ..., & Yanagisawa, M. (1999).
Narcolepsy in orexin knockout mice: molecular genetics of sleep regulation. Cell, 98(4), 437-51. [PubMed:10481909] [WorldCat] [DOI] - ↑
Willie, J.T., Chemelli, R.M., Sinton, C.M., Tokita, S., Williams, S.C., Kisanuki, Y.Y., ..., & Yanagisawa, M. (2003).
Distinct narcolepsy syndromes in Orexin receptor-2 and Orexin null mice: molecular genetic dissection of Non-REM and REM sleep regulatory processes. Neuron, 38(5), 715-30. [PubMed:12797957] [WorldCat] [DOI] - ↑
Mignot, E., Lammers, G.J., Ripley, B., Okun, M., Nevsimalova, S., Overeem, S., ..., & Nishino, S. (2002).
The role of cerebrospinal fluid hypocretin measurement in the diagnosis of narcolepsy and other hypersomnias. Archives of neurology, 59(10), 1553-62. [PubMed:12374492] [WorldCat] [DOI] - ↑
Marcus, J.N., Aschkenasi, C.J., Lee, C.E., Chemelli, R.M., Saper, C.B., Yanagisawa, M., & Elmquist, J.K. (2001).
Differential expression of orexin receptors 1 and 2 in the rat brain. The Journal of comparative neurology, 435(1), 6-25. [PubMed:11370008] [WorldCat] [DOI] - ↑
Mieda, M., Hasegawa, E., Kisanuki, Y.Y., Sinton, C.M., Yanagisawa, M., & Sakurai, T. (2011).
Differential roles of orexin receptor-1 and -2 in the regulation of non-REM and REM sleep. The Journal of neuroscience : the official journal of the Society for Neuroscience, 31(17), 6518-26. [PubMed:21525292] [PMC] [WorldCat] [DOI]
| |||||||||||||||||||||||||||||||||||||||||