脚橋被蓋核
小林 康
大阪大学 大学院生命機能研究科 脳神経工学講座
DOI:10.14931/bsd.1470 原稿受付日:2013年5月11日 原稿完成日:2015年4月24日
担当編集委員:一戸 紀孝(国立精神・神経医療研究センター 神経研究所)
英語名:pedunculopontine tegmental nucleus、pedunculopontine nucleus 羅:nucleus tegmentalis pedunculopontinus、nucleus pedunculopontinus
英略称:PPN、PPTg、PPTN
脚橋被蓋核とは脳幹にある神経核である。上小脳脚を取り囲み、黒質の尾側に位置する。アセチルコリン作動性ニューロンが豊富に存在する他、グルタミン酸作動性、GABA作動性、各種の神経ペプチドを産生するニューロンなどが混在する。脚橋被蓋核ニューロンは主に大脳皮質、基底核より入力を受け、視床や視蓋、基底核、脳幹網様体へ投射する。したがって脚橋被蓋核は基底核-大脳皮質ループおよび網様体脊髄路系を介して運動の発現や姿勢筋活動の制御に関与するとともに、視床-大脳、大脳基底核投射や網様体賦活系を介して意識レベルや睡眠・覚醒、注意、動機付け、学習の調節に関わっていると考えられている。
脚橋被蓋核とは
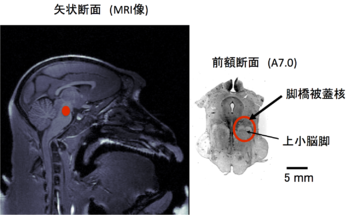
脳幹の神経核であり、ヒトの脳において最初に同定された[1]。 上小脳脚を取り囲み、黒質の尾側に位置する(図1)。
中枢神経系のアセチルコリン神経は、マイネルト核を含む前脳基底部細胞群と脚橋被蓋核を中心とする脚橋被蓋細胞群に大別されるが、脚橋被蓋核は近傍の背外側被蓋核(laterodorsal tegmental nucleus; LDT)と並び脳幹内でアセチルコリン作動性ニューロンが豊富に存在する核である[2][3][4][5]。
脚橋被蓋核ニューロンは主に大脳皮質領域、基底核領域より入力を受け、視床や視蓋領域、基底核領域、脳幹網様体へ投射する[3][5]。したがって脚橋被蓋核は基底核-大脳皮質ループおよび網様体脊髄路系を介して運動の発現や姿勢筋活動の制御に関与するとともに、視床-大脳、大脳基底核投射や網様体賦活系を介して意識レベルや睡眠・覚醒、注意、動機付け、学習の調節に関わっていると考えられている。
実際に、脚橋被蓋核を局所微小電気刺激すると、皮質のアセチルコリン量が上昇する[6]、黒質の活動レベルが上昇し[7]その結果、線条体でのドーパミン量が上昇する[8]ことが知られている。これと共に 歩行運動が誘発され[9]、また皮質の脳波が覚醒的な状態になる[10]。
構造
位置
脚橋被蓋核は中脳網様体の尾外側部を形成する。上小脳脚を取り囲み、黒質の尾側に位置する(図1)。
局所回路
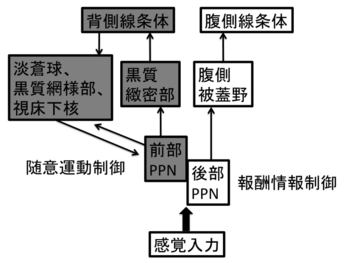
それぞれの細胞は伝達物質・発火様式・線維投射などが異なることから、脚橋被蓋核は複数の細胞群、つまり、複数の機能的単位から構成されていると考えられている(図2)。小型のニューロンが疎に集合する前部分と大型のニューロンが密に集合する後部分がある。脚橋被蓋核前部は消散部 (pars dissipata)、後部は緻密部 (pars compacta)と命名されており、前部にはアセチルコリン、非アセチルコリン作動性ニューロンが混在し、後部は主にアセチルコリン作動性ニューロンが多く存在する(Ch5グループとも呼ばれる)。その他、グルタミン酸作動性ニューロン、GABA作動性ニューロンや、各種の神経ペプチドを産生するニューロンなどが混在する[11]。脚橋被蓋核ではアセチルコリンとグルタミン酸の双方が同一ニューロンの中に混在することなども明らかにされている[4]。
ラット脳幹スライス標本を用いた脚橋被蓋核細胞の細胞内記録より、脚橋被蓋核細胞の発火活動は大きく2群に分けられる。
前者はほぼすべてが非コリン細胞、後者の3分の2がコリン細胞である。また後者の細胞はスパイク幅の狭い細胞と幅の広い細胞の2つのサブタイプから構成される。
- スパイク幅の狭い細胞は発火頻度が高く(8-20Hz)、小、中型の細胞体を持ち、脚橋被蓋核にほぼ均等に分布する。
- スパイク幅の広い細胞は発火頻度が低く(3-10Hz)、大型の細胞体を持ち、脚橋被蓋核の尾側部に位置する。コリン細胞の平均自発発射頻度は約10Hzである。
入出力
脚橋被蓋核への線維入力は、主に大脳皮質、扁桃体、黒質網様部、淡蒼球、視床下核などが由来である。なお、脚橋被蓋核はこれら大脳基底核群と双方性結合をもっている[15][16]。この大脳基底核群との密接な結合関係から、最近では脚橋被蓋核が大脳基底核群の一部として議論されることもある [16]。また、脚橋被蓋核の後部と前部で機能が分かれていると考えられている[17]。
さらに、脚橋被蓋核は脳幹のモノアミンシステム(青斑核:ノルアドレナリン作動性、 縫線核:セロトニン作動性)とも双方的に結合がある[18]。 この、「大脳基底核-脚橋被蓋核-カテコールアミンシステム複合体」が随意運動や、様々な選択的注意に関係した行動をトリガーしていると考えられている[19]。これらに限らず、脚橋被蓋核ニューロンは非常に広範な投射を示す。その投射先は、黒質緻密部、腹側被蓋野、視床下核など大脳基底核の構成要素や、視床、上丘、脊髄、橋、脳幹網様体、運動性三叉神経核、前脳基底部、などである[3][5][20][21][12][22]。
さらに、脚橋被蓋核細胞のコリン細胞、非コリン細胞共に、
- 視床・視蓋前野・上丘方向への上行性投射
- 基底核特に黒質緻密部・視床下核方向への吻側性投射
- 中脳・橋網様体への下行性投射
を持つことが知られている。基底核領域や視床方向へ投射する細胞は脚橋被蓋核の吻側部に、視蓋領域,中脳・橋網様体へ投射する細胞は尾側部に分布する傾向がある。
機能
運動機能
運動の実行系が存在する脳幹、脊髄と高次機能を司る大脳、大脳基底核、小脳との間には脚橋被蓋核を介して密接な線維連絡が存在する。したがって、脚橋被蓋核は運動実行系と高次機能を統合するintegrative interfaceと考えることができる。
脚橋被蓋核の後方でアセチルコリン細胞を多く含む緻密部は中脳歩行中枢または中脳歩行誘発野として知られている領域にほぼ一致する。中脳歩行誘発野を電気刺激するとトレッドミル上の動物が自然な形の歩行運動を行う[9]。この領域からの上行性投射は、いわゆる錐体外路系神経回路の視床、大脳皮質にフィードバックされるが、下行性投射線維は、菱脳網様体に達して、特に延髄網様体と脊髄に終止する。これが脚橋被蓋核を介して歩行、姿勢制御に関係していると思われる。
大脳・大脳基底核の出力は脚橋被蓋核を介してどのように運動の実行系を制御しているのであろうか。高草木らは、脚橋被蓋核から橋網様体へのコリン作動性投射が姿勢筋活動の調節に関与していることを明らかにした[23][24]。姿勢筋活動の抑制系は橋網様体から始まり,両側延髄網様体の網様体脊髄路細胞と脊髄の抑制性介在細胞を介して伸筋・屈筋の運動ニューロンの活動を抑制する。また、松村らはサルの手の随意運動と脚橋被蓋核細胞の発火活動の関連を解析した[25]。そして、多くのニューロンが記録側あるいは反対側の手の運動に際して発火活動を変化させることなどを明らかにした。この結果は脚橋被蓋核に両側肢の随意運動の発現に関与するいくつかの機能的単位が存在することを示唆する。またGABAのアゴニストのムシモールを脚橋被蓋核に微量注入すると、運動開始の遅延や運動速度の減少が観察され、このことは随意運動の開始や運動ダイナミクスを制御する上で、基底核(淡蒼球内節、黒質網様部)からのGABA作動性入力が重要な役割を担うことを推定させる。また、脚橋被蓋核から視床および上丘への上行性投射[26]、また脚橋被蓋核への上丘からの入力があり[27]、脚橋被蓋核でサルの行動の文脈依存的なサッケード(衝動性眼球運動)の準備、実行に関係した活動がみられることが知られている[28][29]。
このように脚橋被蓋核から視床および上丘、基底核(特に黒質緻密部)への上行性投射、そして橋網様体への下行性投射が存在し、また脚橋被蓋核は基底核の黒質網様部や淡蒼球内節からGABA作動性の抑制を受ける。したがって、脚橋被蓋核の機能低下が生じると、黒質緻密部から線条体へ投射するドーパミン作動系の活動は低下し、黒質網様部や淡蒼球内節へ投射する間接路の活動充進と直接路の活動低下が誘発され、その結果、淡蒼球内節・黒質網様部から脚橋被蓋核へのGABA抑制が増強すると思われる。脚橋被蓋核が姿勢反射や歩行運動の制御に関連することや上丘への投射系を介して眼球運動の制御にも関与する可能性を考慮すると、脚橋被蓋核の障害により、姿勢の異常や歩行運動、眼球運動の障害などが発現すると考えられる。また、サルの片側脚橋被蓋核にカイニン酸を注入すると、反対側の上肢と下肢の運動低下が発現することが知られている[30]。
睡眠・覚醒の制御
睡眠・覚醒は覚醒時に発火頻度が低く、レム睡眠時に発火頻度を増大する脚橋被蓋核のアセチルコリン性の細胞群と、覚醒時に発火頻度が高く、レム睡眠時に発火活動が低下する縫線核のセロトニン性、青斑核のノルアドレナリン性の細胞群の相互作用により制御されていると考えられている。脚橋被蓋核では覚醒睡眠に伴って発火特性の異なる2種類のアセチルコリン細胞群が存在することが知られている[21]。一方はスパイク幅が広く、覚醒時には発射せず、徐波睡眠からレム睡眠にかけて徐々に発火頻度を増加させる(<10Hz)細胞群であり、もう一方はスパイク幅が狭く、覚醒時とレム睡眠時に発火を示し(20-30Hz)、特に徐波睡眠からレム睡眠の移行期に発火を一過性に増大させる細胞群である。橋網様体には脚橋被蓋核からのアセチルコリン性線維が投射しており、ネコの橋網様体にアセチルコリン作動薬を注入すると、注入後数分以内に皮質脳波の脱同期、急速眼球運動を伴ったレム睡眠が誘発されることが知られている[10]。このように、脚橋被蓋核からのアセチルコリン作動性経路が運動機能のみならず、睡眠・覚醒の制御や意識レベルの調節にも関与することを示唆する。
強化学習、動機付け
手がかり刺激から適切な行動予測を行い、最大報酬を得る「報酬に基づく強化学習[31]」の神経生理学的研究の発展には神経科学のみならず広い分野から注目が集まっている。黒質緻密部や腹側被蓋野のドーパミンニューロンは報酬との連合で学習された手がかり刺激や報酬に対して一時的なバースト応答をすることによって大脳皮質、基底核などに報酬予測誤差(報酬に対する予測と現実に得られた報酬の差)を送り、強化学習における大脳皮質、大脳基底核でのシナプス可塑性を制御していると考えられている[31]。
強化学習機構を解明する上で、「報酬予測誤差がドーパミンニューロンでどのように計算されているのかということ」が生理学的、計算理論的に最も重要な問題の一つであると考えられる[32]。ドーパミンニューロンはドーパミン放出による投射部位のシナプス可塑性の制御[33]という形で強化学習に重要な役割を果たしているが、ドーパミンニューロンへの入力信号の性質が計算論的に明らかにされていないために、いまだに報酬予測誤差の計算過程がわかっていない。
脚橋被蓋核は大脳基底核[16]、視床下部外側野[34]、大脳皮質[35]、大脳辺縁系[36]などから報酬関連入力を受け取り、ドーパミンニューロンに多くの投射線維を送る[37]ことが知られている。脚橋被蓋核は黒質緻密部のドーパミンニューロンに対して強力な興奮性シナプス入力を供給している[38]。さらに、ドーパミンニューロンはその興奮性入力の主なものが脚橋被蓋核由来であることが知られている。Futamiらはラット脳幹スライス標本を用いて脚橋被蓋核刺激により黒質緻密部のドーパミンニューロンに誘発されるコリン作動性、グルタミン酸作動性入力の興奮作用を解析した。そして、コリン作動性の興奮作用は持続時間が長く(数百ms),グルタミン酸作動性のそれは持続時間が短いこと、2)また前者はムスカリン性アセチルコリン受容体(ムスカリン受容体)およびニコチン性アセチルコリン受容体(ニコチン受容体)を介し、後者はNMDA型グルタミン酸受容体と非NMDA型グルタミン酸受容体を介することなどを明らかにした。これらの結果と脚橋被蓋核ニューロンの律動的、非律動的な発火特性を考慮すると、アセチルコリン作動性の投射はドーパミンニューロンの興奮性を定常状態に維持する上で、グルタミン酸作動性の投射は、その興奮性を一過性に変動させる上で有効であると考えられる。また、さらに脚橋被蓋核の電気刺激によっておきる脚橋被蓋核からのアセチルコリン放出によってドーパミンニューロンのムスカリン受容体[39]、ニコチン受容体[40]の活性化が起こり、ドーパミンニューロンが一過性のバースト活動を引き起こすこと[7]などから、脚橋被蓋核からの興奮性入力がドーパミンニューロンにおける報酬情報処理過程に重要な役割を果たしていることが示唆される。
最近のげっ歯類を使用した破壊実験と薬物投与実験によって、脚橋被蓋核がさまざまな報酬による強化過程(摂食調節、ニコチン嗜癖、強化学習)に関与していることが示されている[41][42][43]。また、脚橋被蓋核を破壊するとドーパミンニューロンが機能しなくなる[44]ことが知られている。また、ネコを用いた生理実験によれば、脚橋被蓋核が条件けされた手がかり刺激や報酬に関係した活動を示し[45]、さらにリドカイン、ムシモールの局所注入による脚橋被蓋核の活動停止が一時的に動物の課題に対する動機付け(報酬への期待)を低下させることが示されている[18]。
岡田らが行った視覚誘導性サッケード課題中のサルのニューロン活動解析[28]によって、以下の2種類のニューロン活動が見つかった。
- 課題の達成度、あるいはサルの報酬期待度によって大きさが変わる、注視刺激呈示から始まり、報酬時まで続く持続的応答するニューロン
- 報酬期待の度合いに無関係で一時的な報酬に対する直接の応答するニューロン
ところで、脚橋被蓋核はどこから動機付け、報酬予測に関連した信号を受け取っているのだろうか。第一に興奮性信号は腹側線条体-腹側淡蒼球経路の二重抑制でやってくると思われる。この経路では脚橋被蓋核の興奮は二重抑制によって生じると思われる。第二に興奮性信号源が扁桃体や視床下核[34]である可能性が考えられる。また、第三に興奮性信号源が大脳皮質であるという可能性が考えられる。また、脚橋被蓋核は帯状回や前頭葉から報酬予測信号を受け取っていると思われる。
または岡田らは脚橋被蓋核で報酬予測には無関係で、与えられた報酬に関係したニューロン活動を記録した。この実報酬信号は視床下部外側野からやってくると思われる[46]。この経路は単シナプス性にPPTNを興奮させ[34]、一過性のバーストを生じさせる[45]。この脚橋被蓋核での一過性バーストが ドーパミンニューロンの「予期せぬ報酬に対する一時的な興奮性応答」を引き起こしているのかもしれない。今後これらのニューロン活動が強化学習に必要な実報酬信号のどの要素(報酬量の正確な計測、報酬予測との関連性)を表現しているのか明らかになると思われる。
疾患との関わり
脚橋被蓋核障害による「脚橋被蓋核から黒質緻密部のドーパミンニューロンへの興奮性投射の機能低下」と「黒質網様部から脚橋被蓋核細胞への抑制性投射の機能充進」がパーキンソン病における運動障害を発現させることを示唆する。最近、従来の視床下核を標的にした脳内深部刺激(Deep Brain Stimulation, DBS)のみならず、脚橋被蓋核を標的としたDBSがパーキンソン病による運動障害の改善に効果がある[47]という報告が数多くなされており、治療に向けた今後の研究が待たれる。
また最近松村はパーキンソン病との関連から脚橋被蓋核に対する大脳皮質由来(特に運動野)の入力に着目している[35]。
関連項目
参考文献
- ↑
Geula, C., Schatz, C.R., & Mesulam, M.M. (1993).
Differential localization of NADPH-diaphorase and calbindin-D28k within the cholinergic neurons of the basal forebrain, striatum and brainstem in the rat, monkey, baboon and human. Neuroscience, 54(2), 461-76. [PubMed:8336832] [WorldCat] [DOI] - ↑
Mesulam, M.M., Mufson, E.J., Wainer, B.H., & Levey, A.I. (1983).
Central cholinergic pathways in the rat: an overview based on an alternative nomenclature (Ch1-Ch6). Neuroscience, 10(4), 1185-201. [PubMed:6320048] [WorldCat] [DOI] - ↑ 3.0 3.1 3.2
Jackson, A., & Crossman, A.R. (1983).
Nucleus tegmenti pedunculopontinus: efferent connections with special reference to the basal ganglia, studied in the rat by anterograde and retrograde transport of horseradish peroxidase. Neuroscience, 10(3), 725-65. [PubMed:6646427] [WorldCat] [DOI] - ↑ 4.0 4.1
Lavoie, B., & Parent, A. (1994).
Pedunculopontine nucleus in the squirrel monkey: distribution of cholinergic and monoaminergic neurons in the mesopontine tegmentum with evidence for the presence of glutamate in cholinergic neurons. The Journal of comparative neurology, 344(2), 190-209. [PubMed:7915726] [WorldCat] [DOI] - ↑ 5.0 5.1 5.2
Mitani, A., Ito, K., Hallanger, A.E., Wainer, B.H., Kataoka, K., & McCarley, R.W. (1988).
Cholinergic projections from the laterodorsal and pedunculopontine tegmental nuclei to the pontine gigantocellular tegmental field in the cat. Brain research, 451(1-2), 397-402. [PubMed:3251602] [WorldCat] [DOI] - ↑
Szerb, J.C. (1967).
Cortical acetylcholine release and electroencephalographic arousal. The Journal of physiology, 192(2), 329-43. [PubMed:6050151] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1
Lokwan, S.J., Overton, P.G., Berry, M.S., & Clark, D. (1999).
Stimulation of the pedunculopontine tegmental nucleus in the rat produces burst firing in A9 dopaminergic neurons. Neuroscience, 92(1), 245-54. [PubMed:10392847] [WorldCat] [DOI] - ↑
Forster, G.L., & Blaha, C.D. (2003).
Pedunculopontine tegmental stimulation evokes striatal dopamine efflux by activation of acetylcholine and glutamate receptors in the midbrain and pons of the rat. The European journal of neuroscience, 17(4), 751-62. [PubMed:12603265] [WorldCat] [DOI] - ↑ 9.0 9.1
Mori, S., Sakamoto, T., Ohta, Y., Takakusaki, K., & Matsuyama, K. (1989).
Site-specific postural and locomotor changes evoked in awake, freely moving intact cats by stimulating the brainstem. Brain research, 505(1), 66-74. [PubMed:2611678] [WorldCat] [DOI] - ↑ 10.0 10.1
Boeve, B.F. (2010).
REM sleep behavior disorder: Updated review of the core features, the REM sleep behavior disorder-neurodegenerative disease association, evolving concepts, controversies, and future directions. Annals of the New York Academy of Sciences, 1184, 15-54. [PubMed:20146689] [PMC] [WorldCat] [DOI] 引用エラー: 無効な<ref>タグ; name "ref9"が異なる内容で複数回定義されています - ↑
Vincent, S.R., Satoh, K., Armstrong, D.M., & Fibiger, H.C. (1983).
Substance P in the ascending cholinergic reticular system. Nature, 306(5944), 688-91. [PubMed:6197654] [WorldCat] [DOI] - ↑ 12.0 12.1
Takakusaki, K., Shiroyama, T., Yamamoto, T., & Kitai, S.T. (1996).
Cholinergic and noncholinergic tegmental pedunculopontine projection neurons in rats revealed by intracellular labeling. The Journal of comparative neurology, 371(3), 345-61. [PubMed:8842892] [WorldCat] [DOI] - ↑
Takakusaki, K., & Kitai, S.T. (1997).
Ionic mechanisms involved in the spontaneous firing of tegmental pedunculopontine nucleus neurons of the rat. Neuroscience, 78(3), 771-94. [PubMed:9153657] [WorldCat] [DOI] - ↑
Takakusaki, K., Shiroyama, T., & Kitai, S.T. (1997).
Two types of cholinergic neurons in the rat tegmental pedunculopontine nucleus: electrophysiological and morphological characterization. Neuroscience, 79(4), 1089-109. [PubMed:9219969] [WorldCat] [DOI] - ↑
Edley, S.M., & Graybiel, A.M. (1983).
The afferent and efferent connections of the feline nucleus tegmenti pedunculopontinus, pars compacta. The Journal of comparative neurology, 217(2), 187-215. [PubMed:6886052] [WorldCat] [DOI] - ↑ 16.0 16.1 16.2
Mena-Segovia, J., Bolam, J.P., & Magill, P.J. (2004).
Pedunculopontine nucleus and basal ganglia: distant relatives or part of the same family? Trends in neurosciences, 27(10), 585-8. [PubMed:15374668] [WorldCat] [DOI] - ↑
Winn, P. (2008).
Experimental studies of pedunculopontine functions: are they motor, sensory or integrative? Parkinsonism & related disorders, 14 Suppl 2, S194-8. [PubMed:18585079] [WorldCat] [DOI] - ↑ 18.0 18.1
Koyama, Y., & Kayama, Y. (1993).
Mutual interactions among cholinergic, noradrenergic and serotonergic neurons studied by ionophoresis of these transmitters in rat brainstem nuclei. Neuroscience, 55(4), 1117-26. [PubMed:8232901] [WorldCat] [DOI] 引用エラー: 無効な<ref>タグ; name "ref46"が異なる内容で複数回定義されています - ↑
Garcia-Rill, E. (1991).
The pedunculopontine nucleus. Progress in neurobiology, 36(5), 363-89. [PubMed:1887068] [WorldCat] [DOI] - ↑
Semba, K., Reiner, P.B., & Fibiger, H.C. (1990).
Single cholinergic mesopontine tegmental neurons project to both the pontine reticular formation and the thalamus in the rat. Neuroscience, 38(3), 643-54. [PubMed:2176719] [WorldCat] [DOI] - ↑ 21.0 21.1
Steriade, M., Datta, S., Paré, D., Oakson, G., & Curró Dossi, R.C. (1990).
Neuronal activities in brain-stem cholinergic nuclei related to tonic activation processes in thalamocortical systems. The Journal of neuroscience : the official journal of the Society for Neuroscience, 10(8), 2541-59. [PubMed:2388079] [WorldCat] 引用エラー: 無効な<ref>タグ; name "ref17"が異なる内容で複数回定義されています - ↑
Tokuno, H., Moriizumi, T., Kudo, M., & Nakamura, Y. (1988).
A morphological evidence for monosynaptic projections from the nucleus tegmenti pedunculopontinus pars compacta (TPC) to nigrostriatal projection neurons. Neuroscience letters, 85(1), 1-4. [PubMed:3362403] [WorldCat] [DOI] - ↑
Takakusaki, K., Kohyama, J., Matsuyama, K., & Mori, S. (1993).
Synaptic mechanisms acting on lumbar motoneurons during postural augmentation induced by serotonin injection into the rostral pontine reticular formation in decerebrate cats. Experimental brain research, 93(3), 471-82. [PubMed:8519336] [WorldCat] [DOI] - ↑
Takakusaki, K., Shimoda, N., Matsuyama, K., & Mori, S. (1994).
Discharge properties of medullary reticulospinal neurons during postural changes induced by intrapontine injections of carbachol, atropine and serotonin, and their functional linkages to hindlimb motoneurons in cats. Experimental brain research, 99(3), 361-74. [PubMed:7957716] [WorldCat] [DOI] - ↑
Matsumura, M., Watanabe, K., & Ohye, C. (1997).
Single-unit activity in the primate nucleus tegmenti pedunculopontinus related to voluntary arm movement. Neuroscience research, 28(2), 155-65. [PubMed:9220472] [WorldCat] [DOI] - ↑
Woolf, N.J., & Butcher, L.L. (1986).
Cholinergic systems in the rat brain: III. Projections from the pontomesencephalic tegmentum to the thalamus, tectum, basal ganglia, and basal forebrain. Brain research bulletin, 16(5), 603-37. [PubMed:3742247] [WorldCat] [DOI] - ↑
Redgrave, P., Mitchell, I.J., & Dean, P. (1987).
Descending projections from the superior colliculus in rat: a study using orthograde transport of wheatgerm-agglutinin conjugated horseradish peroxidase. Experimental brain research, 68(1), 147-67. [PubMed:2826204] [WorldCat] [DOI] - ↑ 28.0 28.1
Kobayashi, Y., Inoue, Y., Yamamoto, M., Isa, T., & Aizawa, H. (2002).
Contribution of pedunculopontine tegmental nucleus neurons to performance of visually guided saccade tasks in monkeys. Journal of neurophysiology, 88(2), 715-31. [PubMed:12163524] [WorldCat] [DOI] 引用エラー: 無効な<ref>タグ; name "ref27"が異なる内容で複数回定義されています - ↑
Okada, K., & Kobayashi, Y. (2009).
Characterization of oculomotor and visual activities in the primate pedunculopontine tegmental nucleus during visually guided saccade tasks. The European journal of neuroscience, 30(11), 2211-23. [PubMed:20128856] [WorldCat] [DOI] - ↑
Kojima, J., Yamaji, Y., Matsumura, M., Nambu, A., Inase, M., Tokuno, H., ..., & Imai, H. (1997).
Excitotoxic lesions of the pedunculopontine tegmental nucleus produce contralateral hemiparkinsonism in the monkey. Neuroscience letters, 226(2), 111-4. [PubMed:9159502] [WorldCat] [DOI] - ↑ 31.0 31.1
Schultz, W. (1998).
Predictive reward signal of dopamine neurons. Journal of neurophysiology, 80(1), 1-27. [PubMed:9658025] [WorldCat] [DOI] - ↑
Doya, K. (2002).
Metalearning and neuromodulation. Neural networks : the official journal of the International Neural Network Society, 15(4-6), 495-506. [PubMed:12371507] [WorldCat] - ↑
Reynolds, J.N., Hyland, B.I., & Wickens, J.R. (2001).
A cellular mechanism of reward-related learning. Nature, 413(6851), 67-70. [PubMed:11544526] [WorldCat] [DOI] - ↑ 34.0 34.1 34.2
Semba, K., & Fibiger, H.C. (1992).
Afferent connections of the laterodorsal and the pedunculopontine tegmental nuclei in the rat: a retro- and antero-grade transport and immunohistochemical study. The Journal of comparative neurology, 323(3), 387-410. [PubMed:1281170] [WorldCat] [DOI] - ↑ 35.0 35.1
Matsumura, M. (2005).
The pedunculopontine tegmental nucleus and experimental parkinsonism. A review. Journal of neurology, 252 Suppl 4, IV5-IV12. [PubMed:16222438] [WorldCat] [DOI] - ↑
Chiba, T., Kayahara, T., & Nakano, K. (2001).
Efferent projections of infralimbic and prelimbic areas of the medial prefrontal cortex in the Japanese monkey, Macaca fuscata. Brain research, 888(1), 83-101. [PubMed:11146055] [WorldCat] [DOI] - ↑
Beninato, M., & Spencer, R.F. (1988).
The cholinergic innervation of the rat substantia nigra: a light and electron microscopic immunohistochemical study. Experimental brain research, 72(1), 178-84. [PubMed:3169185] [WorldCat] [DOI] - ↑
Futami, T., Takakusaki, K., & Kitai, S.T. (1995).
Glutamatergic and cholinergic inputs from the pedunculopontine tegmental nucleus to dopamine neurons in the substantia nigra pars compacta. Neuroscience research, 21(4), 331-42. [PubMed:7777224] [WorldCat] [DOI] - ↑
Scroggs, R.S., Cardenas, C.G., Whittaker, J.A., & Kitai, S.T. (2001).
Muscarine reduces calcium-dependent electrical activity in substantia nigra dopaminergic neurons. Journal of neurophysiology, 86(6), 2966-72. [PubMed:11731553] [WorldCat] [DOI] - ↑
Yamashita, T., & Isa, T. (2003).
Fulfenamic acid sensitive, Ca(2+)-dependent inward current induced by nicotinic acetylcholine receptors in dopamine neurons. Neuroscience research, 46(4), 463-73. [PubMed:12871768] [WorldCat] [DOI] - ↑
Nader, K., Bechara, A., & van der Kooy, D. (1997).
Neurobiological constraints on behavioral models of motivation. Annual review of psychology, 48, 85-114. [PubMed:9046556] [WorldCat] [DOI] - ↑
Inglis, W.L., Olmstead, M.C., & Robbins, T.W. (2000).
Pedunculopontine tegmental nucleus lesions impair stimulus--reward learning in autoshaping and conditioned reinforcement paradigms. Behavioral neuroscience, 114(2), 285-94. [PubMed:10832790] [WorldCat] [DOI] - ↑
Winn, P. (2006).
How best to consider the structure and function of the pedunculopontine tegmental nucleus: evidence from animal studies. Journal of the neurological sciences, 248(1-2), 234-50. [PubMed:16765383] [WorldCat] [DOI] - ↑
Blaha, C.D., & Winn, P. (1993).
Modulation of dopamine efflux in the striatum following cholinergic stimulation of the substantia nigra in intact and pedunculopontine tegmental nucleus-lesioned rats. The Journal of neuroscience : the official journal of the Society for Neuroscience, 13(3), 1035-44. [PubMed:8441002] [WorldCat] - ↑ 45.0 45.1
Dormont, J.F., Condé, H., & Farin, D. (1998).
The role of the pedunculopontine tegmental nucleus in relation to conditioned motor performance in the cat. I. Context-dependent and reinforcement-related single unit activity. Experimental brain research, 121(4), 401-10. [PubMed:9746146] [WorldCat] [DOI] - ↑
Nakamura, K., & Ono, T. (1986).
Lateral hypothalamus neuron involvement in integration of natural and artificial rewards and cue signals. Journal of neurophysiology, 55(1), 163-81. [PubMed:3512788] [WorldCat] [DOI] - ↑
Strafella, A.P., Lozano, A.M., Ballanger, B., Poon, Y.Y., Lang, A.E., & Moro, E. (2008).
rCBF changes associated with PPN stimulation in a patient with Parkinson's disease: a PET study. Movement disorders : official journal of the Movement Disorder Society, 23(7), 1051-1054. [PubMed:18412282] [WorldCat] [DOI]