終脳
黒田 一樹
福井大学医学部形態機能医科学講座
佐藤 真
大阪大学医学系研究科 解剖学講座(神経機能形態学)/大阪大学医学系研究科 連合小児発達学研究科 こころの発達神経科学講座(分子生物遺伝学)
DOI:10.14931/bsd.3243 原稿受付日:2013年3月27日 原稿完成日:2013年5月7日 一部改訂:2021年6月30日
担当編集委員:大隅 典子(東北大学 大学院医学系研究科 附属創生応用医学研究センター 脳神経科学コアセンター 発生発達神経科学分野)
英語名:telencephalon 独:Telenzephalon 仏:le télencéphale
終脳は神経管の最も吻側から形成される脳である。発生途中の胚の背側において、脊索からの誘導を受けて外胚葉から神経板が形成され、つづいて神経板の正中に生じる神経溝に沿って神経板は内側に陥入し、神経板の左右が癒着して神経管が形成される。初期の脳の形成では、神経管の前方において3箇所が膨らみ、前脳胞、中脳胞、菱脳胞の3つの脳胞とそれに続く神経管を肉眼的に認める(3脳胞期)。その後、前脳胞は終脳胞と間脳胞に、菱脳胞は後脳胞と髄脳胞に分かれ、尾方の神経管は脊髄となる(5脳胞期)。神経管の最吻側は前脳胞(間脳胞)の第三脳室終板であり、終脳胞は前脳胞が左右側方に膨らみ形成される。終脳胞から、ヒトでは発生とともに背側から後方に膨らみが形成され後頭葉が生じ、さらに終脳胞は弧状に回転して腹側から前方に伸展して側頭葉を形成する。終脳胞は最終的に大脳となることから、終脳は大脳と同等の意味を持つ。
神経管の発生
中枢神経系の発生において最も初期に起こる出来事は、胚の背側部において神経板(neural plate)が生じ、この神経板から神経管(neural tube)が形成されることである。ヒトを含め脊椎動物の胚は発生のあるステージにおいては最外層から外胚葉(ectoderm)、中間層は中胚葉(mesoderm)および最内層は内胚葉(endoderm)の三胚葉からなる。
胚の背側の外胚葉に生じる神経板は、予定神経板領域に隣接する中胚葉から分泌される分子により外胚葉が肥厚して形成される。この神経板の形成過程を神経誘導(neural induction)と呼ぶ。
次に神経板の腹側の正中線上に中胚葉性の索状の構造である脊索(notochord)が生じ、脊索から放出される分子により神経板の両側が厚くなり、神経板の正中線に沿って神経溝が生じる[1][2]。その後、神経板の左右の縁が癒着することによって神経管が生じる。
神経管の前端と後端は発生初期では完全に閉じておらず、前者を前神経孔(anterior neuropore)、また後者を後神経孔(posterior neuropore)と呼び、発生が進むにつれて閉塞する。後方の神経孔が閉塞せずに開放されたまま発生が継続されると二分脊椎の原因となる[3][4]。
3脳胞の形成
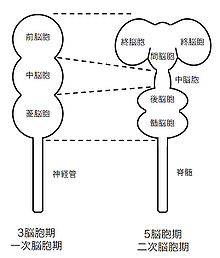
神経管の最前部では3つの中空の膨らみが形成され、この構造を3脳胞と言い、この時期を一次脳胞形成期と呼ぶ(図)。この中空の膨らみは吻側から前脳胞(prosencephalon)、中脳胞(mesencephalon)と菱脳胞(rhombencehanon)と呼ばれる。これら3つの脳胞に続く尾側の神経管は脳胞と比較し、分化が進まず脊髄(spinal cord)を形成する。ヒトでは受精後4週目でこれらの前脳胞、中脳胞、菱脳胞と脊髄に分かれることから、神経管の両端が閉塞する以前に3脳胞が形成される。また神経管は胎児の屈曲位に一致して曲がり、前脳胞と中脳胞の境界で頭屈が、菱脳胞と脊髄の境界で頚屈が生じる[5]。
5脳胞の形成
3脳胞は更に分化し、前脳胞からは終脳胞(telencephalon)と間脳胞(diencephalon)、中脳胞からは中脳胞(mesencephalon, midbrain)、菱脳胞から後脳胞(metencephalon, hindbrain)と髄脳胞(myelencephalon)が形成される(図)。この5つの脳胞からなる構造を5脳胞と言い、またこの時期を二次脳胞形成期と呼ぶ。
ヒトでは受精後5週目に二次脳胞形成期に入る。形態的には前脳胞から左右に脳胞が形成されて終脳胞となり、左右の終脳胞に挟まれた脳胞が間脳胞となる。
終脳胞は主に成体での大脳皮質に、間脳胞は視床、視床下部などを形成する。中脳胞はこれ以後分割されずに中脳のままで、中脳胞と菱脳胞の境界部は狭くなり菱脳峡が形成される。菱脳胞は長く伸び、中央部が左右に広がって全体が吻尾方向に伸びた菱形となり、後脳胞と髄脳胞に分割される。後脳胞と髄脳胞の境界部では背側から腹側に向かって屈曲が生じ、橋屈が生じる。後脳胞からは小脳および橋が、髄脳胞からは延髄が形成される[5]。
終脳の発達
終脳胞からは大脳皮質、海馬や嗅球などが生じる。この終脳胞の発達は前脳胞の左右の背側部が上方に隆起して始まる。ヒトではこの上方に隆起した部位は前頭葉及び頭頂葉になる。続いて終脳胞は後方に伸展して後頭葉を形成し、更に下方へ曲がり込んで前方へと伸展して側頭葉を形成する。ヒトの大脳皮質は終脳の伸展により体積の増加を抑え、大脳皮質の面積を増やすことにより、動物の高等化によって必要とされる中枢神経系での情報処理能力を増強している。更に大脳皮質は脳表に多数の皺や溝を形成し、皮質の表面積を増加させている。
終脳は神経管の先端部分から形成されることから、終脳の内部は中空状である。この中空部分は終脳胞の発達に伴い、終脳の前方から頭頂へ、頭頂から後頭へと伸び、最終的に側頭葉に達している。この中空の空間を側脳室と呼び、前方に伸びる部位は側脳室前角、後方から下方へ曲がる部位は側脳室後角、側頭葉に終わる部位を側脳室下角と呼ぶ。側脳室は間脳の中空部位である第三脳室と室間孔で繋がり、第四脳室から第三脳室を経て側脳室へ続く脈絡叢が存在している。この脈絡叢は脳脊髄液を産生し、側脳室を満たしている[5]。
前脳、中脳と後脳の領域化に関与する転写因子
発生過程の脳では数多くの遺伝子が発現し、特に異なる転写因子の発現の組み合わせにより区画化(コンパートメント)が行われている。ここでは発生過程の脳で発現し、脳の区画化に関わる代表的な転写因子の機能について述べる。
終脳の形成においてOtx遺伝子とEmx遺伝子が協働して機能している[6]。これらの遺伝子は転写因子であり、ショウジョウバエの相同遺伝子(orthodenticleやempty spiracle)と高い類似性を保っている。これらの遺伝子の機能は、ショウジョウバエの頭部形成や、脊椎動物の前脳と中脳の形成に関与している。Otx2+/-Emx2-/- 変異マウスの解析では、脳背側部および間脳領域(視床上部、視床)の欠損が認められ、両遺伝子が前脳形成に重要な役割を果たしている事が示されている[7]。
前脳の発生が進むと背側側に大脳皮質と腹側側に基底核原基が形成され、終脳と成る。終脳の大脳皮質には興奮性神経細胞(グルタミン酸作動性)と抑制性神経細胞(GABA作動性)が存在している。前者は大脳皮質の脳室帯にて生まれ、法線方向(脳室から脳表面)に移動し、後者は基底核原基で生まれ、大脳皮質内には接線方向に移入して、大脳皮質を構成している[8]。近年、これらの興奮性神経細胞や抑制性神経細胞の分化を制御する転写因子や分泌因子が同定されている[9][10]。また興奮性神経細胞や抑制性神経細胞の細胞移動に関しても解明が進んでいる[11][12][13][14]。
中脳と後脳の境目の形成に関与する遺伝子としてOtx2やGbx2遺伝子が知られている。マウスの胎生7.5日目においてOtx2は前方にGbx2が後方に発現し、前後軸が決定される[15]。このOtx2とGbx2の発現境界は中脳と後脳の境(菱脳峡)に一致し、菱脳峡では線維芽細胞増殖因子であるFgf8が発現する[16]。このFgf8は前方の中脳胞から視蓋を、また後方の菱脳胞から小脳を誘導する。Gbx2遺伝子を欠損したマウスでは、Otx2の発現が後脳側に拡大し、通常中脳と後脳の境目に発現するFgf8は菱脳で発現する[17]。
後脳では、発生の一時期に、菱脳節(rhombomerer)と呼ばれる7ないし8個の膨らみが形成される。これらの菱脳節はそれぞれ異なる神経核を持ち、異なった性質を有している。この菱脳節の分節間の違いは発現するHomeobox遺伝子により制御されている。マウスではゲノム4カ所にHoxA、HoxB、HoxCとHoxDという4つのホメオティック遺伝子群のクラスターを持つ[18]。各クラスター内で遺伝子は全て同じ向きに転写され、前後軸に沿って発現する順番と遺伝子の並びが一致し、異なるHomeobox遺伝子の発現により菱脳節の分節間の違いが確立されている。ヒトのHoxa1遺伝子の欠損は脳幹の一部の神経核が欠損し、自閉症に関与する事が示されている[19]。
関連項目
参考文献
- ↑
Bronner-Fraser, M., & Fraser, S.E. (1997).
Differentiation of the vertebrate neural tube. Current opinion in cell biology, 9(6), 885-91. [PubMed:9425355] [WorldCat] [DOI] - ↑
Spörle, R., & Schughart, K. (1997).
Neural tube morphogenesis. Current opinion in genetics & development, 7(4), 507-12. [PubMed:9309182] [WorldCat] [DOI] - ↑
van Straaten, H.W., & Copp, A.J. (2001).
Curly tail: a 50-year history of the mouse spina bifida model. Anatomy and embryology, 203(4), 225-37. [PubMed:11396850] [PMC] [WorldCat] [DOI] - ↑
Copp, A.J., & Greene, N.D. (2010).
Genetics and development of neural tube defects. The Journal of pathology, 220(2), 217-30. [PubMed:19918803] [PMC] [WorldCat] [DOI] - ↑ 5.0 5.1 5.2 ジョン・H・マーティン=著、野村金子武嗣=監訳
マーティン 神経解剖学 テキストとアトラス 初版
西村書店(東京):2007 - ↑
Cecchi, C., Mallamaci, A., & Boncinelli, E. (2000).
Otx and Emx homeobox genes in brain development. The International journal of developmental biology, 44(6), 663-8. [PubMed:11061430] [WorldCat] - ↑
Suda, Y., Hossain, Z.M., Kobayashi, C., Hatano, O., Yoshida, M., Matsuo, I., & Aizawa, S. (2001).
Emx2 directs the development of diencephalon in cooperation with Otx2. Development (Cambridge, England), 128(13), 2433-50. [PubMed:11493561] [WorldCat] - ↑
Nadarajah, B., & Parnavelas, J.G. (2002).
Modes of neuronal migration in the developing cerebral cortex. Nature reviews. Neuroscience, 3(6), 423-32. [PubMed:12042877] [WorldCat] [DOI] - ↑
Wonders, C.P., & Anderson, S.A. (2006).
The origin and specification of cortical interneurons. Nature reviews. Neuroscience, 7(9), 687-96. [PubMed:16883309] [WorldCat] [DOI] - ↑
Molyneaux, B.J., Arlotta, P., Menezes, J.R., & Macklis, J.D. (2007).
Neuronal subtype specification in the cerebral cortex. Nature reviews. Neuroscience, 8(6), 427-37. [PubMed:17514196] [WorldCat] [DOI] - ↑
Gupta, A., Tsai, L.H., & Wynshaw-Boris, A. (2002).
Life is a journey: a genetic look at neocortical development. Nature reviews. Genetics, 3(5), 342-55. [PubMed:11988760] [WorldCat] [DOI] - ↑
Nakajima, K. (2007).
Control of tangential/non-radial migration of neurons in the developing cerebral cortex. Neurochemistry international, 51(2-4), 121-31. [PubMed:17588709] [WorldCat] [DOI] - ↑
Nóbrega-Pereira, S., & Marín, O. (2009).
Transcriptional control of neuronal migration in the developing mouse brain. Cerebral cortex (New York, N.Y. : 1991), 19 Suppl 1, i107-13. [PubMed:19357392] [WorldCat] [DOI] - ↑
Chédotal, A., & Rijli, F.M. (2009).
Transcriptional regulation of tangential neuronal migration in the developing forebrain. Current opinion in neurobiology, 19(2), 139-45. [PubMed:19428236] [WorldCat] [DOI] - ↑
Joyner, A.L., Liu, A., & Millet, S. (2000).
Otx2, Gbx2 and Fgf8 interact to position and maintain a mid-hindbrain organizer. Current opinion in cell biology, 12(6), 736-41. [PubMed:11063941] [WorldCat] [DOI] - ↑
Crossley, P.H., & Martin, G.R. (1995).
The mouse Fgf8 gene encodes a family of polypeptides and is expressed in regions that direct outgrowth and patterning in the developing embryo. Development (Cambridge, England), 121(2), 439-51. [PubMed:7768185] [WorldCat] - ↑
Wassarman, K.M., Lewandoski, M., Campbell, K., Joyner, A.L., Rubenstein, J.L., Martinez, S., & Martin, G.R. (1997).
Specification of the anterior hindbrain and establishment of a normal mid/hindbrain organizer is dependent on Gbx2 gene function. Development (Cambridge, England), 124(15), 2923-34. [PubMed:9247335] [WorldCat] - ↑
Duboule, D. (2007).
The rise and fall of Hox gene clusters. Development (Cambridge, England), 134(14), 2549-60. [PubMed:17553908] [WorldCat] [DOI] - ↑
Ingram, J.L., Stodgell, C.J., Hyman, S.L., Figlewicz, D.A., Weitkamp, L.R., & Rodier, P.M. (2000).
Discovery of allelic variants of HOXA1 and HOXB1: genetic susceptibility to autism spectrum disorders. Teratology, 62(6), 393-405. [PubMed:11091361] [WorldCat] [DOI]