(3人の利用者による、間の55版が非表示) 1行目:
1行目: <div align="right">
<font size="+1">[http://researchmap.jp/ageta-ishihara 上田(石原) 奈津実]、[http://researchmap.jp/makotokinoshita 木下 専]</font><br>
''名古屋大学 理学研究科 生命理学専攻''<br>
DOI:<selfdoi /> 原稿受付日:2012年1月25日 原稿完成日:2012年2月25日<br>
担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br>
</div>
{{Pfam box
|Symbol = SEPT
|Name = Septin
|image =2qag_bio_r_500.jpg
| caption = Crystallographic structure of the septin hexatamer<ref name=pmid17637674></ref>.
|Pfam = PF00735
|Pfam_clan = CL0023
|InterPro = IPR000038
|PROSITE =
|PDB = }}
英語名:Septin 英語略名:SEPT
英語名:Septin 英語略名:SEPT
{{box|text=
セプチンは[[真核生物]]に保存された重合性[[グアノシン三リン酸]](GTP)結合蛋白質ファミリーの総称である。セプチン重合体は多様な分子の足場ないし拡散障壁となり、 [[樹状突起]]・軸索・ [[繊毛]]・[[鞭毛]]の形成、[[微小管]]系やアクトミオシン系の制御、 [[細胞分裂]]、分泌小胞の開口放出など多彩な生命現象に関与する <ref><pubmed>18478031</pubmed></ref>。ヒトでは優性変異型''SEPT9'' が家族性神経痛性筋萎縮症の原因となるほか <ref><pubmed>16186812</pubmed></ref>、[[パーキンソン病]]や[[統合失調症]]では複数のセプチンの量的・質的異常が随伴する。
セプチンは[[wikipedia:ja:真核生物|真核生物]]に保存された重合性[[wikipedia:ja:グアノシン三リン酸|グアノシン三リン酸]](GTP)結合タンパク質ファミリーの総称である。セプチン重合体は多様な分子の足場ないし拡散障壁となり、[[樹状突起]]・[[軸索]]・[[wikipedia:ja:繊毛|繊毛]]・[[wikipedia:ja:鞭毛|鞭毛]]の形成、[[微小管]]系や[[アクトミオシン]]系の制御、[[wikipedia:ja:細胞分裂|細胞分裂]]、[[wikipedia:ja:分泌小胞|分泌小胞]]の[[開口放出]]など多彩な生命現象に関与する<ref><pubmed>18478031</pubmed></ref>。ヒトでは優性変異型''SEPT9'' が[[家族性神経痛性筋萎縮症]]の原因となるほか<ref><pubmed>16186812</pubmed></ref>、[[パーキンソン病]]や[[統合失調症]]では複数のセプチンの量的・質的異常が随伴する。
}}
== 歴史 ==
== 歴史 ==
[[wikipedia:ja:細胞質分裂|細胞質分裂]](septation)と形態形成の異常を呈する[[wikipedia:ja:出芽酵母|出芽酵母]]''Saccharomyces cerevisiae''の変異体''Cdc3''、''Cdc10''、''Cdc11''、''Cdc12''の原因遺伝子産物が[[wikipedia:ja:出芽|出芽]]部位の[[細胞膜]]を環状に裏打ちするフィラメントの構成成分であることと、これらのホモログが多様な生物種に存在することが90年代半ばまでに判明し、セプチン(septin)と命名された<ref><pubmed>8791410</pubmed></ref>。
[[細胞質分裂]](septation)と形態形成の異常を呈する[[出芽酵母]]''Saccharomyces cerevisiae''の変異体''Cdc3''、''Cdc10''、''Cdc11''、''Cdc12''の原因遺伝子産物が[[出芽]]部位の[[細胞膜]]を環状に裏打ちするフィラメントの構成成分であることと、[[Image:図1.jpg|330px|thumb|right|図1:主なモデル生物におけるセプチンファミリーと一次構造による分類(SEPT13は霊長類に存在し、げっ歯類には存在しない]]これらのホモログが多様な生物種に存在することが90年代半ばまでに判明し、セプチン (septin)と命名された<ref><pubmed>8791410</pubmed></ref>。
== ファミリー ==
== ファミリー ==
{| border="1" cellpadding="1" cellspacing="1" style="left;"
|+ '''表1 主なモデル生物におけるセプチンファミリーと一次構造による分類''' <br>SEPT13は霊長類に存在し、げっ歯類には存在しない
|-
! scope="col" | 種
! scope="col" | グループ1A
! scope="col" | グループ1B
! scope="col" | グループ2A
! scope="col" | グループ2B
! scope="col" | グループ2C
! scope="col" | グループ3
! scope="col" | グループ4
|-
| rowspan="3" | '''出芽酵母'''
| Cdc10
|
| Cdc3
|
|
| Cdc11
| Cdc12
|-
|
|
|
|
|
| Shs1
| Spr3
|-
|
|
|
|
|
| Spr28
|
|-
| '''線虫'''
|
| UNC-61
|
| UNC-59
|
|
|
|-
| rowspan="2" | '''ショウジョウバエ'''
|
| Sep2
|
| Pnut
| Sep1
|
|
|-
|
| Sep5
|
|
| Sep4
|
|
|-
| rowspan="5" | '''哺乳類'''
| SEPT3
| SEPT6
|
| SEPT7
| SEPT1
|
|
|-
| SEPT9
| SEPT8
|
| (SEPT13)
| SEPT2
|
|
|-
| SEPT12
| SEPT10
|
|
| SEPT4
|
|
|-
|
| SEPT11
|
|
| SEPT5
|
|
|-
|
| SEPT14
|
|
|
|
|
|}
<br>
セプチンファミリーに属する遺伝子は[[wikipedia:ja:植物|植物]]を除く真核生物の[[wikipedia:ja:ゲノム|ゲノム]]に2-14種類存在し、[[wikipedia:ja:一次構造|一次構造]]によって種ごとに2-4グループに分類できる(表)。[[wikipedia:ja:菌類|菌類]]と[[wikipedia:ja:後生動物|後生動物]]の間ではグループ間の対応関係の推定が困難であることから、多細胞化の過程で生化学的特性(後述)を保存しつつ[[wikipedia:ja:共進化|共進化]]したものと推測される。
セプチンファミリーに属する遺伝子は[[植物]]を除く真核生物の[[ゲノム]]に2-14種類存在し、[[一次構造|一次構造]]によって種ごとに2-4グループに分類できる(図1 )。[[菌類]]と[[後生動物]]の間ではグループ間の対応関係の推定が困難であることから、多細胞化の過程で[[生化学]]的特性 (後述)を保存しつつ[[共進化]]したものと推測される。
== 構造 ==
== 構造 ==
[[Image:nagetaishihara_fig_2.jpg|330px|thumb|right|'''図1:セプチンの3つの集合モード''']]
中核部分に[[Ras]]タンパク質様のGTP結合領域とファミリー固有の相同領域を持ち、多くはC末側に可動性に富む100残基までの[[wikipedia:ja:コイルドコイル|コイルドコイル]]領域を持つ。異なるグループ(表)に属するセプチンが一定の規則で会合してヘテロ2/3/4量体を形成し、これら2つが対向した4/6/8量体が定型的な構造単位とされているが、非定型的な組み合わせの[[wikipedia:ja:オリゴマー|オリゴマー]]も試験管内で調製可能であり、生体内にも存在する可能性が高い。[[wikipedia:ja:哺乳類|哺乳類]]の定型的なセプチン6量体[SEPT7(GDP):SEPT6(GTP):SEPT2(GDP)][SEPT2(GDP):SEPT6(GTP):SEPT7(GDP)]の[[wikipedia:ja:結晶構造|結晶構造]]は解かれたが、[[wikipedia:ja:ヌクレオチド|ヌクレオチド]]の交換/水解反応が極端に遅いこともあり、[[wikipedia:ja:酵素反応|酵素反応]]と[[wikipedia:ja:共役|共役]]した構造変換と[[wikipedia:ja:重合反応|重合反応]]/脱重合との関係は未だ不明である<ref name=pmid17637674><pubmed>17637674</pubmed></ref>。セプチン・ヘテロオリゴマーは長軸方向に連結して無極性フィラメントを形成するが、長軸と直交する方向にコイルドコイルが突出するため短軸方向には非対称となる。2本のフィラメントがコイルドコイルを対向させたpaired filamentも形成されるが、フィラメント濃度が高い場合は中核部分を介して密な線維束を形成する。線維束は湾曲して外径0.6 µm、内径0.4 µm前後の環状またはらせん状となって安定化する(図1.1)<ref><pubmed>12479805</pubmed></ref>。一方、[[イノシトールリン脂質]](PI)含有リポソーム上ではヘテロオリゴマーが柵状に2次元配列し、内径0.4 µm前後の曲率で管状化して脂質膜を変形させる(図1.2)。これら独特の高次集合性、線維束の曲率指向性、PI親和性は種を超えて保存された物性である<ref><pubmed>19167227</pubmed></ref>。さらに、哺乳類のセプチンはPI以外に多様なタンパク質([[チュブリン]]、[[シンタキシン]]、[[ミオシン]]、アニリン(anillin)、[[グルタミン酸トランスポーター]](GLAST)、α-[[シヌクレイン]]など)への親和性を有し、アクトミオシン線維束など既存の細胞内構造を鋳型にして集合する(図1.3)。
== 神経系における発現パタン ==
中核部分に[[Rasタンパク質]]様のGTP結合領域とファミリー固有の相同領域を持ち、多くはC末側に可動性に [[Image:図2 .jpg|330px|thumb|right|図2:セプチンの3つの集合モード ]]富む100残基までの[ [コイルドコイル ]]領域を持つ。異なるグループ(図1)に属するセプチンが一定の規則で会合してヘテロ2 /3 /4量体を形成し、これら2つが対向した4 /6 /8量体が定型的な構造単位とされているが、非定型的な組み合わせの [[オリゴマー ]]も試験管内で調製可能であり、生体内にも存在する可能性が高い。 [[哺乳類 ]]の定型的なセプチン6量体[SEPT7(GDP) :SEPT6(GTP) :SEPT2(GDP) ][SEPT2(GDP) :SEPT6(GTP) :SEPT7(GDP) ]の [[結晶構造 ]]は解かれたが、 [[ヌクレオチド ]]の交換/水解反応が極端に遅いこともあり、 [[酵素反応 ]]と [[共役 ]]した構造変換と [[重合反応 ]]/脱重合との関係は未だ不明である <ref ><pubmed >17637674 </pubmed ></ref >。セプチン・ヘテロオリゴマーは長軸方向に連結して無極性フィラメントを形成するが、長軸と直交する方向にコイルドコイルが突出するため短軸方向には非対称となる。2本のフィラメントがコイルドコイルを対向させたpaired filamentも形成されるが、フィラメント濃度が高い場合は中核部分を介して密な線維束を形成する。線維束は湾曲して外径0 .6 µm、内径0 .4 µm前後の環状またはらせん状となって安定化する(図2 .1) <ref ><pubmed >12479805 </pubmed ></ref >。一方、 [[イノシトールリン脂質 ]](PI)含有リポソーム上ではヘテロオリゴマーが柵状に2次元配列し、内径0.4 µm前後の曲率で管状化して脂質膜を変形させる(図2.2)。これら独特の高次集合性、線維束の [[曲率 ]]指向性、PI親和性は種を超えて保存された物性である <ref><pubmed>19167227 </pubmed></ref>。さらに、哺乳類のセプチンはPI以外に多様な蛋白質([[チューブリン]]、シンタキシン、[[ミオシン]]、アニリン、グルタミン酸トランスポーター(GLAST)、α-シヌクレインなど)への親和性を有し、アクトミオシン線維束など既存の細胞内構造を鋳型にして集合する(図2.3) 。
[[Image:nagetaishihara_fig_3.jpg|330px|thumb|right|'''図2 ニューロンやグリアの特定の膜ドメインにおけるセプチンクラスター''']]
{| cellspacing="1" cellpadding="1" border="1"
|+'''表2:マウス成体脳におけるセプチンサブユニットの発現<ref>[http://mouse.brain-map.org/ Allen Brain Atlas]</ref><ref>[http://www.stjudebgem.org/web/mainPage/mainPage.php Brain Gene Expression Map]</ref><ref>[http://biogps.org BioGPS]</ref>'''<br>
|-
|
<br>
| style="text-align:center" |[[大脳皮質]]
| style="text-align:center" |[[嗅球]]
| style="text-align:center" |[[海馬]]
| style="text-align:center" |[[線条体]]/<br>[[淡蒼球]]
| style="text-align:center" |[[小脳]]
| style="text-align:center" |[[視床]]/<br>[[視床下部]]
| style="text-align:center" |[[中脳]]/[[橋]]<br>/[[延髄]]
| <br>
| style="text-align:center" | [[神経細胞]]/<br>[[グリア]]細胞
| style="text-align:center" | [[シナプス]]<br>[[シナプス前部|前部]]/[[シナプス後部|後部]]
|-
| [http://mouse.brain-map.org/gene/show/33496 Sept1]
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| <br>
| style="text-align:center" | -/-
| style="text-align:center" | -/-
|-
| [http://mouse.brain-map.org/experiment/show/69816834 Sept2]
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | +
| style="text-align:center" | -
| style="text-align:center" | -
| <br>
| style="text-align:center" | -/+
| style="text-align:center" | -/-
|-
| [http://mouse.brain-map.org/experiment/show/69838258 Sept3]
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/-
| style="text-align:center" | +/+
|-
| [http://mouse.brain-map.org/gene/show/18715 Sept4]
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+
| style="text-align:center" | +/-
|-
| [http://mouse.brain-map.org/gene/show/18714 Sept5]
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+
| style="text-align:center" | +/+
|-
| [http://mouse.brain-map.org/experiment/show/532648 Sept6]
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+
| style="text-align:center" | +/+
|-
| [http://mouse.brain-map.org/gene/show/87961 Sept7]
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+
| style="text-align:center" | +/+
|-
| [http://mouse.brain-map.org/gene/show/87961 Sept8]
| style="text-align:center" | +
| style="text-align:center" | -
| style="text-align:center" | +
| style="text-align:center" | -
| style="text-align:center" | +
| style="text-align:center" | -
| style="text-align:center" | -
| <br>
| style="text-align:center" | +/+
| style="text-align:center" | ?
|-
| [http://mouse.brain-map.org/gene/show/33155 Sept9]
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | ++
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+?
| style="text-align:center" | ?
|-
| [http://mouse.brain-map.org/experiment/show/75694304 Sept10]
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+?
| style="text-align:center" | ?
|-
| Sept11
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| style="text-align:center" | +
| <br>
| style="text-align:center" | +/+
| style="text-align:center" | ?
|-
| [http://mouse.brain-map.org/experiment/show/71892113 Sept12]
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| <br>
| style="text-align:center" | -/-
| style="text-align:center" | -/-
|-
| Sept14
| style="text-align:center" | +
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| style="text-align:center" | -
| <br>
| style="text-align:center" | +/-?
| style="text-align:center" | ?
|}
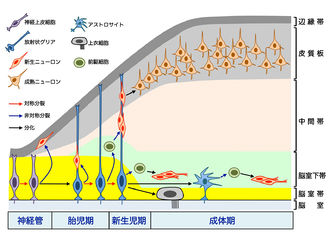
[[マウス]]では脳におけるセプチンの発現・局在パターンはサブユニットや細胞ごとに大きく異なる。例えばSEPT3,5はニューロンに発現して[[樹状突起棘]]や軸索末端に局在し、SEPT2,4はグリアに発現して突起の特定の膜ドメインを裏打ちする(図2)<ref><pubmed>11064363</pubmed></ref>。
== 神経系における生理機能 ==
== 神経系における生理機能 ==
セプチンを最も大量に発現する組織が神経系であることやヒトの精神・神経・筋疾患との関連から神経系におけるセプチン機能に関心が集まっている。[[ショウジョウバエ]]の致死性セプチン変異体''pnut''は初期胚の表割(細胞膜形成/cellularization)の異常を呈し、神経系の形質は不明であるが、眼の[[光受容細胞]]R7を欠損する''sina''変異体のエンハンサーであることが知られている。[[線虫]]の運動障害(''unc'')変異体として見出されたセプチン欠損変異体''unc-59/-61''では特定の細胞を除いて細胞分裂は顕在化せず、[[神経突起]]形成ないし[[ガイダンス]]の異常を呈する<ref><pubmed>12941631</pubmed></ref>。これまでに報告されたセプチン遺伝子欠損マウスのうち、''Sept7'',''9''の欠損は胎生致死となる一方、''Sept3'',''4'',''5'',''6''の欠損による神経系の異常は軽度なレベルにとどまる<ref>'''木下 専'''<br>セプチン細胞骨格の変幻自在な高次集合性と多彩な生理機能<br>''蛋白質・核酸・酵素'' 2009, 54(9);1150-8</ref>。後者の理由として同じグループに属する機能重複遺伝子による代償が推測されるが、興味深い事実も明らかになってきた。例えば''Sept4''欠損マウスでは聴覚性[[プレパルス抑制]]の減弱から、[[黒質]]-[[線条体]]投射系の[[ドーパミン]]ニューロンの軸索末端においてドパミン代謝機構がダウンレギュレーションしていることがわかった<ref><pubmed>17296554</pubmed></ref><ref>'''木下 専'''<br>ドーパミン神経伝達と変性におけるセプチン細胞骨格系の役割<br>''日本神経精神薬理学会誌'' 2012, 32;25-9</ref>。。一方、''Sept5''欠損マウスでは[[聴覚]]系[[シナプス]][[calyx of Held]]の軸索末端における[[シナプス小胞]]の開口放出の調節が異常となる<ref><pubmed>20624595</pubmed></ref>。いずれも足場ないし拡散障壁機能の欠損によるものと想定されるが、詳細なメカニズムの解明や他のニューロンやグリアにおけるセプチン機能の探索は今後の課題である。
セプチンを最も大量に発現する組織が神経系であることやヒトの精神・神経・筋疾患との関連から神経系におけるセプチン機能に関心が集まっている。[[ショウジョウバエ]]の致死性セプチン変異体''pnut''は初期胚の表割(細胞膜形成/cellularization)の異常を呈し、神経系の形質は不明であるが、眼の光受容細胞R7を欠損する ''sina''変異体の [[エンハンサー ]]であることが知られている。線虫の運動障害 (''unc'')変異体として見出されたセプチン欠損変異体''unc-59/-61''では細胞分裂は顕在化せず、神経突起形成ないしガイダンスの異常を呈する<ref><pubmed>12941631</pubmed></ref>。マウスでは脳におけるセプチンの発現・局在パターンは [[サブユニット ]]や細胞ごとに大きく異なる。 [[Image:図3.jpg|330px|thumb|right|図3:ニューロンやグリアの特定の膜ドメインにおけるセプチンクラスター ]]
例えばSEPT3,5はニューロンに発現して[[樹状突起スパイン]]や軸索末端に局在し、SEPT2,4はグリアに発現して突起の特定の膜ドメインを裏打ちする(図3) <ref><pubmed>11064363 </pubmed></ref>。これまでに報告されたセプチン遺伝子欠損マウスのうち、''Sept7'',''9''の欠損は胎生致死となる一方、''Sept3'',''4'',''5'',''6''の欠損による神経系の異常は軽度なレベルにとどまる<ref><pubmed >19588878 </pubmed ></ref>。後者の理由として同じグループに属する機能重複遺伝子による代償が推測されるが、興味深い事実も明らかになってきた。例えば''Sept4''欠損マウスでは聴覚性プレパルス抑制の減弱から、黒質 -線条体投射系のドパミンニューロンの軸索末端においてドパミン代謝機構がダウンレギュレーションしていることがわかった <ref><pubmed>17296554</pubmed></ref>。一方、 ''Sept5''欠損マウスでは聴覚系シナプスcalyx of Heldの軸索末端におけるシナプス小胞の開口放出の調節が異常となる <ref><pubmed>20624595</pubmed></ref>。いずれも足場ないし拡散障壁機能の欠損によるものと想定されるが、詳細なメカニズムの解明や他のニューロンやグリアにおけるセプチン機能の探索は今後の課題である。
== 参考文献 ==
== 参考文献 ==
<references />
<references />
(執筆者:上田(石原)奈津実、木下専 担当編集委員:林康紀)
英語名:Septin 英語略名:SEPT
セプチンは真核生物 に保存された重合性グアノシン三リン酸 (GTP)結合蛋白質ファミリーの総称である。セプチン重合体は多様な分子の足場ないし拡散障壁となり、樹状突起 ・軸索・繊毛 ・鞭毛 の形成、微小管 系やアクトミオシン系の制御、細胞分裂 、分泌小胞の開口放出など多彩な生命現象に関与する[ 1] SEPT9 が家族性神経痛性筋萎縮症の原因となるほか[ 2] パーキンソン病 や統合失調症 では複数のセプチンの量的・質的異常が随伴する。
歴史
細胞質分裂 (septation)と形態形成の異常を呈する出芽酵母 Saccharomyces cerevisiae の変異体Cdc3 、Cdc10 、Cdc11 、Cdc12 の原因遺伝子産物が出芽 部位の細胞膜 を環状に裏打ちするフィラメントの構成成分であることと、
図1:主なモデル生物におけるセプチンファミリーと一次構造による分類(SEPT13は霊長類に存在し、げっ歯類には存在しない これらのホモログが多様な生物種に存在することが90年代半ばまでに判明し、セプチン(septin)と命名された[ 3]
ファミリー セプチンファミリーに属する遺伝子は植物 を除く真核生物のゲノム に2-14種類存在し、一次構造 によって種ごとに2-4グループに分類できる(図1)。菌類 と後生動物 の間ではグループ間の対応関係の推定が困難であることから、多細胞化の過程で生化学 的特性(後述)を保存しつつ共進化 したものと推測される。
構造
中核部分にRasタンパク質 様のGTP結合領域とファミリー固有の相同領域を持ち、多くはC末側に可動性に
ファイル:図2.jpg 図2:セプチンの3つの集合モード 富む100残基までのコイルドコイル 領域を持つ。異なるグループ(図1)に属するセプチンが一定の規則で会合してヘテロ2/3/4量体を形成し、これら2つが対向した4/6/8量体が定型的な構造単位とされているが、非定型的な組み合わせのオリゴマー も試験管内で調製可能であり、生体内にも存在する可能性が高い。哺乳類 の定型的なセプチン6量体[SEPT7(GDP):SEPT6(GTP):SEPT2(GDP)][SEPT2(GDP):SEPT6(GTP):SEPT7(GDP)]の結晶構造 は解かれたが、ヌクレオチド の交換/水解反応が極端に遅いこともあり、酵素反応 と共役 した構造変換と重合反応 /脱重合との関係は未だ不明である[ 4] [ 5] イノシトールリン脂質 (PI)含有リポソーム上ではヘテロオリゴマーが柵状に2次元配列し、内径0.4 µm前後の曲率で管状化して脂質膜を変形させる(図2.2)。これら独特の高次集合性、線維束の曲率 指向性、PI親和性は種を超えて保存された物性である[ 6] チューブリン 、シンタキシン、ミオシン 、アニリン、グルタミン酸トランスポーター(GLAST)、α-シヌクレインなど)への親和性を有し、アクトミオシン線維束など既存の細胞内構造を鋳型にして集合する(図2.3)。
神経系における生理機能
セプチンを最も大量に発現する組織が神経系であることやヒトの精神・神経・筋疾患との関連から神経系におけるセプチン機能に関心が集まっている。ショウジョウバエ の致死性セプチン変異体pnut は初期胚の表割(細胞膜形成/cellularization)の異常を呈し、神経系の形質は不明であるが、眼の光受容細胞R7を欠損するsina 変異体のエンハンサー であることが知られている。線虫の運動障害(unc )変異体として見出されたセプチン欠損変異体unc-59/-61 では細胞分裂は顕在化せず、神経突起形成ないしガイダンスの異常を呈する[ 7] サブユニット や細胞ごとに大きく異なる。
図3:ニューロンやグリアの特定の膜ドメインにおけるセプチンクラスター 例えばSEPT3,5はニューロンに発現して樹状突起スパイン や軸索末端に局在し、SEPT2,4はグリアに発現して突起の特定の膜ドメインを裏打ちする(図3)[ 8] Sept7 ,9 の欠損は胎生致死となる一方、Sept3 ,4 ,5 ,6 の欠損による神経系の異常は軽度なレベルにとどまる[ 9] Sept4 欠損マウスでは聴覚性プレパルス抑制の減弱から、黒質-線条体投射系のドパミンニューロンの軸索末端においてドパミン代謝機構がダウンレギュレーションしていることがわかった[ 10] Sept5 欠損マウスでは聴覚系シナプスcalyx of Heldの軸索末端におけるシナプス小胞の開口放出の調節が異常となる[ 11]
参考文献
↑
Weirich, C.S., Erzberger, J.P., & Barral, Y. (2008). Nature reviews. Molecular cell biology , 9(6), 478-89.
[PubMed:18478031 ]
[WorldCat ]
[DOI ]
↑
Kuhlenbäumer, G., Hannibal, M.C., Nelis, E., Schirmacher, A., Verpoorten, N., Meuleman, J., ..., & Chance, P.F. (2005). Nature genetics , 37(10), 1044-6.
[PubMed:16186812 ]
[WorldCat ]
[DOI ]
↑
Longtine, M.S., DeMarini, D.J., Valencik, M.L., Al-Awar, O.S., Fares, H., De Virgilio, C., & Pringle, J.R. (1996). Current opinion in cell biology , 8(1), 106-19.
[PubMed:8791410 ]
[WorldCat ]
[DOI ]
↑
Sirajuddin, M., Farkasovsky, M., Hauer, F., Kühlmann, D., Macara, I.G., Weyand, M., ..., & Wittinghofer, A. (2007). Nature , 449(7160), 311-5.
[PubMed:17637674 ]
[WorldCat ]
[DOI ]
↑
Kinoshita, M., Field, C.M., Coughlin, M.L., Straight, A.F., & Mitchison, T.J. (2002). Developmental cell , 3(6), 791-802.
[PubMed:12479805 ]
[WorldCat ]
↑
Tanaka-Takiguchi, Y., Kinoshita, M., & Takiguchi, K. (2009). Current biology : CB , 19(2), 140-5.
[PubMed:19167227 ]
[WorldCat ]
[DOI ]
↑
Finger, F.P., Kopish, K.R., & White, J.G. (2003). Developmental biology , 261(1), 220-34.
[PubMed:12941631 ]
[WorldCat ]
[DOI ]
↑
Kinoshita, A., Noda, M., & Kinoshita, M. (2000). The Journal of comparative neurology , 428(2), 223-39.
[PubMed:11064363 ]
[WorldCat ]
[DOI ]
↑
Kinoshita, M. (2009). Tanpakushitsu kakusan koso. Protein, nucleic acid, enzyme , 54(9), 1150-8.
[PubMed:19588878 ]
[WorldCat ]
↑
Ihara, M., Yamasaki, N., Hagiwara, A., Tanigaki, A., Kitano, A., Hikawa, R., ..., & Kinoshita, M. (2007). Neuron , 53(4), 519-33.
[PubMed:17296554 ]
[WorldCat ]
[DOI ]
↑
Yang, Y.M., Fedchyshyn, M.J., Grande, G., Aitoubah, J., Tsang, C.W., Xie, H., ..., & Wang, L.Y. (2010). Neuron , 67(1), 100-15.
[PubMed:20624595 ]
[PMC ]
[WorldCat ]
[DOI ]
(執筆者:上田(石原)奈津実、木下専 担当編集委員:林康紀)