「軸索起始部」の版間の差分
細編集の要約なし |
細 →極性維持 |
||
| (同じ利用者による、間の9版が非表示) | |||
| 1行目: | 1行目: | ||
<div align="right"> | |||
<font size="+1">[http://researchmap.jp/hiroshikuba 久場 博司]</font><br> | |||
''名古屋大学 大学院医学系研究科''<br> | |||
DOI:<selfdoi /> 原稿受付日:2026年2月10日 原稿完成日:2026年2月18日<br> | |||
担当編集委員:[http://researchmap.jp/michisukeyuzaki 柚崎 通介](慶應義塾大学 医学部生理学)<br> | |||
</div> | |||
同義語:軸索初節<br> | |||
英:axon initial segment 独:Axoninitialsegment 仏:segment initial de l'axone <br> | 英:axon initial segment 独:Axoninitialsegment 仏:segment initial de l'axone <br> | ||
英略称:AIS | 英略称:AIS | ||
{{box|text= | {{box|text= 軸索起始部は、細胞体の近傍にある無髄の軸索領域であり、電位依存性Naイオンチャネルや骨格分子が高密度に集積することによって、神経細胞における活動電位の起点として働くとともに、細胞体・樹状突起分子の軸索への侵入を防ぐことで神経細胞の極性維持の役割を担っている。}} | ||
== 軸索起始部とは == | == 軸索起始部とは == | ||
[[ファイル:Kuba Axon Initial Segment Fig1.png|サムネイル|'''図1. 軸索起始部の位置'''<br>文献<ref name=Huang2018 />より改変。]] | |||
軸索起始部は、[[細胞体]]と[[軸索]]を分ける長さ10~60 µmの無髄領域であり、[[軸索小丘]]([[axon hillock]])の遠位に位置する('''図1''')。軸索起始部には[[イオンチャネル]]や[[接着分子]]などの[[膜タンパク質]]、[[足場タンパク質]]、[[細胞骨格]]分子が高密度に集積しており、このことが[[神経細胞]]の出力生成や[[極性]]維持を可能にしている<ref name=Kole2012><pubmed>22284179</pubmed></ref>。軸索起始部は従来、[[電子顕微鏡]]で観察される束化した[[微小管]]や細胞膜の裏打ち構造といった超微細構造によって定義されていたが、現在は[[電位依存性Naチャネル]]の足場タンパク質である[[アンキリンG]]([[AnkG]])が集積する領域として分子レベルで定義されている。軸索起始部と[[ランビエ絞輪]]は分子構築がよく似ており、進化的に関連すると考えられている。これらの構造は480 kDaのアンキリンGを獲得した[[脊椎動物]]から見られ、軸索起始部は[[無顎類]](約500万年前)以降、ランビエ絞輪は[[顎口類]](約440万年前)以降に出現することが知られている<ref name=Jenkins2015><pubmed>25552556</pubmed></ref>。 | |||
[[ファイル:Kuba Axon Initial Segment Fig2.png|サムネイル|'''図2. 軸索起始部の分子構築'''<br>イオンチャネルや接着分子などの膜タンパク質が足場であるアンキリンGを介してリング状のアクチンとβIV/αII スペクトリンの四量体からなる膜直下の骨格に固定されている。微小管はTRIM46やMTCL-1によって架橋された束を形成し、アンキリンGはEB1/EB3およびNdel1を介して微小管と結合する。<br>文献<ref name=Huang2018 />より改変。]] | |||
== 分子 == | == 分子 == | ||
=== 分子構築 === | === 分子構築 === | ||
軸索起始部では、Naチャネルを始めとしたイオンチャネル、足場タンパク質(アンキリンG、[[PSD-93]])、細胞骨格([[βIV/αIIスペクトリン]]、[[アクチン]]、微小管)、接着分子([[neurofascin 186]]([[NF186]])、[[neuronal cell adhesion molecule]]([[NrCAM]])、[[a disintegrin and metalloproteinase domain-containing protein 22]]([[ADAM22]])、[[contactin-associated protein-like 2]]([[Caspr2]])、[[transient axonal glycoprotein 1]]([[Tag1]]))が分子複合体を形成している('''図2''')。近年の超解像顕微鏡技術の進歩により、アクチンは細胞膜をリング状に裏打ちし、βIV/αIIスペクトリンのヘテロ四量体がこれらを繋ぐことで190 nm周期の格子構造をとることが示されている<ref name=Xu2013><pubmed>23239625</pubmed></ref><ref name=Leterrier2018><pubmed>29378864</pubmed></ref>。Naチャネルは足場であるアンキリンGと結合することで、βIV/αII スペクトリンを介してアクチンリングに固定され、NF186を介して細胞外基質(ブレビカン、バーシカン)に結合し、さらに[[End-binding protein 1]]([[EB1]])/[[End-binding protein 3]]([[EB3]])を介して束化した微小管とも結合しており、このことがNaチャネルの軸索起始部への集積を可能にしている。アンキリンGは軸索起始部の形成と維持に最も重要な分子であり、アンキリンGの欠失により軸索起始部は消失する<ref name=Hedstrom2007><pubmed>17724124</pubmed></ref><ref name=Sobotzik2009><pubmed>19805161</pubmed></ref>。 | |||
=== イオンチャネル === | === イオンチャネル === | ||
軸索起始部には様々なイオンチャネルが局在し、その種類や分布は神経細胞の出力様式を決める重要な要素である<ref name=Lorincz2008><pubmed>19118165</pubmed></ref><ref name=Jenkins2025><pubmed>39480263</pubmed></ref> | 軸索起始部には様々なイオンチャネルが局在し、その種類や分布は神経細胞の出力様式を決める重要な要素である<ref name=Lorincz2008><pubmed>19118165</pubmed></ref><ref name=Jenkins2025><pubmed>39480263</pubmed></ref>。 | ||
==== Naチャネル ==== | |||
[[Nav1.1]]、[[Nav1.2]]、[[Nav1.6]]の3つのサブタイプが知られる。Nav1.6は全ての神経細胞に発現し、活性化の閾値も低いことから活動電位の発生を担う最も重要なチャネルといえる。一方、Nav1.1とNav1.2はそれぞれ[[抑制性細胞]]と[[興奮性細胞]]に発現する。これらのチャネルは軸索起始部の近位部に局在し、活動電位の樹状突起への逆行性伝播を増強する。 | |||
==== Kチャネル ==== | |||
[[Kv1]]([[Kv1.1]]、[[Kv1.2|1.2]])、[[Kv7]]([[Kv7.2]]、[[Kv7.3|7.3]])、[[K2Pチャネル]]([[TRAAK]]、[[TREK-1]])などが知られる。これらのチャネルは[[静止膜電位]]付近でも活性化しており、[[短絡コンダクタンス]]として活動電位の発生を抑える一方で、静止膜電位を維持することでNavチャネルの不活性化を防ぐ働きをもつ。 | |||
==== Caチャネル ==== | |||
[[Cav2]]([[Cav2.1]]、[[Cav2.2]]、[[Cav2.3]])、[[Cav3]]([[Cav3.2]])が知られる。Cav2.1やCav2.2は活性化の閾値が高く、[[BKチャネル]]を活性化させることで活動電位の再分極相を加速させるのに対して、Cav2.3やCav3.2は活性化の閾値が低く、後脱分極を増強することで持続的な発火を生じる。 | |||
==== その他 ==== | |||
[[大脳皮質]]や[[海馬]]の錐体細胞では、軸索起始部に[[GABA]]作動性の[[軸索終末]]が[[軸索-軸索シナプス]]を形成する<ref name=Howard2005><pubmed>15927687</pubmed></ref>。これらの神経細胞の軸索起始部では[[K-Cl共輸送体]]([[KCC2]])の発現が低いため、軸索起始部での[[GABAA受容体|GABA<sub>A</sub>受容体]]の活性化は軸索起始部局所の[[脱分極]]を生じるが、一方で、短絡コンダクタンスを増すため活動電位の発生は抑制される<ref name=Szabadics2006><pubmed>16410524</pubmed></ref>。小脳の[[プルキンエ細胞]]の軸索起始部にもGABA作動性の軸索終末が分布するが、シナプスは形成されない<ref name=Howard2005><pubmed>15927687</pubmed></ref>。この他軸索起始部に局在するチャネルや受容体として、[[HCNチャネル]]、[[5HT1受容体|5HT<sub>1</sub>受容体]]、[[P2Y受容体]]、[[D2受容体|D<sub>2</sub>受容体]]などの報告がある<ref name=Jenkins2025><pubmed>39480263</pubmed></ref>。 | |||
== 機能 == | == 機能 == | ||
=== 活動電位発生 === | === 活動電位発生 === | ||
軸索起始部は活動電位の発生に適した特性をもつ<ref name=Kole2012><pubmed>22284179</pubmed></ref> | 軸索起始部は活動電位の発生に適した特性をもつ<ref name=Kole2012><pubmed>22284179</pubmed></ref>。まず、軸索起始部は細胞体の近くにあるため、樹状突起や細胞体に入力する[[シナプス電流]]の電荷が届きやすい。また、軸索起始部は微細な構造であるため、僅かな電荷でも電位が大きく変化する。さらに、軸索起始部にはNaチャネルが高密度に分布するため、活動電位の発生[[閾値]]が特に低い。これらの特性により、軸索起始部は神経細胞における活動電位の起点として働く。 | ||
活動電位が軸索起始部で発生するという考えは、1950年代に行われた[[脊髄運動ニューロン]]での[[細胞内電気記録]]の実験結果に基づいている<ref name=Coombs1957><pubmed>13492209</pubmed></ref><ref name=Debanne2011><pubmed>21527732</pubmed></ref>。この実験では、細胞体で記録される活動電位が軸索に由来する成分([[ISスパイク]])と細胞体に由来する成分([[SDスパイク]])の2つの成分からなり、ISスパイクはSDスパイクに先行することが示された。このことは、シナプス入力が活動電位を軸索で最初に発生させたのち、この活動電位が逆行性に軸索を細胞体へ伝播することによって、細胞体の活動電位が生じることを意味している。1990年代に、一部の神経細胞では樹状突起に強い入力を与えた際に樹状突起が活動電位の起点となり得ることが報告されたものの、その後、単一軸索からの[[パッチクランプ記録]]、[[Naイメージング]]や[[膜電位イメージング]]を用いた実験によって、生理的条件下では軸索起始部が活動電位の起点であることが示された。[[錐体細胞]]では、軸索起始部から細胞体へと伝播した活動電位はさらに樹状突起へ伝播し、シナプス応答を修飾する。 | |||
=== 恒常的可塑性 === | === 恒常的可塑性 === | ||
軸索起始部の長さや軸索上の位置は神経活動の変化に応じて可塑的に変化し、この変化は[[恒常的可塑性]]として神経活動を[[ネガティブフィードバック]]に調節する<ref name=Grubb2010><pubmed>20543823</pubmed></ref><ref name=Kuba2010><pubmed>20543822</pubmed></ref>。軸索起始部可塑性における軸索起始部の変化は細胞種によって異なる。例えば、発達期の[[視覚野]]や[[聴覚神経核]]では感覚入力によって軸索起始部の長さが短縮する<ref name=Gutzmann2014><pubmed>24672466</pubmed></ref><ref name=Akter2020><pubmed>32719016</pubmed></ref>。一方、海馬の[[分散培養]]標本では脱分極によって軸索起始部の位置が細胞体から離れる<ref name=Grubb2010><pubmed>20543823</pubmed></ref>。また、[[嗅球]]では脱分極によって軸索起始部の位置が興奮性細胞と抑制性細胞で逆の変化を示し、興奮性細胞では細胞体から離れるのに対して、抑制性細胞では細胞体に近づく<ref name=Chand2015><pubmed>25632134</pubmed></ref>。軸索起始部可塑性は神経細胞の興奮性が亢進する[[てんかん]]などの病態でもみられる<ref name=Harty2013><pubmed>23602553</pubmed></ref>。 | |||
軸索起始部可塑性は数時間から数日にわたる緩徐な変化であり、これは軸索起始部の分子構築の再編を反映すると考えられている。軸索起始部可塑性にはCaチャネルを介した細胞内[[カルシウム|Ca<sub>2+</sub>イオン]]の濃度変化が重要である。軸索起始部可塑性に関わる分子としては、[[カルシニューリン]]や[[サイクリン依存性タンパク質キナーゼ5]]([[cdk5]])が知られる<ref name=Evans2013><pubmed>23595753</pubmed></ref><ref name=Trunova2011><pubmed>21775591</pubmed></ref><ref name=Jahan2023><pubmed>36639893</pubmed></ref>。これら分子が軸索起始部の分布を変化させるしくみは分かっていないが、エンドサイトーシスや微小管の再編が関わると考えられている。 | |||
=== 極性維持 === | === 極性維持 === | ||
軸索起始部は、細胞体・樹状突起分子の軸索への侵入を防ぐ分子バリアとして働くことで神経細胞の極性を維持する。この分子バリアには[[膜拡散]]と[[細胞内輸送]]の2つのしくみが関わり、アンキリンGはこの両方において重要な役割を担うと考えられている<ref name=Huang2018><pubmed>29749636</pubmed></ref><ref name=Fréal2025><pubmed>39947181</pubmed></ref>。このため、海馬や小脳の神経細胞ではアンキリンGの欠失によって軸索起始部が消失し、さらに軸索には[[スパイン]]や[[シナプス後肥厚]]のような樹状突起の性質がみられるようになる<ref name=Hedstrom2007><pubmed>17724124</pubmed></ref><ref name=Sobotzik2009><pubmed>19805161</pubmed></ref>。膜拡散のバリアとしては、細胞膜直下のアンキリンG-[[βIV スペクトリン]]-アクチンからなる細胞骨格に結合したイオンチャネルや接着分子などの膜貫通タンパク質が物理的に側方拡散を妨げる「[[ピケットフェンスモデル]]」が有力である<ref name=Nakada2003><pubmed>12819789</pubmed></ref>。一方、細胞内輸送によるバリアとしては、[[ミオシンVa]]とアクチンパッチによる細胞体・樹状突起分子の輸送制御、EB1/3を介した微小管へのアンキリンG結合による軸索輸送の障害、微小管結合タンパク質である[[Microtubule-associated protein 2]]([[MAP2]])や[[Microtubule-associated protein 6]]([[MAP6]])による順行性輸送の制御、[[ダイニン]]調節因子である[[Nuclear distribution element-like 1]]([[Ndel1]])による逆行性輸送の制御などの説がある<ref name=Huang2018><pubmed>29749636</pubmed></ref><ref name=Fréal2025><pubmed>39947181</pubmed></ref>。 | |||
<ref name=Fréal2025><pubmed>39947181</pubmed></ref> | |||
== 疾患との関わり == | == 疾患との関わり == | ||
軸索起始部を構成するイオンチャネルや骨格分子の異常は様々な精神神経疾患を引き起こす<ref name=Huang2018><pubmed>29749636</pubmed></ref><ref name=Buffington2011><pubmed>22103418</pubmed></ref> | 軸索起始部を構成するイオンチャネルや骨格分子の異常は様々な精神神経疾患を引き起こす<ref name=Huang2018><pubmed>29749636</pubmed></ref><ref name=Buffington2011><pubmed>22103418</pubmed></ref>。例えば、軸索起始部に局在するNav1.1、Nav1.2、Nav1.6、Kv7.2、Kv7.3などのイオンチャネルには多くの変異が知られ、これらはてんかんの発症と密接に関連する。アンキリンGは[[ゲノムワイド関連解析]]([[Genome-wide association study]]; [[GWAS]])により[[双極性障害]]のリスク遺伝子とされ、アンキリンGの発現が低下したマウスでは精神疾患関連行動が生じる。また、アンキリンGのエクソン1b欠損マウスでは抑制性神経細胞の軸索起始部にNaチャネルが集積できず、双極性障害様行動、てんかん、突然死を示す。さらに、アンキリンGの変異は[[知的障害]]、[[統合失調症]]、[[自閉スペクトラム症]]とも関連する。一方、βIV スペクトリンの欠損や変異では運動障害や聴覚障害が認められ、[[αII スペクトリン]]の変異では[[早期乳児てんかん脳症]]、知的障害がみられる。軸索起始部構造の変化は、[[アンジェルマン症候群]]や[[アルツハイマー病]]、[[自己免疫性脱髄疾患]]、[[外傷性脳損傷]]、[[虚血性障害]]などでもみられ、これらは神経細胞の過興奮や機能障害を伴う。 | ||
== 参考文献 == | == 参考文献 == | ||
2026年4月4日 (土) 17:16時点における最新版
久場 博司
名古屋大学 大学院医学系研究科
DOI:10.14931/bsd.11504 原稿受付日:2026年2月10日 原稿完成日:2026年2月18日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
同義語:軸索初節
英:axon initial segment 独:Axoninitialsegment 仏:segment initial de l'axone
英略称:AIS
軸索起始部は、細胞体の近傍にある無髄の軸索領域であり、電位依存性Naイオンチャネルや骨格分子が高密度に集積することによって、神経細胞における活動電位の起点として働くとともに、細胞体・樹状突起分子の軸索への侵入を防ぐことで神経細胞の極性維持の役割を担っている。
軸索起始部とは
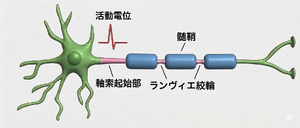
文献[1]より改変。
軸索起始部は、細胞体と軸索を分ける長さ10~60 µmの無髄領域であり、軸索小丘(axon hillock)の遠位に位置する(図1)。軸索起始部にはイオンチャネルや接着分子などの膜タンパク質、足場タンパク質、細胞骨格分子が高密度に集積しており、このことが神経細胞の出力生成や極性維持を可能にしている[2]。軸索起始部は従来、電子顕微鏡で観察される束化した微小管や細胞膜の裏打ち構造といった超微細構造によって定義されていたが、現在は電位依存性Naチャネルの足場タンパク質であるアンキリンG(AnkG)が集積する領域として分子レベルで定義されている。軸索起始部とランビエ絞輪は分子構築がよく似ており、進化的に関連すると考えられている。これらの構造は480 kDaのアンキリンGを獲得した脊椎動物から見られ、軸索起始部は無顎類(約500万年前)以降、ランビエ絞輪は顎口類(約440万年前)以降に出現することが知られている[3]。
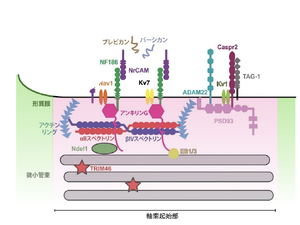
イオンチャネルや接着分子などの膜タンパク質が足場であるアンキリンGを介してリング状のアクチンとβIV/αII スペクトリンの四量体からなる膜直下の骨格に固定されている。微小管はTRIM46やMTCL-1によって架橋された束を形成し、アンキリンGはEB1/EB3およびNdel1を介して微小管と結合する。
文献[1]より改変。
分子
分子構築
軸索起始部では、Naチャネルを始めとしたイオンチャネル、足場タンパク質(アンキリンG、PSD-93)、細胞骨格(βIV/αIIスペクトリン、アクチン、微小管)、接着分子(neurofascin 186(NF186)、neuronal cell adhesion molecule(NrCAM)、a disintegrin and metalloproteinase domain-containing protein 22(ADAM22)、contactin-associated protein-like 2(Caspr2)、transient axonal glycoprotein 1(Tag1))が分子複合体を形成している(図2)。近年の超解像顕微鏡技術の進歩により、アクチンは細胞膜をリング状に裏打ちし、βIV/αIIスペクトリンのヘテロ四量体がこれらを繋ぐことで190 nm周期の格子構造をとることが示されている[4][5]。Naチャネルは足場であるアンキリンGと結合することで、βIV/αII スペクトリンを介してアクチンリングに固定され、NF186を介して細胞外基質(ブレビカン、バーシカン)に結合し、さらにEnd-binding protein 1(EB1)/End-binding protein 3(EB3)を介して束化した微小管とも結合しており、このことがNaチャネルの軸索起始部への集積を可能にしている。アンキリンGは軸索起始部の形成と維持に最も重要な分子であり、アンキリンGの欠失により軸索起始部は消失する[6][7]。
イオンチャネル
軸索起始部には様々なイオンチャネルが局在し、その種類や分布は神経細胞の出力様式を決める重要な要素である[8][9]。
Naチャネル
Nav1.1、Nav1.2、Nav1.6の3つのサブタイプが知られる。Nav1.6は全ての神経細胞に発現し、活性化の閾値も低いことから活動電位の発生を担う最も重要なチャネルといえる。一方、Nav1.1とNav1.2はそれぞれ抑制性細胞と興奮性細胞に発現する。これらのチャネルは軸索起始部の近位部に局在し、活動電位の樹状突起への逆行性伝播を増強する。
Kチャネル
Kv1(Kv1.1、1.2)、Kv7(Kv7.2、7.3)、K2Pチャネル(TRAAK、TREK-1)などが知られる。これらのチャネルは静止膜電位付近でも活性化しており、短絡コンダクタンスとして活動電位の発生を抑える一方で、静止膜電位を維持することでNavチャネルの不活性化を防ぐ働きをもつ。
Caチャネル
Cav2(Cav2.1、Cav2.2、Cav2.3)、Cav3(Cav3.2)が知られる。Cav2.1やCav2.2は活性化の閾値が高く、BKチャネルを活性化させることで活動電位の再分極相を加速させるのに対して、Cav2.3やCav3.2は活性化の閾値が低く、後脱分極を増強することで持続的な発火を生じる。
その他
大脳皮質や海馬の錐体細胞では、軸索起始部にGABA作動性の軸索終末が軸索-軸索シナプスを形成する[10]。これらの神経細胞の軸索起始部ではK-Cl共輸送体(KCC2)の発現が低いため、軸索起始部でのGABAA受容体の活性化は軸索起始部局所の脱分極を生じるが、一方で、短絡コンダクタンスを増すため活動電位の発生は抑制される[11]。小脳のプルキンエ細胞の軸索起始部にもGABA作動性の軸索終末が分布するが、シナプスは形成されない[10]。この他軸索起始部に局在するチャネルや受容体として、HCNチャネル、5HT1受容体、P2Y受容体、D2受容体などの報告がある[9]。
機能
活動電位発生
軸索起始部は活動電位の発生に適した特性をもつ[2]。まず、軸索起始部は細胞体の近くにあるため、樹状突起や細胞体に入力するシナプス電流の電荷が届きやすい。また、軸索起始部は微細な構造であるため、僅かな電荷でも電位が大きく変化する。さらに、軸索起始部にはNaチャネルが高密度に分布するため、活動電位の発生閾値が特に低い。これらの特性により、軸索起始部は神経細胞における活動電位の起点として働く。
活動電位が軸索起始部で発生するという考えは、1950年代に行われた脊髄運動ニューロンでの細胞内電気記録の実験結果に基づいている[12][13]。この実験では、細胞体で記録される活動電位が軸索に由来する成分(ISスパイク)と細胞体に由来する成分(SDスパイク)の2つの成分からなり、ISスパイクはSDスパイクに先行することが示された。このことは、シナプス入力が活動電位を軸索で最初に発生させたのち、この活動電位が逆行性に軸索を細胞体へ伝播することによって、細胞体の活動電位が生じることを意味している。1990年代に、一部の神経細胞では樹状突起に強い入力を与えた際に樹状突起が活動電位の起点となり得ることが報告されたものの、その後、単一軸索からのパッチクランプ記録、Naイメージングや膜電位イメージングを用いた実験によって、生理的条件下では軸索起始部が活動電位の起点であることが示された。錐体細胞では、軸索起始部から細胞体へと伝播した活動電位はさらに樹状突起へ伝播し、シナプス応答を修飾する。
恒常的可塑性
軸索起始部の長さや軸索上の位置は神経活動の変化に応じて可塑的に変化し、この変化は恒常的可塑性として神経活動をネガティブフィードバックに調節する[14][15]。軸索起始部可塑性における軸索起始部の変化は細胞種によって異なる。例えば、発達期の視覚野や聴覚神経核では感覚入力によって軸索起始部の長さが短縮する[16][17]。一方、海馬の分散培養標本では脱分極によって軸索起始部の位置が細胞体から離れる[14]。また、嗅球では脱分極によって軸索起始部の位置が興奮性細胞と抑制性細胞で逆の変化を示し、興奮性細胞では細胞体から離れるのに対して、抑制性細胞では細胞体に近づく[18]。軸索起始部可塑性は神経細胞の興奮性が亢進するてんかんなどの病態でもみられる[19]。
軸索起始部可塑性は数時間から数日にわたる緩徐な変化であり、これは軸索起始部の分子構築の再編を反映すると考えられている。軸索起始部可塑性にはCaチャネルを介した細胞内Ca2+イオンの濃度変化が重要である。軸索起始部可塑性に関わる分子としては、カルシニューリンやサイクリン依存性タンパク質キナーゼ5(cdk5)が知られる[20][21][22]。これら分子が軸索起始部の分布を変化させるしくみは分かっていないが、エンドサイトーシスや微小管の再編が関わると考えられている。
極性維持
軸索起始部は、細胞体・樹状突起分子の軸索への侵入を防ぐ分子バリアとして働くことで神経細胞の極性を維持する。この分子バリアには膜拡散と細胞内輸送の2つのしくみが関わり、アンキリンGはこの両方において重要な役割を担うと考えられている[1][23]。このため、海馬や小脳の神経細胞ではアンキリンGの欠失によって軸索起始部が消失し、さらに軸索にはスパインやシナプス後肥厚のような樹状突起の性質がみられるようになる[6][7]。膜拡散のバリアとしては、細胞膜直下のアンキリンG-βIV スペクトリン-アクチンからなる細胞骨格に結合したイオンチャネルや接着分子などの膜貫通タンパク質が物理的に側方拡散を妨げる「ピケットフェンスモデル」が有力である[24]。一方、細胞内輸送によるバリアとしては、ミオシンVaとアクチンパッチによる細胞体・樹状突起分子の輸送制御、EB1/3を介した微小管へのアンキリンG結合による軸索輸送の障害、微小管結合タンパク質であるMicrotubule-associated protein 2(MAP2)やMicrotubule-associated protein 6(MAP6)による順行性輸送の制御、ダイニン調節因子であるNuclear distribution element-like 1(Ndel1)による逆行性輸送の制御などの説がある[1][23]。
疾患との関わり
軸索起始部を構成するイオンチャネルや骨格分子の異常は様々な精神神経疾患を引き起こす[1][25]。例えば、軸索起始部に局在するNav1.1、Nav1.2、Nav1.6、Kv7.2、Kv7.3などのイオンチャネルには多くの変異が知られ、これらはてんかんの発症と密接に関連する。アンキリンGはゲノムワイド関連解析(Genome-wide association study; GWAS)により双極性障害のリスク遺伝子とされ、アンキリンGの発現が低下したマウスでは精神疾患関連行動が生じる。また、アンキリンGのエクソン1b欠損マウスでは抑制性神経細胞の軸索起始部にNaチャネルが集積できず、双極性障害様行動、てんかん、突然死を示す。さらに、アンキリンGの変異は知的障害、統合失調症、自閉スペクトラム症とも関連する。一方、βIV スペクトリンの欠損や変異では運動障害や聴覚障害が認められ、αII スペクトリンの変異では早期乳児てんかん脳症、知的障害がみられる。軸索起始部構造の変化は、アンジェルマン症候群やアルツハイマー病、自己免疫性脱髄疾患、外傷性脳損傷、虚血性障害などでもみられ、これらは神経細胞の過興奮や機能障害を伴う。
参考文献
- ↑ 1.0 1.1 1.2 1.3 1.4
Huang, C.Y., & Rasband, M.N. (2018).
Axon initial segments: structure, function, and disease. Annals of the New York Academy of Sciences, 1420(1), 46-61. [PubMed:29749636] [PMC] [WorldCat] [DOI] - ↑ 2.0 2.1
Kole, M.H., & Stuart, G.J. (2012).
Signal processing in the axon initial segment. Neuron, 73(2), 235-47. [PubMed:22284179] [WorldCat] [DOI] - ↑
Jenkins, P.M., Kim, N., Jones, S.L., Tseng, W.C., Svitkina, T.M., Yin, H.H., & Bennett, V. (2015).
Giant ankyrin-G: a critical innovation in vertebrate evolution of fast and integrated neuronal signaling. Proceedings of the National Academy of Sciences of the United States of America, 112(4), 957-64. [PubMed:25552556] [PMC] [WorldCat] [DOI] - ↑
Xu, K., Zhong, G., & Zhuang, X. (2013).
Actin, spectrin, and associated proteins form a periodic cytoskeletal structure in axons. Science (New York, N.Y.), 339(6118), 452-6. [PubMed:23239625] [PMC] [WorldCat] [DOI] - ↑
Leterrier, C. (2018).
The Axon Initial Segment: An Updated Viewpoint. The Journal of neuroscience : the official journal of the Society for Neuroscience, 38(9), 2135-2145. [PubMed:29378864] [PMC] [WorldCat] [DOI] - ↑ 6.0 6.1
Maurel, P., Einheber, S., Galinska, J., Thaker, P., Lam, I., Rubin, M.B., ..., & Salzer, J.L. (2007).
Nectin-like proteins mediate axon Schwann cell interactions along the internode and are essential for myelination. The Journal of cell biology, 178(5), 861-74. [PubMed:17724124] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1
Guttmacher, A.E., Nabel, E.G., & Collins, F.S. (2009).
Why data-sharing policies matter. Proceedings of the National Academy of Sciences of the United States of America, 106(40), 16894. [PubMed:19805161] [PMC] [WorldCat] [DOI] - ↑
Lorincz, A., & Nusser, Z. (2008).
Cell-type-dependent molecular composition of the axon initial segment. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(53), 14329-40. [PubMed:19118165] [PMC] [WorldCat] [DOI] - ↑ 9.0 9.1
Jenkins, P.M., & Bender, K.J. (2025).
Axon initial segment structure and function in health and disease. Physiological reviews, 105(2), 765-801. [PubMed:39480263] [PMC] [WorldCat] [DOI] - ↑ 10.0 10.1
Howard, A., Tamas, G., & Soltesz, I. (2005).
Lighting the chandelier: new vistas for axo-axonic cells. Trends in neurosciences, 28(6), 310-6. [PubMed:15927687] [WorldCat] [DOI] - ↑
Szabadics, J., Varga, C., Molnár, G., Oláh, S., Barzó, P., & Tamás, G. (2006).
Excitatory effect of GABAergic axo-axonic cells in cortical microcircuits. Science (New York, N.Y.), 311(5758), 233-5. [PubMed:16410524] [WorldCat] [DOI] - ↑
COOMBS, J.S., CURTIS, D.R., & ECCLES, J.C. (1957).
The interpretation of spike potentials of motoneurones. The Journal of physiology, 139(2), 198-231. [PubMed:13492209] [PMC] [WorldCat] [DOI] - ↑
Debanne, D., Campanac, E., Bialowas, A., Carlier, E., & Alcaraz, G. (2011).
Axon physiology. Physiological reviews, 91(2), 555-602. [PubMed:21527732] [WorldCat] [DOI] - ↑ 14.0 14.1
Grubb, M.S., & Burrone, J. (2010).
Activity-dependent relocation of the axon initial segment fine-tunes neuronal excitability. Nature, 465(7301), 1070-4. [PubMed:20543823] [PMC] [WorldCat] [DOI] - ↑
Jung, C.K., Kang, Y.G., Bae, J.S., Lim, D.J., Choi, Y.J., & Lee, K.Y. (2010).
Unique patterns of tumor growth related with the risk of lymph node metastasis in papillary thyroid carcinoma. Modern pathology : an official journal of the United States and Canadian Academy of Pathology, Inc, 23(9), 1201-8. [PubMed:20543822] [WorldCat] [DOI] - ↑
Rabeyron, T. (2014).
Retro-priming, priming, and double testing: psi and replication in a test-retest design. Frontiers in human neuroscience, 8, 154. [PubMed:24672466] [PMC] [WorldCat] [DOI] - ↑
Akter, N., Fukaya, R., Adachi, R., Kawabe, H., & Kuba, H. (2020).
Structural and Functional Refinement of the Axon Initial Segment in Avian Cochlear Nucleus during Development. The Journal of neuroscience : the official journal of the Society for Neuroscience, 40(35), 6709-6721. [PubMed:32719016] [PMC] [WorldCat] [DOI] - ↑
Chand, A.N., Galliano, E., Chesters, R.A., & Grubb, M.S. (2015).
A distinct subtype of dopaminergic interneuron displays inverted structural plasticity at the axon initial segment. The Journal of neuroscience : the official journal of the Society for Neuroscience, 35(4), 1573-90. [PubMed:25632134] [PMC] [WorldCat] [DOI] - ↑
Harty, R.C., Kim, T.H., Thomas, E.A., Cardamone, L., Jones, N.C., Petrou, S., & Wimmer, V.C. (2013).
Axon initial segment structural plasticity in animal models of genetic and acquired epilepsy. Epilepsy research, 105(3), 272-9. [PubMed:23602553] [WorldCat] [DOI] - ↑
Evans, M.D., Sammons, R.P., Lebron, S., Dumitrescu, A.S., Watkins, T.B., Uebele, V.N., ..., & Grubb, M.S. (2013).
Calcineurin signaling mediates activity-dependent relocation of the axon initial segment. The Journal of neuroscience : the official journal of the Society for Neuroscience, 33(16), 6950-63. [PubMed:23595753] [PMC] [WorldCat] [DOI] - ↑
Trunova, S., Baek, B., & Giniger, E. (2011).
Cdk5 regulates the size of an axon initial segment-like compartment in mushroom body neurons of the Drosophila central brain. The Journal of neuroscience : the official journal of the Society for Neuroscience, 31(29), 10451-62. [PubMed:21775591] [PMC] [WorldCat] [DOI] - ↑
Jahan, I., Adachi, R., Egawa, R., Nomura, H., & Kuba, H. (2023).
CDK5/p35-Dependent Microtubule Reorganization Contributes to Homeostatic Shortening of the Axon Initial Segment. The Journal of neuroscience : the official journal of the Society for Neuroscience, 43(3), 359-372. [PubMed:36639893] [PMC] [WorldCat] [DOI] - ↑ 23.0 23.1
Fréal, A., & Hoogenraad, C.C. (2025).
The dynamic axon initial segment: From neuronal polarity to network homeostasis. Neuron, 113(5), 649-669. [PubMed:39947181] [WorldCat] [DOI] - ↑
Nakada, C., Ritchie, K., Oba, Y., Nakamura, M., Hotta, Y., Iino, R., ..., & Kusumi, A. (2003).
Accumulation of anchored proteins forms membrane diffusion barriers during neuronal polarization. Nature cell biology, 5(7), 626-32. [PubMed:12819789] [WorldCat] [DOI] - ↑
Buffington, S.A., & Rasband, M.N. (2011).
The axon initial segment in nervous system disease and injury. The European journal of neuroscience, 34(10), 1609-19. [PubMed:22103418] [PMC] [WorldCat] [DOI]