有毛細胞
大森 治紀
京都大学学際融合教育研究推進センター健康長寿社会の総合医療開発ユニット
DOI:10.14931/bsd.6398 原稿受付日:2015年8月12日 原稿完成日:2015年9月29日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
英語名:Hair cell 独:Haarzelle 仏:cellule ciliée
有毛細胞は聴覚、前庭覚、さらに魚類では側線器官の受容器細胞である。音、加速度、重力場での体軸方向などの感覚を電気信号に変換する事で、我々の脳神経回路が感覚情報として取り扱える形にする。感覚毛が頂部に生えており、感覚刺激によって引き起こされる感覚毛のわずかな偏位を刺激として受容する。
分布と機械刺激
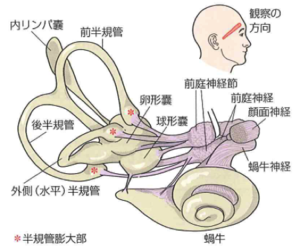
出典は標準生理学 第8版、医学書院の許可を得て掲載。
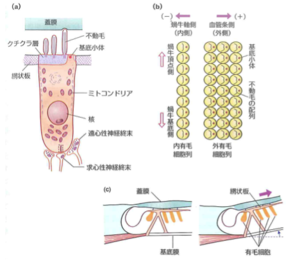
(a) 感覚毛およびシナプス
(b) 内外有毛細胞
(c) 基底膜の振動と機械刺激
出典は標準生理学 第8版、医学書院の許可を得て掲載。
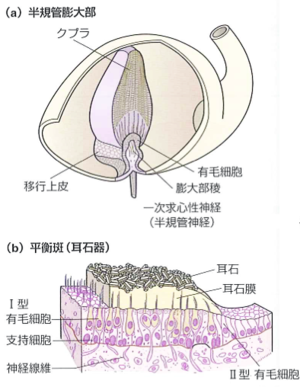
(a) 三半規管膨大部
(b) 耳石器官
出典は標準生理学 第8版、医学書院の許可を得て掲載。
有毛細胞はほ乳類に限らず内耳器官を持つ全動物種の感覚受容器細胞である(図1)。蝸牛器官では音波が基底膜を振動させそれによって生ずる微小な機械振動が有毛細胞の感覚毛を刺激する(図2)。前庭器官特に耳石器官では耳石膜が有毛細胞感覚毛を覆っており、体軸の動きが耳石膜の僅かな偏位を生ずることで機械刺激となる。三半規管の場合は体に加わる加速度がリンパ液の動きを生ずる事で膨大部を塞いでいるゼリー状のクプラに生ずるゆがみが機械刺激となる(図3)。クプラ様の構造は魚類の側線器官にもあり、側線管内の水流の僅かな変化がクプラにゆがみを生ずる事で有毛細胞感覚毛を機械刺激する。
ほ乳類内耳の蝸牛器官にはコルチ器官が、あぶみ骨に面した基部から蝸牛器官中心の頂部まで、およそ35mmの全長に亘り存在する。有毛細胞はコルチ器官の基底膜上に複数の支持細胞と共に存在する。ほ乳類の場合、有毛細胞は内有毛細胞と外有毛細胞の2種類に分類される。(図2b)。ヒトではおよそ3,500個の内有毛細胞が蝸牛軸の近くに1列の細胞群として分布する。その外側にはおよそ20,000個の外有毛細胞が3ないし4列存在する。
機械刺激の受容
有毛細胞は頂部に感覚毛を持つ。感覚毛は数10本の不動毛と1本の動毛(前庭系の有毛細胞には動毛はあるが、蝸牛有毛細胞には動毛は無く細胞体頂部のクチクラ板に隣接して基底小体がある)で構成される。不動毛間および動毛と不動毛の間には繊維状の微小結合がありtip linkと呼ばれる結合を含め機械刺激を線毛間に伝達するとともに線毛をまとめて1体の感覚毛を構成している。感覚毛に加わる微小な機械刺激が電気信号に変換される[1]。蝸牛器官の場合は基底膜の振動により蓋膜と基底膜との間で生ずる機械的なズレが直接あるいはリンパ液の動きを介して感覚毛を機械刺激する(図2c)。三半規管の場合は加速度によって生ずるリンパ液の僅かな動きが膨大部を埋めるクプラを変形させその中に刺さるように伸びている感覚毛を機械刺激する(図3a)。耳石器の場合は重力場での耳石の移動が耳石膜に接触している感覚毛に機械刺激となる(図3b)。いずれも微小な機械刺激量である。基底膜の振動振幅値としては数Å程度が実測されているが、機械振動は蝸牛器官内で能動的に増幅される事でもあり、最大でも10nmから100nm程度の刺激量が内耳蝸牛器官の有毛細胞感覚毛には加わると考えられる。非常に大きな機械刺激が蝸牛器官を破壊する事は過大音による聴覚障害として知られている。
感覚毛に局在する機械受容器チャネルはCa2+に対する透過性が高く[2]TRPチャネルの1種と考えられているがクローニングには成功していない。有毛細胞周囲のイオン環境は複雑である。側壁膜領域を浸し一般の組織液と相同のイオン組成を持つ外リンパ液に対して、感覚毛を生やす頂部は細胞内液と相同のイオン組成を持つ内リンパ液に浸されている。内外のリンパ液は網状板により隔てられている。内リンパ液のK+イオン濃度は高くK+イオンが受容器電流を運ぶ。感覚毛の生えている有毛細胞体頂部の内外ではK+イオン濃度がほぼ等しいと考えられK+イオンの平衡電位は0 mVとされる。また電位環境も複雑であり内リンパ腔(蝸牛器官中心階)は+80 mV程度の内リンパ腔電位をもつ。静止膜電位は細胞内液と側壁膜を隔てた外リンパ液との平衡で決まり通常の神経細胞と同等である(-60mV程度)。網状板は有毛細胞頂部と支持細胞とが強固なギャップ結合を形成する事で電気的には漏れを減らし大きな内リンパ腔電位を維持している。従って静止膜電位と内リンパ腔電位の差(約140 mV)が機械受容器チャンネルを通るK+イオンの駆動力となり、大きな内向きK+電流を生ずる事で蝸牛有毛細胞の機械刺激受容感度を高めている[3]。内リンパ腔電位は前庭器官ではおおよそ0mVであり、前庭器官の有毛細胞が受容器感度を特別に増大させる事は無い。前庭器官では高い受容器感度がめまいを生ずる可能性もある。内リンパ腔電位の分布の違いも合目的に解釈できる。
シナプス伝達
内有毛細胞体の基底部には求心性神経終末がリボンシナプスを作る。リボンシナプス構造により音刺激に対応して安定して高い頻度の伝達物質放出が実現される[4]。有毛細胞の脱分極は側壁膜のL型カルシウムチャネル (Cav1.3)を活性化し[5] [6]、流入するCa2+イオンが神経伝達物質であるグルタミン酸を放出する[7][8][9]。
内有毛細胞体のリボンシナプスは大きさが蝸牛軸側(内側面)と支持細胞である柱細胞側(外側面)とで異なる。蝸牛軸側には構造の大きなリボンシナプスが形成され、柱細胞側には小さなリボンシナプスが形成される。シナプス構造の違いは聴神経の自発発火頻度および閾値の違いに対応する。発火特性の異なる数10本の聴神経が1個の内有毛細胞にシナプス形成する事により広い音圧域に対応した聴神経線維の応答が実現される事が議論されている[10]。およそ30,000本の求心性神経(聴神経)は蝸牛軸を通って蝸牛器官内に入り、内側(蝸牛軸側)から有毛細胞に分布する。聴神経線維の95%が内有毛細胞体に分布する。数10本の聴神経線維が1個の内有毛細胞体にシナプス形成する。
これに対して求心性神経全体の5%程度が分枝を繰り返して複数の外有毛細胞にシナプスを形成する[11]。また遠心性神経線維(オリーブ蝸牛束)の多くは外有毛細胞体上にシナプス形成する。従って音を聞く細胞としての内有毛細胞に対して、外有毛細胞には蝸牛器官の感度を調節する役割が議論されている。
三半規管の有毛細胞には、I型と呼ばれカリックス型の求心性シナプス構造を持つフラスコ型の有毛細胞がほ乳類、鳥類およびは虫類で知られている。一方II型と呼ばれ円柱状でブトン型の求心性シナプス構造を持つ有毛細胞は全動物種で知られている[12]。求心性神経活動には持続的な発火活動および不規則な発火活動が知られ、シナプス構造との対応が議論されている[13]。耳石器官では有毛細胞の形状に特殊性は無いが、機械刺激感度に2方向性がある。これは分水嶺となる耳石器官上の領域を境に感覚毛配列の極性が変わり、機械感覚に対する受容器感度の方向性が異なる2種類の有毛細胞が存在する事による[12]。
受容器感度の調節
蝸牛器官の外有毛細胞は膜電位に応じて細胞体長を伸縮させる機能を持つ事から、蝸牛器官全体の受容器感度を調節する役割が議論されている[14] [15]。音波による振動刺激に応じて基底膜の振動振幅を外有毛細胞が能動的に変動させることが想定されており、結果として内有毛細胞の感覚毛に加わる機械刺激量を増幅し、音刺激に対する受容器感度を上げる働きをしているものと考えられている[16]。
遠心性神経線維の役割
遠心性神経線維(オリーブ蝸牛束)の一部は内有毛細胞に到る聴神経軸索終末にシナプス形成するが、多くは複数の外有毛細胞体にシナプスを形成する[11]。遠心性神経線維はアセチルコリンを神経伝達物質とする。外有毛細胞体にはアセチルコリン受容体(α9)があり、Ca2+イオンに対する透過性が高く、外有毛細胞ではCa2+イオン活性化カリウムチャネルを活性化することで膜過分極を起こし抑制的に働く[17] [18]。遠心性神経線維が下丘からの下降性投射を受けるオリーブ周辺核に起源を持ち、シナプスを外有毛細胞体に形成する事から遠心性神経には、カクテルパーティー現象の様な心理学的な聴覚現象への関与も期待されている。
関連項目
参考文献
- ↑
Hudspeth, A.J. (1983).
Mechanoelectrical transduction by hair cells in the acousticolateralis sensory system. Annual review of neuroscience, 6, 187-215. [PubMed:6301349] [WorldCat] [DOI] - ↑
Ohmori, H. (1985).
Mechano-electrical transduction currents in isolated vestibular hair cells of the chick. The Journal of physiology, 359, 189-217. [PubMed:2582113] [PMC] [WorldCat] [DOI] - ↑
Davis, H. (1965).
A model for transducer action in the cochlea. Cold Spring Harbor symposia on quantitative biology, 30, 181-90. [PubMed:5219471] [WorldCat] [DOI] - ↑
Khimich, D., Nouvian, R., Pujol, R., Tom Dieck, S., Egner, A., Gundelfinger, E.D., & Moser, T. (2005).
Hair cell synaptic ribbons are essential for synchronous auditory signalling. Nature, 434(7035), 889-94. [PubMed:15829963] [WorldCat] [DOI] - ↑
Robertson, D., & Paki, B. (2002).
Role of L-type Ca2+ channels in transmitter release from mammalian inner hair cells. II. Single-neuron activity. Journal of neurophysiology, 87(6), 2734-40. [PubMed:12037175] [WorldCat] [DOI] - ↑
Brandt, A., Khimich, D., & Moser, T. (2005).
Few CaV1.3 channels regulate the exocytosis of a synaptic vesicle at the hair cell ribbon synapse. The Journal of neuroscience : the official journal of the Society for Neuroscience, 25(50), 11577-85. [PubMed:16354915] [PMC] [WorldCat] [DOI] - ↑
Kim, M.H., Li, G.L., & von Gersdorff, H. (2013).
Single Ca2+ channels and exocytosis at sensory synapses. The Journal of physiology, 591(13), 3167-78. [PubMed:23459757] [PMC] [WorldCat] [DOI] - ↑
Kataoka, Y., & Ohmori, H. (1994).
Activation of glutamate receptors in response to membrane depolarization of hair cells isolated from chick cochlea. The Journal of physiology, 477 ( Pt 3), 403-14. [PubMed:7932230] [PMC] [WorldCat] [DOI] - ↑
Glowatzki, E., & Fuchs, P.A. (2002).
Transmitter release at the hair cell ribbon synapse. Nature neuroscience, 5(2), 147-54. [PubMed:11802170] [WorldCat] [DOI] - ↑
Hickman, T.T., Liberman, M.C., & Jacob, M.H. (2015).
Adenomatous Polyposis Coli Protein Deletion in Efferent Olivocochlear Neurons Perturbs Afferent Synaptic Maturation and Reduces the Dynamic Range of Hearing. The Journal of neuroscience : the official journal of the Society for Neuroscience, 35(24), 9236-45. [PubMed:26085645] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Spoendlin, H. (1985).
Anatomy of cochlear innervation. American journal of otolaryngology, 6(6), 453-67. [PubMed:3909832] [WorldCat] [DOI] - ↑ 12.0 12.1
Wersäll, J., Flock, A., & Lundquist, P.G. (1965).
Structural basis for directional sensitivity in cochlear and vestibular sensory receptors. Cold Spring Harbor symposia on quantitative biology, 30, 115-32. [PubMed:5295824] [WorldCat] [DOI] - ↑
Baird, R.A., Desmadryl, G., Fernández, C., & Goldberg, J.M. (1988).
The vestibular nerve of the chinchilla. II. Relation between afferent response properties and peripheral innervation patterns in the semicircular canals. Journal of neurophysiology, 60(1), 182-203. [PubMed:3404216] [WorldCat] [DOI] - ↑
Zheng, J., Shen, W., He, D.Z., Long, K.B., Madison, L.D., & Dallos, P. (2000).
Prestin is the motor protein of cochlear outer hair cells. Nature, 405(6783), 149-55. [PubMed:10821263] [WorldCat] [DOI] - ↑
Liberman, M.C., Gao, J., He, D.Z., Wu, X., Jia, S., & Zuo, J. (2002).
Prestin is required for electromotility of the outer hair cell and for the cochlear amplifier. Nature, 419(6904), 300-4. [PubMed:12239568] [WorldCat] [DOI] - ↑
Ashmore, J. (2008).
Cochlear outer hair cell motility. Physiological reviews, 88(1), 173-210. [PubMed:18195086] [WorldCat] [DOI] - ↑
GALAMBOS, R. (1956).
Suppression of auditory nerve activity by stimulation of efferent fibers to cochlea. Journal of neurophysiology, 19(5), 424-37. [PubMed:13367873] [WorldCat] [DOI] - ↑
Elgoyhen, A.B., Johnson, D.S., Boulter, J., Vetter, D.E., & Heinemann, S. (1994).
Alpha 9: an acetylcholine receptor with novel pharmacological properties expressed in rat cochlear hair cells. Cell, 79(4), 705-15. [PubMed:7954834] [WorldCat] [DOI]