軸索分岐
山本亘彦
大阪大学大学院 生命機能研究科 生命機能専攻 脳神経工学講座
DOI:10.14931/bsd.9320 原稿受付日:2020年8月15日 原稿完成日:2020年8月24日
担当編集委員:山形 方人(ハーバード大学・脳科学センター)
英:axonal branching 独:axonale Verzweigung 仏:branches axonales
軸索分岐は、神経系の発生期に軸索が多数の標的ニューロンと結合するために必要なプロセスである。分岐は細胞外シグナルによってトリガーされ、軸索内のシグナル伝達系を介して、最終的には細胞骨格の再編によって引き起こされる。軸索分岐の数や複雑さは、細胞外シグナルによって制御されるが、ニューロンの電気的活動によっても変化する。このように、軸索分岐は神経回路形成の先天的・後天的な制御の根幹をなしている。
構造
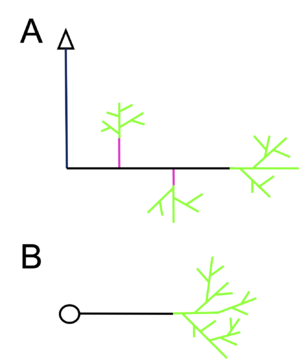
A. 大脳皮質運動野の第5層ニューロンから伸長した軸索は脊髄に投射するが、その途中に中脳や後脳において側枝(赤)を形成する(紋切型分岐)。
B. 網膜神経節細胞や外側膝状体 (LGN)ニューロンは標的領域で分岐を形成する(終末分岐、緑)。紋切型分岐で形成された側枝の末端でも終末分岐が生ずる。
ニューロンの細胞体を起源とする軸索は神経系の発生期に成長し、分岐することによって複数の標的細胞と結合する。軸索分岐は、その様式によって紋切型分岐(stereotyped branching)と終末分岐(terminal branching)に分けることができる。
紋切型分岐では、軸索はその経路上に位置する特定の脳部位あるいは局所領域において分枝を形成する。例えば、大脳皮質運動野の第5層ニューロンから発する軸索は脊髄に投射するが、その途中で側枝を作り中脳や後脳のニューロンと結合する[1](図1A)。この分岐パターンは個体さらには種を越えても保存されている。
一方、終末分岐では、軸索は標的領域に位置する複数の細胞とシナプス結合を形成するために、様々な数や複雑さで分枝を形成する。図1Bに示すように、主軸索から数本の娘枝が出現し、それらの娘枝から孫枝が現れると言った様式で込み入った分枝が形成されるが、その数や複雑さは一定ではない。視覚系における網膜から中継核である外側膝状体(lateral geniculate nucleus, LGN)への投射や外側膝状体から大脳皮質視覚野への投射における軸索分岐はこの終末分岐にあたる。紋切り型分岐によって出現した枝もその末端では終末分岐を形成し、多数の標的細胞と結合する(図1A)。
(注)本稿では、軸索から枝が形成される過程を「分岐」(branching)、その結果として形成された枝を「枝」または「分枝」として表現した。
構成
軸索分岐は主として発生期に生ずるが、紋切型分岐が神経回路形成の比較的初期に起こるのに対して、終末分岐は回路形成の後期に見出される。いずれのモードにおいても、枝は成長途上の軸索先端(成長円錐)よりも後方から出現することがほとんどで、いわゆる側枝分岐(interstitial branching)の様相を呈する[2] 。また、軸索分岐はシナプス形成と連動し、発生期に軸索上に形成される前シナプスが起点となって枝が出現することが報告されている[3][4] 。
分岐によって形成された枝は必ずしも固定化されている訳ではない。実際、終末分岐で分枝が複雑化する過程においては、枝は単に増えるだけでなく、一旦形成された枝が消える過程も同時平行的に生じている[5] 。また、余分に形成された枝が局所的に消失する過程(刈り込み, pruning)があることも知られている[1][6] 。このように、軸索分岐は正と負の2つの要因によって制御されている。
分子機構
細胞外シグナル
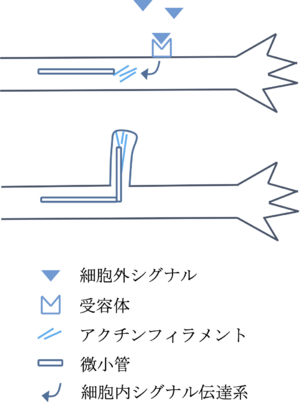
細胞外に発現する成長因子や軸索誘導分子が軸索の受容体に結合し、細胞内シグナル伝達系を介して、アクチンフィラメントによるフィロポディアの形成、微小管の侵入を促進することによって枝の形成が生ずる。
軸索分岐は細胞自律的に生ずることもあり得るが、細胞外シグナルによって誘導される。様々な分子が分岐に関与することが示されているが、基本的には軸索分岐に対して促進的に働く分子と抑制的に働く分子に分けることができる[7][8] 。神経成長因子(nerve growth factor)、脳由来神経栄養因子(brain-derived neurotrophic factor)や軸索ガイダンス分子であるネトリン(Netrin-1)、スリット(Slit2)、ウィント(Wnt3A, Wnt5A)は分岐を促進させ、一方セマフォリン(semaphorin3A)やエフリン(ephrinA, B)が分岐に抑制的に働く。これらの分子は、それぞれの受容体を介して、最終的に軸索内の細胞骨格の再編を制御する(以下参照、図2)。
これら正負の細胞外シグナル分子が時空間的に適切に配置されることによって、軸索分岐が制御される。ただし、細胞タイプや発生時期の違いによる受容体分子の発現パターン、あるいは複数の細胞外シグナルとの相互作用などによって、個々の細胞外シグナルの作用は一様ではないと考えられる。また、分岐の過程は枝の初期生成とその後の枝成長、ならびに主軸索成長との関連性など複数の要素から成るが、それぞれの分子がどの局面に関わるかについては必ずしも分かっていない。
細胞骨格制御
細胞外シグナルは成長中の軸索の細胞膜に分布する受容体に結合し、細胞内シグナル伝達系を介して、最終的に細胞骨格を変化させることによって分岐が生ずる[9][10] 。まず、軸索の局所領域でアクチンフィラメントが集積し(アクチンパッチ)、重合促進酵素の働きによってより長いアクチンフィラメントが作られ、フィロポディア(糸状仮足)と呼ばれる小突起が形成される(図2)。一方、微小管は微小管結合タンパク質(microtubule associated proteins, MAPs)により断片化や重合の制御を受けながら、アクチンフィラメントに沿ってフィロポディアに侵入し、より太く長い分枝へと成長する(図2)。
細胞骨格を制御する細胞内シグナル伝達系には幾つもの経路があるが、その中の一つ低分子量GTPase群は(RhoA, Rac1, cdc42など)、細胞骨格タンパクの再編を制御する舵取り役になる。特に、RhoAの機能を増大または減少させることによって軸索分岐が促進あるいは抑制されることが示されている[11] 。さらに、これらの低分子量GTPaseは様々な受容体からの細胞外シグナルを統括することができるため、軸索分岐の多様な制御が可能になると考えられる。
軸索分岐はシナプス形成とも連動し、前シナプスに集積する分子との相互作用も重要な要素になり得る。また、ミトコンドリアの局在によって分岐が誘導されることが報告され、軸索内での局所的なタンパク合成や集積との関連性が注目されている[12] 。
神経活動依存性
軸索分岐は発火活動やシナプス活動と言った神経活動によっても変化する。外側膝状体軸索は大脳皮質視覚野で終末分岐によって緻密な分枝を形成するが、その発火活動を抑制することによって分枝数は減少する。in vitroの実験においても、外側膝状体や大脳皮質ニューロンの軸索分岐は神経活動を低下させることで抑制され、発火活動を増大させることによって促進される[3] 。しかし、逆に作用するケースもある。網膜から外側膝状体や上丘(superior colliculus)への投射においては、神経活動を抑制することによって分枝の数や範囲が増大する[13][14] 。
このように、神経活動による作用は、神経系や発生段階の違い、あるいは軸索と標的細胞との相互作用によって異なる。さらに、網膜から外側膝状体への投射においては、神経活動に依存してミクログリアが前シナプスを貪食して刈り込みを促進することから[15] 、軸索と標的細胞以外の要因も神経活動依存的な分岐形成に重要な役割を果たしている。
神経活動が軸索分岐を制御するためには、それが分子シグナルに変換される必要がある。一般に神経活動は特定の転写調節因子を介して、その下流に位置する効果分子の発現を制御する[16] 。このメカニズムによって、細胞外シグナルの発現あるいは細胞骨格制御因子の発現や活性化がコントロールされていると考えられる。
参考文献
- ↑ 1.0 1.1
Luo, L., & O'Leary, D.D. (2005).
Axon retraction and degeneration in development and disease. Annual review of neuroscience, 28, 127-56. [PubMed:16022592] [WorldCat] [DOI] - ↑
Yamamoto, N., Higashi, S., & Toyama, K. (1997).
Stop and branch behaviors of geniculocortical axons: a time-lapse study in organotypic cocultures. The Journal of neuroscience : the official journal of the Society for Neuroscience, 17(10), 3653-63. [PubMed:9133388] [PMC] [WorldCat] - ↑ 3.0 3.1
Matsumoto, N., Hoshiko, M., Sugo, N., Fukazawa, Y., & Yamamoto, N. (2016).
Synapse-dependent and independent mechanisms of thalamocortical axon branching are regulated by neuronal activity. Developmental neurobiology, 76(3), 323-36. [PubMed:26061995] [WorldCat] [DOI] - ↑
Ruthazer, E.S., Akerman, C.J., & Cline, H.T. (2003).
Control of axon branch dynamics by correlated activity in vivo. Science (New York, N.Y.), 301(5629), 66-70. [PubMed:12843386] [WorldCat] [DOI] - ↑
Uesaka, N., Hayano, Y., Yamada, A., & Yamamoto, N. (2007).
Interplay between laminar specificity and activity-dependent mechanisms of thalamocortical axon branching. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(19), 5215-23. [PubMed:17494708] [PMC] [WorldCat] [DOI] - ↑
Hashimoto, K., Ichikawa, R., Kitamura, K., Watanabe, M., & Kano, M. (2009).
Translocation of a "winner" climbing fiber to the Purkinje cell dendrite and subsequent elimination of "losers" from the soma in developing cerebellum. Neuron, 63(1), 106-18. [PubMed:19607796] [WorldCat] [DOI] - ↑
Bilimoria, P.M., & Bonni, A. (2013).
Molecular control of axon branching. The Neuroscientist : a review journal bringing neurobiology, neurology and psychiatry, 19(1), 16-24. [PubMed:22179123] [PMC] [WorldCat] [DOI] - ↑
Gibson, D.A., & Ma, L. (2011).
Developmental regulation of axon branching in the vertebrate nervous system. Development (Cambridge, England), 138(2), 183-95. [PubMed:21177340] [PMC] [WorldCat] [DOI] - ↑
Gallo, G. (2011).
The cytoskeletal and signaling mechanisms of axon collateral branching. Developmental neurobiology, 71(3), 201-20. [PubMed:21308993] [WorldCat] [DOI] - ↑
Kalil, K., & Dent, E.W. (2014).
Branch management: mechanisms of axon branching in the developing vertebrate CNS. Nature reviews. Neuroscience, 15(1), 7-18. [PubMed:24356070] [PMC] [WorldCat] [DOI] - ↑
Hall, A., & Lalli, G. (2010).
Rho and Ras GTPases in axon growth, guidance, and branching. Cold Spring Harbor perspectives in biology, 2(2), a001818. [PubMed:20182621] [PMC] [WorldCat] [DOI] - ↑
Courchet, J., Lewis, T.L., Lee, S., Courchet, V., Liou, D.Y., Aizawa, S., & Polleux, F. (2013).
Terminal axon branching is regulated by the LKB1-NUAK1 kinase pathway via presynaptic mitochondrial capture. Cell, 153(7), 1510-25. [PubMed:23791179] [PMC] [WorldCat] [DOI] - ↑
McLaughlin, T., Torborg, C.L., Feller, M.B., & O'Leary, D.D. (2003).
Retinotopic map refinement requires spontaneous retinal waves during a brief critical period of development. Neuron, 40(6), 1147-60. [PubMed:14687549] [WorldCat] [DOI] - ↑
Sretavan, D.W., Shatz, C.J., & Stryker, M.P. (1988).
Modification of retinal ganglion cell axon morphology by prenatal infusion of tetrodotoxin. Nature, 336(6198), 468-71. [PubMed:2461517] [WorldCat] [DOI] - ↑
Schafer, D.P., Lehrman, E.K., Kautzman, A.G., Koyama, R., Mardinly, A.R., Yamasaki, R., ..., & Stevens, B. (2012).
Microglia sculpt postnatal neural circuits in an activity and complement-dependent manner. Neuron, 74(4), 691-705. [PubMed:22632727] [PMC] [WorldCat] [DOI] - ↑
Yamamoto, N., & López-Bendito, G. (2012).
Shaping brain connections through spontaneous neural activity. The European journal of neuroscience, 35(10), 1595-604. [PubMed:22607005] [WorldCat] [DOI]