「一酸化窒素」の版間の差分
細 →合成 |
|||
| (2人の利用者による、間の23版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0180808 澁木 克栄]</font><br> | <font size="+1">[http://researchmap.jp/read0180808 澁木 克栄]</font><br> | ||
''新潟大学脳研究所''<br> | ''新潟大学脳研究所''<br> | ||
DOI [[XXXX]]/XXXX 原稿受付日:2013年12月2日 原稿完成日:2013年月日<br> | |||
DOI | |||
担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | 担当編集委員:[http://researchmap.jp/2rikenbsi 林 康紀](独立行政法人理化学研究所 脳科学総合研究センター)<br> | ||
</div> | </div> | ||
英語名:nitric oxide 独:Stickstoffmonoxid 仏:monoxyde d' | 英語名:nitric oxide 独:Stickstoffmonoxid 仏:monoxyde d'azote | ||
同義語:血管内皮細胞由来弛緩因子、EDRF、 | |||
{{Chembox | {{Chembox | ||
| Verifiedfields = changed | | Verifiedfields = changed | ||
| verifiedrevid = 477001381 | | verifiedrevid = 477001381 | ||
| ImageFile = Nitric-oxide-2D.png | | ImageFile = Nitric-oxide-2D.png | ||
| ImageFile_Ref = {{chemboximage|correct|??}} | | ImageFile_Ref = {{chemboximage|correct|??}} | ||
| ImageSize = 121 | | ImageSize = 121 | ||
| ImageName = Skeletal formula of nitric oxide with bond length | | ImageName = Skeletal formula of nitric oxide with bond length | ||
| ImageFileL1 = Nitric oxide.svg | | ImageFileL1 = Nitric oxide.svg | ||
| ImageNameL1 = Skeletal formula showing three lone pairs and one unpaired electron | | ImageNameL1 = Skeletal formula showing three lone pairs and one unpaired electron | ||
| ImageFileR1 = Nitric-oxide-3D-vdW.png | | ImageFileR1 = Nitric-oxide-3D-vdW.png | ||
| ImageFileR1_Ref = {{chemboximage|correct|??}} | | ImageFileR1_Ref = {{chemboximage|correct|??}} | ||
| ImageNameR1 = Space-filling model of nitric oxide | | ImageSizeR1 = 121 | ||
| ImageNameR1 = Space-filling model of nitric oxide | |||
| IUPACName = Nitric oxide | | IUPACName = Nitric oxide | ||
| SystematicName = Oxidonitrogen(•)<ref>{{cite web|title = Nitric Oxide (CHEBI:16480)|url = https://www.ebi.ac.uk/chebi/searchId.do?chebiId=16480|work = Chemical Entities of Biological Interest (ChEBI)|location = UK|publisher = European Bioinformatics Institute}}</ref> (additive) | | SystematicName = Oxidonitrogen(•)<ref>{{cite web|title = Nitric Oxide (CHEBI:16480)|url = https://www.ebi.ac.uk/chebi/searchId.do?chebiId=16480|work = Chemical Entities of Biological Interest (ChEBI)|location = UK|publisher = European Bioinformatics Institute}}</ref> (additive) | ||
| OtherNames = Nitrogen monoxide<br /> | | OtherNames = Nitrogen monoxide<br /> | ||
Nitrogen(II) oxide | Nitrogen(II) oxide | ||
|Section1={{Chembox Identifiers | | Section1 = {{Chembox Identifiers | ||
| | | CASNo = 10102-43-9 | ||
| ChEMBL_Ref = {{ebicite|changed|EBI}} | | ChEMBL_Ref = {{ebicite|changed|EBI}} | ||
| ChEMBL = 1200689 | | ChEMBL = 1200689 | ||
| CASNo_Ref = {{cascite|correct|CAS}} | | CASNo_Ref = {{cascite|correct|CAS}} | ||
| PubChem = 145068 | | PubChem = 145068 | ||
| ChemSpiderID = 127983 | | PubChem_Ref = {{Pubchemcite|correct|pubchem}} | ||
| ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}} | | ChemSpiderID = 127983 | ||
| UNII = 31C4KY9ESH | | ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}} | ||
| UNII_Ref = {{fdacite|correct|FDA}} | | UNII = 31C4KY9ESH | ||
| EINECS = 233-271-0 | | UNII_Ref = {{fdacite|correct|FDA}} | ||
| UNNumber = 1660 | | EINECS = 233-271-0 | ||
| DrugBank_Ref = {{drugbankcite|correct|drugbank}} | | UNNumber = 1660 | ||
| DrugBank_Ref = {{drugbankcite|correct|drugbank}} | |||
| DrugBank = DB00435 | | DrugBank = DB00435 | ||
| KEGG = D00074 | | KEGG = D00074 | ||
| KEGG_Ref = {{keggcite|correct|kegg}} | | KEGG_Ref = {{keggcite|correct|kegg}} | ||
| ChEBI_Ref = {{ebicite|correct|EBI}} | | ChEBI_Ref = {{ebicite|correct|EBI}} | ||
| ChEBI = 16480 | | ChEBI = 16480 | ||
| RTECS = QX0525000 | | RTECS = QX0525000 | ||
| Gmelin = 451 | | Gmelin = 451 | ||
| 3DMet = B00122 | | 3DMet = B00122 | ||
| ATCCode_prefix = R07 | |||
| SMILES = [N]=O | | ATCCode_suffix = AX01 | ||
| StdInChI = 1S/NO/c1-2 | | SMILES = [N]=O | ||
| StdInChI_Ref = {{stdinchicite|correct|chemspider}} | | StdInChI = 1S/NO/c1-2 | ||
| InChI = 1/NO/c1-2 | | StdInChI_Ref = {{stdinchicite|correct|chemspider}} | ||
| StdInChIKey = MWUXSHHQAYIFBG-UHFFFAOYSA-N | | InChI = 1/NO/c1-2 | ||
| StdInChIKey_Ref = {{stdinchicite|correct|chemspider}} | | StdInChIKey = MWUXSHHQAYIFBG-UHFFFAOYSA-N | ||
| InChIKey = MWUXSHHQAYIFBG-UHFFFAOYAI | | StdInChIKey_Ref = {{stdinchicite|correct|chemspider}} | ||
| InChIKey = MWUXSHHQAYIFBG-UHFFFAOYAI | |||
}} | }} | ||
|Section2={{Chembox Properties | | Section2 = {{Chembox Properties | ||
| N=1 | O=1 | | N = 1 | ||
| Appearance = Colourless gas | | O = 1 | ||
| Density = 1.3402 g dm<sup>−3</sup> | | ExactMass = 29.997988627 g mol<sup>−1</sup> | ||
| MeltingPtC = −164 | | Appearance = Colourless gas | ||
| BoilingPtC = −152 | | Density = 1.3402 g dm<sup>−3</sup> | ||
| Solubility = | | MeltingPtC = −164 | ||
| RefractIndex = 1.0002697 | | BoilingPtC = −152 | ||
| Solubility = 74 cm<sup>3</sup> dm<sup>−3</sup> | |||
| RefractIndex = 1.0002697 | |||
}} | }} | ||
|Section3={{Chembox Structure | | Section3 = {{Chembox Structure | ||
| MolShape = linear ([[point group]] C<sub>∞''v''</sub>) | | MolShape = linear ([[point group]] C<sub>∞''v''</sub>) | ||
}} | }} | ||
| | | Section4 = {{Chembox Thermochemistry | ||
| DeltaHf = | | DeltaHf = 90.29 kJ mol<sup>−1</sup> | ||
| Entropy = 210.76 J K<sup>−1</sup> mol<sup>−1</sup> | | Entropy = 210.76 J K<sup>−1</sup> mol<sup>−1</sup> | ||
}} | }} | ||
| | | Section5 = {{Chembox Pharmacology | ||
| | | AdminRoutes = [[Inhalation]] | ||
| Bioavail = good | |||
| Metabolism = via pulmonary capillary bed | |||
| Bioavail = good | | HalfLife = 2–6 seconds | ||
| Metabolism = via pulmonary capillary bed | |||
| HalfLife = 2–6 seconds | |||
}} | }} | ||
| | | Section6 = {{Chembox Hazards | ||
| | | ExternalMSDS = [http://avogadro.chem.iastate.edu/MSDS/nitric_oxide.pdf External MSDS] | ||
| EUClass = {{Hazchem O}} {{Hazchem T}} | | EUClass = {{Hazchem O}} {{Hazchem T}} | ||
| RPhrases = {{R8}}, {{R23}}, {{R34}}, {{R44}} | | RPhrases = {{R8}}, {{R23}}, {{R34}}, {{R44}} | ||
| SPhrases = {{S1}}, {{S17}}, {{S23}}, {{S36/37/39}}, {{S45}} | | SPhrases = {{S1}}, {{S17}}, {{S23}}, {{S36/37/39}}, {{S45}} | ||
| NFPA-H = 3 | | NFPA-H = 3 | ||
| NFPA-F = 0 | | NFPA-F = 0 | ||
| NFPA-R = 3 | | NFPA-R = 3 | ||
| NFPA- | | NFPA-O = OX | ||
}} | }} | ||
| | | Section7 = {{Chembox Related | ||
| | | Function = [[nitrogen]] [[oxide]]s | ||
| | | OtherFunctn = [[Dinitrogen pentoxide]]<br /> | ||
[[Dinitrogen tetroxide]]<br /> | [[Dinitrogen tetroxide]]<br /> | ||
[[Dinitrogen trioxide]]<br /> | [[Dinitrogen trioxide]]<br /> | ||
[[Nitrogen dioxide]]<br /> | [[Nitrogen dioxide]]<br /> | ||
[[Nitrous oxide]] | [[Nitrous oxide]] | ||
}} | }} | ||
}} | }} | ||
| 113行目: | 106行目: | ||
==合成== | ==合成== | ||
[[ | NOは生体内では[[一酸化窒素合成酵素]]により[[アルギニン]]からNADPHを補酵素として合成される(図1)。アルギニンはNω-ヒドロキシ-L-アルギニンをへて、最終的にNOとシトルリンとなる。 | ||
一酸化窒素合成酵素はヘムを含むタンパク質であり、[[血管内皮型一酸化窒素合成酵素|血管内皮型]](eNOS)、[[神経型一酸化窒素合成酵素|神経型]](nNOS)及び[[誘導型一酸化窒素合成酵素|誘導型]](iNOS)の3タイプがある<ref name=ref1><pubmed>18588525</pubmed></ref>。 | |||
{| class="wikitable" | {| class="wikitable" | ||
| 134行目: | 125行目: | ||
*心血管系 | *心血管系 | ||
*肺など | *肺など | ||
| | || ||[[サイトカイン]]などによる酵素発現の誘導。 | ||
|[[サイトカイン]] | |||
|- | |- | ||
| '''内皮型''' (eNOS) || [http://mouse.brain-map.org/experiment/show/75831750 NOS3] || | | '''内皮型''' (eNOS) || [http://mouse.brain-map.org/experiment/show/75831750 NOS3] || カルシウム/[[カルモジュリン]] | ||
*[[血管内皮細胞]] | *[[血管内皮細胞]] | ||
*[[骨髄]]細胞 | *[[骨髄]]細胞 | ||
| 143行目: | 133行目: | ||
||[[細胞膜]]に結合しやすい性質を持っている。||カルシウム/カルモジュリン | ||[[細胞膜]]に結合しやすい性質を持っている。||カルシウム/カルモジュリン | ||
|} | |} | ||
Wikipediaより改変。遺伝子名はAllen Brain Atlasへのリンク。 | Wikipediaより改変。遺伝子名はAllen Brain Atlasへのリンク。 | ||
[[ファイル:NOS reaction.png|thumb|right|350px|'''図1. 一酸化窒素合成経路'''<br>Arg: アルギキン、NOHLA: Nω-ヒドロキシ-L-アルギニン、NADPH: ニコチンアミドアデニンジヌクレオチドリン酸。図中でオレンジ色で示されているのは酵素のヘム部位。]] | |||
==作用機構== | ==作用機構== | ||
NOの作用機構は多様であるが、主要なものとして[[グアニル酸シクラーゼ]]を活性し、細胞内の[[cGMP]]レベルを上げることが挙げられる。 | |||
== | ==機能== | ||
さらに神経細胞でもNOは合成され、脳の様々な場所で情報伝達を担うことにより、非常に多彩な機能に関与している。主要な脳機能としては、[[シナプス可塑性]]の調節因子、[[脳血流量]]の調節因子、[[神経細胞死]]への関与などが挙げられる。 | |||
=== シナプス可塑性の調節物質=== | === シナプス可塑性の調節物質=== | ||
[[image:一酸化窒素(脳科学辞典).jpg|thumb|240px|''' | [[image:一酸化窒素(脳科学辞典).jpg|thumb|240px|'''図.シナプス可塑性の調節因子としてのNO'''<br>シナプス前部から伝達物質と共に放出される場合(A)やシナプス後部からシナプス伝達の方向とは逆に放出される場合(B)や、シナプス近傍の抑制性のインターニューロンから放出される場合(C)など、様々なケースがある。]] | ||
NOの脳における重要な機能として[[シナプス]]可塑性の調節因子としての働きが挙げられる<ref name=ref2><pubmed>24198758</pubmed></ref>。NOが関与するシナプス可塑性としては[[小脳]]の[[長期抑圧]]、[[海馬]]の[[長期増強]]、[[大脳皮質]]の長期増強などがある。いずれの場合も、特定の膜に閉ざされたコンパートメントから、別の膜に閉ざされたコンパートメントに、NOのガス拡散特性によって情報を伝達しているという点に特徴がある(図)。NOの放出部位はシナプス前部、後部、[[抑制性介在神経]]と多彩であり、NOはシナプスの可塑性に必須な因子というより、状況に応じて誘発を促進する調節因子であるという点が共通している。 | |||
====小脳長期抑圧現象==== | ====小脳長期抑圧現象==== | ||
小脳皮質からの唯一の出力細胞である[[プルキンエ細胞]]は、[[平行線維]]と[[登上線維]]からシナプス入力を受け。この二つが同期して起きたときに平行線維-プルキンエ細胞間シナプスが長期[[抑圧]]を起こす。小脳の長期抑圧は、ある種の運動学習の基礎メカニズムであると考えられている。小脳の長期抑圧は、シナプス後部であるプルキンエ細胞において生ずる。一方、平行線維を出す[[顆粒細胞]]はnNOSを多量に含み、NOは平行線維から放出されてプルキンエ細胞に、あるいは平行線維自身に作用すると考えられている。培養プルキンエ細胞を用た単純な実験系ではNOの関与なしに[[グルタミン酸]]応答の抑圧が起きるが、小脳長期抑圧を必要とする運動学習はNO依存性を示す、つまり標本による違いはあるものの、少なくとも個体レベルにおいて[[運動学習]]はNOによって促進的な修飾作用を受けると考えられる。 | 小脳皮質からの唯一の出力細胞である[[プルキンエ細胞]]は、[[平行線維]]と[[登上線維]]からシナプス入力を受け。この二つが同期して起きたときに平行線維-プルキンエ細胞間シナプスが長期[[抑圧]]を起こす。小脳の長期抑圧は、ある種の運動学習の基礎メカニズムであると考えられている。小脳の長期抑圧は、シナプス後部であるプルキンエ細胞において生ずる。一方、平行線維を出す[[顆粒細胞]]はnNOSを多量に含み、NOは平行線維から放出されてプルキンエ細胞に、あるいは平行線維自身に作用すると考えられている。培養プルキンエ細胞を用た単純な実験系ではNOの関与なしに[[グルタミン酸]]応答の抑圧が起きるが、小脳長期抑圧を必要とする運動学習はNO依存性を示す、つまり標本による違いはあるものの、少なくとも個体レベルにおいて[[運動学習]]はNOによって促進的な修飾作用を受けると考えられる。 | ||
====海馬長期増強現象==== | ====海馬長期増強現象==== | ||
[[海馬]][[錐体細胞]]への入力線維を高頻度で刺激すると、[[シナプス後膜]]の[[NMDA型グルタミン酸受容体]]が活性化されてカルシウムが流入し、長期増強が起きる。長期増強には、シナプス後部のグルタミン酸[[受容体]]数が増加する型と、[[シナプス前部]]からのグルタミン酸放出量が増大する型がある。[[シナプス前]]部でグルタミン酸の放出が起きるためには、カルシウム流入があったシナプス後部からシナプス前部へと逆行性に情報を伝達するメカニズムがあるのではないかと想定され、NOもそのような[[逆行性情報伝達]]物質の候補として考えられた。しかしNOが長期増強の誘導に関与するにしても実験温度や動物の週令、刺激強度や刺激パターンなど様々な実験条件が適切に設定された場合のみであることが判ってきた。即ちNOは長期増強の成立には必須ではないが、実験条件によっては長期増強を促進する調節物質の一つであると思われる。 | [[海馬]][[錐体細胞]]への入力線維を高頻度で刺激すると、[[シナプス後膜]]の[[NMDA型グルタミン酸受容体]]が活性化されてカルシウムが流入し、長期増強が起きる。長期増強には、シナプス後部のグルタミン酸[[受容体]]数が増加する型と、[[シナプス前部]]からのグルタミン酸放出量が増大する型がある。[[シナプス前]]部でグルタミン酸の放出が起きるためには、カルシウム流入があったシナプス後部からシナプス前部へと逆行性に情報を伝達するメカニズムがあるのではないかと想定され、NOもそのような[[逆行性情報伝達]]物質の候補として考えられた。しかしNOが長期増強の誘導に関与するにしても実験温度や動物の週令、刺激強度や刺激パターンなど様々な実験条件が適切に設定された場合のみであることが判ってきた。即ちNOは長期増強の成立には必須ではないが、実験条件によっては長期増強を促進する調節物質の一つであると思われる。 | ||
====大脳皮質長期増強現象==== | ====大脳皮質長期増強現象==== | ||
[[大脳皮質]]でも長期増強は起きる。この長期増強とNOとの関係には大脳皮質の層毎の違いがある。即ち大脳皮質のIV層を刺激するとII/III層及びV層の両方にLTPが起きるが、V層のLTPのみが一酸化窒素合成酵素阻害剤によって有意に小さくなる。大脳皮質のNO合成酵素は主に深い層の小型の[[介在神経細胞]]に局在し、これが活動する時にNOも放出される。 | [[大脳皮質]]でも長期増強は起きる。この長期増強とNOとの関係には大脳皮質の層毎の違いがある。即ち大脳皮質のIV層を刺激するとII/III層及びV層の両方にLTPが起きるが、V層のLTPのみが一酸化窒素合成酵素阻害剤によって有意に小さくなる。大脳皮質のNO合成酵素は主に深い層の小型の[[介在神経細胞]]に局在し、これが活動する時にNOも放出される。 | ||
2013年12月6日 (金) 18:34時点における版
英語名:nitric oxide 独:Stickstoffmonoxid 仏:monoxyde d'azote
同義語:血管内皮細胞由来弛緩因子、EDRF、
| 一酸化窒素 | |
|---|---|

| |
Nitric oxide | |
Oxidonitrogen(•)[1] (additive) | |
別称 Nitrogen monoxide Nitrogen(II) oxide | |
| Identifiers | |
| 10102-43-9 | |
| 3DMet | B00122 |
| ATC code | |
| ChEBI | |
| ChEMBL | ChEMBL1200689 |
| ChemSpider | 127983 |
| DrugBank | {{{value}}} |
| EC-number | [1] |
| Gmelin Reference | 451 |
| |
| Jmol-3D images | Image |
| KEGG | D00074 |
| PubChem | 145068 |
| RTECS番号 | QX0525000 |
| |
| UNII | 31C4KY9ESH |
| 国連番号 | 1660 |
| Properties | |
| NO | |
| Molar mass | 30.006 g·mol−1 |
| Appearance | Colourless gas |
| Density | 1.3402 g dm−3 |
| Melting point | −164 °C (−263 °F; 109 K) |
| Boiling point | |
| 74 cm3 dm−3 | |
| 屈折率 (nD) | 1.0002697 |
| Structure | |
| 分子の形 | linear (point group C∞v) |
| 熱化学 | |
| 標準生成熱 ΔfH |
90.29 kJ mol−1 |
| 標準モルエントロピー S |
210.76 J K−1 mol−1 |
| Pharmacology | |
| Bioavailability | good |
| Routes of administration |
Inhalation |
| Metabolism | via pulmonary capillary bed |
| Elimination half-life |
2–6 seconds |
| 危険性 | |
| MSDS | External MSDS |
| EU分類 | |
| Rフレーズ | R8, R23, R34, R44 |
| S-phrases | (S1), S17, S23, S36/37/39, S45 |
| 関連する物質 | |
| 関連するnitrogen oxides | Dinitrogen pentoxide Dinitrogen tetroxide |
| 特記なき場合、データは常温(25 °C)・常圧(100 kPa)におけるものである。 | |
一酸化窒素とは
一酸化窒素(NO)は分子量30の無色透明なガスで、酸素に触れると直ちに酸化されて酸素二酸化窒素となる。このような不安定な無機ガスは、近年まで生体とは全く無縁であると考えられていたが、血管内皮細胞由来の血管平滑筋弛緩因子(EDRF)として循環制御に重要な役割を果たすことが発見された。NOの物質としての特徴はガス状物質であり、細胞膜を透過して拡散しやすいこと、及び生体内で速やかに酸化され、半減期が1秒程度と短いことである。これらのユニークなNOの特性による情報伝達の発見は1998年のノーベル医学・生理学賞の受賞対象となった。
合成
NOは生体内では一酸化窒素合成酵素によりアルギニンからNADPHを補酵素として合成される(図1)。アルギニンはNω-ヒドロキシ-L-アルギニンをへて、最終的にNOとシトルリンとなる。
一酸化窒素合成酵素はヘムを含むタンパク質であり、血管内皮型(eNOS)、神経型(nNOS)及び誘導型(iNOS)の3タイプがある[2]。
| 名称 | 遺伝子 | 発現 | 細胞局在 | 活性調節 |
| 神経型 (nNOS) | NOS1 | 細胞質。またPSD-95などと結合し、シナプスに集積する。 | カルシウム/カルモジュリン | |
| 誘導型 (iNOS) | NOS2 |
|
サイトカインなどによる酵素発現の誘導。 | |
| 内皮型 (eNOS) | NOS3 | カルシウム/カルモジュリン | 細胞膜に結合しやすい性質を持っている。 | カルシウム/カルモジュリン |
Wikipediaより改変。遺伝子名はAllen Brain Atlasへのリンク。
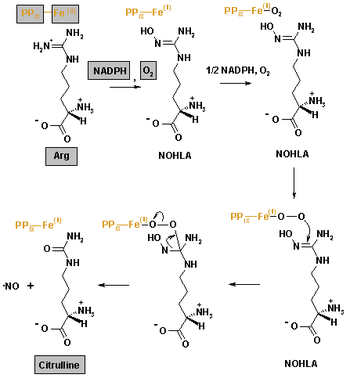
Arg: アルギキン、NOHLA: Nω-ヒドロキシ-L-アルギニン、NADPH: ニコチンアミドアデニンジヌクレオチドリン酸。図中でオレンジ色で示されているのは酵素のヘム部位。
作用機構
NOの作用機構は多様であるが、主要なものとしてグアニル酸シクラーゼを活性し、細胞内のcGMPレベルを上げることが挙げられる。
機能
さらに神経細胞でもNOは合成され、脳の様々な場所で情報伝達を担うことにより、非常に多彩な機能に関与している。主要な脳機能としては、シナプス可塑性の調節因子、脳血流量の調節因子、神経細胞死への関与などが挙げられる。
シナプス可塑性の調節物質
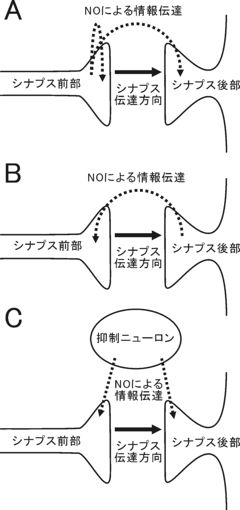
シナプス前部から伝達物質と共に放出される場合(A)やシナプス後部からシナプス伝達の方向とは逆に放出される場合(B)や、シナプス近傍の抑制性のインターニューロンから放出される場合(C)など、様々なケースがある。
NOの脳における重要な機能としてシナプス可塑性の調節因子としての働きが挙げられる[3]。NOが関与するシナプス可塑性としては小脳の長期抑圧、海馬の長期増強、大脳皮質の長期増強などがある。いずれの場合も、特定の膜に閉ざされたコンパートメントから、別の膜に閉ざされたコンパートメントに、NOのガス拡散特性によって情報を伝達しているという点に特徴がある(図)。NOの放出部位はシナプス前部、後部、抑制性介在神経と多彩であり、NOはシナプスの可塑性に必須な因子というより、状況に応じて誘発を促進する調節因子であるという点が共通している。
小脳長期抑圧現象
小脳皮質からの唯一の出力細胞であるプルキンエ細胞は、平行線維と登上線維からシナプス入力を受け。この二つが同期して起きたときに平行線維-プルキンエ細胞間シナプスが長期抑圧を起こす。小脳の長期抑圧は、ある種の運動学習の基礎メカニズムであると考えられている。小脳の長期抑圧は、シナプス後部であるプルキンエ細胞において生ずる。一方、平行線維を出す顆粒細胞はnNOSを多量に含み、NOは平行線維から放出されてプルキンエ細胞に、あるいは平行線維自身に作用すると考えられている。培養プルキンエ細胞を用た単純な実験系ではNOの関与なしにグルタミン酸応答の抑圧が起きるが、小脳長期抑圧を必要とする運動学習はNO依存性を示す、つまり標本による違いはあるものの、少なくとも個体レベルにおいて運動学習はNOによって促進的な修飾作用を受けると考えられる。
海馬長期増強現象
海馬錐体細胞への入力線維を高頻度で刺激すると、シナプス後膜のNMDA型グルタミン酸受容体が活性化されてカルシウムが流入し、長期増強が起きる。長期増強には、シナプス後部のグルタミン酸受容体数が増加する型と、シナプス前部からのグルタミン酸放出量が増大する型がある。シナプス前部でグルタミン酸の放出が起きるためには、カルシウム流入があったシナプス後部からシナプス前部へと逆行性に情報を伝達するメカニズムがあるのではないかと想定され、NOもそのような逆行性情報伝達物質の候補として考えられた。しかしNOが長期増強の誘導に関与するにしても実験温度や動物の週令、刺激強度や刺激パターンなど様々な実験条件が適切に設定された場合のみであることが判ってきた。即ちNOは長期増強の成立には必須ではないが、実験条件によっては長期増強を促進する調節物質の一つであると思われる。
大脳皮質長期増強現象
大脳皮質でも長期増強は起きる。この長期増強とNOとの関係には大脳皮質の層毎の違いがある。即ち大脳皮質のIV層を刺激するとII/III層及びV層の両方にLTPが起きるが、V層のLTPのみが一酸化窒素合成酵素阻害剤によって有意に小さくなる。大脳皮質のNO合成酵素は主に深い層の小型の介在神経細胞に局在し、これが活動する時にNOも放出される。
脳血流量の調節
NOが血管内皮細胞由来弛緩因子という機能を有する以上、脳の血流量の調節も他の臓器と同様に関わる[4]。また、血管内皮細胞以外にも、ある種の自律神経終末はNOを直接放出する機能を持ち、血流調節に関わっている。
脳に特徴的な血流調節として興味深いのは、脳活動によって局所の脳血流量が増大する現象で、神経細胞の少なくとも一部が一酸化窒素合成酵素を有する以上、局所血流量調節の少なくとも一部はNOを介すると思われる。しかし、それ以外の複数の血流調節因子の関与も想定されており、NOの役割は部分的である。
神経細胞死
NOは免疫系の細胞においてiNOSから作られ、細胞障害性を示す。従って脳に炎症があるとき、免疫系の細胞が動員されて、神経細胞死に関わる。また、本来はシナプス可塑性や脳血流の調節因子として作り出されるNOが、脳虚血などの病態に伴って、細胞障害性を示すという場合もある。しかし、その一方でNOは低濃度で神経細胞保護作用を有するという知見もあり、どのような実験条件下でどのような評価法によりその効果を判定したかということに留意する必要がある[5]。
関連語
参考文献
- ↑ "Nitric Oxide (CHEBI:16480)". Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ↑
Garthwaite, J. (2008).
Concepts of neural nitric oxide-mediated transmission. The European journal of neuroscience, 27(11), 2783-802. [PubMed:18588525] [PMC] [WorldCat] [DOI] - ↑
Hardingham, N., Dachtler, J., & Fox, K. (2013).
The role of nitric oxide in pre-synaptic plasticity and homeostasis. Frontiers in cellular neuroscience, 7, 190. [PubMed:24198758] [PMC] [WorldCat] [DOI] - ↑
Gordon, G.R., Mulligan, S.J., & MacVicar, B.A. (2007).
Astrocyte control of the cerebrovasculature. Glia, 55(12), 1214-21. [PubMed:17659528] [WorldCat] [DOI] - ↑
Calabrese, V., Mancuso, C., Calvani, M., Rizzarelli, E., Butterfield, D.A., & Stella, A.M. (2007).
Nitric oxide in the central nervous system: neuroprotection versus neurotoxicity. Nature reviews. Neuroscience, 8(10), 766-75. [PubMed:17882254] [WorldCat] [DOI]