アセチル化
英語名:acetylation 独:Acetylierung 仏:acétylation

代表的なアセチル化反応であるアスピリンの合成反応を示した。円で囲われたサリチル酸の水酸基が無水酢酸との反応によりアセチル基に置換され、アスピリンが合成される。
アセチル化とは、有機化合物の水酸基(-OH)やアミノ基(-NH2)などの水素原子をアセチル基(-COCH3)で置換することである(図1)。IUPAC命名法ではエタノイル化という。逆に、有機化合物からアセチル基が除かれる反応は脱アセチル化という。代表的なアセチル化剤として、無水酢酸、塩化アセチル、酢酸メチル、N-メチルアセトアミドなどが使われている。
タンパク質のアセチル化
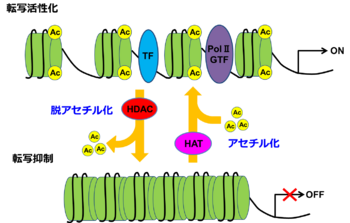
ヒストンがHATによりアセチル化された状態ではヒストン-DNA間の結合が緩むことで、TFやPolⅡの結合が可能となり、転写は活性化される。逆にHDACにより、ヒストンが脱アセチル化されるとTF、PolⅡが結合出来ないため転写は抑制される。
GTF:general transcription factor:基本転写因子群、Ac:acetylation:アセチル化
タンパク質のアセチル化は、クロマチンの構造制御や転写活性制御に重要な働きをしている。転写活性化に働く補因子の多くがアセチル化酵素活性を持っており、逆に転写抑制に働く補因子の多くは脱アセチル化酵素活性を有する。
ヒストン
タンパク質のアセチル化において最も多く報告されているのがヒストンのアセチル化及び脱アセチル化である。これらは遺伝子の発現制御に密接に関わっている。ヒストンはアセチル化されることでヒストン中の特定のリジン残基のアミノ基(-NH2(-NH3+))をアセトアミド(-NHCOCH3)に変換することにより電荷を中和し、ヒストン-DNA間の結合を部分的に弱める。これにより、DNA鎖に対して転写因子やRNAポリメラーゼ(PolⅡ)がより結合しやすい状態になり、結果として転写が活性化される。逆に、ヒストンが脱アセチル化されるとアセチル基が加水分解により除去され、元のアミノ基に戻ることによりヒストンへのDNAの巻きつきが強められ転写が抑制される(図2)。
ヒストンアセチル基転移酵素
- 代表的なヒストンアセチル基転移酵素(HAT、histone acetyltransferase)として、CBP/p300(CREB binding protein)やPCAF(p300/CBP-associated factor)などが存在する。
ヒストン脱アセチル化酵素
- ヒストン脱アセチル化酵素(HDAC、histone deacetylase)には5つのファミリーがあり、それぞれCLASSⅠ(HDAC1、2、3、8)、CLASSⅡa(HDAC4、5、7、9)、CLASSⅡb(HDAC6、10)、CLASSⅢ(SIRT1~7)、CLASSⅣ(HDAC11)である。これらの酵素を含む複合体は、様々なシグナル経路に応答して、DNA に結合する転写因子(Transcription factor:TF)と協調して働くことが知られている。
- HDAC阻害剤も多く存在し、代表的なものとして、バルプロ酸(Valproic acid:VPA)、酪酸ナトリウム(Sodium butyrate:SB)、トリコスタチンA(Trichostatin A:TSA)、スベロイルアニリドヒドロキサム酸(suberoylanilide hydroxamic acid:SAHA)が知られている。
非ヒストンタンパク質
その他にも、p53 、E2F、MyoD、STAT3など数多くの非ヒストンタンパク質もまた、部位特異的にアセチル化されることが知られている[1](表1、2)。アセチル化により、これらタンパク質の安定性や分解をはじめ、活性や局在、特異的相互作用などが制御され、転写、増殖、アポトーシス、分化など、細胞の様々な過程がコントロールされている。現在では、ヒストンおよび非ヒストンタンパク質のアセチル化が、メチル化やリン酸化など他の修飾とクロストークし、最終的なシグナル発現に重要な働きをしていることが明らかとなっている。いくつかの修飾がある決まった順序で組み合わさることが、ある機能発現には必要であり、一方では、互いに阻害し合うこともある。このように組み合わせを変えることで、細胞内情報伝達のネットワークの多様性を生み出している[2]。
| ACTR、ATF-2、CBP、CDY、CLOCK、EWI、Elp3、GCN5L、GRIP、HAT1、HBO1、MCM3AP、MORF、MOZ、p300、PCAF、p/CIP、SRC-1、HTAFII250、TFIIB、Tip60 |
| ACS、ACTR、AP endonuclease、AR、ATM、Brm、E2F1, 2, 3、EKLF、ERα、FoxO1, 2, 3、GATA1、HIF-1α、HMG A1、HSP90、Importin-α、Ku70、MEF2A、ミトコンドリアタンパク質、MyoD、C-Myb、C-Myc、NF-κB、p21、p53、p73、P300、PCNA、PGC-1α、PR、STAT3 |
| タンパク質の安定性 | |
| 増加 | 減少 |
| p53, p73, Smad7, c-Myc, Runx3, AR, H2A.z, E2F1, NF-E4, ER81, SREBP1a, HNF6, BACE1 | GATA1, HIF-1α, PRb |
| DNAへの結合 | |
| 増加 | 減少 |
| p53, SRY, STAT3, GATA, E2F1, P50 (NF-κB), ERα, P65 (NF-κB), c-Myb, MyoD, HNF-4, AML1, BETA2, NF-E2, KLF13, TAL1/SCL, TAF(I)68, AP endonuclease | YY1, HMG-A1, HMG-N2, P65 (NF-κB), DEK, KLF13, Fen-1 |
| 遺伝子の発現 | |
| 転写活性化 | 転写抑制 |
| p53, HMG-A1, STAT3, AR, ERα (basal), GATA, EKLF, MyoD, E2F1, p65 (NF-κB), GR, p73, PGC1α, MEF2D, GCMa, PLAG1, PLAG2, Bcl-6, Β-カテニン, KLF5, Sp1, BETA2, Cart1, RIP140, TAF(I)68 | ERα (ligand-bound), HIF-1α, STAT1, FOXO1, FOXO4, RIP140 |
| タンパク質との相互作用 | |
| 亢進 | 抑制 |
| STAT3, AR, EKLF, Importin A, STAT1, TFIIB, α-チュブリン, アクチン, コータクチン | P65 (RelA), Ku70, HSP90 |
| 局在化 | |
| アセチル化→核 | アセチル化→細胞質ゾル |
| PCAF, SRY, CtBP2, POP-1, HNF-4, PCNA | C-Abl, p300, PAP |
| mRNAの安定性 | |
| 増加 | 減少 |
| P21, Brm | TH, eNOS |
| 酵素活性 | |
| 増加 | 減少 |
| p300, ATM | PTEN, HDAC1, Mdm2, ACS, Neil2, Polβ |
略称一覧(ABC順) ACS: アセチルコエンチームA合成酵素、 ACTR: Histone acetyltransferase and nuclear receptor coactivator、 AML: 急性骨髄性白血病タンパク質、 AP endonuclease: Apurinic/apyrimidinic endonuclease 1、 AR: アンドロゲン受容体、 ATF: Activating transcription factor、 ATM: Ataxia telangiectasia mutated、 BACE: βセクレターゼ、 Bcl: B-cell CLL/lymphoma、 BETA2: BETA2転写因子、 Brm: The catalytic subunit of SWI/SNF chromatin remodeling complex、 c-Abl: C-abl癌遺伝子、 c-Myb: V-myb myeloblastosis viral oncogene homolog、 c-Myc: V-myc myelocytomatosis viral oncogene homolog、 Cart: Cartilage homeoprotein、 CBP(CREBBP): CREB結合タンパク質、 CDY: Chromodomain protein, Y-linked、 CLOCK: Circadian locomotor output cycles kaput、 CtBP(CTBP): C-terminal-binding protein、 DEK: DEK癌遺伝子、 E2F: E2F転写因子、 EKLF: Erythroid Krüppel様因子、 Elp3: Elongator complex protein、 eNOS: 内皮型一酸化窒素合成酵素、 ER: エストロゲン受容体、 ER81: Ets-related protein 81、 EWI: Egg-white inhibitor of cysteine proteinase、 Fen-1: Flap endonuclease-1、 Fox: Forkhead box、 GATA: GATA-binding protein、 GCM: Glial cells missing homolog、 GCN(KAT2): General control non-derepressible (K(lysine) acetyltransferase)、 GR: グルココルチコイド受容体、 GRIP(NCOA2): グルココルチコイド受容体結合蛋白質(Nuclear receptor coactivator 2)、 H2A: ヒストン2Aサブユニット、 HAT: ヒストンアセチル基転移酵素、 HBO: Histone acetyltransferase binding to ORC、 HDAC: ヒストン脱アセチル酵素、 HIF: 低酸素誘導因子、 HMG: High mobility group、 HNF: Hepatocyte nuclear factor、 HSP: 熱ショックタンパク質、 hTAFII: Human TATA-binding protein-associated factor、 KLF: Krüppel様因子、 Ku70(XRCC6): Lupus Ku autoantigen protein p70 (X-ray repair complementing defective repair in Chinese hamster cells 6)、 MCM3AP: Minichromosome maintenance complex component 3 associated protein、 Mdm(MDM2): Murine double minute (P53 E3 ubiquitin protein ligase homolog)、 MEF: Myocyte-specific enhancer factor、 MORF(KAT6B): Monocytic leukemia zinc-finger protein related factor (K(lysine) acetyltransferase 6B )、 MOZ(KAT6A): Monocytic leukemia zinc-finger protein (K(lysine) acetyltransferase 6A )、 MyoD: Myogenic differentiation、 Neil: DNA Glycosylase Nei-like、 NF-E: Nuclear factor, erythroid-derived、 NF-κB: Nuclear factor of kappa light polypeptide gene enhancer in B-cells、 p/CIP: P300/CBP interacting protein、 p21: Cyclin-dependent kinase inhibitor、 p300: E1A binding protein p300、 p50 (NF-κB): Nuclear factor of kappa light polypeptide gene enhancer in B-cells 1、 p53: Tumor protein p53、 p65 (NF-κB): Nuclear factor of kappa light polypeptide gene enhancer in B-cells subunit protein 65、 p65 (RelA): V-rel reticuloendotheliosis viral oncogene homolog A、 p73: Tumor protein p73、 PAP: Poly(A) polymerase、 PCAF(KAT2B): p300/CBP-associated factor(K(lysine) acetyltransferase 2B)、 PCNA: Proliferating cell nuclear antigen、 PGC: PPAR-γ coactivator、 PLAG: Pleiomorphic adenoma gene、 Pol: Polymerase (DNA directed)、 POP-1: Wnt signaling nuclear effector、 PR: プロゲステロン受容体、 pRb(RB): Retinoblastoma、 PTEN: Phosphatase and tensin homolog deleted from chromosome 10、 RIP140: Receptor interacting protein 140、 Runx: Runt-related transcription factor、 Smad: Sma and Mad Related Family、 Sp1: Specificity protein 1、 SRC-1: ステロイド受容体コアクチベーター1、 SREBP1a: Sterol regulatory element binding transcription factor 1、 SRY: Sex-determining region Y、 STAT: シグナル伝達兼転写活性化因子、 TAF(I)68: TATA box binding protein (TBP)-associated factor (I)68、 TAL1/SCL: T-cell acute lymphoblastic leukemia 1/Stem cell leukemia、 TFIIB(GTF2B): General transcription factor IIB、 TH:チロシン水酸化酵素 、Tip60(KAT5): Tat interactive protein, 60kDa(K(lysine) acetyltransferase 5)、 YY1: 転写抑制因子yin-yang 1
神経系でのタンパク質アセチル化
アセチル化は神経機能にも関与している。特にヒストンのアセチル化、脱アセチル化は神経幹細胞の分化や神経機能、神経系疾患に密接に関わっていることが報告されている。神経幹細胞の分化は「ヒストン」の項を参考にして頂き、ここではヒストンアセチル化と神経機能、及び神経系疾患に着目する。
ヒストンアセチル化と神経機能
哺乳類においてヒストンのアセチル化、脱アセチル化、及びHAT、HDACの活性はシナプスの可塑性や記憶の形成に関与する。NMDA型グルタミン酸受容体の活性化及びそれに伴うprotein kinase A(PKA)、protein kinase C(PKC)経路の活性化はヒストンH3のアセチル化を誘導し[3]、海馬神経のKClによる脱分極はヒストンH2Bのアセチル化を促進する[4]。さらに、マウスでの記憶学習訓練もヒストンH3のアセチル化を誘導することが知られている[3][5]。また、恐怖条件付けが脳由来神経栄養因子(brain-derived neurotrophic factor:BDNF)プロモーター領域のヒストンH3のアセチル化とホスホアセチル化を亢進することが報告されている[6][7]。ヒストンH3のアセチル化亢進は記憶の再固定や想起の際に誘導されることも明らかになっており、ヒストンのアセチル化が記憶に密接に関わっていることが示されている[8]。同様にHDACやHATの活性も神経機能に重要である。HDACの阻害は、シナプス間での神経伝達物質の伝達効率の指標であり、学習・記憶に重要とされる長期増強(long-term potentiation:LTP)や記憶形成を増強させ[9][10]、恐怖条件付けによる恐怖の消去を促進させる[6][11]。代表的なHATであるCBPの変異マウスはLTP及び記憶形成が障害を受け[12]、抑制性の切断型p300のトランスジェニックマウスやPCAF欠損マウスでは記憶障害が起こることが報告されている[13][14]。さらに、重度の脳萎縮、及び神経脱落を起こしたマウスにHDAC阻害剤を投与すると、樹状突起の再形成とシナプスの増加が観察され、学習能力や長期記憶が回復することが明らかになっている[15]。これらのように、シナプス可塑性(LTP)や記憶形成においてヒストンのアセチル化とそれを制御する酵素は非常に重要な役割を果たしている。
ヒストンアセチル化と神経疾患
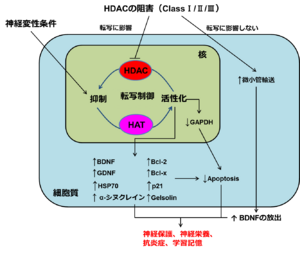
HDAC阻害剤は神経変性状態におけるヒストンの低アセチル化状態を改善し、結果的に種々のタンパク質の発現を上昇させる。また、微小管タンパク質を高アセチル化状態にすることで微小管輸送を上昇させ、BDNFの細胞外放出を促進させる。これらによりHDAC阻害剤は神経保護、神経栄養、抗炎症、学習記憶の上昇等を示し、神経変性状態を改善する。
Bcl-2:B-cell lymphoma 2:B細胞リンパ腫2、BDNF:brain-derived neurotrophic factor:脳由来神経栄養因子、GAPDH:glycelaldehyde-3-phosphate dehydrogenase:グリセルアルデヒド3リン酸脱水素酵素、GDNF:glial cell line-derived neurotrophic factor:グリア細胞由来神経栄養因子、HSP70:heat shock protein 70:熱ショックタンパク質70
HDACはヒストンタンパク質のアセチル化状態の恒常性を維持することで転写等の細胞の基本的な活性を制御するのに重要な役割を果たしており、多くの脳疾患でタンパク質のアセチル化レベルが不均衡となっていることが知られている。このような点からも種々のHDAC阻害剤が新たな脳疾患治療薬として有用である可能性が示唆されている。HDAC阻害剤は神経保護、神経栄養性、及び抗炎症の特徴を有し、学習記憶や脳疾患にみられる他の表現型などを改善できることが示されている[16][17](図3)。具体的には、脳血管障害、ハンチントン病、筋萎縮性側索硬化症、脊髄性筋委縮症、パーキンソン病、アルツハイマー病、ルビンシュタイン・テイビ症候群、レット症候群、フリードリッヒ運動失調症、多発性硬化症などが挙げられ、多くの脳疾患でヒストンの低アセチル化及び転写の機能障害が起こっている。ヒストンのアセチル化が関与する脳疾患の例を以下に示す。
ルビンシュタイン・テイビ症候群
ルビンシュタイン・テイビ症候群はHATとしての機能をもつCBPやp300の変異により引き起こされ、精神遅滞や記憶障害を示す脳疾患である[18]。CBPのヘテロ欠損マウスは発達遅滞や骨格異常がみられ[19]、クロマチンのアセチル化の欠損、及びLTPの障害などを示す[20]。近年の研究により、HDAC阻害剤であるトリコスタチンAを投与することでLTPの障害による長期記憶能低下の改善、及びシナプス可塑性の回復がみられることが明らかになっている[21]。このような研究結果から、HDAC阻害剤がルビンシュタイン・テイビ症候群治療の選択肢のひとつとして考えられている。
パーキンソン病
パーキンソン病は神経変性疾患で、黒質でのドーパミン神経の選択的欠損に伴う運動機能障害を特徴としている。パーキンソン病の大部分は孤発性である。ドーパミン毒素によりパーキンソン病様症状を呈したモデル動物に、HDAC阻害剤のフェニルブチレートを投与すると、黒質でのドーパミンの欠乏とドーパミンの生合成酵素であるチロシン水酸化酵素を発現する神経の減少が抑制される[22]。また、HDAC阻害剤の投与により中脳のアストロサイトで誘導されるグリア細胞株由来神経栄養因子(glial cell line-derived neurotrophic factor:GDNF)は、ドーパミン神経特異的に生存と軸索伸長に作用する因子である(図3)。そのため、HDAC阻害剤投与はパーキンソン病を含む神経変性疾患の治療において有望な治療法となると考えられている[23]。
家族性のパーキンソン病ではシナプス前タンパク質であるΑ-シヌクレインの遺伝子変異が原因のひとつとされている。ヒト神経芽腫細胞において、α-シヌクレインはヒストンに結合し、HATであるCBPやp300、PCAFを不活性化することでヒストンの低アセチル化、及びアポトーシスを引き起こすことが示されている[24]。現在までの研究により、HDAC阻害剤のSBやSAHAの投与が、in vitro、in vivo両方においてα-シヌクレインの過剰発現による神経細胞死を減弱させることが明らかとなっている[24]。これらのことも、パーキンソン病においてHDAC阻害剤が治療に有効であると考えられる根拠となっている。
脳血管障害
脳血管障害は急性の神経変性疾患であり日本では死因の第三位を占めている。脳血管障害の一つの大きな原因として脳虚血が挙げられる。脳虚血のモデル動物は中大脳動脈閉塞術(midle cerebral artery occlusion:MCAO)により作成することができる。ラット及びマウスのMCAOモデルでは、虚血脳全体のヒストンのリジン残基でアセチル化が抑制されるが、この変化はHDAC阻害剤の投与により梗塞体積の減少と共に回復される[25][26][27]。ラットのMCAOモデルでは傷害後のVPA、SB、TSAの投与により、状態の改善がみられることが示されている[25][26]。SBを投与したMCAOラットでは虚血脳で、神経新生の増加が確認されるが、これはBDNF-TrkBの経路を遮断すると消失してしまう[28]。
さらに、マウスへのフェニルブチレートの投与はeukaryotic translation initiation factor2α(EIF2α)のリン酸化減少とeIF2αに制御されるC/EBP homologous protein(CHOP)の発現によってERストレス(endoplasmic reticulum stress)から虚血脳を保護できることが報告されている[29]。HDAC阻害剤の投与は虚血によって引き起こされるp53の発現上昇を抑制し、heat-shock protein 70(HSP70)の発現を誘導することが知られている[25][26][27](図3)。HSP70はマウスMCAOモデルでHSP70- I-κBα- NF-κB(nuclear factor-kappa B)の安定な複合体を形成することにより、 NF-κBを不活性化することで抗炎症作用を示すことが明らかにされている[30]。
細胞骨格タンパク質の発現は虚血条件においてHDAC阻害による神経保護効果と関連している。例としてHDACの阻害はアクチンフィラメントの構成に重要なゲルソリンタンパク質を増加させ、虚血傷害から神経を保護する[31]。加えてVPAはHDAC阻害と転写活性化、及びfas ligand protein(Fas-L)、interleukin-6(IL-6)、matrix metalloproteinase-9(MMP-9)を含む炎症誘発性因子発現を抑制して抗炎症効果を示すことにより、脳血管障害の脳内出血モデルにおいて神経保護を示す[32]。以上の報告より、急性の神経疾患においてもHDACの阻害が効果的であることが示されている。
本文では以上3つの例を紹介したが、これらの例からも、脳機能においてヒストンのアセチル化は重要な役割を担い、HDAC阻害剤は脳疾患治療薬として有用であると考えられる。
非ヒストンタンパク質のアセチル化と神経機能・神経疾患
上述してきたように、一般にHDACの阻害は脳疾患治療に有用であると思われる。しかし、HDAC6のようにHDACの働きが脳機能に重要であることも知られており、HDACの阻害が常によい方向に働くとは限らない。HDAC6は脳で高く発現しており、ヒストンのみならずα-チュブリン、HSP90、コルタクチンを脱アセチル化する。なかでもHDAC6の主要な基質はα-チュブリンであり、α-チュブリンのアセチル化レベルを制御することで微小管の安定性をコントロールし、その輸送等に重要な役割を果たすことが報告されている[33][34]。微小管のアセチル化が促進されると、神経細胞において微小管とキネシン-1との結合が促進され、JNK-interacting Protein 1やBDNFなどのキネシン-1のカーゴタンパク質の極性輸送が促進される[35]。HDAC6による微小管の安定性制御は神経細胞におけるキネシン-1によるミトコンドリアの輸送にも重要であり[33][36]、異常なミトコンドリア輸送は、アルツハイマー病、パーキンソン病、ハンチントン病、筋委縮性側索硬化症などの脳疾患に関係することが知られている[37]。また、HDAC6は軸索の末端領域に局在することで軸索の伸長にも重要な役割を果たしており、TSAなどのHDAC阻害剤によるtubulinの脱アセチル化阻害は軸索の伸長を阻害することが報告されている[38]。
しかし逆に、HDAC6はマウスの情動行動に関与し、HDAC6の欠損やHDAC6阻害剤が運動亢進、不安の軽減などの抗うつ様の行動を誘導することで、うつ病等の治療によい影響を与えることも明らかになっている。HDAC6は、気分障害等の精神疾患に深く関与するセロトニン神経細胞の豊富な中脳の縫線核、青斑核、黒質の神経細胞に多く存在している。しかし、HDAC6の欠損マウスにおいて、セロトニンの量、及び既存の抗うつ薬である選択的セロトニン再取り込み阻害薬/セロトニン・ノルアドレナリン再取り込み阻害薬(Selective Serotonin Reuptake Inhibitors/ Serotonin & Norepinephrine Reuptake Inhibitors:SSRI/SNRI)に対する応答性には変化がなく、SSRI/SNRIの急性投与による大幅なうつ様行動の改善はHDAC6の欠損マウスと野生型マウスで同程度である。このことからHDAC6阻害剤による抗うつ作用メカニズムは既存の抗うつ薬とは異なると考えられており、HDAC6の阻害はうつ病の病態解明や新規抗うつ薬の開発につながる可能性が示唆されている[39]。
終わりに
今回紹介した例以外にも、タンパク質のアセチル化と脳機能に関しては多くの報告がなされており、ヒストンのアセチル化や非ヒストンタンパク質のアセチル化は脳の発達や機能に重要な機構であるといえる。一般にHDAC阻害剤は脳疾患の治療に有用であり、記憶形成を増強させることなどが知られている。しかし、上に示したように、軸索輸送や軸索伸長に対してHDAC6が重要な役割を果たすこと、また、HDACがオリゴデンドロサイトの分化を促進させること(ヒストンの項参照)、さらにはHDAC1、2を同時に欠損させたマウスでは海馬や小脳、大脳皮質の形成に異常が生じ、胎生致死となることなども知られている[40]。これらのことから、HDACは脳の発生や機能に重要な役割を果たすものでもあり、HDACによる脳でのアセチル化レベルのバランスの維持が、正常な脳機能を果たす上では重要であるといえる。
関連項目
参考文献
- ↑ 1.0 1.1 1.2 1.3
Spange, S., Wagner, T., Heinzel, T., & Krämer, O.H. (2009).
Acetylation of non-histone proteins modulates cellular signalling at multiple levels. The international journal of biochemistry & cell biology, 41(1), 185-98. [PubMed:18804549] [WorldCat] [DOI] - ↑
Yang, X.J., & Seto, E. (2008).
Lysine acetylation: codified crosstalk with other posttranslational modifications. Molecular cell, 31(4), 449-61. [PubMed:18722172] [PMC] [WorldCat] [DOI] - ↑ 3.0 3.1
Chwang, W.B., Arthur, J.S., Schumacher, A., & Sweatt, J.D. (2007).
The nuclear kinase mitogen- and stress-activated protein kinase 1 regulates hippocampal chromatin remodeling in memory formation. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(46), 12732-42. [PubMed:18003853] [PMC] [WorldCat] [DOI] - ↑
Maharana, C., Sharma, K.P., & Sharma, S.K. (2010).
Depolarization induces acetylation of histone H2B in the hippocampus. Neuroscience, 167(2), 354-60. [PubMed:20167251] [WorldCat] [DOI] - ↑
Fontán-Lozano, A., Romero-Granados, R., Troncoso, J., Múnera, A., Delgado-García, J.M., & Carrión, A.M. (2008).
Histone deacetylase inhibitors improve learning consolidation in young and in KA-induced-neurodegeneration and SAMP-8-mutant mice. Molecular and cellular neurosciences, 39(2), 193-201. [PubMed:18638560] [WorldCat] [DOI] - ↑ 6.0 6.1
Bredy, T.W., Wu, H., Crego, C., Zellhoefer, J., Sun, Y.E., & Barad, M. (2007).
Histone modifications around individual BDNF gene promoters in prefrontal cortex are associated with extinction of conditioned fear. Learning & memory (Cold Spring Harbor, N.Y.), 14(4), 268-76. [PubMed:17522015] [PMC] [WorldCat] [DOI] - ↑
Lubin, F.D., Roth, T.L., & Sweatt, J.D. (2008).
Epigenetic regulation of BDNF gene transcription in the consolidation of fear memory. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(42), 10576-86. [PubMed:18923034] [PMC] [WorldCat] [DOI] - ↑
Lubin, F.D., & Sweatt, J.D. (2007).
The IkappaB kinase regulates chromatin structure during reconsolidation of conditioned fear memories. Neuron, 55(6), 942-57. [PubMed:17880897] [PMC] [WorldCat] [DOI] - ↑
Guan, J.S., Haggarty, S.J., Giacometti, E., Dannenberg, J.H., Joseph, N., Gao, J., ..., & Tsai, L.H. (2009).
HDAC2 negatively regulates memory formation and synaptic plasticity. Nature, 459(7243), 55-60. [PubMed:19424149] [PMC] [WorldCat] [DOI] - ↑
Stefanko, D.P., Barrett, R.M., Ly, A.R., Reolon, G.K., & Wood, M.A. (2009).
Modulation of long-term memory for object recognition via HDAC inhibition. Proceedings of the National Academy of Sciences of the United States of America, 106(23), 9447-52. [PubMed:19470462] [PMC] [WorldCat] [DOI] - ↑
Lattal, K.M., Barrett, R.M., & Wood, M.A. (2007).
Systemic or intrahippocampal delivery of histone deacetylase inhibitors facilitates fear extinction. Behavioral neuroscience, 121(5), 1125-31. [PubMed:17907845] [WorldCat] [DOI] - ↑
Wood, M.A., Kaplan, M.P., Park, A., Blanchard, E.J., Oliveira, A.M., Lombardi, T.L., & Abel, T. (2005).
Transgenic mice expressing a truncated form of CREB-binding protein (CBP) exhibit deficits in hippocampal synaptic plasticity and memory storage. Learning & memory (Cold Spring Harbor, N.Y.), 12(2), 111-9. [PubMed:15805310] [PMC] [WorldCat] [DOI] - ↑
Oliveira, A.M., Wood, M.A., McDonough, C.B., & Abel, T. (2007).
Transgenic mice expressing an inhibitory truncated form of p300 exhibit long-term memory deficits. Learning & memory (Cold Spring Harbor, N.Y.), 14(9), 564-72. [PubMed:17761541] [PMC] [WorldCat] [DOI] - ↑
Maurice, T., Duclot, F., Meunier, J., Naert, G., Givalois, L., Meffre, J., ..., & Gongora, C. (2008).
Altered memory capacities and response to stress in p300/CBP-associated factor (PCAF) histone acetylase knockout mice. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology, 33(7), 1584-602. [PubMed:17805310] [PMC] [WorldCat] [DOI] - ↑
Fischer, A., Sananbenesi, F., Wang, X., Dobbin, M., & Tsai, L.H. (2007).
Recovery of learning and memory is associated with chromatin remodelling. Nature, 447(7141), 178-82. [PubMed:17468743] [WorldCat] [DOI] - ↑
Kazantsev, A.G., & Thompson, L.M. (2008).
Therapeutic application of histone deacetylase inhibitors for central nervous system disorders. Nature reviews. Drug discovery, 7(10), 854-68. [PubMed:18827828] [WorldCat] [DOI] - ↑
Chuang, D.M., Leng, Y., Marinova, Z., Kim, H.J., & Chiu, C.T. (2009).
Multiple roles of HDAC inhibition in neurodegenerative conditions. Trends in neurosciences, 32(11), 591-601. [PubMed:19775759] [PMC] [WorldCat] [DOI] - ↑
Petrij, F., Giles, R.H., Dauwerse, H.G., Saris, J.J., Hennekam, R.C., Masuno, M., ..., & Peters, D.J. (1995).
Rubinstein-Taybi syndrome caused by mutations in the transcriptional co-activator CBP. Nature, 376(6538), 348-51. [PubMed:7630403] [WorldCat] [DOI] - ↑
Alarcón, J.M., Malleret, G., Touzani, K., Vronskaya, S., Ishii, S., Kandel, E.R., & Barco, A. (2004).
Chromatin acetylation, memory, and LTP are impaired in CBP+/- mice: a model for the cognitive deficit in Rubinstein-Taybi syndrome and its amelioration. Neuron, 42(6), 947-59. [PubMed:15207239] [WorldCat] [DOI] - ↑
Barco, A. (2007).
The Rubinstein-Taybi syndrome: modeling mental impairment in the mouse. Genes, brain, and behavior, 6 Suppl 1, 32-9. [PubMed:17543037] [WorldCat] [DOI] - ↑
Vecsey, C.G., Hawk, J.D., Lattal, K.M., Stein, J.M., Fabian, S.A., Attner, M.A., ..., & Wood, M.A. (2007).
Histone deacetylase inhibitors enhance memory and synaptic plasticity via CREB:CBP-dependent transcriptional activation. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(23), 6128-40. [PubMed:17553985] [PMC] [WorldCat] [DOI] - ↑
Gardian, G., Yang, L., Cleren, C., Calingasan, N.Y., Klivenyi, P., & Beal, M.F. (2004).
Neuroprotective effects of phenylbutyrate against MPTP neurotoxicity. Neuromolecular medicine, 5(3), 235-41. [PubMed:15626823] [WorldCat] [DOI] - ↑
Airaksinen, M.S., & Saarma, M. (2002).
The GDNF family: signalling, biological functions and therapeutic value. Nature reviews. Neuroscience, 3(5), 383-94. [PubMed:11988777] [WorldCat] [DOI] - ↑ 24.0 24.1
Kontopoulos, E., Parvin, J.D., & Feany, M.B. (2006).
Alpha-synuclein acts in the nucleus to inhibit histone acetylation and promote neurotoxicity. Human molecular genetics, 15(20), 3012-23. [PubMed:16959795] [WorldCat] [DOI] - ↑ 25.0 25.1 25.2
Ren, M., Leng, Y., Jeong, M., Leeds, P.R., & Chuang, D.M. (2004).
Valproic acid reduces brain damage induced by transient focal cerebral ischemia in rats: potential roles of histone deacetylase inhibition and heat shock protein induction. Journal of neurochemistry, 89(6), 1358-67. [PubMed:15189338] [WorldCat] [DOI] - ↑ 26.0 26.1 26.2
Kim, H.J., Rowe, M., Ren, M., Hong, J.S., Chen, P.S., & Chuang, D.M. (2007).
Histone deacetylase inhibitors exhibit anti-inflammatory and neuroprotective effects in a rat permanent ischemic model of stroke: multiple mechanisms of action. The Journal of pharmacology and experimental therapeutics, 321(3), 892-901. [PubMed:17371805] [WorldCat] [DOI] - ↑ 27.0 27.1
Faraco, G., Pancani, T., Formentini, L., Mascagni, P., Fossati, G., Leoni, F., ..., & Chiarugi, A. (2006).
Pharmacological inhibition of histone deacetylases by suberoylanilide hydroxamic acid specifically alters gene expression and reduces ischemic injury in the mouse brain. Molecular pharmacology, 70(6), 1876-84. [PubMed:16946032] [WorldCat] [DOI] - ↑
Kim, H.J., Leeds, P., & Chuang, D.M. (2009).
The HDAC inhibitor, sodium butyrate, stimulates neurogenesis in the ischemic brain. Journal of neurochemistry, 110(4), 1226-40. [PubMed:19549282] [PMC] [WorldCat] [DOI] - ↑
Qi, X., Hosoi, T., Okuma, Y., Kaneko, M., & Nomura, Y. (2004).
Sodium 4-phenylbutyrate protects against cerebral ischemic injury. Molecular pharmacology, 66(4), 899-908. [PubMed:15226415] [WorldCat] [DOI] - ↑
Zheng, Z., Kim, J.Y., Ma, H., Lee, J.E., & Yenari, M.A. (2008).
Anti-inflammatory effects of the 70 kDa heat shock protein in experimental stroke. Journal of cerebral blood flow and metabolism : official journal of the International Society of Cerebral Blood Flow and Metabolism, 28(1), 53-63. [PubMed:17473852] [WorldCat] [DOI] - ↑
Yildirim, F., Gertz, K., Kronenberg, G., Harms, C., Fink, K.B., Meisel, A., & Endres, M. (2008).
Inhibition of histone deacetylation protects wildtype but not gelsolin-deficient mice from ischemic brain injury. Experimental neurology, 210(2), 531-42. [PubMed:18234195] [WorldCat] [DOI] - ↑
Sinn, D.I., Kim, S.J., Chu, K., Jung, K.H., Lee, S.T., Song, E.C., ..., & Roh, J.K. (2007).
Valproic acid-mediated neuroprotection in intracerebral hemorrhage via histone deacetylase inhibition and transcriptional activation. Neurobiology of disease, 26(2), 464-72. [PubMed:17398106] [WorldCat] [DOI] - ↑ 33.0 33.1
Matsuyama, A., Shimazu, T., Sumida, Y., Saito, A., Yoshimatsu, Y., Seigneurin-Berny, D., ..., & Yoshida, M. (2002).
In vivo destabilization of dynamic microtubules by HDAC6-mediated deacetylation. The EMBO journal, 21(24), 6820-31. [PubMed:12486003] [PMC] [WorldCat] [DOI] - ↑
Chen, S., Owens, G.C., Makarenkova, H., & Edelman, D.B. (2010).
HDAC6 regulates mitochondrial transport in hippocampal neurons. PloS one, 5(5), e10848. [PubMed:20520769] [PMC] [WorldCat] [DOI] - ↑
Reed, N.A., Cai, D., Blasius, T.L., Jih, G.T., Meyhofer, E., Gaertig, J., & Verhey, K.J. (2006).
Microtubule acetylation promotes kinesin-1 binding and transport. Current biology : CB, 16(21), 2166-72. [PubMed:17084703] [WorldCat] [DOI] - ↑
Hollenbeck, P.J., & Saxton, W.M. (2005).
The axonal transport of mitochondria. Journal of cell science, 118(Pt 23), 5411-9. [PubMed:16306220] [PMC] [WorldCat] [DOI] - ↑
Deheshi, S., Pasqualotto, B.A., & Rintoul, G.L. (2013).
Mitochondrial trafficking in neuropsychiatric diseases. Neurobiology of disease, 51, 66-71. [PubMed:22750523] [WorldCat] [DOI] - ↑
Tapia, M., Wandosell, F., & Garrido, J.J. (2010).
Impaired function of HDAC6 slows down axonal growth and interferes with axon initial segment development. PloS one, 5(9), e12908. [PubMed:20886111] [PMC] [WorldCat] [DOI] - ↑
Fukada, M., Hanai, A., Nakayama, A., Suzuki, T., Miyata, N., Rodriguiz, R.M., ..., & Kawaguchi, Y. (2012).
Loss of deacetylation activity of Hdac6 affects emotional behavior in mice. PloS one, 7(2), e30924. [PubMed:22328923] [PMC] [WorldCat] [DOI] - ↑
Montgomery, R.L., Hsieh, J., Barbosa, A.C., Richardson, J.A., & Olson, E.N. (2009).
Histone deacetylases 1 and 2 control the progression of neural precursors to neurons during brain development. Proceedings of the National Academy of Sciences of the United States of America, 106(19), 7876-81. [PubMed:19380719] [PMC] [WorldCat] [DOI]
(執筆者:村尾直哉、中島欽一 担当編集委員:村上富士夫)