伝令RNA
朝光世煌、王 丹
理化学研究所 生命科学機能センター 脳エピトランスクリプトミクス研究チーム
DOI:10.14931/bsd.9972 原稿受付日:2021年12月21日 改訂版受付日:2022年8月16日 原稿完成日:2022年8月16日
担当編集委員:林 康紀(京都大学大学院医学研究科 システム神経薬理学分野)
英語:messenger RNA 独:Boten-RNA 仏:ARN messager
同義語:メッセンジャーRNA
英略語:mRNA
伝令RNA (messenger RNA, mRNA)は、タンパク質合成反応の鋳型となる一本鎖のリボ核酸である。遺伝情報はDNAを鋳型としてRNAに写し取られる(転写)。RNAプロセシング・核外輸送を経てmRNAに引き継がれる遺伝情報は、細胞質においてタンパク質合成装置リボソームによって読み取られ、タンパク質が合成される(翻訳)。固有の形態的特徴を有する神経細胞では、細胞質から細胞小器官へのmRNAの輸送とその場所でのタンパク質の翻訳(局所翻訳)が多くの神経機能の調節メカニズムに直結する。またmRNAは多様な化学修飾を受け、固有の修飾パターンにより遺伝情報を拡張させることができる。この化学修飾によるmRNAの機能化が神経細胞における精密なmRNA制御機構の一端を担うと考えられている。
mRNAとは
mRNAは、細胞がタンパク質を合成する過程で、DNAから転写される一本鎖のリボ核酸である。その遺伝情報はリボソームによって読み取られ、タンパク質へと翻訳される。
mRNAの転写・輸送・翻訳の制御はタンパク質の量と細胞内局在を規定する。特に神経細胞は、多数の枝分かれや突起形成により特徴づけられ、軸索・樹状突起・シナプスといった形態的区画が独立した機能を有するため、神経活動や局所シグナルに応じて、mRNAの転写・輸送・翻訳を精密に制御するmRNA制御機構が重要である[1][2] 。
これまでに、神経細胞内のmRNA分子を軸索、成長円錐、樹状突起、シナプスといった細胞体から遠い場所に輸送し、その場所で翻訳する(局所翻訳 local translation)メカニズムが存在することが知られてきた。このmRNAの輸送と翻訳制御メカニズムは、軸索伸長と誘導・損傷の再生・シナプス形成・刈り込み・可塑性等、神経細胞が機能を果たす上で欠かせない[3] 。神経変性疾患および精神疾患においては、このメカニズムの破綻が多く報告されている[4][5][6] 。
合成
真核細胞では、核内でRNAポリメラーゼによるDNAの転写によりmRNA前駆体 (pre-mRNA)が合成される。mRNA前駆体には、通常、エクソン(アミノ酸配列をコードする配列を含む領域)とイントロン(アミノ酸配列をコードしない領域)が含まれる。
転写途中あるいは転写完了後にRNAプロセシングが開始される。この過程でイントロンは取り除かれ、エクソンだけが継ぎ合わされる(図1)。なお、このスプライシングの過程において、一種類のmRNA前駆体から異なるパターンのエクソン連結が行われることで複数種の成熟mRNAが合成され得る(選択的スプライシング)。
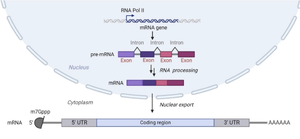
RNAポリメラーゼによりmRNA前駆体 (pre-mRNA)が合成される。mRNA前駆体に含まれるイントロン(intron)は取り除かれエクソン(exon)だけが継ぎ合わされる。RNAプロセシングを経て成熟したmRNAは、5'Cap構造(m7Gppp)、5'非翻訳領域 (5'UTR)、 コーディング領域 (coding sequence)、3'非翻訳領域UTR (3'UTR)、ポリA配列によって構成される。成熟したmRNAは、核内から核膜孔を通って細胞質に運び出される。図はBioRenderより作成。
構造
RNAプロセシングを経て成熟したmRNAは、5'キャップ構造(m7Gppp)、5'非翻訳領域(5' untranslated region, 5'UTR; 翻訳開始コドンより前の配列)、 コーディング領域 (coding sequence, CDS; アミノ酸配列をコードする配列)、3'非翻訳領域 (3'UTR; 翻訳終始コドンより後ろの配列)、ポリA配列によって構成される (図1)。成熟したmRNAは、核内から核膜孔を通って細胞質に運び出される。細胞質の成熟mRNAはタンパク質合成装置リボソームによって読み取られ、タンパク質が合成される。神経細胞では、多くのmRNAは細胞質から軸索・樹状突起・シナプス等の細胞小器官に運ばれ、局所翻訳を受ける。
細胞内局在
神経細胞では、分子と小器官の輸送メカニズムが高度に発達して、細胞体とシナプスを繋ぐ細胞内輸送システムがミトコンドリア・シナプス小胞・脂質・タンパク質等を両方向に運んでいる。mRNAの細胞内輸送に関しては、RNAとタンパク質から成る膜に囲まれない複合体である「RNA輸送顆粒」の状態で、微小管等の細胞骨格上を通って輸送される[7][8][9][10] 。
RNA輸送顆粒に含まれるRNA結合タンパク質はこれまでに多く同定されている。特に注目されているタンパク質は、神経疾患に関連し軸索内で検出されるRNA結合タンパク質であるTAR DNA-binding protein of 43 kDa (TDP-43)・Fused-in sarcoma (FUS) / Translocated in liposarcoma (TLS)・survival motor neuron (SMN) protein・ splicing factor proline and glutamine rich (SFPQ)である。TDP-43とFUS/TLSは筋萎縮性側索硬化症(ALS)の患者において変異が見られる。SMN遺伝子の欠損は脊髄性筋萎縮症(SMA)を引き起こす。また、SFPQの軸索からの喪失は末梢神経障害に寄与する[11][12][13][14][15][16] 。
これまでに、機能的に関連するタンパク質をコードするmRNA群がRNA結合タンパク質によって同じ輸送顆粒上に存在するメカニズムの例[17] ; [18] )が示され、液-液相分離がRNA輸送顆粒の形成制御メカニズムとして提唱されたが[19] 、その詳細は解明されていない。
軸索におけるmRNA制御
1960年代には既に、軸索においてmRNA局在やタンパク質合成が起きているという示唆がなされていた[20][21] 。しかし、1980-90年代における電子顕微鏡を用いた観察では、成熟した中枢神経系神経細胞の軸索内部にポリリボソームが認められなかった。ポリリボソームは翻訳に必須であるため、当時は、「哺乳動物の中枢神経系では成熟した軸索からは局所翻訳メカニズムが排除される」と結論づけられた[22] 。
しかしその後、損傷した軸索の修復過程において軸索内でmRNAの局所翻訳が起きることがわかり、軸索修復におけるその重要性が示された。さらに、蛍光イメージング手法の発展に伴い、成熟した軸索における局所翻訳のin vivoでの証拠も多く報告されてきた。これらの発見から、軸索におけるmRNAの局所制御メカニズムと軸索損傷・修復とのつながりが改めて議論されている[23][24][25] 。
軸索におけるmRNAの局所制御研究は、軸索を脳組織から単離する工学的技術・高感度RNA検出・画像検出・解析手法等の進歩により進化している。また、近年の大規模RNAシーケンシング技術によって、数千種類にのぼるRNAが軸索において検出され、生理的な環境や損傷等に応答し局所翻訳が生じることが示された[26][27] 。これまでに、受容体と翻訳因子の複合体[28] 、局所Ca2+の上昇に応答するマイクロRNAやRNA結合タンパク質の制御[29][30][31][32][33][34]等が局所翻訳のメカニズムとして報告されてきた一方で、特異的な応答を生み出すために特定の機能に関係する対象分子を選択するメカニズムの詳細は明らかになっていない。
ミエリンにおけるmRNA制御と翻訳制御
軸索の周りはミエリン(myelin; 髄鞘)というオリゴデンドロサイトの細胞膜の多層構造体に覆われている。mRNA局在研究の初期に、ミエリンの構成タンパク質の一つであるmyelin basic protein (MBP)をコードするMbp mRNAがオリゴデンドロサイトの細胞体の外に輸送されることが発見された[35] 。さらに、蛍光ラベルされたMbp mRNAを用いることにより、オリゴデンドロサイト内でMbp mRNAを含むRNA顆粒が形成され、微小管に沿って末端へ輸送される様子が観察された[36][37] 。これらの研究はmRNA輸送メカニズムの存在を鮮明に示した。MBPは可溶性が低く、また細胞内膜を圧縮する機能を持つことから、細胞体でタンパク質が作られると細胞機能に大きく障害をもたらすと予想されていた。
その後、Mbp mRNAを分子モデルとして、3'UTRに存在する、長距離のmRNA輸送に必要なRNA配列 (A2REと呼ばれるGCCAAGGAGCC配列)[38] およびそれを認識して結合するタンパク質heterogeneous nuclear ribonucleoprotein (hnRNP) A2 がそれぞれ同定された[39] 。また、キネシンタンパク質であるKif1bがMbp mRNAの輸送に必須な分子であること、Kif1b遺伝子に変異を持つゼブラフィッシュではMBPおよびミエリン形成場所に異常が起きることが報告された[40] 。このA2RE配列はオリゴデンドロサイトや神経細胞において輸送される様々なmRNAに保存されていることが明らかになった。これらの研究から、微小管による細胞内長距離輸送メカニズムに対して、特異的なRNA配列が局在情報をコードするというモデルが確立された[41][42] 。
しかし、Mbp mRNAが輸送される途中で翻訳が起きると細胞機能に障害をもたらすことが予想される。そのため、輸送メカニズムを想定するだけでは不十分であり、「mRNAの輸送途中では何らかのメカニズムで翻訳が抑制される」とする仮説が提唱された。その抑制分子の候補として、内在性siRNA[43] およびhnRNPE1[44] が同定された。いずれの分子も輸送中のRNA顆粒に存在する。また、MBPが正常に産生されない慢性多発性硬化症においてはsmall non-coding RNA 715 (sncRNA715)の発現量が異常に多い。
さらに、Mbp mRNAが輸送された場所でミエリンを形成するには、前述の翻訳抑制状態が解除される必要がある。翻訳を活性化するシグナル経路は、神経軸索の表面にあるL1膜タンパク質とオリゴデンドロサイトの表面に発現するコンタクチン/インテグリン分子の結合から開始する。その結合はオリゴデンドロサイトにあるFYNキナーゼを活性化し、Mbp mRNA輸送顆粒上にあるhnRNPFがリン酸化を受ける。このリン酸化により輸送顆粒が崩壊し、hnRNPFはhnRNPA2・hnRNPE2と共に Mbp mRNAから離れ、翻訳抑制が解除されるという仕組みが報告されている[45][46][47] 。さらに、軸索の発火に応答して、L1膜タンパク質の発現量およびFYNキナーゼ活性は調節されることが報告され、軸索に伝わる電気シグナルによって、Mbp mRNAの局所翻訳やミエリン形成が制御される動的な制御機構が明らかとなった[48] 。
このように、軸索における電気信号の伝達に重要な役割を果たすミエリン形成という現象には、Mbp mRNAの輸送と翻訳制御分子機構が巧みに関わっている[49] 。
樹状突起におけるmRNA制御
樹状突起は軸索と神経細胞の反対極に存在する構造である。樹状突起上には多数のシナプス後樹状突起棘(スパイン)があり、シグナルの受容面積を拡張している。そのため、樹状突起は、神経回路網における配線ロジックや計算そのものに影響を及ぼす。
樹状突起でタンパク質合成が起きていることは、1964年にBodianによって報告されていた。Bodianはサル脊髄運動神経細胞の樹状突起を用いて、樹状突起がシナプス前部と接する部分に、小胞体とその膜上にポリソームが存在することを観察した[50] 。ポリソームの存在は樹状突起における翻訳活性を意味しており、小胞体膜の存在は翻訳後にタンパク質の糖鎖修飾が生じることを示していた。
1988年、in situハイブリダイゼーション法により樹状突起に局在するmRNAとしてMap2が初めて同定された。Map2 mRNAは樹状突起にて検出されるが、チューブリン(tubulin) mRNAは細胞体でのみ検出された。Map2は微小管に結合して安定化させるタンパク質をコードする。このことから、遺伝子特異的なmRNA分布パターンの存在が示唆された[51] 。
2000年代には、大規模RNAシーケンシング技術の発展に伴い、グルタミン酸受容体サブユニットやリボソームのサブユニットをコードする遺伝子等、数百種ものmRNAが樹状突起に局在することが報告された。2010年以降の研究では、リストアップされる遺伝子は数千種類に上っており、樹状突起に局在するとされるRNAの種類は検出手法の感度の向上によって増え続けている[52][53] 。加えて、in situハイブリダイゼーション法の感度の向上により、1分子RNAの検出が可能となった[54] 。
軸索におけるmRNAの局所翻訳については論争があった一方で、樹状突起においてはポリソーム・リボソームRNA・mRNAが次々に発見され、細胞体から切断された樹状突起に直接導入したmRNAが翻訳活性を示すことが確認された[55] 。さらに、シナプス伝達に関わるタンパク質をコードするRNAが神経活動依存的に樹状突起に局在していることが報告され、樹状突起におけるmRNA制御がシナプス形成および可塑性において重要であることが広く認識されてきている[55][56] 。
今日では数千のmRNAが軸索や樹状突起に局在することが確認されている。脳の体積において軸索と樹状突起それぞれが占める割合を考えれば、局所翻訳 (local translation) は決して「局所 (local)」な現象ではなく、多くの脳機能に関わっていることが想定される。

mRNAの内部配列には様々な化学修飾塩基が存在し、mRNAの安定性・輸送・翻訳を調節している;5-メチルシトシン(m5C)、N 1-メチルアデノシン(m1A)、N 6-メチルアデノシン (m6A)、シュードウリジン(Ψ)。BioRenderより作成。
化学修飾
RNAをターゲットとした化学修飾が自然界に多種多様に存在することは以前から知られていた。近年、その遺伝子発現制御メカニズムの全貌を表す「エピトランスクリプトミクス」研究分野が隆盛している。
mRNAには様々な化学修飾塩基が存在し、その安定性・輸送・翻訳を調節している。mRNAの5'末端ではm7Gppp(m7G)修飾が共通して見られる。mRNAの内部配列では、2'-O-メチル化をはじめとして、イノシン(I)・5-メチルシトシン(m5C)・5-ヒドロキシメチルシトシン(hm5C)・シュードウリジン(Ψ)・N1-メチルアデノシン(m1A)・2'-O-メチルヌクレオチド(Nm)等が主要な修飾として挙げられる(図2)[57] 。
RNA化学修飾はRNAが転写された後の遺伝子コードの情報を大きく拡張する。神経細胞は、外部からの入力に柔軟に対応するため、脳内活動依存的遺伝子発現メカニズムを持っていると考えられる。RNA化学修飾はその遺伝子情報制御相の1つではないかと想定される。
mRNAのメチル化とシナプス機能
神経活動依存的エピジェネティクス制御モデルは、シナプスと細胞核間の遠い距離のシグナル伝達が必要とされる「中央集権型」的制御であり、細胞全体の機能的変化を引き起こす。対照的に、エピトランスクリプトミクス制御はシナプスのような空間的に限られた神経細胞の一部に機能変化をもたらすことができる。
2018年京都大学のWangグループらは、マウス脳から神経シナプスに含まれるRNAを精製し、6-メチルアデノシン(m6A)修飾の状況を次世代シーケンサーを用いて解読した。その結果、シナプスに存在するRNAにおいて特異的にm6A修飾が増加している遺伝子1266個を同定した。これらの遺伝子にはシナプス機能、精神疾患、神経発達障害に関連するものが多く含まれており、m6A修飾は様々なmRNAを修飾することで正常なシナプス機能やその破綻に深く関わっていることが示唆された。今後、脳におけるRNA化学修飾の役割の理解がさらに進むことが期待される[58] 。
関連項目
参考文献
- ↑
Baser, A., Skabkin, M., Kleber, S., Dang, Y., Gülcüler Balta, G.S., Kalamakis, G., ..., & Martin-Villalba, A. (2019).
Onset of differentiation is post-transcriptionally controlled in adult neural stem cells. Nature, 566(7742), 100-104. [PubMed:30700908] [WorldCat] [DOI] - ↑
Kojima, S., Shingle, D.L., & Green, C.B. (2011).
Post-transcriptional control of circadian rhythms. Journal of cell science, 124(Pt 3), 311-20. [PubMed:21242310] [PMC] [WorldCat] [DOI] - ↑
Wang, G., Grone, B., Colas, D., Appelbaum, L., & Mourrain, P. (2011).
Synaptic plasticity in sleep: learning, homeostasis and disease. Trends in neurosciences, 34(9), 452-63. [PubMed:21840068] [PMC] [WorldCat] [DOI] - ↑
Conlon, E.G., & Manley, J.L. (2017).
RNA-binding proteins in neurodegeneration: mechanisms in aggregate. Genes & development, 31(15), 1509-1528. [PubMed:28912172] [PMC] [WorldCat] [DOI] - ↑
Fernandopulle, M.S., Lippincott-Schwartz, J., & Ward, M.E. (2021).
RNA transport and local translation in neurodevelopmental and neurodegenerative disease. Nature neuroscience, 24(5), 622-632. [PubMed:33510479] [PMC] [WorldCat] [DOI] - ↑
Tank, E.M., Figueroa-Romero, C., Hinder, L.M., Bedi, K., Archbold, H.C., Li, X., ..., & Barmada, S.J. (2018).
Abnormal RNA stability in amyotrophic lateral sclerosis. Nature communications, 9(1), 2845. [PubMed:30030424] [PMC] [WorldCat] [DOI] - ↑
Elvira, G., Wasiak, S., Blandford, V., Tong, X.K., Serrano, A., Fan, X., ..., & Sossin, W.S. (2006).
Characterization of an RNA granule from developing brain. Molecular & cellular proteomics : MCP, 5(4), 635-51. [PubMed:16352523] [WorldCat] [DOI] - ↑
Kanai, Y., Dohmae, N., & Hirokawa, N. (2004).
Kinesin transports RNA: isolation and characterization of an RNA-transporting granule. Neuron, 43(4), 513-25. [PubMed:15312650] [WorldCat] [DOI] - ↑
Kar, A.N., Lee, S.J., & Twiss, J.L. (2018).
Expanding Axonal Transcriptome Brings New Functions for Axonally Synthesized Proteins in Health and Disease. The Neuroscientist : a review journal bringing neurobiology, neurology and psychiatry, 24(2), 111-129. [PubMed:28593814] [PMC] [WorldCat] [DOI] - ↑
Krichevsky, A.M., & Kosik, K.S. (2001).
Neuronal RNA granules: a link between RNA localization and stimulation-dependent translation. Neuron, 32(4), 683-96. [PubMed:11719208] [WorldCat] [DOI] - ↑
Alami, N.H., Smith, R.B., Carrasco, M.A., Williams, L.A., Winborn, C.S., Han, S.S.W., ..., & Taylor, J.P. (2014).
Axonal transport of TDP-43 mRNA granules is impaired by ALS-causing mutations. Neuron, 81(3), 536-543. [PubMed:24507191] [PMC] [WorldCat] [DOI] - ↑
Cosker, K.E., Fenstermacher, S.J., Pazyra-Murphy, M.F., Elliott, H.L., & Segal, R.A. (2016).
The RNA-binding protein SFPQ orchestrates an RNA regulon to promote axon viability. Nature neuroscience, 19(5), 690-696. [PubMed:27019013] [PMC] [WorldCat] [DOI] - ↑
Khalil, M., Teunissen, C.E., Otto, M., Piehl, F., Sormani, M.P., Gattringer, T., ..., & Kuhle, J. (2018).
Neurofilaments as biomarkers in neurological disorders. Nature reviews. Neurology, 14(10), 577-589. [PubMed:30171200] [WorldCat] [DOI] - ↑
Pease-Raissi, S.E., Pazyra-Murphy, M.F., Li, Y., Wachter, F., Fukuda, Y., Fenstermacher, S.J., ..., & Segal, R.A. (2017).
Paclitaxel Reduces Axonal Bclw to Initiate IP3R1-Dependent Axon Degeneration. Neuron, 96(2), 373-386.e6. [PubMed:29024661] [PMC] [WorldCat] [DOI] - ↑
Rotem, N., Magen, I., Ionescu, A., Gershoni-Emek, N., Altman, T., Costa, C.J., ..., & Perlson, E. (2017).
ALS Along the Axons - Expression of Coding and Noncoding RNA Differs in Axons of ALS models. Scientific reports, 7, 44500. [PubMed:28300211] [PMC] [WorldCat] [DOI] - ↑
Saal, L., Briese, M., Kneitz, S., Glinka, M., & Sendtner, M. (2014).
Subcellular transcriptome alterations in a cell culture model of spinal muscular atrophy point to widespread defects in axonal growth and presynaptic differentiation. RNA (New York, N.Y.), 20(11), 1789-802. [PubMed:25246652] [PMC] [WorldCat] [DOI] - ↑
Preitner, N., Quan, J., Nowakowski, D.W., Hancock, M.L., Shi, J., Tcherkezian, J., ..., & Flanagan, J.G. (2014).
APC is an RNA-binding protein, and its interactome provides a link to neural development and microtubule assembly. Cell, 158(2), 368-382. [PubMed:25036633] [PMC] [WorldCat] [DOI] - ↑
Mili, S., Moissoglu, K., & Macara, I.G. (2008).
Genome-wide screen reveals APC-associated RNAs enriched in cell protrusions. Nature, 453(7191), 115-9. [PubMed:18451862] [PMC] [WorldCat] [DOI] - ↑
Ohashi, R., & Shiina, N. (2020).
Cataloguing and Selection of mRNAs Localized to Dendrites in Neurons and Regulated by RNA-Binding Proteins in RNA Granules. Biomolecules, 10(2). [PubMed:31978946] [PMC] [WorldCat] [DOI] - ↑
KOENIG, E. (1965).
SYNTHETIC MECHANISMS IN THE AXON. I. LOCAL AXONAL SYNTHESIS OF ACETYLCHOLINESTERASE. Journal of neurochemistry, 12, 343-55. [PubMed:14333291] [WorldCat] [DOI] - ↑
KOENIG, E. (1965).
SYNTHETIC MECHANISMS IN THE AXON. II. RNA IN MYELIN-FREE AXONS OF THE CAT. Journal of neurochemistry, 12, 357-61. [PubMed:14333292] [WorldCat] [DOI] - ↑
Steward, O. (1997).
mRNA localization in neurons: a multipurpose mechanism? Neuron, 18(1), 9-12. [PubMed:9010200] [WorldCat] [DOI] - ↑
Kalinski, A.L., Sachdeva, R., Gomes, C., Lee, S.J., Shah, Z., Houle, J.D., & Twiss, J.L. (2015).
mRNAs and Protein Synthetic Machinery Localize into Regenerating Spinal Cord Axons When They Are Provided a Substrate That Supports Growth. The Journal of neuroscience : the official journal of the Society for Neuroscience, 35(28), 10357-70. [PubMed:26180210] [PMC] [WorldCat] [DOI] - ↑
Shigeoka, T., Jung, H., Jung, J., Turner-Bridger, B., Ohk, J., Lin, J.Q., ..., & Holt, C.E. (2016).
Dynamic Axonal Translation in Developing and Mature Visual Circuits. Cell, 166(1), 181-92. [PubMed:27321671] [PMC] [WorldCat] [DOI] - ↑
Taliaferro, J.M., Vidaki, M., Oliveira, R., Olson, S., Zhan, L., Saxena, T., ..., & Burge, C.B. (2016).
Distal Alternative Last Exons Localize mRNAs to Neural Projections. Molecular cell, 61(6), 821-33. [PubMed:26907613] [PMC] [WorldCat] [DOI] - ↑
Bigler, R.L., Kamande, J.W., Dumitru, R., Niedringhaus, M., & Taylor, A.M. (2017).
Messenger RNAs localized to distal projections of human stem cell derived neurons. Scientific reports, 7(1), 611. [PubMed:28377585] [PMC] [WorldCat] [DOI] - ↑
Taylor, A.M., Berchtold, N.C., Perreau, V.M., Tu, C.H., Li Jeon, N., & Cotman, C.W. (2009).
Axonal mRNA in uninjured and regenerating cortical mammalian axons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 29(15), 4697-707. [PubMed:19369540] [PMC] [WorldCat] [DOI] - ↑
Tcherkezian, J., Brittis, P.A., Thomas, F., Roux, P.P., & Flanagan, J.G. (2010).
Transmembrane receptor DCC associates with protein synthesis machinery and regulates translation. Cell, 141(4), 632-44. [PubMed:20434207] [PMC] [WorldCat] [DOI] - ↑
Ben-Yaakov, K., Dagan, S.Y., Segal-Ruder, Y., Shalem, O., Vuppalanchi, D., Willis, D.E., ..., & Fainzilber, M. (2012).
Axonal transcription factors signal retrogradely in lesioned peripheral nerve. The EMBO journal, 31(6), 1350-63. [PubMed:22246183] [PMC] [WorldCat] [DOI] - ↑
Hanz, S., Perlson, E., Willis, D., Zheng, J.Q., Massarwa, R., Huerta, J.J., ..., & Fainzilber, M. (2003).
Axoplasmic importins enable retrograde injury signaling in lesioned nerve. Neuron, 40(6), 1095-104. [PubMed:14687545] [WorldCat] [DOI] - ↑
Perlson, E., Hanz, S., Ben-Yaakov, K., Segal-Ruder, Y., Seger, R., & Fainzilber, M. (2005).
Vimentin-dependent spatial translocation of an activated MAP kinase in injured nerve. Neuron, 45(5), 715-26. [PubMed:15748847] [WorldCat] [DOI] - ↑
Vuppalanchi, D., Merianda, T.T., Donnelly, C., Pacheco, A., Williams, G., Yoo, S., ..., & Twiss, J.L. (2012).
Lysophosphatidic acid differentially regulates axonal mRNA translation through 5'UTR elements. Molecular and cellular neurosciences, 50(2), 136-46. [PubMed:22522146] [PMC] [WorldCat] [DOI] - ↑
Ying, Z., Misra, V., & Verge, V.M. (2014).
Sensing nerve injury at the axonal ER: activated Luman/CREB3 serves as a novel axonally synthesized retrograde regeneration signal. Proceedings of the National Academy of Sciences of the United States of America, 111(45), 16142-7. [PubMed:25349404] [PMC] [WorldCat] [DOI] - ↑
Yudin, D., Hanz, S., Yoo, S., Iavnilovitch, E., Willis, D., Gradus, T., ..., & Fainzilber, M. (2008).
Localized regulation of axonal RanGTPase controls retrograde injury signaling in peripheral nerve. Neuron, 59(2), 241-52. [PubMed:18667152] [PMC] [WorldCat] [DOI] - ↑
Colman, D.R., Kreibich, G., Frey, A.B., & Sabatini, D.D. (1982).
Synthesis and incorporation of myelin polypeptides into CNS myelin. The Journal of cell biology, 95(2 Pt 1), 598-608. [PubMed:6183276] [PMC] [WorldCat] [DOI] - ↑
Ainger, K., Avossa, D., Morgan, F., Hill, S.J., Barry, C., Barbarese, E., & Carson, J.H. (1993).
Transport and localization of exogenous myelin basic protein mRNA microinjected into oligodendrocytes. The Journal of cell biology, 123(2), 431-41. [PubMed:7691830] [PMC] [WorldCat] [DOI] - ↑
Carson, J.H., Worboys, K., Ainger, K., & Barbarese, E. (1997).
Translocation of myelin basic protein mRNA in oligodendrocytes requires microtubules and kinesin. Cell motility and the cytoskeleton, 38(4), 318-28. [PubMed:9415374] [WorldCat] [DOI] - ↑
Munro, T.P., Magee, R.J., Kidd, G.J., Carson, J.H., Barbarese, E., Smith, L.M., & Smith, R. (1999).
Mutational analysis of a heterogeneous nuclear ribonucleoprotein A2 response element for RNA trafficking. The Journal of biological chemistry, 274(48), 34389-95. [PubMed:10567417] [WorldCat] [DOI] - ↑
Hoek, K.S., Kidd, G.J., Carson, J.H., & Smith, R. (1998).
hnRNP A2 selectively binds the cytoplasmic transport sequence of myelin basic protein mRNA. Biochemistry, 37(19), 7021-9. [PubMed:9578590] [WorldCat] [DOI] - ↑
Lyons, D.A., Naylor, S.G., Scholze, A., & Talbot, W.S. (2009).
Kif1b is essential for mRNA localization in oligodendrocytes and development of myelinated axons. Nature genetics, 41(7), 854-8. [PubMed:19503091] [PMC] [WorldCat] [DOI] - ↑
Barbarese, E., Brumwell, C., Kwon, S., Cui, H., & Carson, J.H. (2000).
RNA on the road to myelin. Journal of neurocytology, 28(4-5), 263-70. [PubMed:10739569] [WorldCat] [DOI] - ↑
Gao, Y., Tatavarty, V., Korza, G., Levin, M.K., & Carson, J.H. (2008).
Multiplexed dendritic targeting of alpha calcium calmodulin-dependent protein kinase II, neurogranin, and activity-regulated cytoskeleton-associated protein RNAs by the A2 pathway. Molecular biology of the cell, 19(5), 2311-27. [PubMed:18305102] [PMC] [WorldCat] [DOI] - ↑
Bauer, N.M., Moos, C., van Horssen, J., Witte, M., van der Valk, P., Altenhein, B., ..., & White, R. (2012).
Myelin basic protein synthesis is regulated by small non-coding RNA 715. EMBO reports, 13(9), 827-34. [PubMed:22744314] [PMC] [WorldCat] [DOI] - ↑
Kosturko, L.D., Maggipinto, M.J., Korza, G., Lee, J.W., Carson, J.H., & Barbarese, E. (2006).
Heterogeneous nuclear ribonucleoprotein (hnRNP) E1 binds to hnRNP A2 and inhibits translation of A2 response element mRNAs. Molecular biology of the cell, 17(8), 3521-33. [PubMed:16775011] [PMC] [WorldCat] [DOI] - ↑
Krämer-Albers, E.M., & White, R. (2011).
From axon-glial signalling to myelination: the integrating role of oligodendroglial Fyn kinase. Cellular and molecular life sciences : CMLS, 68(12), 2003-12. [PubMed:21207100] [WorldCat] [DOI] - ↑
White, R., Gonsior, C., Bauer, N.M., Krämer-Albers, E.M., Luhmann, H.J., & Trotter, J. (2012).
Heterogeneous nuclear ribonucleoprotein (hnRNP) F is a novel component of oligodendroglial RNA transport granules contributing to regulation of myelin basic protein (MBP) synthesis. The Journal of biological chemistry, 287(3), 1742-54. [PubMed:22128153] [PMC] [WorldCat] [DOI] - ↑
White, R., Gonsior, C., Krämer-Albers, E.M., Stöhr, N., Hüttelmaier, S., & Trotter, J. (2008).
Activation of oligodendroglial Fyn kinase enhances translation of mRNAs transported in hnRNP A2-dependent RNA granules. The Journal of cell biology, 181(4), 579-86. [PubMed:18490510] [PMC] [WorldCat] [DOI] - ↑
Wake, H., Lee, P.R., & Fields, R.D. (2011).
Control of local protein synthesis and initial events in myelination by action potentials. Science (New York, N.Y.), 333(6049), 1647-51. [PubMed:21817014] [PMC] [WorldCat] [DOI] - ↑
Müller, C., Bauer, N.M., Schäfer, I., & White, R. (2013).
Making myelin basic protein -from mRNA transport to localized translation. Frontiers in cellular neuroscience, 7, 169. [PubMed:24098271] [PMC] [WorldCat] [DOI] - ↑
BODIAN, D. (1964).
AN ELECTRON-MICROSCOPIC STUDY OF THE MONKEY SPINAL CORD. I. FINE STRUCTURE OF NORMAL MOTOR COLUMN. II. EFFECTS OF RETROGRADE CHROMATOLYSIS. III. CYTOLOGIC EFFECTS OF MILD AND VIRULENT POLIOVIRUS INFECTION. Bulletin of the Johns Hopkins Hospital, 114, 13-119. [PubMed:14115595] [WorldCat] - ↑
Garner, C.C., Tucker, R.P., & Matus, A. (1988).
Selective localization of messenger RNA for cytoskeletal protein MAP2 in dendrites. Nature, 336(6200), 674-7. [PubMed:3200318] [WorldCat] [DOI] - ↑
Cajigas, I.J., Tushev, G., Will, T.J., tom Dieck, S., Fuerst, N., & Schuman, E.M. (2012).
The local transcriptome in the synaptic neuropil revealed by deep sequencing and high-resolution imaging. Neuron, 74(3), 453-66. [PubMed:22578497] [PMC] [WorldCat] [DOI] - ↑
Miyashiro, K., Dichter, M., & Eberwine, J. (1994).
On the nature and differential distribution of mRNAs in hippocampal neurites: implications for neuronal functioning. Proceedings of the National Academy of Sciences of the United States of America, 91(23), 10800-4. [PubMed:7971965] [PMC] [WorldCat] [DOI] - ↑
Buxbaum, A.R., Wu, B., & Singer, R.H. (2014).
Single β-actin mRNA detection in neurons reveals a mechanism for regulating its translatability. Science (New York, N.Y.), 343(6169), 419-22. [PubMed:24458642] [PMC] [WorldCat] [DOI] - ↑ 55.0 55.1
Eberwine, J., Miyashiro, K., Kacharmina, J.E., & Job, C. (2001).
Local translation of classes of mRNAs that are targeted to neuronal dendrites. Proceedings of the National Academy of Sciences of the United States of America, 98(13), 7080-5. [PubMed:11416191] [PMC] [WorldCat] [DOI] - ↑
Weiler, I.J., & Greenough, W.T. (1993).
Metabotropic glutamate receptors trigger postsynaptic protein synthesis. Proceedings of the National Academy of Sciences of the United States of America, 90(15), 7168-71. [PubMed:8102206] [PMC] [WorldCat] [DOI] - ↑
Fratiglioni, L., & Qiu, C. (2011).
Prevention of cognitive decline in ageing: dementia as the target, delayed onset as the goal. The Lancet. Neurology, 10(9), 778-9. [PubMed:21775212] [WorldCat] [DOI] - ↑
Merkurjev, D., Hong, W.T., Iida, K., Oomoto, I., Goldie, B.J., Yamaguti, H., ..., & Wang, D.O. (2018).
Synaptic N6-methyladenosine (m6A) epitranscriptome reveals functional partitioning of localized transcripts. Nature neuroscience, 21(7), 1004-1014. [PubMed:29950670] [WorldCat] [DOI]