「ソニック・ヘッジホッグ」の版間の差分
細編集の要約なし |
細 →疾患との関わり |
||
| (同じ利用者による、間の14版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0118148 笹井紀明]</font><br> | <font size="+1">[http://researchmap.jp/read0118148 笹井紀明]</font><br> | ||
''奈良先端科学技術大学院大学''<br> | ''奈良先端科学技術大学院大学''<br> | ||
DOI:<selfdoi /> | DOI:<selfdoi /> 原稿受付日:2017年1月17日 原稿完成日:2017年5月8日<br> | ||
担当編集委員:[http://researchmap.jp/fujiomurakami 村上 富士夫](大阪大学 大学院生命機能研究科)<br> | 担当編集委員:[http://researchmap.jp/fujiomurakami 村上 富士夫](大阪大学 大学院生命機能研究科)<br> | ||
</div> | </div> | ||
| 12行目: | 12行目: | ||
1980年、ドイツの生物学者[[wj:クリスティアーネ・ニュスライン=フォルハルト|Christiane Nüsslein-Volhard]]は、[[ショウジョウバエ]]における[[変異体]]スクリーニングから、幼虫表面の[[剛毛]](bristle)が規則正しく配置されず[[ハリネズミ]]の毛のように体表面全体に散らばる変異個体を発見し、それに[[hedgehog]]変異体と命名した<ref name=ref4><pubmed>6776413</pubmed></ref><ref name=ref5><pubmed>17928586</pubmed></ref>。その後の研究から、これは[[分泌]]因子をコードする[[wj:遺伝子|遺伝子]]の変異によるものであることが明らかとなった<ref><pubmed>11731473</pubmed></ref>。 | 1980年、ドイツの生物学者[[wj:クリスティアーネ・ニュスライン=フォルハルト|Christiane Nüsslein-Volhard]]は、[[ショウジョウバエ]]における[[変異体]]スクリーニングから、幼虫表面の[[剛毛]](bristle)が規則正しく配置されず[[ハリネズミ]]の毛のように体表面全体に散らばる変異個体を発見し、それに[[hedgehog]]変異体と命名した<ref name=ref4><pubmed>6776413</pubmed></ref><ref name=ref5><pubmed>17928586</pubmed></ref>。その後の研究から、これは[[分泌]]因子をコードする[[wj:遺伝子|遺伝子]]の変異によるものであることが明らかとなった<ref><pubmed>11731473</pubmed></ref>。 | ||
一方、1990年の前半に[[脊椎動物]]においても3つのヘッジホッグ相同遺伝子が単離され、そのうち[[desert hedgehog]]([[Dhh]])と[[indian hedgehog]]([[Ihh]] | 一方、1990年の前半に[[脊椎動物]]においても3つのヘッジホッグ相同遺伝子が単離され、そのうち[[desert hedgehog]]([[Dhh]])と[[indian hedgehog]]([[Ihh]])は実在するハリネズミの種名から、ソニック・ヘッジホッグ (sonic hedgehog, Shh)はテレビゲームのキャラクターからそれぞれ命名された。Dhhは精子形成に<ref><pubmed>11090455</pubmed></ref>、Ihhが軟骨細胞の形成・増殖にそれぞれ重要な役割を果たす<ref><pubmed>21364421</pubmed></ref><ref><pubmed>10631175</pubmed></ref>一方で、ソニック・ヘッジホッグ<ref><pubmed>8269518</pubmed></ref><ref><pubmed>8269519</pubmed></ref><ref><pubmed>7916661</pubmed></ref>は[[中枢神経系]]や[[wj:四肢|四肢]]形成をはじめとする[[胚発生]]([[器官発生]])の多くに重要であることが示され、現在ヘッジホッグ関連遺伝子の中で最も解析が進んでいる。 | ||
==ファミリー== | ==ファミリー== | ||
| 22行目: | 22行目: | ||
ソニック・ヘッジホッグ遺伝子からは転写・翻訳されて、まず45 kDa程度の[[wj:ポリペプチド|ポリペプチド]]が前駆体として生じる。このポリペプチドは[[wj:小胞体|小胞体]]に運ばれ、アミノ末端とカルボキシル末端の2つの部分に分解される('''図1''')。 | ソニック・ヘッジホッグ遺伝子からは転写・翻訳されて、まず45 kDa程度の[[wj:ポリペプチド|ポリペプチド]]が前駆体として生じる。このポリペプチドは[[wj:小胞体|小胞体]]に運ばれ、アミノ末端とカルボキシル末端の2つの部分に分解される('''図1''')。 | ||
分泌されてその活性を発揮するのはアミノ末端側のポリペプチド([[ShhN]]; 19kDa程度)である<ref><pubmed>21357747</pubmed></ref>。その構造は2つのαヘリックスと6つのβストランドからなるα+βサンドイッチ構造を形成しており、[[wj:亜鉛|亜鉛]]イオンを一分子配位している<ref name= | 分泌されてその活性を発揮するのはアミノ末端側のポリペプチド([[ShhN]]; 19kDa程度)である<ref><pubmed>21357747</pubmed></ref>。その構造は2つのαヘリックスと6つのβストランドからなるα+βサンドイッチ構造を形成しており、[[wj:亜鉛|亜鉛]]イオンを一分子配位している<ref name=ref14><pubmed>7477329</pubmed></ref>。 | ||
ShhNには[[パルミチン酸]](アミノ末端)と[[コレステロール]](カルボキシル末端)が付加されるが、これらの修飾はShhNの効率的な分泌と、組織内での適切な分布に重要である<ref><pubmed>16611729</pubmed></ref><ref><pubmed>11486055</pubmed></ref><ref><pubmed>15075292</pubmed></ref><ref><pubmed>8824192</pubmed></ref><ref><pubmed>11389830</pubmed></ref><ref><pubmed>23112049</pubmed></ref>。一方、カルボキシル末端側([[ShhC]])はこの分解を制御するほか、[[コレステロール転移酵素]]としてアミノ末端側フラグメントの修飾に寄与する<ref><pubmed>15189162</pubmed></ref>。 | ShhNには[[パルミチン酸]](アミノ末端)と[[コレステロール]](カルボキシル末端)が付加されるが、これらの修飾はShhNの効率的な分泌と、組織内での適切な分布に重要である<ref><pubmed>16611729</pubmed></ref><ref><pubmed>11486055</pubmed></ref><ref><pubmed>15075292</pubmed></ref><ref><pubmed>8824192</pubmed></ref><ref><pubmed>11389830</pubmed></ref><ref><pubmed>23112049</pubmed></ref>。一方、カルボキシル末端側([[ShhC]])はこの分解を制御するほか、[[コレステロール転移酵素]]としてアミノ末端側フラグメントの修飾に寄与する<ref><pubmed>15189162</pubmed></ref>。 | ||
| 29行目: | 29行目: | ||
分解と修飾によって成熟型となったShhNは細胞から分泌されるが、その分泌には[[膜タンパク質]][[Dispatched]]と、分泌因子[[Scube]]の存在が必要である<ref name=ref24></ref>。 | 分解と修飾によって成熟型となったShhNは細胞から分泌されるが、その分泌には[[膜タンパク質]][[Dispatched]]と、分泌因子[[Scube]]の存在が必要である<ref name=ref24></ref>。 | ||
この分泌経路のほかに最近、ソニック・ヘッジホッグタンパク質が[[サイトニーム]](cytoneme)と呼ばれる突起上の[[細胞膜]]構造の先端まで運搬され、そこで小胞を形成して細胞外へ分泌されるという経路が提唱されている。サイトニームは[[糸状仮足]]([[filopodia]])が長く変形した形状をしており、内部には[[アクチン]]が含まれている。ショウジョウバエの[[翅原基]](wing disc)ではヘッジホッグを産生する細胞がこのような構造を持っており<ref><pubmed>10367889</pubmed></ref>、発現部位から遠い細胞までシグナルを届けている<ref name=ref1></ref><ref><pubmed>23276604</pubmed></ref><ref><pubmed>25483805</pubmed></ref><ref><pubmed>25472772</pubmed></ref> | この分泌経路のほかに最近、ソニック・ヘッジホッグタンパク質が[[サイトニーム]](cytoneme)と呼ばれる突起上の[[細胞膜]]構造の先端まで運搬され、そこで小胞を形成して細胞外へ分泌されるという経路が提唱されている。サイトニームは[[糸状仮足]]([[filopodia]])が長く変形した形状をしており、内部には[[アクチン]]が含まれている。ショウジョウバエの[[翅原基]](wing disc)ではヘッジホッグを産生する細胞がこのような構造を持っており<ref><pubmed>10367889</pubmed></ref>、発現部位から遠い細胞までシグナルを届けている<ref name=ref1></ref><ref><pubmed>23276604</pubmed></ref><ref><pubmed>25483805</pubmed></ref><ref><pubmed>25472772</pubmed></ref>。サイトニームは近年[[脊椎動物]]でもその存在が知られるようになった<ref><pubmed>23624372</pubmed></ref>。 | ||
==発現== | |||
胚発生期では[[頭尾軸]]にかけて[[神経管]]の最も腹側に位置する[[底板]]領域(floor plate)とその下部に位置する[[中胚葉]]系の組織([[脊策]]:notochord)、さらに[[前脳]]の腹側と[[zona limitans intrathalamica]] | 胚発生期では[[頭尾軸]]にかけて[[神経管]]の最も腹側に位置する[[底板]]領域(floor plate)とその下部に位置する[[中胚葉]]系の組織([[脊策]]:notochord)、さらに[[前脳]]の腹側と[[zona limitans intrathalamica]](ZLI)と呼ばれるる前脳の一領域、さらに[[肢芽]](limb bud; 四肢が発生する場所)の一部に、主に発現することが知られている。成体では[[脳室下帯]](subventricular zone)の[[神経幹細胞]]の周辺部に見られる<ref name=ref1 /><ref name=ref2 /><ref name=ref3 />。 | ||
==機能== | ==機能== | ||
===シグナル経路=== | ===シグナル経路=== | ||
[[image:Shh2.png|thumb|300px|'''図2.ソニック・ヘッジホッグによる細胞内シグナル伝達経路'''<br> | [[image:Shh2.png|thumb|300px|'''図2.ソニック・ヘッジホッグによる細胞内シグナル伝達経路'''<br>[[PIP3|PIP<sub>3</sub>]]:[[フォスファチジルイノシトール3リン酸]]、Gli<sup>FL</sup>:全長Gli、Gli<sup>Rep</sup>:抑制型Gli、Gli<sup>Act</sup>:活性化型Gli、Cul3:Cullin3。<br>主に<ref name=ref37 /><ref name=ref39 /><ref name=ref40 />を参考に作成。]] | ||
==== Ptc-Smo-Gli経路 ==== | ==== Ptc-Smo-Gli経路 ==== | ||
| 45行目: | 45行目: | ||
細胞膜で受容されたシグナルを核に伝達するのは、[[Gli]](ショウジョウバエでは[[Cubitus interruptus]]; Ci)と呼ばれる[[Znフィンガー型転写因子]]であり、脊椎動物に存在する3種類のGli([[Gli1]]-[[Gli3|3]])<ref name=ref31><pubmed>21801010</pubmed></ref> のうちソニック・ヘッジホッグのシグナルを1次的に伝達するのは[[Gli2]],3である('''図3''')。Gli2,3は繊毛内でSmoと何らかの相互作用をすることにより、シグナルを繊毛から核へと伝達する<ref name=ref32><pubmed>16254602</pubmed></ref>。 | 細胞膜で受容されたシグナルを核に伝達するのは、[[Gli]](ショウジョウバエでは[[Cubitus interruptus]]; Ci)と呼ばれる[[Znフィンガー型転写因子]]であり、脊椎動物に存在する3種類のGli([[Gli1]]-[[Gli3|3]])<ref name=ref31><pubmed>21801010</pubmed></ref> のうちソニック・ヘッジホッグのシグナルを1次的に伝達するのは[[Gli2]],3である('''図3''')。Gli2,3は繊毛内でSmoと何らかの相互作用をすることにより、シグナルを繊毛から核へと伝達する<ref name=ref32><pubmed>16254602</pubmed></ref>。 | ||
Gli2/3は転写活性領域と抑制領域を併せ持つ転写因子で、ソニック・ヘッジホッグシグナルが存在しないときには翻訳されたポリペプチドが恒常的に分解([[ユビキチン化]])されてアミノ末端側だけの断片として存在し、転写抑制因子として働く。Gli2/3のユビキチン化は、まず[[PKA]]([[プロテインキナーゼA]])と[[Glycogen synthase kinase 3|Glycogen Synthase Kinase 3]]β([[GSK3β]])によって[[セリン]]残基が[[リン酸化]]され、それを、 [[β | Gli2/3は転写活性領域と抑制領域を併せ持つ転写因子で、ソニック・ヘッジホッグシグナルが存在しないときには翻訳されたポリペプチドが恒常的に分解([[ユビキチン化]])されてアミノ末端側だけの断片として存在し、転写抑制因子として働く。Gli2/3のユビキチン化は、まず[[PKA]]([[プロテインキナーゼA]])と[[Glycogen synthase kinase 3|Glycogen Synthase Kinase 3]]β([[GSK3β]])によって[[セリン]]残基が[[リン酸化]]され、それを、 [[β-TrCP]]([[E3ユビキチンリガーゼ]])と[[足場タンパク質]][[Cullin3]]を含むSCF β-TrCP複合体がターゲットすることによって進む<ref><pubmed>16705181</pubmed></ref><ref name=ref34><pubmed>16611981</pubmed></ref><ref><pubmed>16651270</pubmed></ref>。 | ||
いったんソニック・ヘッジホッグシグナルが細胞に導入されるとPKAが不活化され<ref name=ref36><pubmed>24336288</pubmed></ref><ref name=ref37><pubmed>27799542</pubmed></ref>、Gli2/3のユビキチン分解が抑制されて全長型Gli2/3は繊毛内に移動する<ref name=ref32><pubmed>16254602</pubmed></ref><ref><pubmed>20154143</pubmed></ref>。その後、核に移動して遺伝子発現を誘導する<ref name=ref39><pubmed>23799571</pubmed></ref>。この際にはGli2/3に対してSPOPと呼ばれるユビキチンリガーゼによるユビキチン化が起こってタンパク質自体の安定性が変化する<ref name=ref40><pubmed>20360384</pubmed></ref><ref><pubmed>20463034</pubmed></ref>ほか、さまざまな修飾(リン酸化、[[アセチル化]]、[[SUMO化]])も関与してその転写活性を制御する<ref name=ref40><pubmed>20360384</pubmed></ref><ref><pubmed>20711444</pubmed></ref><ref><pubmed>23762415</pubmed></ref><ref><pubmed>24373970</pubmed></ref>。 | いったんソニック・ヘッジホッグシグナルが細胞に導入されるとPKAが不活化され<ref name=ref36><pubmed>24336288</pubmed></ref><ref name=ref37><pubmed>27799542</pubmed></ref>、Gli2/3のユビキチン分解が抑制されて全長型Gli2/3は繊毛内に移動する<ref name=ref32><pubmed>16254602</pubmed></ref><ref><pubmed>20154143</pubmed></ref>。その後、核に移動して遺伝子発現を誘導する<ref name=ref39><pubmed>23799571</pubmed></ref>。この際にはGli2/3に対してSPOPと呼ばれるユビキチンリガーゼによるユビキチン化が起こってタンパク質自体の安定性が変化する<ref name=ref40><pubmed>20360384</pubmed></ref><ref><pubmed>20463034</pubmed></ref>ほか、さまざまな修飾(リン酸化、[[アセチル化]]、[[SUMO化]])も関与してその転写活性を制御する<ref name=ref40><pubmed>20360384</pubmed></ref><ref><pubmed>20711444</pubmed></ref><ref><pubmed>23762415</pubmed></ref><ref><pubmed>24373970</pubmed></ref>。 | ||
| 53行目: | 53行目: | ||
Gli1-3は多くの臓器に発現しているためにそれらの遺伝子変異マウスの表現型も多様であり<ref><pubmed>9731531</pubmed></ref>、神経系で強い表現型が現れるものもある。Gli2変異マウスでは、Shhシグナルの影響を受ける底板とV3[[介在神経]]領域の[[分化]]が抑制され、パターン形成に異常が生じて出生直後に死亡する<ref><pubmed>9636069</pubmed></ref>。一方、Gli3変異マウスでは、主に脳領域でソニック・ヘッジホッグシグナルがむしろ亢進した表現型になるため<ref><pubmed>8387379</pubmed></ref><ref><pubmed>11017169</pubmed></ref>、Gli3が主に転写抑制型として働くことが示唆される。Gli1単独の変異マウスでは神経系では大きな表現型が見つかっていないが、Gli2変異による表現型をGli1のノックインによって相補することができるため、Gli2の転写活性型と同様の働きをしていると考えられる<ref><pubmed>10725236</pubmed></ref><ref><pubmed>11748151</pubmed></ref>。 | Gli1-3は多くの臓器に発現しているためにそれらの遺伝子変異マウスの表現型も多様であり<ref><pubmed>9731531</pubmed></ref>、神経系で強い表現型が現れるものもある。Gli2変異マウスでは、Shhシグナルの影響を受ける底板とV3[[介在神経]]領域の[[分化]]が抑制され、パターン形成に異常が生じて出生直後に死亡する<ref><pubmed>9636069</pubmed></ref>。一方、Gli3変異マウスでは、主に脳領域でソニック・ヘッジホッグシグナルがむしろ亢進した表現型になるため<ref><pubmed>8387379</pubmed></ref><ref><pubmed>11017169</pubmed></ref>、Gli3が主に転写抑制型として働くことが示唆される。Gli1単独の変異マウスでは神経系では大きな表現型が見つかっていないが、Gli2変異による表現型をGli1のノックインによって相補することができるため、Gli2の転写活性型と同様の働きをしていると考えられる<ref><pubmed>10725236</pubmed></ref><ref><pubmed>11748151</pubmed></ref>。 | ||
[[image:Shh3.png|thumb|300px|'''図3.Gliタンパク質の構造'''<br> | [[image:Shh3.png|thumb|300px|'''図3.Gliタンパク質の構造'''<br>アミノ酸番号は、マウスのものである。*はPKAによるリン酸化サイト、ZnF:Znフィンガー、矢頭は分解されて転写抑制型を生じる部位<ref name=ref34 />。<br><ref name=ref31 /><ref name=ref34 />から改変。]] | ||
ソニック・ヘッジホッグシグナルのターゲット遺伝子として代表的なものは、[[神経前駆細胞]]における[[Olig2]]や[[Nkx2.2]], [[FoxA2]]のように細胞の個性付けに関与する転写因子、またソニック・ヘッジホッグシグナルに直接関与するもの(Ptc, Gli1)などである<ref name=ref1></ref><ref name=ref3></ref>。 | ソニック・ヘッジホッグシグナルのターゲット遺伝子として代表的なものは、[[神経前駆細胞]]における[[Olig2]]や[[Nkx2.2]], [[FoxA2]]のように細胞の個性付けに関与する転写因子、またソニック・ヘッジホッグシグナルに直接関与するもの(Ptc, Gli1)などである<ref name=ref1></ref><ref name=ref3></ref>。 | ||
| 68行目: | 68行目: | ||
==== ほかの経路 ==== | ==== ほかの経路 ==== | ||
ソニック・ヘッジホッグは交連神経細胞のガイダンスに必須である<ref name=ref58><pubmed>15746914</pubmed></ref><ref name=ref59><pubmed>19447091</pubmed></ref><ref name=ref60><pubmed>12679031</pubmed></ref>。ソニック・ヘッジホッグは神経のガイダンス因子として知られる[[ネトリン]]と協調して働き、[[交連神経]]が[[脊髄]]正中(midline)を交差するのに必要である<ref name=ref60><pubmed>12679031</pubmed></ref>。このガイダンスにはPtc/Smoではなく[[HIP]]([[hedgehog interacting protein]])がソニック・ヘッジホッグの受容体になっており<ref name=ref58 /> 、さらに細胞内では[[Srcファミリーキナーゼ]]([[Src family kinase]]; [[SFK]])が活性化されている<ref name=ref59 /> | ソニック・ヘッジホッグは交連神経細胞のガイダンスに必須である<ref name=ref58><pubmed>15746914</pubmed></ref><ref name=ref59><pubmed>19447091</pubmed></ref><ref name=ref60><pubmed>12679031</pubmed></ref>。ソニック・ヘッジホッグは神経のガイダンス因子として知られる[[ネトリン]]と協調して働き、[[交連神経]]が[[脊髄]]正中(midline)を交差するのに必要である<ref name=ref60><pubmed>12679031</pubmed></ref>。このガイダンスにはPtc/Smoではなく[[HIP]]([[hedgehog interacting protein]])がソニック・ヘッジホッグの受容体になっており<ref name=ref58 /> 、さらに細胞内では[[Srcファミリーキナーゼ]]([[Src family kinase]]; [[SFK]])が活性化されている<ref name=ref59 /> 。また、線維芽細胞の化学遊走にもソニック・ヘッジホッグが関与しているという報告があり、さらにこの現象においてはSmoが繊毛に局在しなくても細胞内シグナルが惹起されるため、従来とは異なるメカニズムが示唆されている<ref><pubmed>22912493</pubmed></ref>。 | ||
===神経系での機能=== | ===神経系での機能=== | ||
| 75行目: | 75行目: | ||
1991年、[[w:Thomas Jessell|Thomas M. Jessell]]と山田俊哉は、ニワトリ胚の脊策を神経管の別の場所に移植し、移植した周辺領域の細胞が[[底板]]([[floor plate]])や[[運動神経]]([[motor neuron]])に異所的に分化することを発見し、脊策と底板から分化誘導因子が分泌されていることを示した<ref><pubmed>1991324</pubmed></ref><ref><pubmed>8500163</pubmed></ref>。 | 1991年、[[w:Thomas Jessell|Thomas M. Jessell]]と山田俊哉は、ニワトリ胚の脊策を神経管の別の場所に移植し、移植した周辺領域の細胞が[[底板]]([[floor plate]])や[[運動神経]]([[motor neuron]])に異所的に分化することを発見し、脊策と底板から分化誘導因子が分泌されていることを示した<ref><pubmed>1991324</pubmed></ref><ref><pubmed>8500163</pubmed></ref>。 | ||
その後、この分泌因子がソニック・ヘッジホッグであること<ref><pubmed>8124714</pubmed></ref> 、さらにソニック・ヘッジホッグが[[神経管]]内で濃度勾配を形成して<ref><pubmed>7736596</pubmed></ref><ref><pubmed>20066087</pubmed></ref | その後、この分泌因子がソニック・ヘッジホッグであること<ref><pubmed>8124714</pubmed></ref> 、さらにソニック・ヘッジホッグが[[神経管]]内で濃度勾配を形成して<ref><pubmed>7736596</pubmed></ref><ref><pubmed>20066087</pubmed></ref>、[[モルフォゲン]]とし働いて濃度依存的に運動神経や介在神経の前駆細胞を誘導する(詳細は別項で議論する)。 | ||
詳細な発現・機能解析の結果、Shhは神経発生の初期には前脳の領域化に<ref><pubmed>883777</pubmed></ref><ref><pubmed>17030124</pubmed></ref> | 詳細な発現・機能解析の結果、Shhは神経発生の初期には前脳の領域化に<ref><pubmed>883777</pubmed></ref><ref><pubmed>17030124</pubmed></ref>)、その後中枢神経全体のパターン形成に関与することが明らかとなった。さらに胚発生が進み、出生前後になると、小脳のプルキンエ細胞(Purkinje cells)からShhが分泌され、顆粒細胞の前駆細胞に作用してその増殖を促進し、さらにバーグマングリア細胞への分化を誘導することが知られている<ref><pubmed>10226030</pubmed></ref><ref><pubmed>15183722</pubmed></ref><ref><pubmed>10375501</pubmed></ref>。 | ||
また生後の脳においても神経前駆細胞の存在が知られており、ソニック・ヘッジホッグシグナルが微小環境(ニッチ:niche)において活性化されて前駆細胞の幹細胞性を維持している<ref><pubmed>16208373</pubmed></ref><ref><pubmed>27666792</pubmed></ref>。 | また生後の脳においても神経前駆細胞の存在が知られており、ソニック・ヘッジホッグシグナルが微小環境(ニッチ:niche)において活性化されて前駆細胞の幹細胞性を維持している<ref><pubmed>16208373</pubmed></ref><ref><pubmed>27666792</pubmed></ref>。 | ||
==実験手法 == | ==実験手法 == | ||
細胞レベルでの解析においてソニック・ヘッジホッグシグナルに反応する培養細胞は少なく、よく使われるのはマウスの線維芽細胞NIH3T3細胞<ref name=ref69><pubmed>25833741</pubmed></ref>やヒト角化細胞<ref><pubmed>16880536</pubmed></ref>、ニワトリやマウスの神経前駆細胞([[胚性幹細胞]]から分化させたものや胚から単離したもの)である<ref name=ref71><pubmed>26972603</pubmed></ref><ref><pubmed>25026549</pubmed></ref>。ソニック・ヘッジホッグシグナルを受容する1次繊毛は、[[細胞周期]]のG0/G1期にのみ生じるため、特にNIH3T3でソニック・ヘッジホッグシグナルの実験を行う際にはあらかじめ血清飢餓状態にしてG0/G1期の細胞を多数得ておくことが重要である。細胞において実験的にソニック・ヘッジホッグシグナルを活性化する場合、大腸菌で作成した(つまりコレステロール修飾がされていない)リコンビナントタンパク質も活性は持っている<ref name=ref71><pubmed>26972603</pubmed></ref><ref><pubmed>10564658</pubmed></ref><ref name=ref74><pubmed>18046410</pubmed></ref>。化合物としては、purmorphamineとSAGがSmoを標的とし<ref><pubmed>16408082</pubmed></ref>、ソニック・ヘッジホッグのアゴニストとして用いられている。一方、cyclopamineとSANT-1は同じくSmoを標的とし、その活性を阻害することによりソニック・ヘッジホッグシグナルの[[アンタゴニスト]]として働く<ref name=ref77><pubmed>12414725</pubmed></ref><ref name=ref078><pubmed>23548480</pubmed></ref>。 | |||
ソニック・ヘッジホッグシグナルの強度を計測する方法としては、luciferaseまたはGFPのレポーターコンストラクトが多用されるが<ref name=ref45><pubmed>9118802</pubmed></ref><ref name=ref76><pubmed>22265416</pubmed></ref>、ほかの方法として、定量PCRを用いてソニック・ヘッジホッグシグナルのターゲット遺伝子であるGli1やPtc1の発現量を解析してもよい<ref name=ref69><pubmed>25833741</pubmed></ref><ref name=ref74><pubmed>18046410</pubmed></ref>。NIH3T3では、ソニック・ヘッジホッグシグナルの添加時間とともにGli1やPtc1の発現量が増加する<ref name=ref69><pubmed>25833741</pubmed></ref>。一方、神経前駆細胞内ではソニック・ヘッジホッグシグナルは数時間以内にいったん活性化し、その後、負のフィードバックが起こって鎮静化する<ref name=ref74><pubmed>18046410</pubmed></ref><ref name=ref76><pubmed>22265416</pubmed></ref><ref><pubmed>20532235</pubmed></ref>。この負のフィードバックが起きるメカニズムとしては、Ptcが細胞膜上に多数存在するようになってソニック・ヘッジホッグタンパク質が枯渇するというもの<ref name=ref74><pubmed>18046410</pubmed></ref>や、活性型Gliタンパク質が不活性型に比べて不安定であるというもの<ref name=ref40><pubmed>20360384</pubmed></ref>などがあるが、全容はまだ明らかになっていない。 | ソニック・ヘッジホッグシグナルの強度を計測する方法としては、luciferaseまたはGFPのレポーターコンストラクトが多用されるが<ref name=ref45><pubmed>9118802</pubmed></ref><ref name=ref76><pubmed>22265416</pubmed></ref>、ほかの方法として、定量PCRを用いてソニック・ヘッジホッグシグナルのターゲット遺伝子であるGli1やPtc1の発現量を解析してもよい<ref name=ref69><pubmed>25833741</pubmed></ref><ref name=ref74><pubmed>18046410</pubmed></ref>。NIH3T3では、ソニック・ヘッジホッグシグナルの添加時間とともにGli1やPtc1の発現量が増加する<ref name=ref69><pubmed>25833741</pubmed></ref>。一方、神経前駆細胞内ではソニック・ヘッジホッグシグナルは数時間以内にいったん活性化し、その後、負のフィードバックが起こって鎮静化する<ref name=ref74><pubmed>18046410</pubmed></ref><ref name=ref76><pubmed>22265416</pubmed></ref><ref><pubmed>20532235</pubmed></ref>。この負のフィードバックが起きるメカニズムとしては、Ptcが細胞膜上に多数存在するようになってソニック・ヘッジホッグタンパク質が枯渇するというもの<ref name=ref74><pubmed>18046410</pubmed></ref>や、活性型Gliタンパク質が不活性型に比べて不安定であるというもの<ref name=ref40><pubmed>20360384</pubmed></ref>などがあるが、全容はまだ明らかになっていない。 | ||
| 91行目: | 91行目: | ||
細胞内コレステロール輸送に関与する遺伝子NPC1/2に変異が生じると[[リソソーム]]にコレステロールが蓄積するためにShhNに十分なコレステロールが供給されずに修飾不全となり、効率的な分泌が不可能になってしまう。[[C型ニーマン・ピック病]](C型Niemann-Pick syndrome)はこのNPC1/2遺伝子の変異に起因する遺伝性疾患であり、[[小脳]]の不完全形成や肝不全、[[発達障害]]や運動障害、新生児黄疸などの重篤な小児障害を引き起こす<ref><pubmed>9211850</pubmed></ref><ref name=ref24><pubmed>22902404</pubmed></ref>。 | 細胞内コレステロール輸送に関与する遺伝子NPC1/2に変異が生じると[[リソソーム]]にコレステロールが蓄積するためにShhNに十分なコレステロールが供給されずに修飾不全となり、効率的な分泌が不可能になってしまう。[[C型ニーマン・ピック病]](C型Niemann-Pick syndrome)はこのNPC1/2遺伝子の変異に起因する遺伝性疾患であり、[[小脳]]の不完全形成や肝不全、[[発達障害]]や運動障害、新生児黄疸などの重篤な小児障害を引き起こす<ref><pubmed>9211850</pubmed></ref><ref name=ref24><pubmed>22902404</pubmed></ref>。 | ||
逆にヘッジホッグシグナルが亢進しすぎると[[ | 逆にヘッジホッグシグナルが亢進しすぎると[[髄芽腫]]([[medulloblastoma]])という[[wj:小児がん|小児がん]]を引き起こすことが知られている<ref name=ref78><pubmed>25150496</pubmed></ref>。この疾患は元来放射線治療や外科的手術による腫瘍の除去しか治療法がなかったが、最近、[[三量体Gタンパク質|Gタンパク質]]の一種[[Gαs]]を活性化させることによりソニック・ヘッジホッグシグナルをブロックする方法が検討されつつある<ref name=ref78><pubmed>25150496</pubmed></ref>。 | ||
==参考文献== | ==参考文献== | ||
<references/> | <references/> | ||
2020年12月25日 (金) 18:48時点における最新版
笹井紀明
奈良先端科学技術大学院大学
DOI:10.14931/bsd.7348 原稿受付日:2017年1月17日 原稿完成日:2017年5月8日
担当編集委員:村上 富士夫(大阪大学 大学院生命機能研究科)
英語名:Sonic Hedgehog 英略称:Shh
ソニック・ヘッジホッグは細胞外シグナル因子の1つで、胚発生において細胞の増殖や分化、四肢の発生、神経細胞の誘引に働くほか、成体期においては幹細胞性の維持や腫瘍形成などに関与する多機能タンパク質である[1][2][3]。
発見の歴史
1980年、ドイツの生物学者Christiane Nüsslein-Volhardは、ショウジョウバエにおける変異体スクリーニングから、幼虫表面の剛毛(bristle)が規則正しく配置されずハリネズミの毛のように体表面全体に散らばる変異個体を発見し、それにhedgehog変異体と命名した[4][5]。その後の研究から、これは分泌因子をコードする遺伝子の変異によるものであることが明らかとなった[6]。
一方、1990年の前半に脊椎動物においても3つのヘッジホッグ相同遺伝子が単離され、そのうちdesert hedgehog(Dhh)とindian hedgehog(Ihh)は実在するハリネズミの種名から、ソニック・ヘッジホッグ (sonic hedgehog, Shh)はテレビゲームのキャラクターからそれぞれ命名された。Dhhは精子形成に[7]、Ihhが軟骨細胞の形成・増殖にそれぞれ重要な役割を果たす[8][9]一方で、ソニック・ヘッジホッグ[10][11][12]は中枢神経系や四肢形成をはじめとする胚発生(器官発生)の多くに重要であることが示され、現在ヘッジホッグ関連遺伝子の中で最も解析が進んでいる。
ファミリー
脊椎動物ではdesert hedgehog(Dhh)とindian hedgehog(Ihh)とともにヘッジホッグファミリーを形成し、これらとともに受容体や細胞内シグナル伝達経路を共有している。
構造
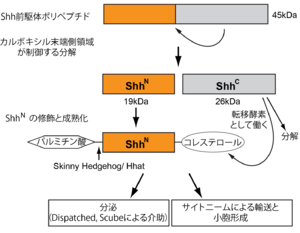
ソニック・ヘッジホッグ遺伝子からは転写・翻訳されて、まず45 kDa程度のポリペプチドが前駆体として生じる。このポリペプチドは小胞体に運ばれ、アミノ末端とカルボキシル末端の2つの部分に分解される(図1)。
分泌されてその活性を発揮するのはアミノ末端側のポリペプチド(ShhN; 19kDa程度)である[13]。その構造は2つのαヘリックスと6つのβストランドからなるα+βサンドイッチ構造を形成しており、亜鉛イオンを一分子配位している[14]。
ShhNにはパルミチン酸(アミノ末端)とコレステロール(カルボキシル末端)が付加されるが、これらの修飾はShhNの効率的な分泌と、組織内での適切な分布に重要である[15][16][17][18][19][20]。一方、カルボキシル末端側(ShhC)はこの分解を制御するほか、コレステロール転移酵素としてアミノ末端側フラグメントの修飾に寄与する[21]。
分泌
分解と修飾によって成熟型となったShhNは細胞から分泌されるが、その分泌には膜タンパク質Dispatchedと、分泌因子Scubeの存在が必要である[22]。
この分泌経路のほかに最近、ソニック・ヘッジホッグタンパク質がサイトニーム(cytoneme)と呼ばれる突起上の細胞膜構造の先端まで運搬され、そこで小胞を形成して細胞外へ分泌されるという経路が提唱されている。サイトニームは糸状仮足(filopodia)が長く変形した形状をしており、内部にはアクチンが含まれている。ショウジョウバエの翅原基(wing disc)ではヘッジホッグを産生する細胞がこのような構造を持っており[23]、発現部位から遠い細胞までシグナルを届けている[1][24][25][26]。サイトニームは近年脊椎動物でもその存在が知られるようになった[27]。
発現
胚発生期では頭尾軸にかけて神経管の最も腹側に位置する底板領域(floor plate)とその下部に位置する中胚葉系の組織(脊策:notochord)、さらに前脳の腹側とzona limitans intrathalamica(ZLI)と呼ばれるる前脳の一領域、さらに肢芽(limb bud; 四肢が発生する場所)の一部に、主に発現することが知られている。成体では脳室下帯(subventricular zone)の神経幹細胞の周辺部に見られる[1][2][3]。
機能
シグナル経路
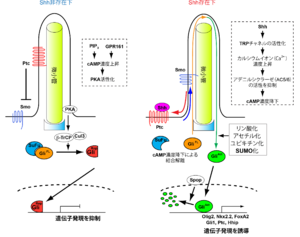
PIP3:フォスファチジルイノシトール3リン酸、GliFL:全長Gli、GliRep:抑制型Gli、GliAct:活性化型Gli、Cul3:Cullin3。
主に[28][29][30]を参考に作成。
Ptc-Smo-Gli経路
ソニック・ヘッジホッグによる主要な細胞内シグナル経路は、2つの膜タンパク質 – 12回膜貫通型Patched(Ptc)と7回膜貫通型のGタンパク質共役型受容体(G-protein coupled receptor; GPCR)の1つSmoothened(Smo) − によって仲介されている(図2)。
Patchedは細胞膜の中でも特に1次繊毛と呼ばれる細胞の突起部分に局在し、ソニック・ヘッジホッグと直接結合する。いったんソニック・ヘッジホッグがPatchedに結合するとソニック・ヘッジホッグ/Patched複合体は繊毛から細胞膜へと移動する[31]。一方、もう1つの膜タンパク質Smoは、細胞がソニック・ヘッジホッグに暴露されていないときには繊毛の周辺の細胞膜上に存在するが、細胞がソニック・ヘッジホッグによって刺激され、ソニック・ヘッジホッグ/Ptc複合体が繊毛から退去すると、代わりに繊毛内へと進入する。
細胞膜で受容されたシグナルを核に伝達するのは、Gli(ショウジョウバエではCubitus interruptus; Ci)と呼ばれるZnフィンガー型転写因子であり、脊椎動物に存在する3種類のGli(Gli1-3)[32] のうちソニック・ヘッジホッグのシグナルを1次的に伝達するのはGli2,3である(図3)。Gli2,3は繊毛内でSmoと何らかの相互作用をすることにより、シグナルを繊毛から核へと伝達する[33]。
Gli2/3は転写活性領域と抑制領域を併せ持つ転写因子で、ソニック・ヘッジホッグシグナルが存在しないときには翻訳されたポリペプチドが恒常的に分解(ユビキチン化)されてアミノ末端側だけの断片として存在し、転写抑制因子として働く。Gli2/3のユビキチン化は、まずPKA(プロテインキナーゼA)とGlycogen Synthase Kinase 3β(GSK3β)によってセリン残基がリン酸化され、それを、 β-TrCP(E3ユビキチンリガーゼ)と足場タンパク質Cullin3を含むSCF β-TrCP複合体がターゲットすることによって進む[34][35][36]。
いったんソニック・ヘッジホッグシグナルが細胞に導入されるとPKAが不活化され[37][28]、Gli2/3のユビキチン分解が抑制されて全長型Gli2/3は繊毛内に移動する[33][38]。その後、核に移動して遺伝子発現を誘導する[29]。この際にはGli2/3に対してSPOPと呼ばれるユビキチンリガーゼによるユビキチン化が起こってタンパク質自体の安定性が変化する[30][39]ほか、さまざまな修飾(リン酸化、アセチル化、SUMO化)も関与してその転写活性を制御する[30][40][41][42]。
Gliタンパク質のDNA結合配列にはGACCACCCAという配列が提唱されてきた[43] が、最近、解離定数(結合のアフィニティー)が異なる別の配列も見つかっている[44]。
Gli1-3は多くの臓器に発現しているためにそれらの遺伝子変異マウスの表現型も多様であり[45]、神経系で強い表現型が現れるものもある。Gli2変異マウスでは、Shhシグナルの影響を受ける底板とV3介在神経領域の分化が抑制され、パターン形成に異常が生じて出生直後に死亡する[46]。一方、Gli3変異マウスでは、主に脳領域でソニック・ヘッジホッグシグナルがむしろ亢進した表現型になるため[47][48]、Gli3が主に転写抑制型として働くことが示唆される。Gli1単独の変異マウスでは神経系では大きな表現型が見つかっていないが、Gli2変異による表現型をGli1のノックインによって相補することができるため、Gli2の転写活性型と同様の働きをしていると考えられる[49][50]。
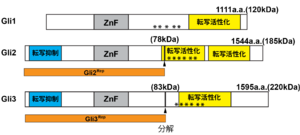
アミノ酸番号は、マウスのものである。*はPKAによるリン酸化サイト、ZnF:Znフィンガー、矢頭は分解されて転写抑制型を生じる部位[35]。
[32][35]から改変。
ソニック・ヘッジホッグシグナルのターゲット遺伝子として代表的なものは、神経前駆細胞におけるOlig2やNkx2.2, FoxA2のように細胞の個性付けに関与する転写因子、またソニック・ヘッジホッグシグナルに直接関与するもの(Ptc, Gli1)などである[1][3]。
先に述べたようにソニック・ヘッジホッグシグナルには細胞膜上に形成される1次繊毛の存在が必須である。1次繊毛に形成不全が生じるとソニック・ヘッジホッグシグナルが細胞に導入されず、結果として神経管はソニック・ヘッジホッグ遺伝子変異マウスに類似した表現型になる[29]。また、Gli3の不活性型を生じるプロセシングにはPKAが必要であり、PKA遺伝子のノックアウトはソニック・ヘッジホッグシグナルの異常亢進を反映した表現型となる[51]。
Shh-Ptc-Smo-Gliを主軸とするソニック・ヘッジホッグシグナルを制御する調節因子の存在も知られている。細胞質に局在するタンパク質の一種SuFu(Suppressor of Fused)はcAMP依存的に抑制型Gli2/3と結合して、安定化する[30]。
そのほかにGPR161(Gタンパク質共役型受容体)のように繊毛に局在してそのcAMP濃度を上昇させ、ソニック・ヘッジホッグシグナルを負に制御する因子の存在も知られている[52][53][54]。
さらに最近、ソニック・ヘッジホッグが細胞に到達するとカルシウムイオンがTRPチャネルを介して繊毛内に流入し、アデニルシクラーゼ(AC5/6)の活性が阻害されることによって繊毛内のcAMP濃度が低下し、結果的にGliが活性化されるという現象が報告された[37][28]。
これらをはじめとして、20種類程度のタンパク質がソニック・ヘッジホッグシグナルの伝達を正または負に制御している[55] 。調節因子が多数存在する理由としては、ソニック・ヘッジホッグの活性が細胞依存的であることや、ソニック・ヘッジホッグは細胞増殖も制御するために細胞ががん化する危険があり、シグナル活性を厳密に制御する必要があることなどが考えられる[29] 。
ほかの経路
ソニック・ヘッジホッグは交連神経細胞のガイダンスに必須である[56][57][58]。ソニック・ヘッジホッグは神経のガイダンス因子として知られるネトリンと協調して働き、交連神経が脊髄正中(midline)を交差するのに必要である[58]。このガイダンスにはPtc/SmoではなくHIP(hedgehog interacting protein)がソニック・ヘッジホッグの受容体になっており[56] 、さらに細胞内ではSrcファミリーキナーゼ(Src family kinase; SFK)が活性化されている[57] 。また、線維芽細胞の化学遊走にもソニック・ヘッジホッグが関与しているという報告があり、さらにこの現象においてはSmoが繊毛に局在しなくても細胞内シグナルが惹起されるため、従来とは異なるメカニズムが示唆されている[59]。
神経系での機能
ソニック・ヘッジホッグの神経系における機能解析の歴史は1990年代にさかのぼる。
1991年、Thomas M. Jessellと山田俊哉は、ニワトリ胚の脊策を神経管の別の場所に移植し、移植した周辺領域の細胞が底板(floor plate)や運動神経(motor neuron)に異所的に分化することを発見し、脊策と底板から分化誘導因子が分泌されていることを示した[60][61]。
その後、この分泌因子がソニック・ヘッジホッグであること[62] 、さらにソニック・ヘッジホッグが神経管内で濃度勾配を形成して[63][64]、モルフォゲンとし働いて濃度依存的に運動神経や介在神経の前駆細胞を誘導する(詳細は別項で議論する)。
詳細な発現・機能解析の結果、Shhは神経発生の初期には前脳の領域化に[65][66])、その後中枢神経全体のパターン形成に関与することが明らかとなった。さらに胚発生が進み、出生前後になると、小脳のプルキンエ細胞(Purkinje cells)からShhが分泌され、顆粒細胞の前駆細胞に作用してその増殖を促進し、さらにバーグマングリア細胞への分化を誘導することが知られている[67][68][69]。
また生後の脳においても神経前駆細胞の存在が知られており、ソニック・ヘッジホッグシグナルが微小環境(ニッチ:niche)において活性化されて前駆細胞の幹細胞性を維持している[70][71]。
実験手法
細胞レベルでの解析においてソニック・ヘッジホッグシグナルに反応する培養細胞は少なく、よく使われるのはマウスの線維芽細胞NIH3T3細胞[72]やヒト角化細胞[73]、ニワトリやマウスの神経前駆細胞(胚性幹細胞から分化させたものや胚から単離したもの)である[74][75]。ソニック・ヘッジホッグシグナルを受容する1次繊毛は、細胞周期のG0/G1期にのみ生じるため、特にNIH3T3でソニック・ヘッジホッグシグナルの実験を行う際にはあらかじめ血清飢餓状態にしてG0/G1期の細胞を多数得ておくことが重要である。細胞において実験的にソニック・ヘッジホッグシグナルを活性化する場合、大腸菌で作成した(つまりコレステロール修飾がされていない)リコンビナントタンパク質も活性は持っている[74][76][77]。化合物としては、purmorphamineとSAGがSmoを標的とし[78]、ソニック・ヘッジホッグのアゴニストとして用いられている。一方、cyclopamineとSANT-1は同じくSmoを標的とし、その活性を阻害することによりソニック・ヘッジホッグシグナルのアンタゴニストとして働く[79][80]。
ソニック・ヘッジホッグシグナルの強度を計測する方法としては、luciferaseまたはGFPのレポーターコンストラクトが多用されるが[43][81]、ほかの方法として、定量PCRを用いてソニック・ヘッジホッグシグナルのターゲット遺伝子であるGli1やPtc1の発現量を解析してもよい[72][77]。NIH3T3では、ソニック・ヘッジホッグシグナルの添加時間とともにGli1やPtc1の発現量が増加する[72]。一方、神経前駆細胞内ではソニック・ヘッジホッグシグナルは数時間以内にいったん活性化し、その後、負のフィードバックが起こって鎮静化する[77][81][82]。この負のフィードバックが起きるメカニズムとしては、Ptcが細胞膜上に多数存在するようになってソニック・ヘッジホッグタンパク質が枯渇するというもの[77]や、活性型Gliタンパク質が不活性型に比べて不安定であるというもの[30]などがあるが、全容はまだ明らかになっていない。
疾患との関わり
ヒトでソニック・ヘッジホッグは全前脳胞症(全前脳症;holoprosencephaly)の原因遺伝子として同定され[83]、実際に遺伝子欠損マウスから神経発生とパターン形成に必須の役割を果たすことが証明された[84]。
細胞内コレステロール輸送に関与する遺伝子NPC1/2に変異が生じるとリソソームにコレステロールが蓄積するためにShhNに十分なコレステロールが供給されずに修飾不全となり、効率的な分泌が不可能になってしまう。C型ニーマン・ピック病(C型Niemann-Pick syndrome)はこのNPC1/2遺伝子の変異に起因する遺伝性疾患であり、小脳の不完全形成や肝不全、発達障害や運動障害、新生児黄疸などの重篤な小児障害を引き起こす[85][22]。
逆にヘッジホッグシグナルが亢進しすぎると髄芽腫(medulloblastoma)という小児がんを引き起こすことが知られている[86]。この疾患は元来放射線治療や外科的手術による腫瘍の除去しか治療法がなかったが、最近、Gタンパク質の一種Gαsを活性化させることによりソニック・ヘッジホッグシグナルをブロックする方法が検討されつつある[86]。
参考文献
- ↑ 1.0 1.1 1.2 1.3
Briscoe, J., & Thérond, P.P. (2013).
The mechanisms of Hedgehog signalling and its roles in development and disease. Nature reviews. Molecular cell biology, 14(7), 416-29. [PubMed:23719536] [WorldCat] [DOI] - ↑ 2.0 2.1
Petrova, R., & Joyner, A.L. (2014).
Roles for Hedgehog signaling in adult organ homeostasis and repair. Development (Cambridge, England), 141(18), 3445-57. [PubMed:25183867] [PMC] [WorldCat] [DOI] - ↑ 3.0 3.1 3.2
Varjosalo, M., & Taipale, J. (2008).
Hedgehog: functions and mechanisms. Genes & development, 22(18), 2454-72. [PubMed:18794343] [WorldCat] [DOI] - ↑
Nüsslein-Volhard, C., & Wieschaus, E. (1980).
Mutations affecting segment number and polarity in Drosophila. Nature, 287(5785), 795-801. [PubMed:6776413] [WorldCat] [DOI] - ↑
van den Brink, G.R. (2007).
Hedgehog signaling in development and homeostasis of the gastrointestinal tract. Physiological reviews, 87(4), 1343-75. [PubMed:17928586] [WorldCat] [DOI] - ↑
Ingham, P.W., & McMahon, A.P. (2001).
Hedgehog signaling in animal development: paradigms and principles. Genes & development, 15(23), 3059-87. [PubMed:11731473] [WorldCat] [DOI] - ↑
Clark, A.M., Garland, K.K., & Russell, L.D. (2000).
Desert hedgehog (Dhh) gene is required in the mouse testis for formation of adult-type Leydig cells and normal development of peritubular cells and seminiferous tubules. Biology of reproduction, 63(6), 1825-38. [PubMed:11090455] [WorldCat] [DOI] - ↑
Levi, B., James, A.W., Nelson, E.R., Brugmann, S.A., Sorkin, M., Manu, A., & Longaker, M.T. (2011).
Role of Indian hedgehog signaling in palatal osteogenesis. Plastic and reconstructive surgery, 127(3), 1182-90. [PubMed:21364421] [PMC] [WorldCat] [DOI] - ↑
Karp, S.J., Schipani, E., St-Jacques, B., Hunzelman, J., Kronenberg, H., & McMahon, A.P. (2000).
Indian hedgehog coordinates endochondral bone growth and morphogenesis via parathyroid hormone related-protein-dependent and -independent pathways. Development (Cambridge, England), 127(3), 543-8. [PubMed:10631175] [WorldCat] - ↑
Riddle, R.D., Johnson, R.L., Laufer, E., & Tabin, C. (1993).
Sonic hedgehog mediates the polarizing activity of the ZPA. Cell, 75(7), 1401-16. [PubMed:8269518] [WorldCat] [DOI] - ↑
Krauss, S., Concordet, J.P., & Ingham, P.W. (1993).
A functionally conserved homolog of the Drosophila segment polarity gene hh is expressed in tissues with polarizing activity in zebrafish embryos. Cell, 75(7), 1431-44. [PubMed:8269519] [WorldCat] [DOI] - ↑
Echelard, Y., Epstein, D.J., St-Jacques, B., Shen, L., Mohler, J., McMahon, J.A., & McMahon, A.P. (1993).
Sonic hedgehog, a member of a family of putative signaling molecules, is implicated in the regulation of CNS polarity. Cell, 75(7), 1417-30. [PubMed:7916661] [WorldCat] [DOI] - ↑
Chen, X., Tukachinsky, H., Huang, C.H., Jao, C., Chu, Y.R., Tang, H.Y., ..., & Salic, A. (2011).
Processing and turnover of the Hedgehog protein in the endoplasmic reticulum. The Journal of cell biology, 192(5), 825-38. [PubMed:21357747] [PMC] [WorldCat] [DOI] - ↑
Hall, T.M., Porter, J.A., Beachy, P.A., & Leahy, D.J. (1995).
A potential catalytic site revealed by the 1.7-A crystal structure of the amino-terminal signalling domain of Sonic hedgehog. Nature, 378(6553), 212-6. [PubMed:7477329] [WorldCat] [DOI] - ↑
Li, Y., Zhang, H., Litingtung, Y., & Chiang, C. (2006).
Cholesterol modification restricts the spread of Shh gradient in the limb bud. Proceedings of the National Academy of Sciences of the United States of America, 103(17), 6548-53. [PubMed:16611729] [PMC] [WorldCat] [DOI] - ↑
Chamoun, Z., Mann, R.K., Nellen, D., von Kessler, D.P., Bellotto, M., Beachy, P.A., & Basler, K. (2001).
Skinny hedgehog, an acyltransferase required for palmitoylation and activity of the hedgehog signal. Science (New York, N.Y.), 293(5537), 2080-4. [PubMed:11486055] [WorldCat] [DOI] - ↑
Chen, M.H., Li, Y.J., Kawakami, T., Xu, S.M., & Chuang, P.T. (2004).
Palmitoylation is required for the production of a soluble multimeric Hedgehog protein complex and long-range signaling in vertebrates. Genes & development, 18(6), 641-59. [PubMed:15075292] [PMC] [WorldCat] [DOI] - ↑
Porter, J.A., Young, K.E., & Beachy, P.A. (1996).
Cholesterol modification of hedgehog signaling proteins in animal development. Science (New York, N.Y.), 274(5285), 255-9. [PubMed:8824192] [WorldCat] [DOI] - ↑
Lewis, P.M., Dunn, M.P., McMahon, J.A., Logan, M., Martin, J.F., St-Jacques, B., & McMahon, A.P. (2001).
Cholesterol modification of sonic hedgehog is required for long-range signaling activity and effective modulation of signaling by Ptc1. Cell, 105(5), 599-612. [PubMed:11389830] [WorldCat] [DOI] - ↑
Hardy, R.Y., & Resh, M.D. (2012).
Identification of N-terminal residues of Sonic Hedgehog important for palmitoylation by Hedgehog acyltransferase. The Journal of biological chemistry, 287(51), 42881-9. [PubMed:23112049] [PMC] [WorldCat] [DOI] - ↑
Mann, R.K., & Beachy, P.A. (2004).
Novel lipid modifications of secreted protein signals. Annual review of biochemistry, 73, 891-923. [PubMed:15189162] [WorldCat] [DOI] - ↑ 22.0 22.1
Tukachinsky, H., Kuzmickas, R.P., Jao, C.Y., Liu, J., & Salic, A. (2012).
Dispatched and scube mediate the efficient secretion of the cholesterol-modified hedgehog ligand. Cell reports, 2(2), 308-20. [PubMed:22902404] [PMC] [WorldCat] [DOI] - ↑
Ramírez-Weber, F.A., & Kornberg, T.B. (1999).
Cytonemes: cellular processes that project to the principal signaling center in Drosophila imaginal discs. Cell, 97(5), 599-607. [PubMed:10367889] [WorldCat] [DOI] - ↑
Bilioni, A., Sánchez-Hernández, D., Callejo, A., Gradilla, A.C., Ibáñez, C., Mollica, E., ..., & Guerrero, I. (2013).
Balancing Hedgehog, a retention and release equilibrium given by Dally, Ihog, Boi and shifted/DmWif. Developmental biology, 376(2), 198-212. [PubMed:23276604] [WorldCat] [DOI] - ↑
Vyas, N., Walvekar, A., Tate, D., Lakshmanan, V., Bansal, D., Lo Cicero, A., ..., & Dhawan, J. (2014).
Vertebrate Hedgehog is secreted on two types of extracellular vesicles with different signaling properties. Scientific reports, 4, 7357. [PubMed:25483805] [PMC] [WorldCat] [DOI] - ↑
Gradilla, A.C., González, E., Seijo, I., Andrés, G., Bischoff, M., González-Mendez, L., ..., & Guerrero, I. (2014).
Exosomes as Hedgehog carriers in cytoneme-mediated transport and secretion. Nature communications, 5, 5649. [PubMed:25472772] [WorldCat] [DOI] - ↑
Sanders, T.A., Llagostera, E., & Barna, M. (2013).
Specialized filopodia direct long-range transport of SHH during vertebrate tissue patterning. Nature, 497(7451), 628-32. [PubMed:23624372] [PMC] [WorldCat] [DOI] - ↑ 28.0 28.1 28.2
Moore, B.S., Stepanchick, A.N., Tewson, P.H., Hartle, C.M., Zhang, J., Quinn, A.M., ..., & Mirshahi, T. (2016).
Cilia have high cAMP levels that are inhibited by Sonic Hedgehog-regulated calcium dynamics. Proceedings of the National Academy of Sciences of the United States of America, 113(46), 13069-13074. [PubMed:27799542] [PMC] [WorldCat] [DOI] - ↑ 29.0 29.1 29.2 29.3
Sasai, N., & Briscoe, J. (2013).
Primary cilia and graded Sonic Hedgehog signaling. Wiley interdisciplinary reviews. Developmental biology, 1(5), 753-72. [PubMed:23799571] [WorldCat] [DOI] - ↑ 30.0 30.1 30.2 30.3 30.4
Humke, E.W., Dorn, K.V., Milenkovic, L., Scott, M.P., & Rohatgi, R. (2010).
The output of Hedgehog signaling is controlled by the dynamic association between Suppressor of Fused and the Gli proteins. Genes & development, 24(7), 670-82. [PubMed:20360384] [PMC] [WorldCat] [DOI] - ↑
Rohatgi, R., Milenkovic, L., & Scott, M.P. (2007).
Patched1 regulates hedgehog signaling at the primary cilium. Science (New York, N.Y.), 317(5836), 372-6. [PubMed:17641202] [WorldCat] [DOI] - ↑ 32.0 32.1
Hui, C.C., & Angers, S. (2011).
Gli proteins in development and disease. Annual review of cell and developmental biology, 27, 513-37. [PubMed:21801010] [WorldCat] [DOI] - ↑ 33.0 33.1
Haycraft, C.J., Banizs, B., Aydin-Son, Y., Zhang, Q., Michaud, E.J., & Yoder, B.K. (2005).
Gli2 and Gli3 localize to cilia and require the intraflagellar transport protein polaris for processing and function. PLoS genetics, 1(4), e53. [PubMed:16254602] [PMC] [WorldCat] [DOI] - ↑
Tempé, D., Casas, M., Karaz, S., Blanchet-Tournier, M.F., & Concordet, J.P. (2006).
Multisite protein kinase A and glycogen synthase kinase 3beta phosphorylation leads to Gli3 ubiquitination by SCFbetaTrCP. Molecular and cellular biology, 26(11), 4316-26. [PubMed:16705181] [PMC] [WorldCat] [DOI] - ↑ 35.0 35.1 35.2
Pan, Y., Bai, C.B., Joyner, A.L., & Wang, B. (2006).
Sonic hedgehog signaling regulates Gli2 transcriptional activity by suppressing its processing and degradation. Molecular and cellular biology, 26(9), 3365-77. [PubMed:16611981] [PMC] [WorldCat] [DOI] - ↑
Bhatia, N., Thiyagarajan, S., Elcheva, I., Saleem, M., Dlugosz, A., Mukhtar, H., & Spiegelman, V.S. (2006).
Gli2 is targeted for ubiquitination and degradation by beta-TrCP ubiquitin ligase. The Journal of biological chemistry, 281(28), 19320-6. [PubMed:16651270] [WorldCat] [DOI] - ↑ 37.0 37.1
Delling, M., DeCaen, P.G., Doerner, J.F., Febvay, S., & Clapham, D.E. (2013).
Primary cilia are specialized calcium signalling organelles. Nature, 504(7479), 311-4. [PubMed:24336288] [PMC] [WorldCat] [DOI] - ↑
Wen, X., Lai, C.K., Evangelista, M., Hongo, J.A., de Sauvage, F.J., & Scales, S.J. (2010).
Kinetics of hedgehog-dependent full-length Gli3 accumulation in primary cilia and subsequent degradation. Molecular and cellular biology, 30(8), 1910-22. [PubMed:20154143] [PMC] [WorldCat] [DOI] - ↑
Wang, C., Pan, Y., & Wang, B. (2010).
Suppressor of fused and Spop regulate the stability, processing and function of Gli2 and Gli3 full-length activators but not their repressors. Development (Cambridge, England), 137(12), 2001-9. [PubMed:20463034] [PMC] [WorldCat] [DOI] - ↑
Cox, B., Briscoe, J., & Ulloa, F. (2010).
SUMOylation by Pias1 regulates the activity of the Hedgehog dependent Gli transcription factors. PloS one, 5(8), e11996. [PubMed:20711444] [PMC] [WorldCat] [DOI] - ↑
Coni, S., Antonucci, L., D'Amico, D., Di Magno, L., Infante, P., De Smaele, E., ..., & Canettieri, G. (2013).
Gli2 acetylation at lysine 757 regulates hedgehog-dependent transcriptional output by preventing its promoter occupancy. PloS one, 8(6), e65718. [PubMed:23762415] [PMC] [WorldCat] [DOI] - ↑
Niewiadomski, P., Kong, J.H., Ahrends, R., Ma, Y., Humke, E.W., Khan, S., ..., & Rohatgi, R. (2014).
Gli protein activity is controlled by multisite phosphorylation in vertebrate Hedgehog signaling. Cell reports, 6(1), 168-181. [PubMed:24373970] [PMC] [WorldCat] [DOI] - ↑ 43.0 43.1
Sasaki, H., Hui, C., Nakafuku, M., & Kondoh, H. (1997).
A binding site for Gli proteins is essential for HNF-3beta floor plate enhancer activity in transgenics and can respond to Shh in vitro. Development (Cambridge, England), 124(7), 1313-22. [PubMed:9118802] [WorldCat] - ↑
Oosterveen, T., Kurdija, S., Alekseenko, Z., Uhde, C.W., Bergsland, M., Sandberg, M., ..., & Ericson, J. (2012).
Mechanistic differences in the transcriptional interpretation of local and long-range Shh morphogen signaling. Developmental cell, 23(5), 1006-19. [PubMed:23153497] [WorldCat] [DOI] - ↑
Motoyama, J., Liu, J., Mo, R., Ding, Q., Post, M., & Hui, C.C. (1998).
Essential function of Gli2 and Gli3 in the formation of lung, trachea and oesophagus. Nature genetics, 20(1), 54-7. [PubMed:9731531] [WorldCat] [DOI] - ↑
Ding, Q., Motoyama, J., Gasca, S., Mo, R., Sasaki, H., Rossant, J., & Hui, C.C. (1998).
Diminished Sonic hedgehog signaling and lack of floor plate differentiation in Gli2 mutant mice. Development (Cambridge, England), 125(14), 2533-43. [PubMed:9636069] [WorldCat] - ↑
Hui, C.C., & Joyner, A.L. (1993).
A mouse model of greig cephalopolysyndactyly syndrome: the extra-toesJ mutation contains an intragenic deletion of the Gli3 gene. Nature genetics, 3(3), 241-6. [PubMed:8387379] [WorldCat] [DOI] - ↑
Litingtung, Y., & Chiang, C. (2000).
Specification of ventral neuron types is mediated by an antagonistic interaction between Shh and Gli3. Nature neuroscience, 3(10), 979-85. [PubMed:11017169] [WorldCat] [DOI] - ↑
Park, H.L., Bai, C., Platt, K.A., Matise, M.P., Beeghly, A., Hui, C.C., ..., & Joyner, A.L. (2000).
Mouse Gli1 mutants are viable but have defects in SHH signaling in combination with a Gli2 mutation. Development (Cambridge, England), 127(8), 1593-605. [PubMed:10725236] [WorldCat] - ↑
Bai, C.B., & Joyner, A.L. (2001).
Gli1 can rescue the in vivo function of Gli2. Development (Cambridge, England), 128(24), 5161-72. [PubMed:11748151] [WorldCat] - ↑
Huang, Y., Roelink, H., & McKnight, G.S. (2002).
Protein kinase A deficiency causes axially localized neural tube defects in mice. The Journal of biological chemistry, 277(22), 19889-96. [PubMed:11886853] [WorldCat] [DOI] - ↑
Svärd, J., Heby-Henricson, K., Henricson, K.H., Persson-Lek, M., Rozell, B., Lauth, M., ..., & Teglund, S. (2006).
Genetic elimination of Suppressor of fused reveals an essential repressor function in the mammalian Hedgehog signaling pathway. Developmental cell, 10(2), 187-97. [PubMed:16459298] [WorldCat] [DOI] - ↑
Tukachinsky, H., Lopez, L.V., & Salic, A. (2010).
A mechanism for vertebrate Hedgehog signaling: recruitment to cilia and dissociation of SuFu-Gli protein complexes. The Journal of cell biology, 191(2), 415-28. [PubMed:20956384] [PMC] [WorldCat] [DOI] - ↑
Mukhopadhyay, S., Wen, X., Ratti, N., Loktev, A., Rangell, L., Scales, S.J., & Jackson, P.K. (2013).
The ciliary G-protein-coupled receptor Gpr161 negatively regulates the Sonic hedgehog pathway via cAMP signaling. Cell, 152(1-2), 210-23. [PubMed:23332756] [WorldCat] [DOI] - ↑
Chen, M.H., Wilson, C.W., & Chuang, P.T. (2007).
SnapShot: hedgehog signaling pathway. Cell, 130(2), 386. [PubMed:17662951] [WorldCat] [DOI] - ↑ 56.0 56.1
Bourikas, D., Pekarik, V., Baeriswyl, T., Grunditz, A., Sadhu, R., Nardó, M., & Stoeckli, E.T. (2005).
Sonic hedgehog guides commissural axons along the longitudinal axis of the spinal cord. Nature neuroscience, 8(3), 297-304. [PubMed:15746914] [WorldCat] [DOI] - ↑ 57.0 57.1
Yam, P.T., Langlois, S.D., Morin, S., & Charron, F. (2009).
Sonic hedgehog guides axons through a noncanonical, Src-family-kinase-dependent signaling pathway. Neuron, 62(3), 349-62. [PubMed:19447091] [WorldCat] [DOI] - ↑ 58.0 58.1
Charron, F., Stein, E., Jeong, J., McMahon, A.P., & Tessier-Lavigne, M. (2003).
The morphogen sonic hedgehog is an axonal chemoattractant that collaborates with netrin-1 in midline axon guidance. Cell, 113(1), 11-23. [PubMed:12679031] [WorldCat] [DOI] - ↑
Bijlsma, M.F., Damhofer, H., & Roelink, H. (2012).
Hedgehog-stimulated chemotaxis is mediated by smoothened located outside the primary cilium. Science signaling, 5(238), ra60. [PubMed:22912493] [PMC] [WorldCat] [DOI] - ↑
Yamada, T., Placzek, M., Tanaka, H., Dodd, J., & Jessell, T.M. (1991).
Control of cell pattern in the developing nervous system: polarizing activity of the floor plate and notochord. Cell, 64(3), 635-47. [PubMed:1991324] [WorldCat] [DOI] - ↑
Yamada, T., Pfaff, S.L., Edlund, T., & Jessell, T.M. (1993).
Control of cell pattern in the neural tube: motor neuron induction by diffusible factors from notochord and floor plate. Cell, 73(4), 673-86. [PubMed:8500163] [WorldCat] [DOI] - ↑
Roelink, H., Augsburger, A., Heemskerk, J., Korzh, V., Norlin, S., Ruiz i Altaba, A., ..., & Jessell, T.M. (1994).
Floor plate and motor neuron induction by vhh-1, a vertebrate homolog of hedgehog expressed by the notochord. Cell, 76(4), 761-75. [PubMed:8124714] [WorldCat] [DOI] - ↑
Roelink, H., Porter, J.A., Chiang, C., Tanabe, Y., Chang, D.T., Beachy, P.A., & Jessell, T.M. (1995).
Floor plate and motor neuron induction by different concentrations of the amino-terminal cleavage product of sonic hedgehog autoproteolysis. Cell, 81(3), 445-55. [PubMed:7736596] [WorldCat] [DOI] - ↑
Ribes, V., & Briscoe, J. (2009).
Establishing and interpreting graded Sonic Hedgehog signaling during vertebrate neural tube patterning: the role of negative feedback. Cold Spring Harbor perspectives in biology, 1(2), a002014. [PubMed:20066087] [PMC] [WorldCat] [DOI] - ↑
Barraquer-Bordas, L., Ley-Gracia, A., & Rovira, M. (1977).
Paroxysmal pains with parietal falx meningioma. Annals of neurology, 1(6), 601-2. [PubMed:883777] [WorldCat] [DOI] - ↑
Bertrand, N., & Dahmane, N. (2006).
Sonic hedgehog signaling in forebrain development and its interactions with pathways that modify its effects. Trends in cell biology, 16(11), 597-605. [PubMed:17030124] [WorldCat] [DOI] - ↑
Wallace, V.A. (1999).
Purkinje-cell-derived Sonic hedgehog regulates granule neuron precursor cell proliferation in the developing mouse cerebellum. Current biology : CB, 9(8), 445-8. [PubMed:10226030] [WorldCat] [DOI] - ↑
Lewis, P.M., Gritli-Linde, A., Smeyne, R., Kottmann, A., & McMahon, A.P. (2004).
Sonic hedgehog signaling is required for expansion of granule neuron precursors and patterning of the mouse cerebellum. Developmental biology, 270(2), 393-410. [PubMed:15183722] [WorldCat] [DOI] - ↑
Dahmane, N., & Ruiz i Altaba, A. (1999).
Sonic hedgehog regulates the growth and patterning of the cerebellum. Development (Cambridge, England), 126(14), 3089-100. [PubMed:10375501] [WorldCat] - ↑
Ahn, S., & Joyner, A.L. (2005).
In vivo analysis of quiescent adult neural stem cells responding to Sonic hedgehog. Nature, 437(7060), 894-7. [PubMed:16208373] [WorldCat] [DOI] - ↑
Daynac, M., Tirou, L., Faure, H., Mouthon, M.A., Gauthier, L.R., Hahn, H., ..., & Ruat, M. (2016).
Hedgehog Controls Quiescence and Activation of Neural Stem Cells in the Adult Ventricular-Subventricular Zone. Stem cell reports, 7(4), 735-748. [PubMed:27666792] [PMC] [WorldCat] [DOI] - ↑ 72.0 72.1 72.2
Cohen, M., Kicheva, A., Ribeiro, A., Blassberg, R., Page, K.M., Barnes, C.P., & Briscoe, J. (2015).
Ptch1 and Gli regulate Shh signalling dynamics via multiple mechanisms. Nature communications, 6, 6709. [PubMed:25833741] [PMC] [WorldCat] [DOI] - ↑
Kasper, M., Schnidar, H., Neill, G.W., Hanneder, M., Klingler, S., Blaas, L., ..., & Aberger, F. (2006).
Selective modulation of Hedgehog/GLI target gene expression by epidermal growth factor signaling in human keratinocytes. Molecular and cellular biology, 26(16), 6283-98. [PubMed:16880536] [PMC] [WorldCat] [DOI] - ↑ 74.0 74.1
Kutejova, E., Sasai, N., Shah, A., Gouti, M., & Briscoe, J. (2016).
Neural Progenitors Adopt Specific Identities by Directly Repressing All Alternative Progenitor Transcriptional Programs. Developmental cell, 36(6), 639-53. [PubMed:26972603] [PMC] [WorldCat] [DOI] - ↑
Sasai, N., Kutejova, E., & Briscoe, J. (2014).
Integration of signals along orthogonal axes of the vertebrate neural tube controls progenitor competence and increases cell diversity. PLoS biology, 12(7), e1001907. [PubMed:25026549] [PMC] [WorldCat] [DOI] - ↑
Williams, K.P., Rayhorn, P., Chi-Rosso, G., Garber, E.A., Strauch, K.L., Horan, G.S., ..., & Pepinsky, R.B. (1999).
Functional antagonists of sonic hedgehog reveal the importance of the N terminus for activity. Journal of cell science, 112 ( Pt 23), 4405-14. [PubMed:10564658] [WorldCat] - ↑ 77.0 77.1 77.2 77.3
Dessaud, E., Yang, L.L., Hill, K., Cox, B., Ulloa, F., Ribeiro, A., ..., & Briscoe, J. (2007).
Interpretation of the sonic hedgehog morphogen gradient by a temporal adaptation mechanism. Nature, 450(7170), 717-20. [PubMed:18046410] [WorldCat] [DOI] - ↑
Briscoe, J. (2006).
Agonizing hedgehog. Nature chemical biology, 2(1), 10-1. [PubMed:16408082] [WorldCat] [DOI] - ↑
Chen, J.K., Taipale, J., Cooper, M.K., & Beachy, P.A. (2002).
Inhibition of Hedgehog signaling by direct binding of cyclopamine to Smoothened. Genes & development, 16(21), 2743-8. [PubMed:12414725] [PMC] [WorldCat] [DOI] - ↑
Dixit, D., Ghildiyal, R., Anto, N.P., Ghosh, S., Sharma, V., & Sen, E. (2013).
Guggulsterone sensitizes glioblastoma cells to Sonic hedgehog inhibitor SANT-1 induced apoptosis in a Ras/NFκB dependent manner. Cancer letters, 336(2), 347-58. [PubMed:23548480] [WorldCat] [DOI] - ↑ 81.0 81.1
Balaskas, N., Ribeiro, A., Panovska, J., Dessaud, E., Sasai, N., Page, K.M., ..., & Ribes, V. (2012).
Gene regulatory logic for reading the Sonic Hedgehog signaling gradient in the vertebrate neural tube. Cell, 148(1-2), 273-84. [PubMed:22265416] [PMC] [WorldCat] [DOI] - ↑
Dessaud, E., Ribes, V., Balaskas, N., Yang, L.L., Pierani, A., Kicheva, A., ..., & Sasai, N. (2010).
Dynamic assignment and maintenance of positional identity in the ventral neural tube by the morphogen sonic hedgehog. PLoS biology, 8(6), e1000382. [PubMed:20532235] [PMC] [WorldCat] [DOI] - ↑
Roessler, E., Belloni, E., Gaudenz, K., Jay, P., Berta, P., Scherer, S.W., ..., & Muenke, M. (1996).
Mutations in the human Sonic Hedgehog gene cause holoprosencephaly. Nature genetics, 14(3), 357-60. [PubMed:8896572] [WorldCat] [DOI] - ↑
Chiang, C., Litingtung, Y., Lee, E., Young, K.E., Corden, J.L., Westphal, H., & Beachy, P.A. (1996).
Cyclopia and defective axial patterning in mice lacking Sonic hedgehog gene function. Nature, 383(6599), 407-13. [PubMed:8837770] [WorldCat] [DOI] - ↑
Loftus, S.K., Morris, J.A., Carstea, E.D., Gu, J.Z., Cummings, C., Brown, A., ..., & Pavan, W.J. (1997).
Murine model of Niemann-Pick C disease: mutation in a cholesterol homeostasis gene. Science (New York, N.Y.), 277(5323), 232-5. [PubMed:9211850] [WorldCat] [DOI] - ↑ 86.0 86.1
He, X., Zhang, L., Chen, Y., Remke, M., Shih, D., Lu, F., ..., & Lu, Q.R. (2014).
The G protein α subunit Gαs is a tumor suppressor in Sonic hedgehog-driven medulloblastoma. Nature medicine, 20(9), 1035-42. [PubMed:25150496] [PMC] [WorldCat] [DOI]