「PSD-95」の版間の差分
細 →ファミリー |
|||
| 24行目: | 24行目: | ||
==ファミリー== | ==ファミリー== | ||
PSDには同様の構造を持ったタンパク質として[[PSD-93]]、[[SAP97]]、[[SAP102]]が存在し、これらを含めてPSD-95 familyあるいは[[membrane-associated guanylate kinase]] ([[MAGUK]]) | PSDには同様の構造を持ったタンパク質として[[PSD-93]]、[[SAP97]]、[[SAP102]]が存在し、これらを含めてPSD-95 familyあるいは[[membrane-associated guanylate kinase]] ([[MAGUK]])と呼ぶ。(編集コメント:抄録にあった文章を持ってきました。適宜御編集下さい)。 | ||
==発現パターン== | ==発現パターン== | ||
2019年4月23日 (火) 22:54時点における版
坪山 幸太郎、田中 慎二、岡部 繁男
東京大学大学院医学系研究科
DOI:10.14931/bsd.4392 原稿受付日:2013年10月31日 原稿完成日:2015年12月30日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
同義語:synapse-associated protein 90(SAP-90)、disks large homolog 4(DLG4)
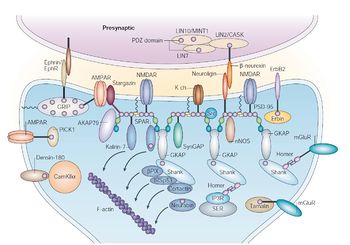
PSD-95(postsynaptic density protein 95)は、シナプス後部の主要な足場タンパク質であり、シナプス後肥厚部(postsynaptic density; PSD)において最も豊富に存在しているタンパク質の一つである。NR2A-D、GluR6、ニューロリギン、nNOSなど様々な分子と相互作用し、シナプス機能の維持や可塑性などに寄与すると考えられている。プロテオミクス解析や全反射顕微鏡を用いたシナプス分子の数の定量結果から、PSD family分子はシナプス後部に300個ほど存在するとされている[1] [2]。
構造
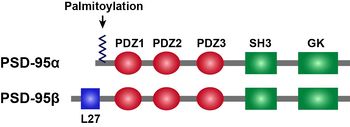
N末端側から、3つのPDZドメイン、1つのSrc homology 3(SH3)ドメイン、1つのGuanylate kinase-like(GK)ドメインを持つ。PSD-95のαアイソフォームは、N末端にパルミトイル化反応を受けうる2つのシステインを含み、βアイソフォームはL27ドメインを持つ。L27ドメインはSAP97にも存在し、他のL27ドメインを有するタンパク質や自分自身と会合しシナプス後膜への局在とクラスター化に重要である[3]。パルミトイル化はPSD-95のシナプス後膜への局在に重要である[4]。
PDZ ドメイン
PDZドメインは、リガンドタンパク質のC末端に結合する90程度のアミノ酸残基を含む構造である。PSD-95に含まれる、リガンドタンパク質のC末端から3番目の位置がセリンまたはスレオニンであるPDZドメインをクラスIとよぶ。PSD-95の3つのPDZドメインはすべて、クラスIである。PSD-95のPDZドメインと結合するタンパク質としてNR2A-D、GluR6、nAChRc、ErbB4、Kir2-5、ニューロリギン、nNosなどがあげられ、これらのC末端がいずれかのPDZドメインに結合する[5]。また、AMPA型グルタミン酸受容体は補助サブユニットであるtransmembrane AMPAR regulatory proteins(TARP)がPDZドメインと結合することによって間接的にPSD-95と結合することが示されている[6]。
SH3ドメイン、GKドメイン
SH3ドメインとGKドメインはPSD-95のC末端側に位置する。GKドメインは酵素活性をもたず、SH3ドメインと分子内で相互作用しており、PSD-95の分子的な安定性の向上に役だっていると考えられている。また、この相互作用は分子間でも見られ、複数のPSD-95間における会合にも資している。SH3ドメインやGKドメインには同種の分子だけでなくGKAP、SPAR、AKAP79/150、Pyk2など様々な分子と相互作用する[6] [7]。
ファミリー
PSDには同様の構造を持ったタンパク質としてPSD-93、SAP97、SAP102が存在し、これらを含めてPSD-95 familyあるいはmembrane-associated guanylate kinase (MAGUK)と呼ぶ。(編集コメント:抄録にあった文章を持ってきました。適宜御編集下さい)。
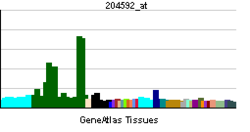
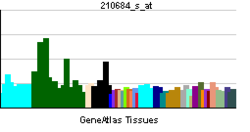
発現パターン
組織発現パターン
これら分子の発達に伴う発現パターンは異なっており、げっ歯類の海馬においては、PSD-95およびPSD-93は生後10日目あたりから発現量が増えるのに対し、SAP102は生後1週齢で既に発現量が高い[8]。SAP-97については生後2週齢頃から遺伝子発現が増加することが報告されている[9]。
細胞内分布
シナプス後部に存在するPSDに強く集積する。生化学、イメージングによる解析からPSDに存在するPSD-95は300個ほどであると見積もられている[1][2]。
機能
PSD-95はシナプスを構成する幅広い分子の足場となることで、シナプス機能やシナプス可塑性に重要な役割を果たす。PSD-95の発現を変化させた様々な実験から、PSD-95がシナプス伝達、特にAMPA型グルタミン酸受容体を介したシナプス伝達機能に重要であるという知見が報告されている。
海馬スライス培養系においてshRNAによりPSD-95をノックダウンした錐体細胞では、AMPA型グルタミン酸受容体依存性のevoked EPSC振幅およびmEPSC頻度 の低下が見られる[10]。一方、PSD-95ノックアウトマウスの急性スライスを用いた研究では、AMPA型グルタミン酸受容体を介したEPSCに変化が見られないと報告されたが[11]、PSD-93とのダブルノックアウトマウスではEPSCが大きく低下することが分かり、PSD-95単独のノックアウトマウスではその機能がPSD-93によって補償されている可能性が示唆されている[10]。
さらに、別系統のノックアウトマウスでは、幼若期(生後14-24日)において、AMPA型グルタミン酸受容体依存性のevoked EPSC振幅およびmEPSC頻度の低下が見られている[12]。また、PSD-95を過剰発現させた場合には、evoked EPSC振幅やmEPSC振幅が増加することが報告されている[13] [14]。
NMDA型グルタミン酸受容体を介したシナプス伝達についても同様の実験が行われているが、PSD-95の発現操作によりNMDA型受容体を介したEPSCは変化しない[10][11]。一方、PSD-95の発現低下やPSD-95とNMDA型受容体の結合を阻害する事で、NMDA依存的な細胞死や細胞形態の変化が軽減されることが報告されており、NMDA型受容体依存的な興奮毒性の誘発にPSD-95が関与する可能性が指摘されている[15][16][17]。
PSD-95はシナプス伝達の長期可塑性にも関与する。PSD-95ノックアウトマウスの海馬スライスでは、高頻度刺激で生じるシナプス長期増強(long-term potentiation; LTP)が促進される一方で、低頻度刺激で生じるシナプス長期抑制(long-term depression; LTD)は抑制される[11]。逆に、PSD-95を過剰発現させた細胞では、LTPが抑制され、LTDが亢進する[18]。
ノックアウトマウスにおいても空間学習能力の異常が認められており、脳機能の可塑的な変化が個体レベルでも阻害されることが分かっている[11]。
シナプス長期可塑性を調節する分子機構として、LTDに関しては、PSD-95がLTD発現に必要なシグナルタンパク質であるAKAP79/150とPP2Bの足場となり、NMDA型グルタミン酸受容体から流入するカルシウムシグナルとこれらシグナルタンパク質を結び付けているとするモデルが提唱されている[19]。
また、シナプスへの局在に重要な295番目のセリン残基がシナプス長期可塑性の発現に重要であることが報告されている[20]。
関連項目
参考文献
- ↑ 1.0 1.1
Chen, X., Vinade, L., Leapman, R.D., Petersen, J.D., Nakagawa, T., Phillips, T.M., ..., & Reese, T.S. (2005).
Mass of the postsynaptic density and enumeration of three key molecules. Proceedings of the National Academy of Sciences of the United States of America, 102(32), 11551-6. [PubMed:16061821] [PMC] [WorldCat] [DOI] - ↑ 2.0 2.1
Sugiyama, Y., Kawabata, I., Sobue, K., & Okabe, S. (2005).
Determination of absolute protein numbers in single synapses by a GFP-based calibration technique. Nature methods, 2(9), 677-84. [PubMed:16118638] [WorldCat] [DOI] - ↑
Nakagawa, T., Futai, K., Lashuel, H.A., Lo, I., Okamoto, K., Walz, T., ..., & Sheng, M. (2004).
Quaternary structure, protein dynamics, and synaptic function of SAP97 controlled by L27 domain interactions. Neuron, 44(3), 453-67. [PubMed:15504326] [WorldCat] [DOI] - ↑
El-Husseini, A.e.l.-.D., Schnell, E., Dakoji, S., Sweeney, N., Zhou, Q., Prange, O., ..., & Bredt, D.S. (2002).
Synaptic strength regulated by palmitate cycling on PSD-95. Cell, 108(6), 849-63. [PubMed:11955437] [WorldCat] [DOI] - ↑
Kim, E., & Sheng, M. (2004).
PDZ domain proteins of synapses. Nature reviews. Neuroscience, 5(10), 771-81. [PubMed:15378037] [WorldCat] [DOI] - ↑ 6.0 6.1
Chen, L., Chetkovich, D.M., Petralia, R.S., Sweeney, N.T., Kawasaki, Y., Wenthold, R.J., ..., & Nicoll, R.A. (2001).
Stargazin regulates synaptic targeting of AMPA receptors by two distinct mechanisms. Nature, 408(6815), 936-43. [PubMed:11140673] [WorldCat] [DOI] - ↑
Han, K., & Kim, E. (2008).
Synaptic adhesion molecules and PSD-95. Progress in neurobiology, 84(3), 263-83. [PubMed:18206289] [WorldCat] [DOI] - ↑
Sans, N., Petralia, R.S., Wang, Y.X., Blahos, J., Hell, J.W., & Wenthold, R.J. (2000).
A developmental change in NMDA receptor-associated proteins at hippocampal synapses. The Journal of neuroscience : the official journal of the Society for Neuroscience, 20(3), 1260-71. [PubMed:10648730] [PMC] [WorldCat] - ↑
Müller, B.M., Kistner, U., Veh, R.W., Cases-Langhoff, C., Becker, B., Gundelfinger, E.D., & Garner, C.C. (1995).
Molecular characterization and spatial distribution of SAP97, a novel presynaptic protein homologous to SAP90 and the Drosophila discs-large tumor suppressor protein. The Journal of neuroscience : the official journal of the Society for Neuroscience, 15(3 Pt 2), 2354-66. [PubMed:7891172] [WorldCat] - ↑ 10.0 10.1 10.2
Elias, G.M., Funke, L., Stein, V., Grant, S.G., Bredt, D.S., & Nicoll, R.A. (2006).
Synapse-specific and developmentally regulated targeting of AMPA receptors by a family of MAGUK scaffolding proteins. Neuron, 52(2), 307-20. [PubMed:17046693] [WorldCat] [DOI] - ↑ 11.0 11.1 11.2 11.3
Migaud, M., Charlesworth, P., Dempster, M., Webster, L.C., Watabe, A.M., Makhinson, M., ..., & Grant, S.G. (1998).
Enhanced long-term potentiation and impaired learning in mice with mutant postsynaptic density-95 protein. Nature, 396(6710), 433-9. [PubMed:9853749] [WorldCat] [DOI] - ↑
Müller, B.M., Kistner, U., Veh, R.W., Cases-Langhoff, C., Becker, B., Gundelfinger, E.D., & Garner, C.C. (1995).
Molecular characterization and spatial distribution of SAP97, a novel presynaptic protein homologous to SAP90 and the Drosophila discs-large tumor suppressor protein. The Journal of neuroscience : the official journal of the Society for Neuroscience, 15(3 Pt 2), 2354-66. [PubMed:7891172] [WorldCat] - ↑
El-Husseini, A.E., Schnell, E., Chetkovich, D.M., Nicoll, R.A., & Bredt, D.S. (2000).
PSD-95 involvement in maturation of excitatory synapses. Science (New York, N.Y.), 290(5495), 1364-8. [PubMed:11082065] [WorldCat] - ↑
Schnell, E., Sizemore, M., Karimzadegan, S., Chen, L., Bredt, D.S., & Nicoll, R.A. (2002).
Direct interactions between PSD-95 and stargazin control synaptic AMPA receptor number. Proceedings of the National Academy of Sciences of the United States of America, 99(21), 13902-7. [PubMed:12359873] [PMC] [WorldCat] [DOI] - ↑
Cui, H., Hayashi, A., Sun, H.S., Belmares, M.P., Cobey, C., Phan, T., ..., & Tymianski, M. (2007).
PDZ protein interactions underlying NMDA receptor-mediated excitotoxicity and neuroprotection by PSD-95 inhibitors. The Journal of neuroscience : the official journal of the Society for Neuroscience, 27(37), 9901-15. [PubMed:17855605] [PMC] [WorldCat] [DOI] - ↑
Tseng, C.Y., & Firestein, B.L. (2011).
The role of PSD-95 and cypin in morphological changes in dendrites following sublethal NMDA exposure. The Journal of neuroscience : the official journal of the Society for Neuroscience, 31(43), 15468-80. [PubMed:22031893] [PMC] [WorldCat] [DOI] - ↑
Zhou, L., Li, F., Xu, H.B., Luo, C.X., Wu, H.Y., Zhu, M.M., ..., & Zhu, D.Y. (2010).
Treatment of cerebral ischemia by disrupting ischemia-induced interaction of nNOS with PSD-95. Nature medicine, 16(12), 1439-43. [PubMed:21102461] [WorldCat] [DOI] - ↑
Stein, V., House, D.R., Bredt, D.S., & Nicoll, R.A. (2003).
Postsynaptic density-95 mimics and occludes hippocampal long-term potentiation and enhances long-term depression. The Journal of neuroscience : the official journal of the Society for Neuroscience, 23(13), 5503-6. [PubMed:12843250] [PMC] [WorldCat] - ↑
Xu, W., Schlüter, O.M., Steiner, P., Czervionke, B.L., Sabatini, B., & Malenka, R.C. (2008).
Molecular dissociation of the role of PSD-95 in regulating synaptic strength and LTD. Neuron, 57(2), 248-62. [PubMed:18215622] [PMC] [WorldCat] [DOI] - ↑
Kim, M.J., Futai, K., Jo, J., Hayashi, Y., Cho, K., & Sheng, M. (2007).
Synaptic accumulation of PSD-95 and synaptic function regulated by phosphorylation of serine-295 of PSD-95. Neuron, 56(3), 488-502. [PubMed:17988632] [WorldCat] [DOI]